接受体外膜肺氧合治疗患者预后的影响因素研究
2020-09-25周亮邵敏王昌会刘念余超黄锐崔良文
周亮,邵敏,王昌会,刘念,余超,黄锐,崔良文
体外膜肺氧合(ECMO)是对常规治疗难以治愈的严重循环衰竭或呼吸衰竭患者的一种生命支持疗法[1],其可以通过增加氧输送和组织灌注来稳定生命体征,为患者心肺功能恢复争取时间[2]。近年来ECMO的应用挽救了大量患者的生命,有研究选取2009-10-01至2017-03-31将ECMO作为心肺支持治疗的692例成年患者,其住院期间死亡率为40.0%,1、2、5年死亡率分别为45.1%、49.0%、57.4%[3]。较高的死亡率提示具有某些特征的患者未能从ECMO中获益,而寻找出这些特征非常必要,但目前绝大多数研究未涉及此领域。本研究旨在分析接受ECMO治疗患者预后的影响因素,以期为ECMO的临床应用提供依据。
本研究创新点:
虽然近年来体外膜肺氧合(ECMO)治疗越来越广泛,每年接受ECMO治疗的患者例数也越来越多,然而许多研究主要关注ECMO治疗后的并发症或者不同的置管途径,而对接受ECMO治疗患者的急性生理学指标关注较少。在使用ECMO治疗心肺功能衰竭患者之前,通过不同生理指标的分析,找出并更有效地利用ECMO去治疗能够明显获益的患者,这不仅能够获得较好的社会效应,而且会减轻社会经济负担,而这也是本文所关注和研究的重点。
1 对象与方法
1.1 研究对象 回顾性选择2018-01-01至2020-02-01安徽医科大学第一附属医院绩溪路病区和高新病区重症医学科患者35例为研究对象。收治途径包括自外院直接转入重症医学科,自本院普通病房转入重症医学科,从急诊抢救室直接收入重症医学科。纳入标准:符合ECMO治疗的适应证,包括:(1)各种原因引起的其他治疗无效的严重心源性休克[4],如急性暴发性心肌炎[5]、急性心肌梗死、脓毒症心肌抑制、应激性心肌病、儿茶酚胺性心肌病、心脏手术后、心脏移植术后。(2)各种原因引起的严重急性呼吸衰竭[6],如重度急性呼吸窘迫综合征(ARDS)[7]、危及生命的哮喘[8]、肺移植前肺脏替代治疗、肺移植后原发性移植物功能衰竭、弥漫性肺泡出血、肺动脉高压危象、肺栓塞、严重支气管胸膜瘘等。(3)各种原因引起的严重循环衰竭,如脓毒症休克、冻伤、大面积重度烧伤、药物中毒、一氧化碳(CO)中毒、溺水、严重创伤等。排除标准:(1)开始ECMO治疗后24 h内死亡或者自动出院的患者;(2)由于急性气道梗阻或者为避免急性气道梗阻预防性进行ECMO治疗的患者;(3)在等待器官移植期间,作为供体方使用ECMO维持生命的脑死亡患者;(4)患有不可逆的心、肺病变且无心脏移植术和使用心室辅助装置的可能[9];(5)患有不可逆的中枢神经系统损伤[9];(6)心搏骤停超过60 min[10];(7)终末期多器官功能衰竭患者。本研究患者均签署了ECMO治疗知情同意书。
1.2 治疗方法 所有患者内科治疗失败后选择ECMO治疗。采用Maquet CARDIOHELP-i或者Medtronic公司的Extracorproreal Blood Pumping Console两款装置进行ECMO治疗。治疗方式分为两种,即静脉-静脉体外膜肺氧合(veno-venous extracorporeal membrane oxygenation,VV-ECMO)和静脉-动脉体外膜肺氧合(veno-arterial extracorporeal membrane oxygenation,VA-ECMO)。首先两名护士进行套包预充,两名医生开始在器械护士的协助下进行经皮穿刺置管。静脉导管多选择21 Fr、19 Fr,动脉导管多选择17 Fr、15 Fr(一般不超过动脉直径的75%)。穿刺部位:VV-ECMO选择颈内静脉-股静脉插管,VA-ECMO选择股静脉-股动脉插管。置管位置:颈内静脉插管尖端位于颈内静脉,股静脉插管尖端位置在下腔静脉和右心房的交界处。采用胸部X线检查结合经胸超声(必要时经食管超声)定位静脉插管的尖端位置,股动脉插管尖端一般置于髂动脉处。VA-ECMO常规从股动脉插管处置入8 F远端灌注管,提供远端肢体的灌注,置管成功后妥善固定,连接机器,开始进行ECMO治疗。VV-ECMO置管成功后调整呼吸机参数为:(1)吸入氧浓度:21%~30%;(2)潮气量:4~6 ml/kg;(3)驱动压 <15 cm H2O(1 cm H2O=0.098 kPa);(4)呼吸末正压:8~12 cm H2O;(5)呼吸频率:5~10次/min。股静脉置入导管前3~5 min泵入肝素(30~50 U/kg)(严重的凝血功能障碍或血小板减少患者除外),然后采用微量泵维持泵入肝素,肝素泵入期间保持活化部分凝血活酶时间为55~65 s。根据不同的支持力度,ECMO血流量维持在3.5~5.0 L/min。符合以下条件可进行主动撤机:(1)VV-ECMO:原发病已控制;肺部CT明显改善;吸入氧浓度<40%;气道峰压<25 cm H2O;呼吸频率<30次/min,暂停ECMO治疗(关闭气源),观察至少1 h,复查血气分析指标正常。(2)VA-ECMO:血流量降至1 L/min,小剂量血管活性药物可以维持血液循环,评估结束恢复至原血流量。撤机拔管方式:所有静脉导管在床边拔除并缝合切口,然后按压穿刺部位30 min,再加压包扎24 h。动脉插管的处理需要前往手术室,在心脏大血管外科医生手术切开直视下拔除动脉导管,并进行缝合切口,加压包扎24 h。
1.3 观察指标 收集患者一般资料,包括性别、年龄、合并症(包括高血压、糖尿病)和治疗当天急性生理学与慢性健康状况评分系统Ⅱ(APACHEⅡ)评分、实验室检查指标〔包括总胆红素、肌酐(Cr)、尿素氮、天冬氨酸氨基转移酶(AST)、丙氨酸氨基转移酶(ALT)、降钙素原(PCT)、C反应蛋白、白细胞计数(WBC)、淋巴细胞计数、中性粒细胞计数、球蛋白(GLO)、白蛋白〕及治疗方式(VA-ECMO、VV-ECMO)、住院时间、治疗时间。统计患者最终结局,包括存活、死亡。部分患者治疗后病情仍然不可逆地恶化,家属在救治无望的情况下放弃治疗,其最终结局按照死亡判定。
1.4 统计学方法 采用SPSS 22.0统计学软件进行数据分析。符合正态分布的计量资料以(±s)表示,两组间比较采用独立样本t检验;不符合正态分布的计量资料以M(P25,P75)表示,两组间比较采用Mann-Whitney U检验;计数资料以相对数表示,因总体样本量<40例,故组间比较采用Fisher's确切概率法;患者住院期间死亡的影响因素分析采用单因素、多因素Cox回归分析。以P<0.05为差异有统计学意义。
2 结果
2.1 一般情况 35例患者中,男25例(71.4%),女10例(28.6%);平均年龄(56.3±13.9)岁;合并症:高血压10例(28.6%),糖尿病5例(14.3%);APACHEⅡ评分(27.7±6.5)分;治疗方式:VAECMO 14例(40.0%),VV-ECMO 21例(60.0%);治疗时间2~33 d,平均治疗时间7(4,11)d;住院时间2~120 d,平均住院时间22(10,34)d;最终结局:存活15例(42.9%),死亡20例(57.1%)。男性患者死亡率为68.0%(17/25),女性患者死亡率为3/10;男性患者死亡率与女性患者死亡率比较,差异无统计学意义(P=0.062)。采用VA-ECMO治疗的患者死亡率为6/14,采用VV-ECMO治疗的患者死亡率为66.7%(14/21);采用VA-ECMO治疗的患者死亡率与采用VV-ECMO治疗的患者死亡率比较,差异无统计学意义(P=0.187)。
2.2 存活患者与死亡患者一般资料比较 存活患者与死亡患者男性占比、年龄、高血压发生率、糖尿病发生率、总胆红素、Cr、尿素氮、AST、ALT、PCT、C反应蛋白、WBC、中性粒细胞计数、GLO、白蛋白、治疗方式、治疗时间比较,差异无统计学意义(P>0.05);死亡患者APACHEⅡ评分高于存活患者,淋巴细胞计数低于存活患者,住院时间短于存活患者,差异有统计学意义(P<0.05,见表1)。
2.3 患者住院期间死亡影响因素分析
2.3.1 总体患者住院期间死亡影响因素分析 以患者住院期间最终结局为因变量,分别以Cr、AST、PCT、WBC、GLO为自变量(赋值见表2),进行单因素Cox回归分析,结果显示,PCT、WBC、GLO是患者住院期间死亡的影响因素(P<0.05,见表3)。
以患者住院期间最终结局为因变量,Cr、AST、PCT、WBC、GLO为自变量,年龄(赋值:实测值)、性别(赋值:女=0,男=1)、高血压发生情况(赋值:无=0,有=1)为协变量,进行多因素Cox回归分析,结果显示,PCT、WBC是患者住院期间死亡的独立影响因素(P<0.05,见表3)。

表1 存活患者与死亡患者一般资料比较Table 1 Comparison of general data between surviving patients and dead patients
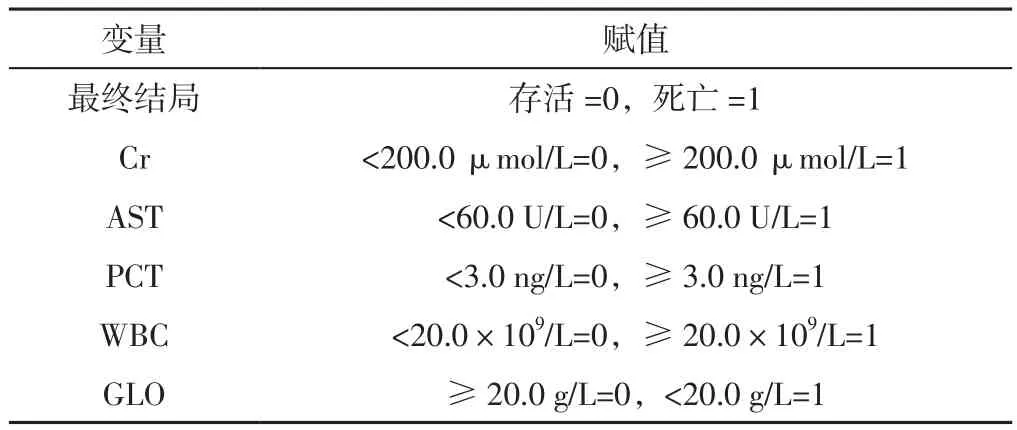
表2 患者住院期间死亡影响因素的Cox回归分析赋值Table 2 Cox regression analysis assignment for influencing factors of patients' death during hospitalization
2.3.2 不同性别患者住院期间死亡影响因素分析 以男性患者住院期间最终结局为因变量,分别以Cr、AST、PCT、WBC、GLO为自变量(赋值同表2),进行单因素Cox回归分析,结果显示,Cr、AST、PCT、WBC是男性患者住院期间死亡的影响因素(P<0.05,见表4)。以男性患者住院期间最终结局为因变量,Cr、AST、PCT、WBC、GLO为自变量,年龄(赋值:实测值)、高血压发生情况(赋值:无=0,有=1)为协变量,进行多因素Cox回归分析,结果显示,Cr、AST、PCT、WBC是男性患者住院期间死亡的独立影响因素(P<0.05,见表 4)。
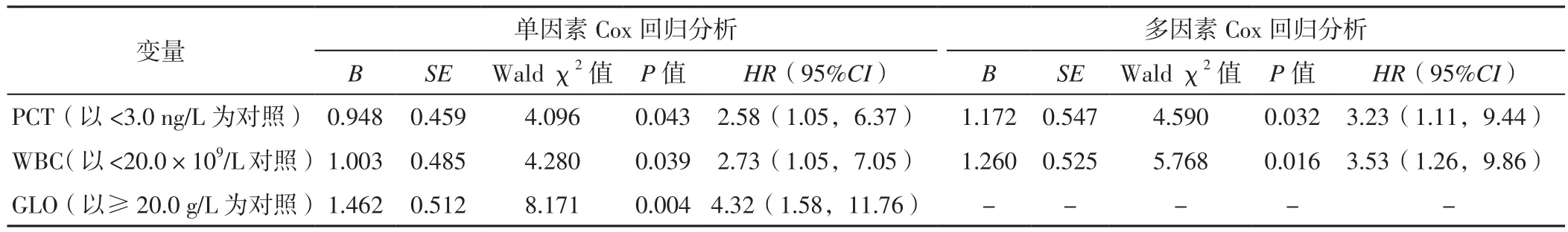
表3 患者住院期间死亡影响因素的Cox回归分析Table 3 Cox regression analysis of influencing factors of patients' death during hospitalization
以女性患者住院期间最终结局为因变量,分别以Cr、AST、PCT、WBC、GLO为自变量(赋值同表2),进行单因素Cox回归分析,结果显示,以上指标均不是女性患者住院期间死亡的影响因素(P>0.05)。以女性患者住院期间最终结局为因变量,Cr、AST、PCT、WBC、GLO为自变量,年龄(赋值:实测值)、高血压发生情况(赋值:无=0,有=1)为协变量,进行多因素Cox回归分析,结果显示,以上指标均不是女性患者住院期间死亡的独立影响因素(P>0.05)。
3 讨论
ECMO治疗常用于急性心肌梗死、重症肺炎等需要心肺支持的患者,尽管近年来其应用还存在争议,但其已逐渐应用于脓毒症休克、脓毒症心肌抑制等患者,用以提高患者的住院生存率[2]。患者预后是ECMO研究的一个方向,2017年来自体外生命支持组织(ELSO)注册中心的一项研究显示,ECMO治疗4 d或更短时间内的患者死亡率更高[11]。如果通过某些指标在ECMO治疗前就能预测患者预后,无疑有利于制定有针对性的治疗方案,进而改善患者预后。因此本研究分析了接受ECMO治疗患者预后的影响因素,以期为临床ECMO治疗提供依据。
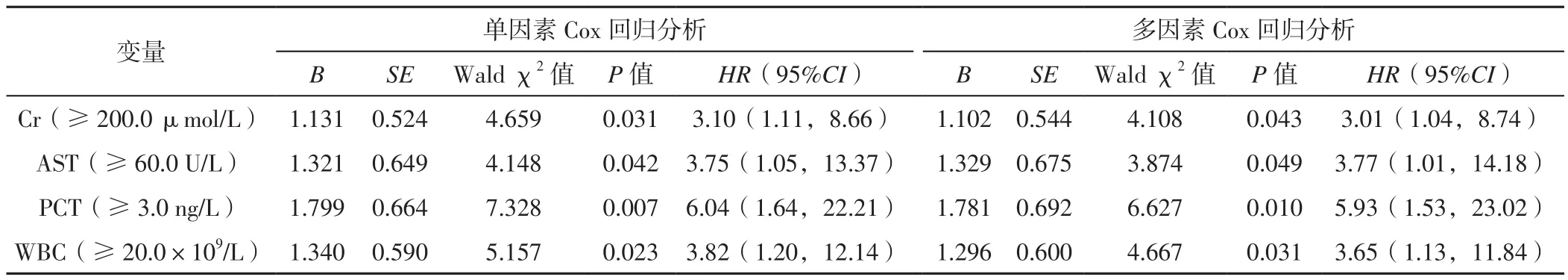
表4 男性患者住院期间死亡影响因素的Cox回归分析Table 4 Cox regression analysis of influencing factors of death in male patients during hospitalization
APACHEⅡ评分作为ICU死亡率的一项预测指标,具有良好的预测能力[12]。本研究结果显示,死亡患者APACHEⅡ评分高于存活患者,提示急性生理学与慢性健康状况可能会影响接受ECMO治疗患者的预后。死亡患者住院时间短于存活患者,究其原因主要为ECMO常用于常规治疗无效的患者,这类患者病情危重,如能存活其病情恢复耗时长,住院时间也会延长;相反,死亡患者因治疗无效很快死亡,因此住院时间短。值得注意的是,与上文提到的2017年来自ELSO注册中心的研究[11]结果不同,本研究中存活患者和死亡患者治疗时间比较无差异,其原因可能与纳入研究对象不同有关,如本研究未纳入心搏骤停后进行心肺复苏的同时使用ECMO进行补救治疗的患者,此类患者抢救成功率极低,常在治疗<24 h甚至数小时内因死亡而终止ECMO治疗。
淋巴细胞减少常提示机体处于免疫抑制状态,有研究显示,持续性淋巴细胞减少甚至可预测脓毒症早期和晚期死亡率[13]。ECMO管道植入机体后,其非生理性表面与血液接触会出现炎性反应,同时ECMO治疗时产生的再灌注性损伤也会加重全身炎性反应[14]。因此如果ECMO治疗前患者淋巴细胞计数低下,机体将难以应对炎性反应,这也解释了本研究中死亡患者淋巴细胞计数低于存活患者的原因。本研究结果提示,淋巴细胞计数减少的患者可能难以从ECMO治疗中获益,此时临床医师在选择ECMO治疗时需更加谨慎。
临床中,WBC升高提示机体出现全身或者局部炎性反应。PCT是反映细菌感染和全身炎性反应的生物标志物,与细菌性感染严重程度相关[15],其有助于监测脓毒症患者对治疗的反应[16]以及预测脓毒症患者的预后[17]。本研究结果显示,PCT、WBC是患者住院期间死亡的独立影响因素;PCT<3.0 μg/L患者存活率大于PCT≥3.0 μg/L患者,WBC<20.0×109/L患者存活率大于WBC≥20.0×109/L患者。由此可见,一旦出现细菌感染,接受ECMO治疗患者的住院死亡风险将会明显增加,提示ECMO治疗前将炎性指标作为判断依据,有助于评估患者的死亡风险。GLO代表血浆中免疫球蛋白水平,具有激活补体、参与初步免疫应答和再次免疫应答以及参与机体局部黏膜的防御感染等作用[18]。本研究结果显示,GLO是患者住院期间死亡的影响因素,且GLO<20.0 g/L患者存活率小于GLO≥20.0 g/L患者,但多因素Cox回归分析并未发现GLO是患者住院期间死亡的独立影响因素,可能与治疗过程中外源性补充GLO提高了血清GLO水平有关。后续可进一步研究GLO水平动态变化对ECMO患者预后的影响。
本研究经过性别分层分析后发现,Cr、AST、PCT、WBC是男性患者住院期间死亡的独立影响因素,Cr<200.0 μmol/L男性患者存活率大于Cr≥200.0 μmol/L男性患者,AST<60.0 U/L男性患者存活率大于AST≥60.0 U/L男性患者,PCT<3.0 μg/L男性患者存活率大于PCT≥3.0 μg/L男性患者,WBC<20.0×109/L男性患者存活率大于WBC≥20.0×109/L男性患者。其中AST和Cr代表肝功能和肾功能,提示肝肾功能异常可能会对男性患者住院死亡风险产生影响。Cr、AST、PCT、WBC、GLO均不是女性患者住院期间死亡的独立影响因素,应该与本研究中女性患者数量太少有关。后续研究需要收集更多的样本量进一步分析。
综上所述,ECMO治疗当天PCT、WBC是患者住院期间死亡的独立影响因素,ECMO治疗当天Cr、AST、PCT、WBC是男性患者住院期间死亡的独立影响因素。
作者贡献:周亮负责文章的构思设计、可行性分析,文献资料和数据的收集、整理,统计学处理和结果的分析、解释,撰写论文;周亮、邵敏负责论文、英文的修订,对文章整体负责、监督管理;邵敏、王昌会负责文章的质量控制和审校;刘念、余超、黄锐、崔良文协助文献资料的收集。
本文无利益冲突。
本研究局限性:
(1)纳入研究的患者例数较少,后续可增加患者例数进一步分析。(2)体外膜肺氧合(ECMO)基础治疗方式分为两种:静脉-静脉体外膜肺氧合(VVECMO)和静脉-动脉体外膜肺氧合(VA-ECMO),今后研究可根据疾病分类或者ECMO治疗方式的不同来讨论不同生理指标对ECMO患者预后的影响。
