气相环境下Na+催化丙氨酸分子手性转变的机理
2020-09-14陈静思徐锐英杨晓翠王佐成
李 冰,陈静思,徐锐英,潘 宇,刘 芳,杨晓翠,王佐成
(1. 白城师范学院 机械工程学院,吉林 白城 137000; 2. 白城医学高等专科学校 临床医学系,吉林 白城 137000; 3. 白城师范学院 传媒学院,吉林 白城 137000; 4. 白城师范学院 物理学院,吉林 白城 137000)
丙氨酸(Alanine, Ala)是重要的氨基酸,根据光学活性不同分为左旋丙氨酸(L-Ala)和右旋丙氨酸(D-Ala),根据构型不同分为S-型丙氨酸(S-Ala)和R-型丙氨酸(R-Ala).L-Ala对生命体具有活性,可促进葡萄糖代谢,D-Ala在手性制药中用做中间体,还有抑菌作用.已有研究表明,通常生命体内有微量的D-Ala存在,体内过量的D-Ala可引起机体衰老,导致帕金森症等[1-2].
为了解释生命体内有D-Ala存在、说明生命体内Ala可能损伤以及为在实验上实现其手性转变提供理论指导,学者们进行了广泛的研究.文献[3]的实验研究说明了Ala分子可能旋光异构.文献[4-9]的理论研究发现: α-氢以氨基氮为桥迁移是Ala实现手性转变的最具优势通道,气相反应决速步的内禀能垒是266.1kJ·mol-1,水分子簇的催化使该能垒下降到138.6kJ·mol-1.文献[10]的理论研究发现: SWBNNT(5,5)对Ala的手性转变具有限域催化作用,使决速步能垒降至201.1kJ·mol-1,SWBNNT(5,5)可作为Ala旋光异构的纳米反应器.文献[11-12]的理论研究表明,在水溶剂环境下,氨基与羧基间具有分子内单氢键和双氢键的中性Ala分子旋光异构决速步骤的能垒分别是109.61和113.37kJ·mol-1,说明了生命体内的Ala可以缓慢地旋光异构.文献[13]的理论研究表明,水与MOR(Mordenite)分子筛对Ala的手性转变具有共催化作用,水液相环境下MOR分子筛可作为Ala旋光异构的纳米反应器.文献[14]的理论研究表明,羟自由基可使处在水中的MOR分子筛内的Ala旋光异构与损伤同时发生,并且损伤过程具有明显的优势.文献[15]的理论研究表明,甲醇溶剂环境下两种稳定构象的Ala手性转变决速步的能垒分别为109.8kJ·mol-1和111.0kJ·mol-1,丙氨酸分子可以缓慢地消旋.
讨论体系的气相结构和性质能获得较为本质的物理与化学性质等信息,金属离子对生命具有重要作用,学者们针对“金属离子对氨基酸结构和性质的影响”问题开展了很多气相化学研究工作.文献[16]的研究表明,Na+、K+、Mg2+、Ca2+、Ni2+、Cu2+、Zn2+等金属离子与甘氨酸配位增加了甘氨酸结构的稳定性.Na+在维持人体细胞外流质的体积、渗透压、酸碱平衡等方面具有重要作用,对于通过细胞膜的能量传输也是必不可少的[17].氨基酸的旋光异构会对生命体的健康产生重要的影响,文献[18]研究了气相环境下Cu2+对Ala手性转变的催化作用.然而,关于Na+对Ala手性转变的研究鲜见报道,基于此,采用密度泛函理论对标题反应进行了研究.
1 研究与计算方法
采用对计算含有金属元素和弱键作用体系能量具有较高精度的杂化泛函M06方法[19],在全电子基组6-311++G(d,p)水平下优化反应过程中单重态(计算表明本工作研究的体系在可能的自旋态1、3和5中,单重态最稳定)势能面上的驻点结构(体系带电+1),计算了相关体系的NBO(natural bond orbital)电荷.通过对过渡态[20]进行IRC(内禀反应坐标)计算[21],确认过渡态连接所期望的局域稳定点.为得到较高水平的反应过程势能面,并考虑到计算成本,在M06/6-311++G(2df,pd)高角动量基组水平计算单点能.用Gtotal=Gtc+ESP计算总吉布斯自由能(其中Gtc和ESP分别为吉布斯自由能热校正和单点能,自由能矫正的温度是298.15K).Ala_1与Na+相距较远(物理上的无穷远)没相互作用时,记作Ala_1+Na+;所有通道共用的S-型Ala_1与Na+的配合物记作S-A_1;A_1在a通道的第1个过渡态记作S-TS1a_1,第1个S-型中间体记作S-I1a_1,S-TS1a(b)中的a(b)表示S-TS1为a和b通道公用,其他体系的表示方法以此类推.全部计算工作采用Gaussian09[22]程序在白城师范学院理论计算中心完成.
2 结果与讨论
把文献[4]和[6]的Ala分子两种稳定构型作为初始构型,优化后的两对手性对映体见图1,优化的Na+亦见图1.计算表明,S-Ala_2相对于S-Ala_1的吉布斯自由能是-3.0kJ·mol-1,S-Ala_2的稳定性稍好些.Na+催化S-Ala_1和S-Ala_2手性转变的机理不同,下面分别讨论:

图1 丙氨酸分子手性对映体及Na+的几何构型Fig.1 Geometric conformation of chiral enantiomer of Ala and Na+
2.1 Na+催化S-Ala_1手性转变
Na+催化S-Ala_1手性转变的反应有a、b、c和d 4个通道,反应历程及过渡态在虚频下的振动模式见图2,反应的吉布斯自由能势能剖面见图3.

图2 Na+催化S-Ala_1的手性转变历程(键长单位: nm)Fig.2 Reaction process of chiral transition of S-Ala_1 catalyzed by Na+ (unit of bond length: nm)
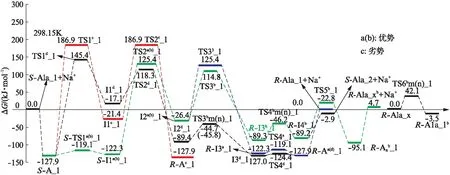
图3 Na+催化S-Ala_1手性转变反应的吉布斯自由能势能面Fig.3 Gibbs free energy surfaces of chiral enantiomer transition of S-Ala_1 catalyzed by Na+
第1基元反应(共用基元): 相距“物理无穷远”的S-Ala_1和Na+,经无势垒过程Na+和羧基的2个氧配位,形成底物配合物S-A_1.配合物S-A_1与S-Ala_1和Na+体系的相对吉布斯自由能是-127.9kJ·mol-1,亦即S-A_1的结合能为127.9kJ·mol-1,其构象十分稳定,很难解离成S-Ala_1和Na+.
对于a,b通道,第2、3基元反应公用.
第2基元反应:S-A_1经12H向6N迁移的过渡态S-TS1a(b)_1,构型异构成中间体配合物S-I1a(b)_1.从S-A_1到S-TS1a(b)_1过程,10O—12H键长从0.1005nm拉伸至0.1312nm断裂,S-TS1a(b)_1产生的内禀能垒是8.8kJ·mol-1.

接下来的反应历程分为a和b通道.
a通道:
第4基元反应: I2a(b)_1经13H从11O在纸面里向1C迁移的过渡态TS3a_1,构型异构成中间体产物配合物R-I3a_1,至此S-A1实现了手性转变.从I2a(b)_1到TS3a_1过程,11O—13H键从0.0966拉伸至0.1211nm断裂,11O—13H的拉伸幅度小于前一基元1C—13H键的拉伸,又O—H键较C—H键容易断裂,TS3a_1产生的内禀能垒是151.8kJ·mol-1.该能垒小于TS2a(b)_1产生的内禀能垒许多原因是O—H键较C—H键容易断裂,并且从I2a(b)_1到TS3a_1过程O—H键的拉伸幅度小.
第5基元反应:R-I3a_1经8H向6N迁移的过渡态R-TS4a_1,构型异构得到产物配合物R-Aa_1.结构分析表明,R-Aa_1和S-A_1的构象镜像对称,S-A_1实现了手性对映体转变.从R-I3a_1到TS4a_1过程,6N—8H键长从0.1054拉伸至0.1214nm断裂,6N—8H键的拉伸小于第2基元10O—12H键长的拉伸,TS4a_1产生的内禀能垒是3.2kJ·mol-1,小于S-TS1a(b)_1产生的内禀能垒.
第6基元反应:R-Aa_1获得127.9kJ·mol-1的能量后解离成R-Ala_1a和Na+.结构分析表明,R-Ala_1a和S-Ala_1的构象镜像对称,至此S-Ala_1实现了手性对映体转变.解离历程同于d通道第6基元反应,为节省篇幅,在本通道反应历程中没有给出.
b通道:
第4基元反应: I2a(b)_1经8H从6N在纸面里向1C迁移的过渡态TS3b_1,构型异构成中间体产物配合物R-I3b_1,S-A1实现手性转变.从I2a(b)_1到TS3b_1过程,6N—8H键从0.1026拉伸至0.1235nm 断裂,6N—8H键的拉伸幅度大于从I2a(b)_1到TS3b_1过程1C—13H键的拉伸,TS3b_1产生的内禀能垒是141.2kJ·mol-1.这与裸环境下此基元的能垒106.5kJ·mol-1[6]相比较明显升高,说明Na+对此基元反应具有显著的负催化作用.原因是Na+与羰基氧的配位导致I2a(b)_1的8H的NBO电荷从0.436e增加到0.460e,6N的NBO电荷基本没变,1C的NBO电荷从-0.245e降到-0.170e.这导致了6N对8H的库仑引力增加,1C对8H的库仑减小,从而8H向1C迁移所需的能量增加.
第5基元反应:R-I3b_1经9C—11O键内旋转的过渡态R-TS4bm_1或R-TS4bn_1,构象异构得到中间体配合物R-I4b_1.从R-I3b_1到R-TS4mb_1或R-TS4mb_1过程,键内旋转所需能量不多,R-TS4bm_1和R-TS4bn_1产生的内禀能垒分别是43.1和43.0kJ·mol-1.R-I4b_1获得86.3kJ·mol-1的能量后解离成S-Ala_2和Na+,至此完成了S-Ala_1向S-Ala_2的异构.
第6基元反应:R-I4b_1经羧基内质子迁移的过渡态R-TS5b_1,实现了13H从11O迁移到10O,得到产物配合物R-Axb_1.从R-I4b_1到R-TS5b_1过程,11O—13H键长从0.0972拉伸至0.1317nm断裂,R-TS5b_1产生的内禀能垒是112.0kJ·mol-1.
第7基元反应:R-Axb_1获得99.8kJ·mol-1的能量后解离成R-Ala_xb和Na+.
第8基元反应:R-Ala_xb经羧羟基旋转的过渡态R-TS6bm或R-TS6bn,实现了羧基从顺式平面结构向反式平面结构的异构,构型异构成R-Ala_1b,结构分析表明,R-Ala_1b和S-Ala_1的构象镜像对称,至此S-Ala_1实现了手性对映体转变.此基元反应是9O—10C键内旋转,能垒很低,R-TS6bm和R-TS6bn产生的能垒是42.1和51.3kJ·mol-1(篇幅所限,图3没有给出此基元反应的势能面).
对于c通道:

第3基元反应: I1c_1经13H从11O在纸面里向1C迁移的过渡态TS2c_1,异构成中间体配合物R-A1c_1.结构分析表明,R-A1c_1和S-A_1的构象镜像对称,S-A_1实现了手性对映体转变.从I1c_1到TS2c_1,11O—13H键从0.0966拉伸至0.1284nm断裂,TS2c_1产生的内禀能垒是204.0kJ·mol-1.
第4基元反应:R-Ac_1获得127.9kJ·mol-1的能量后解离成R-Ala_1c和Na+.结构分析表明,R-Ala_1c和S-Ala_1的构象镜像对称,至此S-Ala_1实现了手性对映体转变.解离历程同于d通道第6基元反应,为节省篇幅,在本通道反应历程中没有给出.
对于d通道:
第2基元反应:S-A_1经13H从1C向6N迁移的过渡态TS1d_1,构型异构成中间体产物配合物 I1d_1.从S-A_1到TS1d_1过程,1C—13H键从0.1100nm拉伸至0.1374nm断裂,反应活性中心骨架二面角6N—1C—4C—9C从121.1°变为153.2°,骨架形变31.2°,需要一定的能量,TS1d_1产生了273.3kJ·mol-1的内禀能垒,这比裸环境下此基元的能垒326.9kJ·mol-1[6]明显降低,说明Na+对此基元反应较好的催化作用.原因相似与a和b通道的第3基元反应,不再赘述.
第3基元反应: I1d_1经8H从6N在纸面里向1C迁移的过渡态TS2d_1,构型异构成中间体产物配合物R-I2d_1.从I1d_1到TS2d_1过程,6N—8H键从0.1027nm拉伸至0.1222nm断裂,N—H健拉伸不是很长,所需能量不多,TS2d_1产生了135.4kJ·mol-1的内禀能垒.这与裸环境下此基元的能垒106.5kJ·mol-1[6]相比较有所升高,说明Na+对此基元反应具有一定的负催化作用.
第4基元反应:R-I2d_1经羧羟基旋转与氨基左右翻转协同进行的过渡态R-TS3md_1或R-TS3nd_1,构象异构得到中间体配合物R-I3d_1.从R-I2d_1到R-TS3md_1过程,10O—9C键内旋转,二面角12H—10O—9C—11O从-1.01°变为-90.13°,化学键的内旋转所需能量较少,R-TS3md_1产生的内禀能垒是44.7kJ·mol-1,相似的R-TS3nd_1产生的内禀能垒是43.6kJ·mol-1.
第5基元反应:R-I3d_1经键角9C—11O—14Na做剪式运动的过渡态R-TS4d_1,构象异构得到产配合物R-Ad_1.从R-I3d_1到过渡态R-TS4d_1,键角9C—11O—14Na从140.8°收缩到125.7°,键角的小幅改变需要的能量很小,R-TS4d_1产生的内禀能垒只有2.6kJ·mol-1,此基元反应可视为无势垒反应.
第6基元反应:R-Ad_1获得127.9kJ·mol-1的能量后解离成R-Ala_1d和Na+.结构分析表明,R-Ala_1d和S-Ala_1的构象镜像对称,至此S-Ala_1实现了手性对映体转变.
从图3可以看出,Na+催化S-Ala_1手性转变反应的a和b通道具有优势,反应的总包能垒是 125.4kJ·mol-1.这远远低于单体Ala手性转变优势通道的总包能垒274.26kJ·mol-1[7],说明Na+对S-Ala_1的手性转变具有极好的催化作用,通常情况下S-Ala_1可在该通道少量或微量地实现手性转变.从图3还可以看出,S-A_1、S-I1a(b)_1、R-I3a_1和R-A1a_1都在势阱最底部,构象很稳定.S-A_1和S-I1a(b)_1之间相互异构的能垒很低,在反应物配合物中是它们两者共存,只是前者的分布高些.相似的,R-I3a_1和R-Aa_1在产物配合物中也是它们两者共存,只是后者的分布高些.c通道最具劣势,反应的总包能垒是186.9kJ·mol-1,由于能垒太高,该通道只在理论上存在.d通道上反应的总包能垒是145.4kJ·mol-1,通常情况下S-Ala_1可在该通道痕量地实现手性转变.
2.2 Na+催化S-Ala_2的手性对映体转变
Na+催化S-Ala_2的手性转变反应有2个通道a和b,反应历程及过渡态在虚频下的振动模式见图4,反应过程的相对吉布斯自由能剖面见图5.
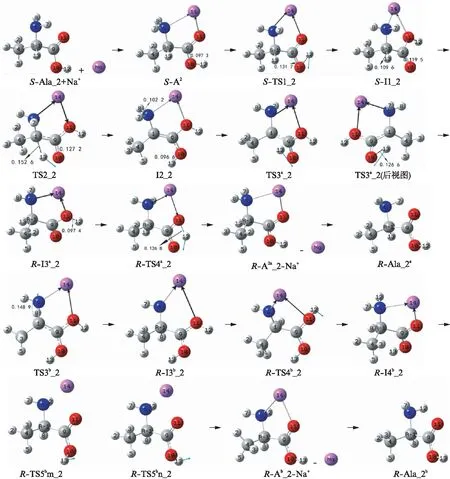
图4 Na+催化S-Ala_2的手性转变历程(键长单位: nm)Fig.4 Reaction process of chiral transition of S-Ala_2 catalyzed by Na+ (unit of bond length: nm)
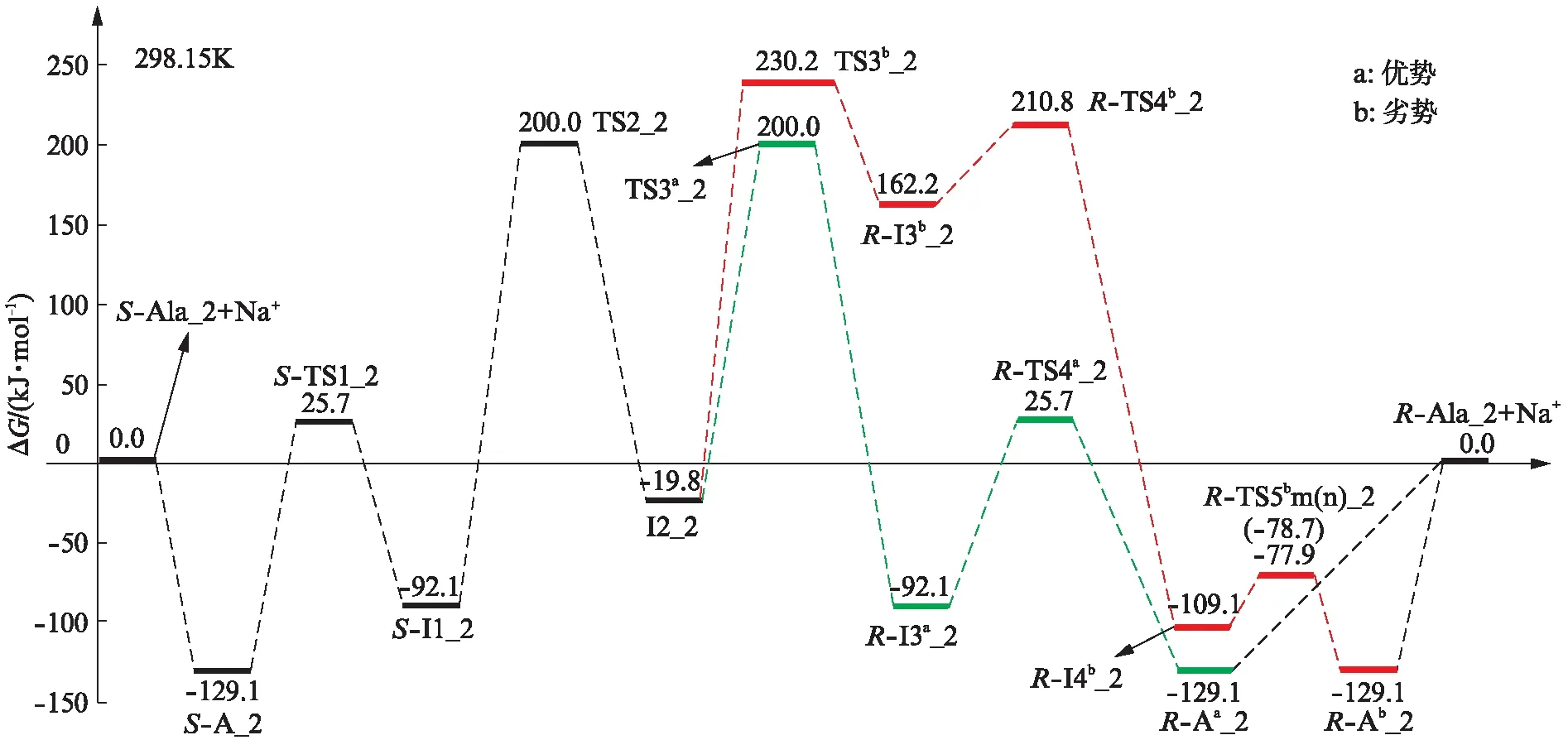
图5 Na+催化S-Ala_2手性转变反应的吉布斯自由能势能面Fig.5 Gibbs free energy surfaces of chiral enantiomer transition of S-Ala_2 catalyzed by Na+
第1和第2基元反应为a、b通道共用.
第1基元反应,相距“物理无穷远”的S-Ala_2和Na+,经过无势垒过程,Na+和羰基氧11O和氨基氮6N配位,形成底物配合物S-A_2,S-A_2的结合能是129.1kJ·mol-1,构象稳定.
第2基元反应,S-A_2经羧基内H迁移的过渡态S-TS1_2,异构成中间体S-I1_2.从S-A_2到S-TS1_2,10O—12H键长从0.0973nm拉伸至0.1317nm断裂,O—H键的拉伸断裂需要一定的能量,S-TS1_2产生的能垒是154.8kJ·mol-1.这与裸环境下此基元的能垒195.1kJ·mol-1[5]相比较明显降低,说明Na+对此基元反应具有一定的催化作用,原因相似与从S-I1a(b)_1经TS2a(b)_1到I2a(b)_1过程,不再赘述.

接下来的I2_2异构分为a和b两个路径.
对于a路径:
第4基元反应,I2_2经过渡态TS3a_2,实现了13H在纸面里从质子化羧基向α-碳的迁移,异构成R-I3a_2,至此S-A_2实现了手性转变.从I2_2到TS3a_2过程,10O—13H键长从0.0966nm拉伸至0.1266nm 断裂,O—H键较大幅度的拉伸断裂需要较高的能量,TS3a_2产生的能垒是 219.8kJ·mol-1.这与裸环境下此基元的能垒213.9kJ·mol-1[5]相差无几,说明Na+对此基元反应基本没影响.
第5基元反应,R-I3a_2经和S-TS1_2相似的过渡态R-TS4a_2,实现了12H在羧基内的回迁,异构成R-Aa_2.从R-I3a_2到R-TS4a_2过程,11O—12H键长从0.0974nm拉伸至0.1268nm断裂,R-TS4a_2产生的能垒是117.8kJ·mol-1.结构分析表明,R-Aa_2和S-A_2的构象镜像对称,至此S-A_2实现了手性对映体转变.
第6基元反应,R-Aa_2获得129.1kJ·mol-1的能量解离成R-Ala_2a和Na+,结构分析表明,R-Ala_2a和S-Ala_2的构象镜像对称,至此S-Ala_2实现了手性对映体转变.
对于b路径:
第4基元反应,I2_2经8H在纸面里从氨基氮6N向α-碳1C迁移的过渡态TS3b_2,构型异构成中间体R-I3b_2,至此,S-A_2在b通道实现了手性转变.从I2_2到TS3b_2过程,8H—6N键长从0.1022nm拉伸至0.1489nm断裂,TS3b_2产生的能垒是250.0kJ·mol-1.这与裸环境下此基元的能垒 106.5kJ·mol-1[6]相比较明显升高,说明Na+对此基元反应具有显著的负催化作用.原因是Na+与羰基氧和氨基氮的配位导致I2_2与其单体相比较,8H的NBO电荷从0.385e增加到0.420e,6N的NBO电荷从0.894e增加到0.990e,1C的NBO电荷从-0.245e降到-0.170e,6N—8H键长从0.1335nm增加到0.1450nm.这导致了6N对8H的库仑引力增加,1C对8H的库仑减小,从而8H向1C迁移所需的能量增加.
第5基元反应,R-I3b_2经9C—11O键俯视逆时针内旋转的过渡态TS4b_2,异构成中间体配合物R-I4b_2.从R-I3b_2到TS4b_2过程,二面角12H—11O—9C—10O从2.80°变为98.36°.化学键的内旋转所需能量不高,TS4b_2产生的能垒是48.6kJ·mol-1.
第6基元反应,R-I4b_2经9C—10O键内旋转的过渡态R-TS5bm_2或R-TS5bn_2,构型异构成产物配合物R-Ab_2.从R-I4b_2到R-TS5bm_2或R-TS5bn_2过程,相似与前一基元,化学键的内旋转所需能量不高,R-TS5bm_2和R-TS5bn_2产生的能垒分别是31.1和30.3kJ·mol-1.结构分析表明,R-Ab_2和S-A_2的构象镜像对称,至此S-A_2实现了手性对映体转变.
第7基元反应,R-Ab_2获得129.1kJ·mol-1的能量解离成R-Ala_2b和Na+,结构分析表明,R-Ala_2b和S-Ala_2的构象镜像对称,至此S-Ala_2实现了手性对映体转变.从图5可以看出,Na+催化S-Ala_2手性转变反应的a通道具有优势,反应的总包能垒是200.0kJ·mol-1.这远远低于单体Ala手性转变优势通道的总包能垒381.4kJ·mol-1[5],说明Na+对S-Ala_2的手性转变具有极好的催化作用.200.0kJ·mol-1的能垒很高,通常情况下S-A_2构象很稳定.从图3还可以看出,在反应物配合物中主要是S-A_2,在产物配合物中主要是R-Aa_2.
3 结 论
在M06/6-311++G(2df,pd)//M06/6-31++G(d,p)双水平,研究了气相环境下Na+催化Ala两种稳定构型的手性转变,得到如下结论:
(1) Ala_1的手性转变有a、b、c和d 4个通道,a是羧羟基氢迁移后α-氢以羰基氧为桥迁移,b是羧羟基氢迁移后α-氢向羰基氧迁移再接质子从质子化氨基向α-碳迁移,c和d是α-氢分别以氨基氮和羰基氧为桥迁移.Ala_2的手性转变有2个通道a和b,a是α-氢只以羰基氧为桥迁移,b是α-氢迁移到羰基氧后氨基上的质子再向α-碳迁移.
(2) Na+的存在改变了Ala分子的不同原子的电荷分布,Na+对Ala手性转变反应的作用,有的基元反应表现为正催化,有的基元反应则表现为负催化,对整个反应过程表现为正催化.
(3) Ala_1手性转变的优势通道是a和b,反应的总包能垒是125.4kJ·mol-1.Ala_2手性转变的优势通道是a,反应的总包能垒是200.0kJ·mol-1.
结果表明: 通常情况下Na+的催化可使S-Ala_1在a通道少量或微量地实现手性对映体转变,在d通道痕量地实现手性转变;S-Ala_2不能实现对映体手性转变.
