三唑类抗真菌药物泊沙康唑注射液无菌检查方法研究
2020-09-10陈青连
陈青连,姚 振,万 超
(杭州澳亚生物技术有限公司,浙江 杭州 310018)
三唑类抗真菌药物(如伏立康唑和泊沙康唑)抗真菌谱广,抗菌效力强[1],对念珠菌属(包括耐氟康唑的克柔念珠菌、光滑念珠菌和白念珠菌耐药株)具有抗菌作用,对所有检测的曲菌属真菌均有杀菌作用[2],属注射剂类制剂。为确保用药安全,质量标准规定应作无菌检查,但由于此类药物抗菌活性很强,因此,如何消除其抑菌性,使检验顺利进行,建立方法极重要,也较困难[3]。2015 年版《中国药典(四部)》对无菌产品控制与国际标准趋于一致,实现了与国际人用药品注册技术协调会(ICH)的要求统一协调[4]。同时,2015 年版《中国药典》编制大纲强调,要加强药品无菌检查方法的建立与验证方面的标准研究工作[5]。本研究中对抗真菌药物制剂泊沙康唑注射液进行了试验研究,主要针对冲洗液、过滤膜材质、流速、冲洗量、阳性对照菌的选择及加入顺序等全过程进行考察,建立了三唑类抗真菌药泊沙康唑注射液的无菌检查方法,并进行了方法适用性验证。现报道如下。
1 仪器与试药
1.1 仪器
ClassⅡType AIB3 型生化培养箱(广东泰宏群科学仪器股份有限公司);DGB330/DGB220 型一次性全封闭集菌培养器(浙江泰林生物技术股份有限公司);HTY-2000B 型智能集菌仪(杭州泰林生物技术设备有限公司);KB115 E3-1 型低温生化培养箱(德国宾得公司),GSP-9270MBE 型隔水式恒温培养箱(上海博迅实业有限公司医疗设备厂);XG1.DTE-0.6 型脉动真空干燥灭菌器(山东新华医疗器械股份有限公司);尼龙膜(上海兴亚净化材料厂);混合纤维素脂膜(上海兴亚净化材料厂);PVDF 膜(上海半岛实业有限公司净化器材厂)。
1.2 试药
泊沙康唑注射液(杭州澳亚生物技术有限公司,批号分别为19042311,19042511,19042611,规格为每支16.7 mL ∶300 mg);硫乙醇酸盐流体培养基(批号为190429),0.9%无菌氯化钠溶液(含0.1%聚山梨酯80,pH 3.8,批号为190305),均为杭州澳亚生物技术有限公司自制;胰酪大豆胨液体培养基(青岛高科技工业园海博生物技术有限公司,批号为20190328);无菌0.9%氯化钠溶液(山东齐都药业有限公司,批号为2A18090803)。
1.3 菌株
金黄色葡萄球菌Staphylococcus aureus[CMCC(B)26 003],铜绿假单胞菌Pseudomonas aeruginosa[CMCC(B)10 104],大肠埃希菌Escherichia coli[CMCC(B)44 102],枯草芽孢杆菌Bacillus subtilis[CMCC(B)63 501],生孢梭菌Clostridium sporogenes[CMCC(B)64 941],白色念珠菌Candida albicans[CMCC(F)98 001],黑曲霉Aspergillus niger[CMCC(F)98 003],均购自中国药品生物制品检定所菌种室,按2015 年版《中国药典(四部)》附录要求将以上7 种验证菌配制成每1 mL 含菌数小于100 cfu 的菌悬液[6]。
2 方法与结果
2.1 菌液制备和培养基检查
2.1.1 菌液制备
分别接种金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌和大肠埃希菌的新鲜培养物至胰酪大豆胨液体培养基中或胰酪大豆胨琼脂培养基中,接种生孢梭菌的新鲜培养物至硫乙醇酸盐流体培养基中,30~35 ℃培养18~24 h;接种白色念珠菌的新鲜培养物至沙氏葡萄糖液体培养基中,20~25 ℃培养24~48 h。上述培养物用无菌0.9%氯化钠溶液制成每1 mL 含菌数小于100 cfu的菌悬液。
接种黑曲霉的新鲜培养物至沙氏葡萄糖琼脂斜面培 养 基 上,20~25 ℃培 养5~7 d,加 入3~5 mL 含0.05%聚山梨酯80 的无菌0.9%氯化钠溶液,将孢子洗脱。然后采用适宜方法吸出孢子悬液至无菌试管内,用含0.05%聚山梨酯80 的无菌0.9%氯化钠溶液制成1 mL 含孢子数小于100 cfu 的孢子悬液。
菌悬液若在室温下放置,应在2 h 内使用;若保存在2~8 ℃可在24 h 内使用。黑曲霉孢子悬液可保存在2~8 ℃,在验证过的贮存期内使用。
2.1.2 培养基无菌性和灵敏度检查
培养基无菌性检查:取2 种培养基,各5 支,硫乙醇酸盐流体培养基置30~35 ℃环境下培养,胰酪大豆胨液体培养基置20~25 ℃环境下培养,均培养14 d。结果无菌生长,即所用培养基无菌性检查符合验证要求。
培养基灵敏度检查:取每管装量为12 mL 的硫乙醇酸盐流体培养基7 支,分别接种小于100 cfu 的金黄色葡萄球菌、铜绿假单孢菌、生孢梭菌各2 支。另1 支不接种,作为空白对照,培养3 d。取每管装量为9 mL 的胰酪大豆胨液体培养基7 支,分别接种小于100 cfu 的枯草芽孢杆菌、白色念珠菌、黑曲霉各2 支,另1 支不接种,作为空白对照,培养5 d。结果空白对照管无菌生长,接种菌液的培养基均生长良好,即所用培养基的灵敏度检查符合验证要求。
2.2 无菌检查方法建立
2.2.1 冲洗液选择
取泊沙康唑注射液1 瓶,加入pH 7.0 无菌氯化钠-蛋白胨缓冲液、0.1%无菌蛋白胨水溶液、0.9%氯化钠注射液、无菌0.9%氯化钠溶液(含0.1%聚山梨酯80,pH 3.8)和SBECD 溶液(pH 3.5)。5 种冲洗液各20 mL,观察混合过程中的性状变化,初步筛选可使用的冲洗液,结果pH 7.0 无菌氯化钠-蛋白胨缓冲液,0.1%无菌蛋白胨水溶液,0.9%氯化钠注射液均析出白色絮状物;无菌0.9% 氯化钠溶液(含0.1% 聚山梨酯80,pH 3.8),SBECD 溶液(pH 3.5)溶液澄清。
由于泊沙康唑注射液pH 为2.0~3.0,pH 7.0 无菌氯化钠-蛋白胨缓冲液、0.1%无菌蛋白胨水溶液和0.9%氯化钠注射液的pH 接近中性,采用该冲洗液进行冲洗时会使泊沙康唑注射液样品析出,导致析出物残留在膜上,抑制微生物的生长。马仕洪等[7]的报道指出,泊沙康唑注射液无菌检查用稀释液pH 的筛选,pH 在3.45~3.8 范围内微生物生长良好,故初步选择pH 3.8的无菌0.9%氯化钠溶液(含0.1%聚山梨酯80)和泊沙康唑注射液处方中的助溶剂辅料磺丁基倍他环糊精钠(调节pH 至3.5~3.8)作为冲洗液进行无菌检查方法学适用性研究。
2.2.2 冲洗量选择
预试验方案1:供试品组中,取供试品20 支,每10 支稀释至500 mL pH 3.8 的无菌0.9%氯化钠溶液(含0.1%聚山梨酯80)中,先用约20 mL pH 3.8 的无菌0.9%氯化钠溶液(含0.1%聚山梨酯80)润湿集菌管,吸取供试品置集菌器中,过滤,每管先用900 mL pH 3.8 的无菌0.9%氯化钠溶液(含0.1%聚山梨酯80)冲洗,分次冲洗,每次100 mL,再用无菌0.9% 氯化钠注射液冲洗,每管的冲洗量为100 mL,分次冲洗,每次100 mL,试验完成后,在生物安全柜里,往每个滤管加入小于100 cfu/mL 的白色念珠菌、黑曲霉菌各1 mL,置20~25 ℃培养,培养时间不超过5 d。
预试验方案2:供试品组中,取供试品20 支,每10 支稀释至500 mL SBECD 溶液(pH 3.5)中,先用约20 mL SBECD 溶液(pH 3.5)润湿集菌管,吸取供试品置集菌器中,过滤,每管先用300 mL SBECD 溶液(pH 3.5)冲洗,分次冲洗,每次50 mL(每次需振荡2 min),再用0.9%氯化钠注射液冲洗,每管冲洗量为700 mL,分次冲洗,每次100 mL,然后在生物安全柜里,往每个滤管加入小于100 cfu/mL 的白色念珠菌、黑曲霉菌各1 mL,置20~25 ℃培养,培养时间不超过5 d。
预试验方案3:供试品组中,取供试品20 支,每10 支稀释至500 mL SBECD 溶液(pH 3.5)中,先用约20 mL SBECD 溶液(pH 3.5)润湿集菌管,吸取供试品置集菌器中,过滤,每管先用500 mL SBECD 溶液(pH 3.5)冲洗,分次冲洗,每次50 mL(每次需振荡2 min),再用0.9%氯化钠注射液冲洗,每管冲洗量为500 mL,分次冲洗,每次100mL,试验完成后,在生物安全柜里,往每个滤管加入小于100 cfu/mL 的白色念珠菌、黑曲霉菌各1 mL,置20~25 ℃培养,培养时间不超过5 d。
预试验方案4:供试品组中,取供试品20 支,每10 支稀释至500 mL SBECD 溶液(pH 3.5)中,先用约20 mL SBECD 溶液(pH 3.5)润湿集菌管,吸取供试品置集菌器中,过滤,每管先用700 mL SBECD 溶液(pH 3.5)冲洗,分次冲洗,每次50 mL(每次需振荡2 min),再用0.9%氯化钠注射液冲洗,每管冲洗量为300 mL,分次冲洗,每次100 mL,试验完成后,在生物安全柜里,往每个滤管加入小于100 cfu/mL 的试验菌(白色念珠菌、黑曲霉菌)各1 mL,置20~25 ℃培养,培养时间不超过5 d。阳性对照组中,另取滤管,不过滤供试液。分别向每个管中加入胰酪大豆胨液体培养基100 mL,作为阳性对照。试验完成后,在生物安全柜里,往每个滤管加入小于100 cfu/mL 的试验菌(白色念珠菌、黑曲霉菌)各1 mL,将含培养基的容器置20~25 ℃培养,培养时间不超过5 d。阴性对照组中,取相应方案的稀释剂、冲洗液,同法操作,然后加入胰酪大豆胨液体培养基100 mL,不加对照菌液,置20~25 ℃培养,培养时间不超过5 d。
结果分析:结果见表1。可见,方案1 采用无菌0.9%氯化钠溶液(含0.1%聚山梨酯80,pH 3.8)作为冲洗液,白色念珠菌和黑曲霉菌均未生长;方案2 至方案4 采用不同梯度的SBECD 溶液(pH 3.5)冲洗液进行冲洗,结果显示,SBECD 溶液(pH 3.5)用量越大,白色念珠菌和黑曲霉菌生长情况越好;方案4 为较优选方案,但白色念珠菌在供试品中的长势略弱于阳性对照组中菌的长势,故继续对该方法进行优化。

表1 冲洗量的选择预试验结果
2.2.3 过滤膜材质选择
1)高效液相色谱(HPLC)法
鉴于泊沙康唑注射液有强烈的抗真菌作用,无菌检查时如何有效地冲洗掉滤膜上残留的药物,从而降低抗真菌活性十分关键。滤膜的成分、结构和性能决定了其应用范围,在2.2.2 项下预试验方案4 的基础上,考察不同材质滤膜对泊沙康唑注射液的吸附性差异,结果尼龙膜、混合纤维素脂膜和PVDF 膜过滤后膜上的样品残留量分别为0.035 7,0.003 5,0.117 5 mg/mL。故选择残留量较小的滤膜材质进行无菌检查适用性试验。
2)无菌检查方法学适用性预试验
同步取混合纤维素脂膜、尼龙膜和PVDF 膜材质的集菌器进行无菌检查方法学适用性预试验。
供试品组:取供试品20 支,每10 支稀释至500 mL SBECD 溶液(pH 3.5)中,先用约20 mL SBECD 溶液(pH 3.5)润湿集菌管,吸取供试品置集菌器(混合纤维素脂膜、尼龙膜和PVDF 膜)中,过滤,每管先用700 mL SBECD 溶液(pH 3.5)冲洗,分次冲洗,每次50 mL,再用0.9%氯化钠注射液冲洗,每管冲洗量为300 mL,分次冲洗,每次100 mL。试验完成后,在生物安全柜里,往每个滤管加入小于100 cfu/mL 的试验菌(白色念珠菌、黑曲霉菌)各1 mL,置20~25 ℃培养,培养时间不超过5 d。
阳性对照组:另取滤管,不过滤供试液。然后分别向每个管中加入胰酪大豆胨液体培养基100 mL,作为阳性对照。试验完成后,在生物安全柜里,往每个滤管加入小于100 cfu/mL 的试验菌(白色念珠菌、黑曲霉菌)各1 mL,将含培养基的容器置20~25 ℃培养,培养时间不超过5 d。
阴性对照组:取稀释剂、冲洗液,同法操作,然后加入胰酪大豆胨液体培养基100 mL,不加对照菌液,置20~25 ℃培养,培养时间不超过5 d。
3)结果分析
结果见表2。可见,不同材质的滤膜对泊沙康唑的吸附程度不一致,其中以混合纤维素脂膜材质的滤膜吸附最小,且通过无菌检查方法学适用性验证预试验确认,采用混合纤维素脂膜的结果最优,因此,选用混合纤维素脂膜材质的薄膜过滤器进行正式的方法学适用性验证。
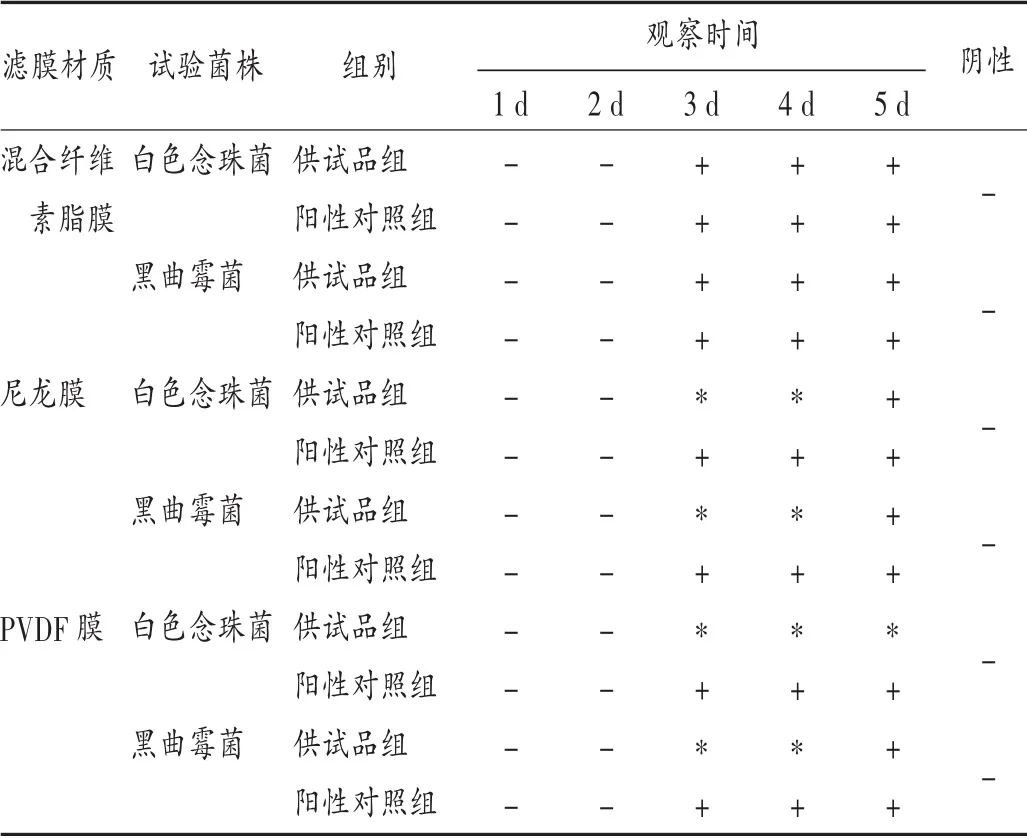
表2 3 种不同材质滤膜对泊沙康唑注射液方法学适用性预试验结果
2.3 无菌检查方法适用性验证
2.3.1 验证方法
供试品阳性对照组(PPC):取3 批供试品,每批60 瓶,每10 瓶供试品稀释至500 mL SBECD 溶液(pH 3.5)中,每10 瓶供试品接种于1 个集菌管;先用约20 mL SBECD溶液(pH 3.5)润湿滤筒,再吸取供试品置集菌器中,每管用SBECD 溶液(pH 3.5)冲洗,冲洗量为700 mL,分次冲洗,每次100 mL,再用0.9%氯化钠注射液冲洗,每管冲洗量300 mL,分次冲洗,每次100 mL。然后分别向每个管中加入相应培养基(培养细菌的3 管加入硫乙醇酸盐流体培养基,培养真菌的3 管加入胰酪大豆胨液体培养基)100 mL。试验完成后,在生物安全柜里,往每个滤管加入小于100 cfu/mL 的试验菌各1 mL(硫乙醇酸盐流体培养基加入金黄色葡萄球菌、大肠埃希菌和生孢梭菌,胰酪大豆胨液体培养基加枯草芽孢杆菌、白色念珠菌和黑曲霉),置规定温度(30~35 ℃、20~25 ℃)培养,培养时间不超过5 d。
阳性对照组(PC):另取滤管,不过滤供试液。然后分别向每个管中加入相应培养基,作为阳性对照。试验完成后,在生物安全柜里,往每个滤管加入小于100cfu/mL 的试验菌各1 mL,将含培养基的容器置规定温度(30~35 ℃、20~25 ℃)培养,培养时间不超过5 d。
阴性对照组:另取滤管,不过滤供试液,每管先用SBECD 溶液(pH 3.5)冲洗,冲洗量为700 mL,分次冲洗,每次100 mL,再用0.9%氯化钠注射液进行冲洗,每管冲洗量为300 mL,分次冲洗,每次100 mL。然后分别加入硫乙醇酸盐流体培养基和胰酪大豆胨液体培养基各100 mL,不加对照菌液,将含培养基的容器置规定温度(30~35 ℃、20~25 ℃)培养,培养时间为不超过5 d。
冲洗液阳性对照组(PPC):另取滤管,不过滤供试液,每管先用SBECD 溶液(pH 3.5)冲洗,冲洗量为700mL,分次冲洗,每次100 mL,再用0.9%氯化钠注射液冲洗,每管冲洗量为300 mL,分次冲洗,每次100 mL。然后分别加入硫乙醇酸盐流体培养基和胰酪大豆胨液体培养基各100 mL,作为冲洗液阳性对照组。试验完成后,在生物安全柜里,往每个滤管加入小于100 cfu/mL 的试验菌各1 mL,将含培养基的容器置规定温度(30~35 ℃、20~25 ℃)培养,培养时间不超过5 d。
2.3.2 结果分析
根据3 批泊沙康唑注射液和冲洗液方法学适用性试验结果,金黄色葡萄球菌、大肠埃希菌、生孢梭菌、枯草芽孢杆菌、白色念珠菌与黑曲霉供试品与阳性对照组中菌的长势一致。结果见表3 和表4。取3 批供试品,每批60 瓶,每10 瓶供试品稀释至500 mL SBECD 溶液(pH 3.5)中,每10 瓶供试品接种于1 个集菌管;先用约20 mL SBECD 溶液(pH 3.5)润湿滤筒,再吸取供试品置集菌器中,每管用SBECD 溶液(pH 3.5)冲洗,冲洗量为700 mL,分次冲洗,每次100 mL,再用0.9%氯化钠注射液冲洗,每管冲洗量为300 mL,分次冲洗,每次100 mL。然后分别向每个管中加入相应培养基(培养细菌的3 管加入硫乙醇酸盐流体培养基,培养真菌的3 管加入胰酪大豆胨液体培养基)100 mL。根据检查结果,金黄色葡萄球菌、大肠埃希菌、生孢梭菌、枯草芽孢杆菌、白色念珠菌与黑曲霉供试品与阳性对照中菌的长势一致,故本品可采用该方法进行无菌检查。
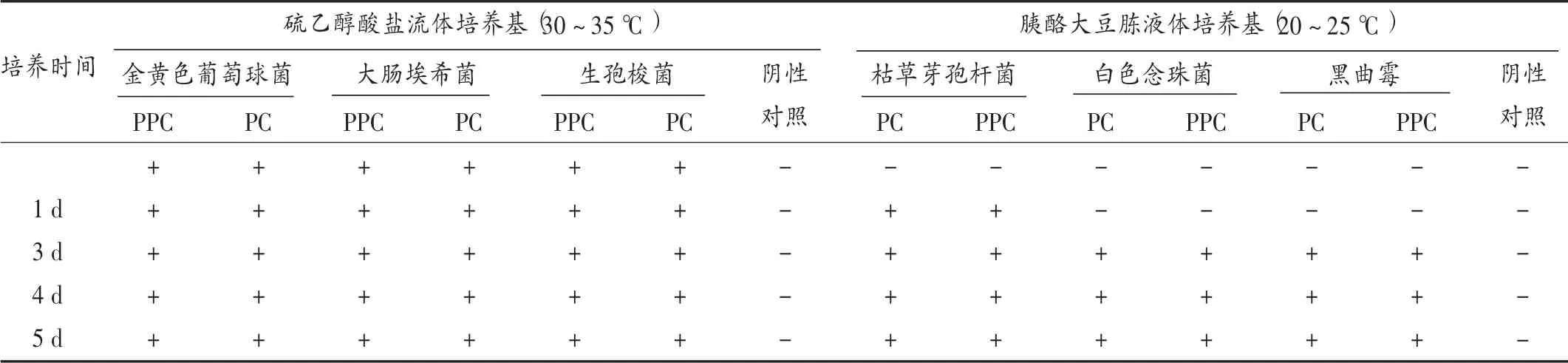
表3 3 批泊沙康唑注射液无菌检查方法适用性试验检查结果
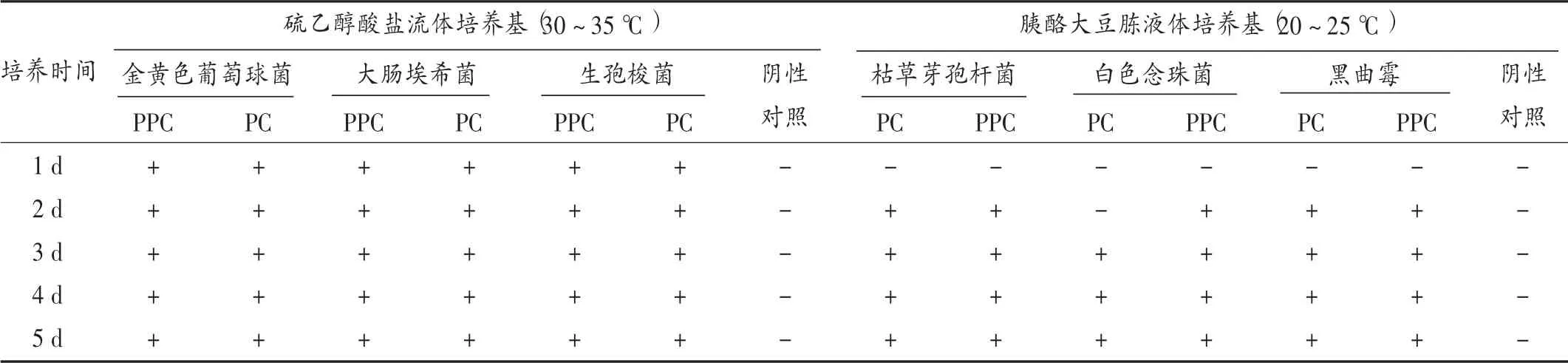
表4 冲洗液无菌检查方法适用性试验检查结果
2.4 无菌检查结果
根据2.2.4 项下的验证方法,按2015 年版《中国药典(四部)》通则1101 无菌检查法薄膜过滤法对泊沙康唑注射液3 批样品进行检测,培养14 d,均无菌生长,产品符合质量标准要求。
3 讨论
本研究结果显示,三唑类抗真菌药对真菌有很强的抑菌作用,对于这类具有较强抗菌活性的药物必须首先摸索处理方式来消除其抑菌作用,然后才能顺利进行无菌检查[8],确保检测结果的准确性。
本研究中采用薄膜过滤法,对冲洗液、冲洗量、滤膜的材质、冲洗条件等进行了筛选和优化[9-10],在研究过程中还考虑了样品的过滤速度和冲洗速度对冲洗效果的影响。以自制的SBECD 溶液(pH 3.5)作为冲洗液进行冲洗,考虑其pH 与样品本身的pH 相近,防止样品的析出残留在滤膜上增加抑菌性[11],同时对冲洗液同步进行方法学适用性验证,确保冲洗液本身无抑菌性[12]。
在进行泊沙康唑注射液无菌检查方法学适用性预试验时,以2015 年版《中国药典(四部)》规定的6 种无菌检查试验菌株是否能正常生长为指标,通过一系列的筛选和优化,最终建立了适合泊沙康唑注射液无菌检查的方法。在验证无菌检查方法时,选择敏感菌株白色念珠菌作为阳性菌[13]。通过方法学适用性验证试验证明,该方法可行、结果可靠,同时给其他三唑类产品的无菌检查提供了参考。
