甲状腺功能检测的性能验证分析*
2020-08-11吴卫星吴宗勇张晓煜党秀敏
吴卫星,吴宗勇,张 丽,张晓煜,党秀敏,齐 军△
1.国家癌症中心/国家肿瘤临床医学研究中心/中国医学科学院北京协和医学院肿瘤医院深圳医院检验科,广东深圳 518116;2.国家癌症中心/国家肿瘤临床医学研究中心/中国医学科学院北京协和医学院肿瘤医院检验科,北京 100021
2018年国际癌症研究机构发布的全球肿瘤流行病调查显示,甲状腺癌已成为全球第11位高发癌症,占女性癌症发病率的第5位[1]。为了预防和监控甲状腺癌的发生、发展,甲状腺功能血清学检查作为实验室诊断的重要依据,对提高甲状腺疾病的诊疗水平具有重要的作用,而精密的仪器和稳定的性能是获得甲状腺功能准确稳定结果的重要保障。
近年来,随着医疗器械技术水平的迅速提升,国产医疗器械迅速崛起,打破了国外医疗器械在国内检验实验室的垄断地位。然而,相对于国外仪器,国产仪器普遍存在的稳定性和可靠性不足的问题,导致各大医院对国产仪器的认可度、信任度不高。因此,本文按照美国临床和实验室标准协会(CLSI)的要求[2],针对中国医学科学院北京协和医学院肿瘤医院深圳医院检验科实验室的迈瑞CL6000i全自动化学发光免疫分析仪检测甲状腺功能五项开展全面的性能验证,包括精密度、正确度、线性、生物参考区间、最低检出限和携带污染,综合判断其性能特性,以确保该仪器满足临床诊断需求。
1 材料与方法
1.1仪器与试剂 迈瑞CL6000i全自动化学发光免疫分析仪。游离三碘甲状腺原氨酸(FT3)的试剂批号为180701,定标品批号为180601,质控品批号为180701;游离甲状腺素(FT4)的试剂批号为180601,定标品批号为180501,质控品批号为180701;三碘甲状腺原氨酸(T3)的试剂批号为180701,定标品批号为180701,质控品批号为180701;甲状腺素(T4)的试剂批号为180701,定标品批号为180601,质控品批号为180701;促甲状腺激素(TSH)的试剂批号为180701,定标品批号为180901,质控品批号为180701。
1.2标本来源 从中国医学科学院北京协和医学院肿瘤医院深圳医院就诊患者或体检健康者中选取高、中、低水平的新鲜血清,并要求标本无黄疸、溶血、脂血。
1.3方法
1.3.1精密度 参考CLSI EP5-A3文件[3],选择低值和高值2个水平的质控品,分装于多个EP管,保存至-20 ℃冰箱备用。每天复融新的2个水平的质控,重复做4次,连续做5 d,共做20次。计算批内精密度和批间精密度。批内精密度以1/4 TEa(CLIA′88)为质量目标,批间精密度以1/3 TEa(CLIA′88)为质量目标。
1.3.2正确度 参考CLSI EP15-A3文件[4],采用迈瑞具有溯源性的企业参考物质,计量上溯源至国际单位制,检测3次,计算平均值。以参考物质的靶值为标准,计算该实验室的检测结果与靶值的偏倚。要求偏倚<1/2 TEa,能力验证实验(PT)≥80%,即为合格。
1.3.3线性 参考NCCLS EP6-A3文件[5],收集靠近线性高值水平和线性低值水平的标本,若收集不到高值标本,可加高水平的分析物。为减少对标本基质的影响,加入分析物体积不应超过总体积的10%。将线性高值标本和线性低值标本按照5L、4L+1H、3L+2H、2L+3H、1L+4H、5L的比例稀释并混匀,配置成6个水平的标本(L表示低值,H表示高值)。每个标本测试2次,分别求出测定结果的均值。将测定水平均值和理论水平进行回归拟合,计算线性相关系数(r)和斜率(b),要求r≥0.990,b为0.95~1.05,即为合格。
1.3.4生物参考区间 参考美国临床实验室标准化委员会(NCCLS)C28-A2文件[6],收集20例健康者,男10例,女10例,年龄20~70岁,对生物参考区间进行验证。仅允许5%的数据超出所验证的生物参考区间,即95%以上的健康者检测值在参考区间内,则表明该生物参考区间可用于该实验室。



2 结 果
2.1精密度验证 应用该型全自动化学发光免疫分析仪对甲状腺功能五项FT3、FT4、T3、T4、TSH进行测定,虽然厂家声明的批内和批间精密度高于1/4 TEa(CLIA′88)和1/3 TEa(CLIA′88),但各个项目的批内精密度均小于1/4 TEa(CLIA′88),批间精密度均小于1/3 TEa(CLIA′88),表明精密度验证通过。见表1。

表1 批内及批间精密度验证结果(%,n=20)
2.2正确度验证 采用具有溯源性的企业参考物质进行检测,结果显示,FT3、FT4、T3、T4、TSH的高值和低值参考物质的检测值均在厂商声明的允许范围内,并且偏倚均小于1/2 TEa,能力验证成绩为100%,表明正确度验证通过。见表2。
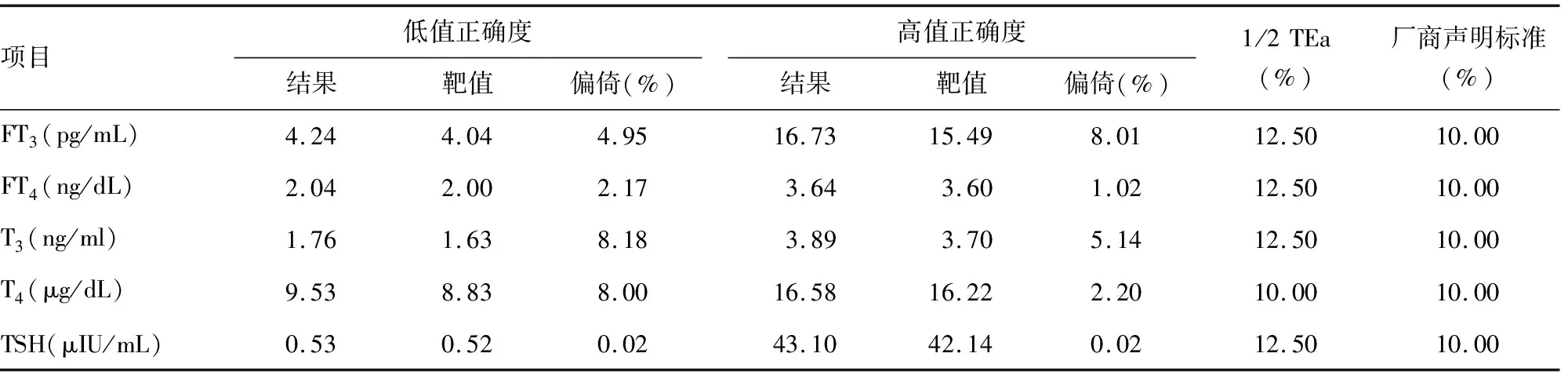
表2 正确度验证结果
2.3线性验证 按照线性标准要求,以理论稀释水平为x值,实际检测水平为y值,计算拟合线性回归方程和r。TSH、T3、T4的实际验证范围与厂家声明线性范围相近,结果显示,TSH、T3、T4呈线性相关,r≥0.990,b为0.95~1.05,均在可接受范围内。由于T4与FT4存在一个动态平衡,标本稀释会影响FT4的动态平衡[9],FT3与FT4具有相同效应,因此,FT4和FT3不适合做线性稀释。见表3。

表3 线性验证结果
2.4生物参考区间验证 按照NCCLS C28-A2文件要求,选择20例体检合格的健康者进行检测。结果显示,甲状腺功能五项的检测值100%分布在该实验室应用的生物参考区间内,说明该参考区间可用于实验室。见表4。

表4 生物参考区间验证结果
2.5检测低限验证 结果显示,检测低限TSH为0.001 μIU/mL,FT3为0.054 pg/mL,FT4为-0.012 ng/dL,T3为0.146 ng/mL,T4为0.007 μg/dL,均小于厂家声明的检测低限,表明厂家声明检测低限适用于该实验室。见表5。

表5 检测低限验证结果
2.6携带污染验证 携带污染量TSH为0.002 μIU/mL,FT3为0.000 pg/mL,FT4为0.000 ng/dL,T3为0.000 ng/mL,T4为0.012 μg/dL,均≤3σL-L,说明迈瑞CL6000i全自动化学发光免疫分析仪的携带污染率符合相应的仪器要求。见表6。
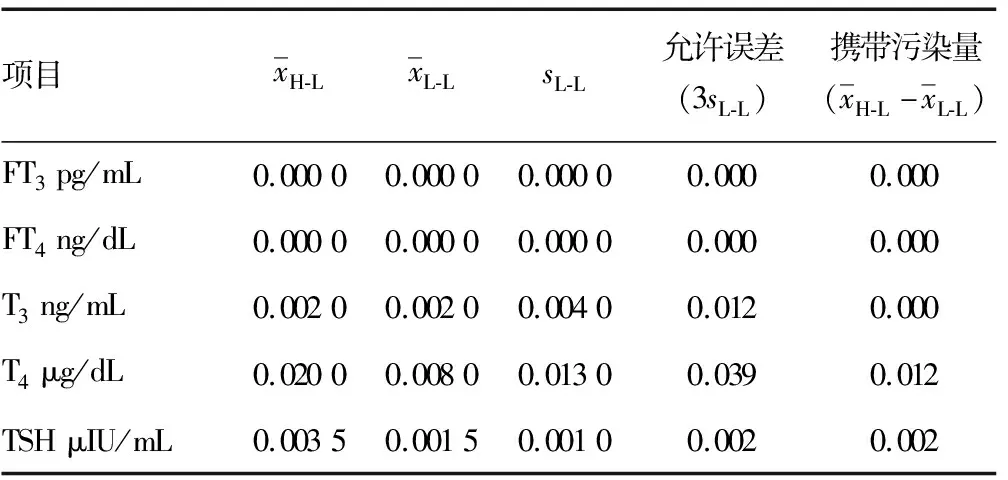
表6 携带污染验证结果
3 讨 论
根据美国《医疗机构临床实验室管理办法》和ISO15189医学实验室认可的规定[10],在用于临床检测之前,仪器设备、检验系统和方法的主要分析性能需进行验证,并要求验证结果能达到临床检测所要求的标准。本文依照CLSI EP5-A3、EP15-A3、EP6-A3、EP17-A2和NCCLS C28-A2等文件的要求,对迈瑞CL-6000i全自动化学发光免疫分析仪检测FT3、FT4、T3、T4、TSH 5个甲状腺功能项目的精密度、正确度、线性、生物参考区间、检测低值、携带污染等进行评估。
精密度是对同一份标本重复检测所得检测结果之间的一致程度,即可重复性,通常以变异系数表示[11]。良好的精密度是其他各项性能验证指标的前提。本研究结果显示,该型化学发光免疫分析仪对甲状腺功能五项的批内精密度小于1/4 TEa(CLIA′88),批间精密度小于1/3 TEa(CLIA′88),说明仪器的可重复性好,符合质量标准要求。
正确度是检测结果的均值与参考值(约定真值)之间的一致程度,常用偏倚表示[11-12]。偏倚越低正确率越高。该实验室采用迈瑞具有溯源性的企业参考物质进行检测,结果显示,FT3、FT4、T3、T4、TSH的检测均值与靶值之间的偏倚均小于1/2 TEa,每项能力验证成绩均为100%,说明仪器的检测值可信度高,可以满足临床要求。
线性范围是利用接近线性的高低值标本及高低值标本按比例混匀的标本的理论水平和实际检测值之间的线性关系,从而评估仪器的可报告范围[13]。若检测值超出该线性范围,被视为不准确的检测值。考虑到肿瘤患者的结果多为异常,因此,良好的检测方法或检测系统各项目的线性范围不仅要覆盖医学决定水平还应具有较宽的线性范围。本研究显示,T3、T4、TSH的r≥0.990,并且b为0.95~1.05,表明T3、T4、TSH等项目在厂家声明的线性范围内均具有很好的线性。由于T4与FT4存在一个满足结合常数K公式的动态平衡,稀释液和标本之间存在着蛋白种类和水平的差异,结合常数K也不尽相同,因此,FT4不宜做线性稀释[9]。大部分的FT3是由T4转变而来,并维持着一个动态平衡,FT3与FT4具有相同效应。如需对FT3与FT4进行溯源,可采用平衡透析或者超滤的方法,这被认为是目前检测游离激素的“金标准”[9]。
生物参考区间是健康者中间95%分布区间的检测值范围[8]。实验室确定一个可靠的生物参考区间非常重要。随着新引进的检验项目的增大,考虑到人力、物力和成本,每个项目建立本实验的生物参考区间并不现实,大部分实验室会采用其他实验室或仪器试剂厂家提供的生物参考区间数据,并进行验证。本研究按照NCCLS C28-A2文件要求,随机抽取20例健康者的血清进行检测,FT3、FT4、T3、T4、TSH的检测值均100%在参考区间内,说明厂家声明的生物参考区间适用于该实验室。
检测低值是检测系统能检测出的最低分析物水平,体现仪器的反应灵敏度。TSH是筛查甲状腺功能异常和原发性甲状腺功能减退甲状腺激素替代治疗的关键方法,甲状腺功能亢进患者的TSH经常出现极低检测值[14],因此,检测系统良好的检测低限对甲状腺功能的判断与监测至关重要。本研究显示,各项的检测低值均小于厂家声明的检测低值,其中TSH的检测低限迈瑞CL6000i厂家声明为0.005 0 μIU/mL,本实验验证为0.001 0 μIU/mL,同类型仪器罗氏Cobas 601的检测低限为0.002 5 μIU/mL[15],表明迈瑞CL6000i具备与罗氏Cobas 601同样良好的反应灵敏度。
携带污染是不同水平标本依次检测,高水平标本对低水平标本的污染程度。本研究显示,FT3、FT4、T3、T4、TSH等项目的携带污染率均小于允许污染范围,说明迈瑞CL6000i的冲洗功能良好,并且该仪器采用的是一次性吸头取样,能有效减少标本间的交叉污染,提高检测结果的可信性。
综上所述,迈瑞CL6000i全自动化学发光免疫分析仪检测FT3、FT4、T3、T4、TSH等项目的精密度、正确度、线性、生物参考区间、携带污染均能达到厂商声明要求,符合CLIA′88和ISO15189实验室认可要求。本研究的性能验证具有实用性和可操作性,证明迈瑞CL6000i全自动化学发光免疫分析仪具有优良的性能,能够满足临床需求。
