清热解毒类中兽药中非法添加吲哚美辛的HPLC-PDA检测方法的建立
2020-07-15张浩然张亦菲华贤辉
张浩然,徐 汀,张亦菲,田 恺,华贤辉,商 军
(上海市兽药饲料检测所,上海 201103)
吲哚美辛为解热镇痛类非甾体抗炎药,收载于《中华人民共和国药典》2015年版(二部)[1],《中华人民共和国兽药典》中并未收载。该药物主要通过抑制环氧合酶的合成,下调体温中枢的温度调定点,从而使机体达到正常的产热散热平衡,故可用来治疗非特异性发热[2]。但其副作用大,长期使用的不良反应发生率为35%~50%[3],如消化性溃疡、穿孔、水肿、高血压等[4]。最近,在兽药监督抽检工作中首次发现了中兽药梅香片中非法添加吲哚美辛的情况,因此有必要建立清热解毒类中兽药中非法添加吲哚美辛的检测方法。
板二黄片由黄芪、淫羊藿、盐黄柏、山楂及地黄五味药材用水煎煮,滤过浓缩至膏状后,先与板蓝根细粉混匀制粒,后粉碎并与连翘、白术粉末混匀,过筛,加入适量辅料,制粒压片而成[5];三黄散由黄芩、黄柏、大黄及大青叶四味药材粉碎、过筛、混匀而成[5];扶正解毒散主要是由板蓝根、黄芪和淫羊藿三味中药材粉碎、过筛、混匀而成[6]。因此,为使本法有一定的代表性,本文选取了工艺、成分均较复杂的板二黄片以及相对简单的三黄散和扶正解毒散,在参考了相关文献后[7-9],结合非法添加检测方法的技术特点,建立了清热解毒类中兽药中非法添加吲哚美辛的HPLC-PDA检测方法,为中兽药中非法添加吲哚美辛的检测提供依据。
1 仪器与试药
1.1 仪器 高效液相色谱仪:Waters e2695,配二极管阵列检测器(PDA),沃特世公司;电子天平:感量0.01 mg,AB265-S,梅特勒-托利多仪器(上海)有限公司;纯水机:Molatom 1810A,中国重庆摩尔水处理设备有限公司。
1.2 试药 吲哚美辛对照品(Dr. Ehrenstorfer GmbH,批号为G832449,含量99.4%);实验用水(电阻率>18 MΩ·cm,符合GB/T6682一级用水的规定);乙腈(色谱纯);乙酸(色谱纯);板二黄片阴性样品(批号:20181001);三黄散阴性样品(批号:17070255);扶正解毒散阴性样品(批号:2016110201);梅香片阳性样品(批号:20190301)。
2 方法与结果
2.1 色谱条件 色谱柱:采用ODSC18色谱柱(柱长150 mm,内径4.6 mm,粒径5 μm);流动相∶乙腈∶0.1 mol/L冰醋酸(50∶50,V1∶V2);流速∶1.0 mL/min;柱温:30℃;进样量:10 μL;PDA参考条件:采集波长范围200 ~ 400 nm,分辨率为1.2 nm;定量波长:317 nm。
2.2 溶液的制备
2.2.1 供试品溶液的制备 取供试品1 g,精密称定,置50 mL离心管中,精密加入流动相20.00 mL,超声提取20 min,静置,滤过,精密量取滤液1.00 mL置10 mL容量瓶中,用流动相稀释至刻度,摇匀,经0.22 μm滤膜滤过,滤液作为供试品溶液。
2.2.2 对照品储备溶液 取吲哚美辛对照品100.35 mg,置10 mL容量瓶中,加甲醇溶解并稀释至刻度,摇匀,作为对照品储备溶液。
2.2.3 对照品工作溶液 精密量取1.00 mL对照品储备溶液置100 mL容量瓶中,用流动相稀释至刻度,经0.22 μm滤膜滤过,滤液作为对照品工作溶液。
2.2.4 建立光谱数据库的溶液 以对照品工作溶液(2.2.3)作为建立光谱数据库的溶液,建立光谱数据库。
2.3 供试品的测定 按照2.1的色谱条件及2.2的溶液制备方法,将供试品溶液和对照品工作溶液注入高效液相色谱仪。按外标法以峰面积计算,即得吲哚美辛的含量。
2.4 线性关系考察 将对照品储备液精密稀释,制备200、100、50、20、10、5 μg/mL的吲哚美辛对照品溶液。每个浓度点重复5次进样,按照2.1的色谱条件进行测定,以吲哚美辛对照品浓度为横坐标(x),以相应浓度测得的峰面积为纵坐标(y),绘制标准曲线。得到线性方程为y= 11214x- 10416。本方法在吲哚美辛浓度为5 ~ 200 μg/mL范围内线性关系良好(r=0.9999)。
2.5 专属性考察 取板二黄片阴性样品、三黄散阴性样品及扶正解毒散阴性样品,按照2.2的制备方法得到空白基质溶液。通过空白基质溶液及对照品工作溶液进行专属性试验。结果表明,基质对吲哚美辛的出峰没有干扰,不影响含量测定。典型色谱图见图1~图4。

图1 吲哚美辛的色谱图(0.1 mg/mL)Fig 1 Chromatogram of Indomethacine (0.1 mg/mL)

图2 板二黄片阴性基质溶液的色谱图Fig 2 Negative solution chromatogram of Ban’er Huang tablets

图3 三黄散空白基质溶液的色谱图Fig 3 Negative solution chromatogram of Sanhuang power
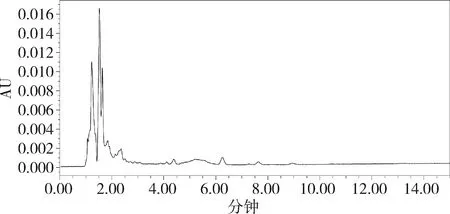
图4 扶正解毒散空白基质溶液的色谱图Fig. 4 Negative solution chromatogram of Fuzheng Jiedu power
2.6 峰纯度检查 取板二黄片阴性样品、三黄散阴性样品及扶正解毒散阴性样品各1 g,加入适量对照品储备溶液,制成吲哚美辛添加量为1 g/kg的阴性添加样品,按照2.1的色谱条件及2.2处理方法制成峰纯度检查溶液,进行测定。结果表明,样品色谱峰的纯度角度均小于纯度阈值,说明吲哚美辛的出峰没有干扰,可确定为单一物质峰(表1)。

表1 峰纯度和光谱相似度检查结果表Tab 1 The results of peak purity and spectra matching test
2.7 光谱相似度检查 将峰纯度检查溶液(2.6)中吲哚美辛的光谱图和光谱数据库进行匹配。结果表明,PDA匹配角度均小于PDA匹配阈值,说明光谱的相似度高,可确定为同一物质(表1)。
2.8 检测限 取板二黄片阴性样品、三黄散阴性样品及扶正解毒散阴性样品各1 g,逐级加入适量对照品储备溶液,制成吲哚美辛添加量为2 g/kg、1 g/kg、0.4 g/kg的阴性添加样品,按照2.1的色谱条件及2.2处理方法进行测定。考虑到非法添加的成分含量大都较高,故选择光谱图失真的最大浓度作为本方法的检测限[10]。结果表明,检测限为1.0 g/kg。典型图谱见图5~图10。

图5 板二黄片中添加吲哚美辛的色谱图(1 g/kg)Fig 5 Chromatogram of Indomethacine added in Ban’er Huang tablets (1 g/kg)

图6 板二黄片中添加吲哚美辛的光谱图(1 g/kg)Fig 6 Spectrum of Indomethacine added in Ban’er Huang tablets (1 g/kg)

图7 三黄散中添加吲哚美辛的色谱图(1 g/kg)Fig 7 Chromatogram of Indomethacine added in Sanhuang powder (1 g/kg)

图8 三黄散中添加吲哚美辛的光谱图(1 g/kg)Fig 8 Spectrum of Indomethacine added in Sanhuang powder (1 g/kg)
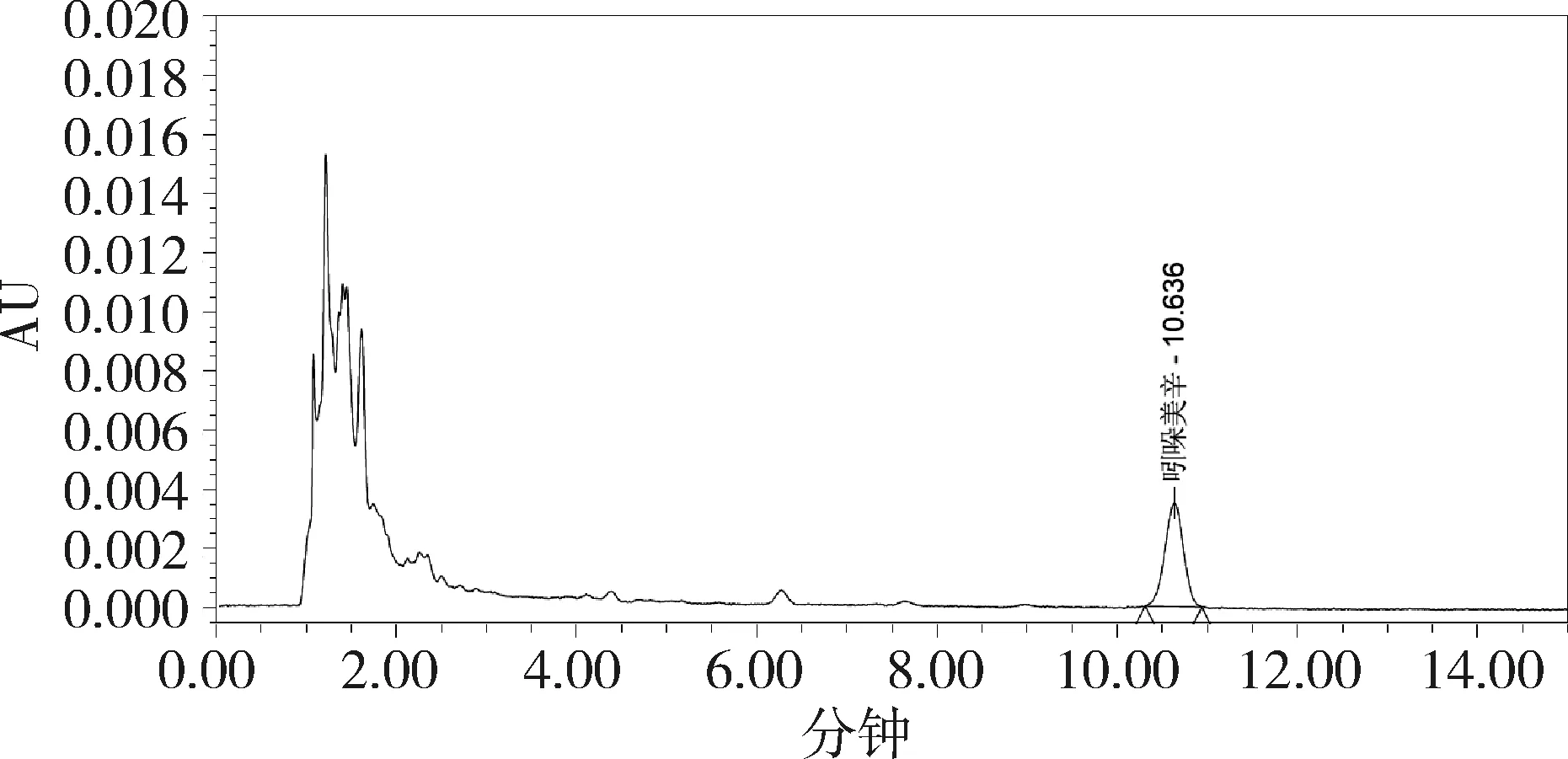
图9 扶正解毒散中添加吲哚美辛的色谱图(1 g/kg)Fig 9 Chromatogram of Indomethacine added in Fuzheng Jiedu power (1 g/kg)
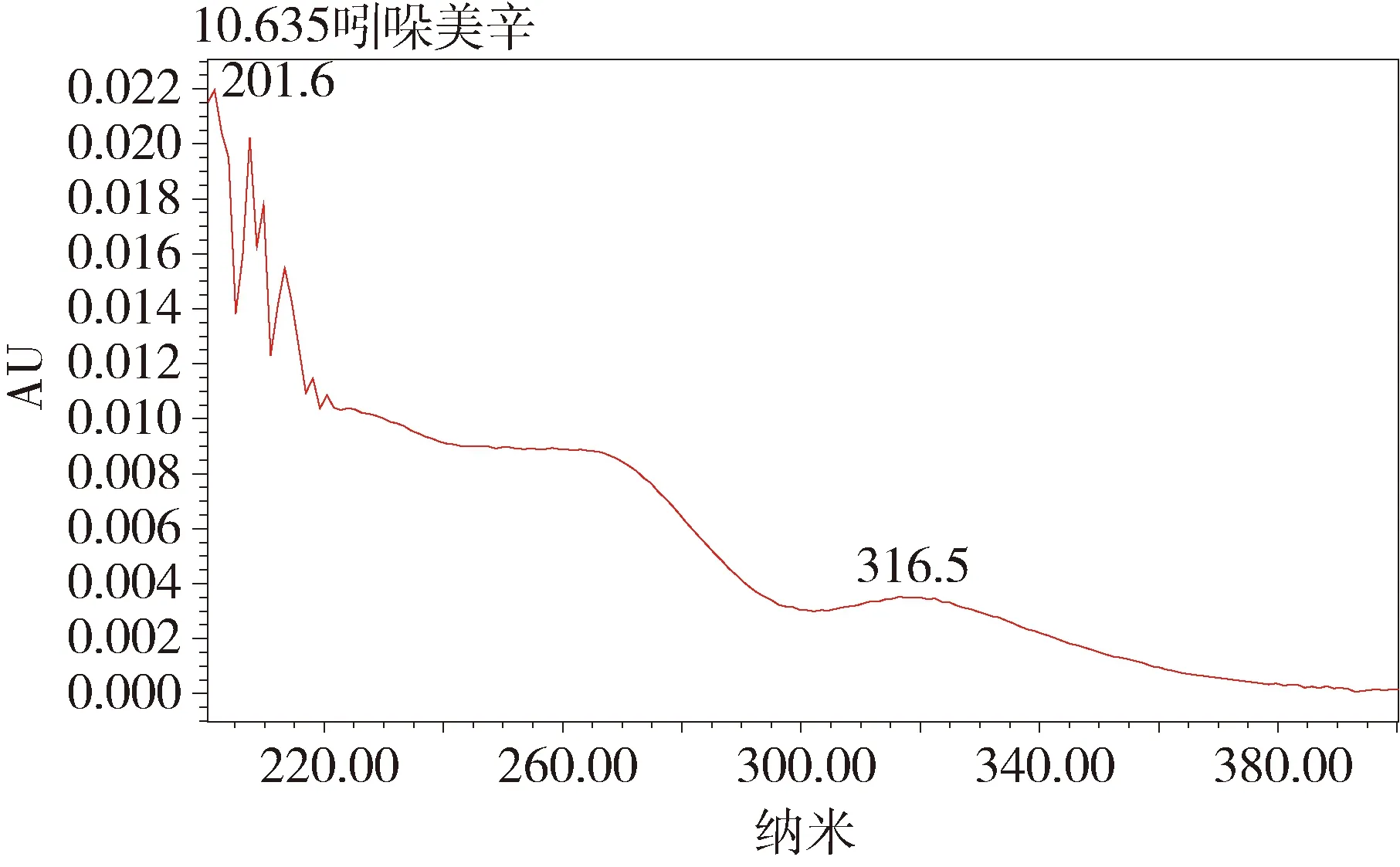
图10 扶正解毒散中添加吲哚美辛的光谱图(1 g/kg)Fig 10 Spectrum of Indomethacine added in Fuzheng Jiedu power (1 g/kg)
2.9 准确度试验 取板二黄片阴性样品、三黄散阴性样品及扶正解毒散阴性样品各1 g,加入适量对照品储备溶液,制成吲哚美辛添加量约为3 g/kg的阴性添加样品。每个基质6个平行,按照2.1的色谱条件及2.2处理方法,进行测定。板二黄片中吲哚美辛的平均回收率为96.5%,RSD为0.9%;三黄散中吲哚美辛的平均回收率为99.3%,RSD为1.3%;扶正解毒散中吲哚美辛的平均回收率为100.6%,RSD为0.8%(表2)。试验结果符合《中华人民共和国兽药典》[11]2015年版附录9101的要求。
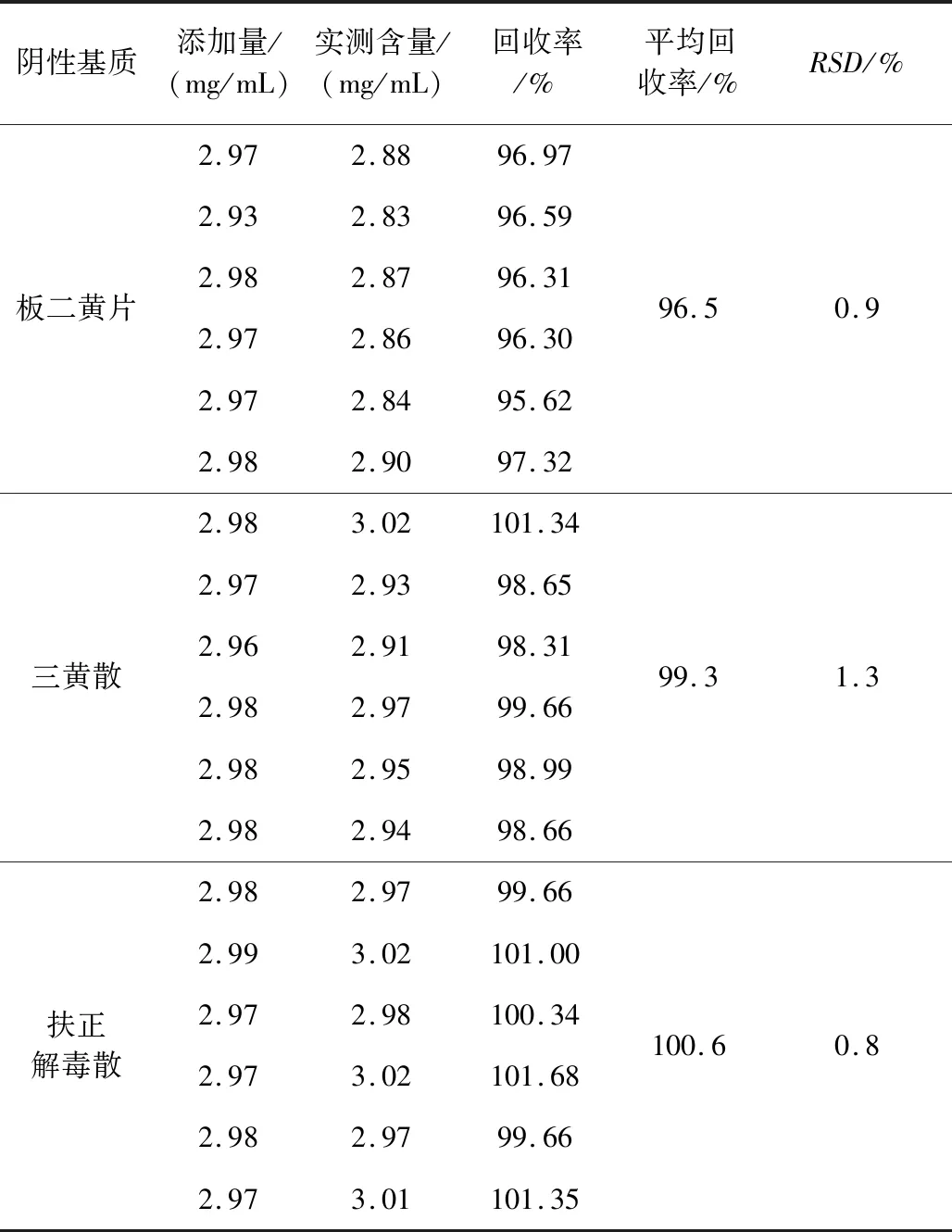
表2 准确度试验结果(n=6)Tab 2 The results of accuracy test (n=6)
2.10 稳定性试验 按照2.2的处理方法,制备各基质阴性添加的供试品溶液进行稳定性试验,室温下分别在0、4、8、12、16、20、24 h后按照2.1的色谱条件进行测定。吲哚美辛峰面积的RSD均小于0.6%,说明供试品溶液24 h内的稳定性良好。
2.11 耐用性试验 选取各基质的准确度试验溶液进行耐用性试验,考察柱温及不同色谱柱的影响。调节柱温分别为25℃、30℃、35℃,结果表明,随着柱温的提升,吲哚美辛的出峰时间略有提前,相差约1 min;不同规格及不同厂商的色谱柱(Shiseido MGⅡ 250 mm×4.6 mm,5 μm;Shiseido MGⅡ 150 mm×4.6 mm,5 μm;Waters symmetry 150 mm×4.6 mm,5 μm)在本方法中所得的吲哚美辛色谱峰的理论塔板数、拖尾因子均符合检测要求,说明本方法耐用性较好。
2.12 阳性供试品测定 采用本法,对梅香片阳性样品进行测定,结果表明,该阳性样品中吲哚美辛的添加量为15 g/kg,具体结果见表3,图11。
3 讨论与结论
3.1 检测波长的确定 将对照品工作溶液按照2.1的色谱条件注入液相色谱仪,在200~400 nm波长范围内进行波长扫描,选择其最大吸收波长317 nm作为定量波长。
3.2 流动相的选择 本文参考了《中华人民共和国药典》[1]中吲哚美辛肠溶片的液相色谱条件,该条件下,吲哚美辛色谱峰的对称性好,出峰时间适宜,在基质中不受其他杂质峰的干扰,故选择乙腈:0.1 mol/L冰醋酸(50∶50,V1∶V2)为流动相,与相关文献报道一致[12~14]。
3.3 阳性样品的确证 对于非法添加阳性样品的确证,除保留时间要求一致外,还需要辅以最大吸收波长、峰纯度和光谱相似度三个条件。首先,供试品和对照品的紫外光谱图相匹配,并且最大吸收波长相差不超过±2 nm。其次,利用事先建立的光谱数据库,可以进行峰纯度和光谱相似度检查,若纯度角度小于纯度阈值,则确认为单一物质;若匹配角度小于匹配阈值,则认为光谱高度相似。最后,结合以上四个条件,避免了保留时间一致但光谱不同的物质的干扰,从而做出确证。

表3 阳性样品检测结果表(n=2)Tab 3 The results of the positive sample test (n=2)
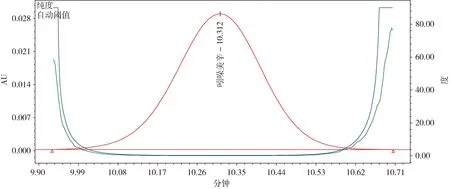
图11 梅香片阳性样品中吲哚美辛的纯度图Fig 11 Purity plot of Indomethacine in Meixiang tablets
3.4 本法的通用性 本文利用建立好的方法对阳性供试品(2.12)梅香片中的吲哚美辛进行检测。结合3.3中总结的四个条件,完成了梅香片中吲哚美辛的确证(表3)并进行了定量。此外,为验证定量的准确性,按照添加量和本底浓度之比为0.8∶1,1∶1,1.2∶1进行低、中、高三种浓度的准确度试验,每个浓度3份平行,得到平均回收率为101.2%,RSD为0.4%~1.1%。结果表明,本法定量准确。因此,本方法在两种散剂和两种片剂基质的应用,体现了较好的通用性。
以上试验结果表明,本法操作简便快速,准确性、重复性均较好,可应用于中兽药中非法添加吲哚美辛的检测工作。
