2,3-吡啶二羧酸合成尾气吸收实验研究
2020-07-09张兵兵任建坡沈志红蒋志强
张兵兵,任建坡,沈志红,蒋志强
(1.中化河北有限公司,河北石家庄050000;2.河北中化滏恒股份有限公司)
2,3-吡啶二羧酸也称吡啶酸, 是合成农药、医药和染料的重要原料[1]。 吡啶酸主要用来合成含吡啶或喹啉环的咪唑啉酮类除草剂(灭草烟)[2],也是合成抗生素(如抗分支杆菌喹诺酮)的主原料[3]。 吡啶酸的合成方法较多, 目前使用较多的是喹啉氧化工艺。 但是在氧化反应中,会释放大量的Cl2和CO2气体。 Cl2是有毒有害气体,直接排放会严重污染环境[4]。 含氯尾气多见于氯碱工业中,尾气中Cl2多用液碱吸收。Cl2含量较高的尾气可以用来合成次氯酸钠溶液,作为副产品进行销售,提高产品附加值[5]。四氯化钛生产过程中, 用石灰水吸收尾气中的Cl2,使尾气达标排放[6]。单纯的Cl2尾气吸收处理报道较多, 关于2,3-吡啶二羧酸合成尾气处理报道较少。本文研究Na2SO3吸收合成尾气中的Cl2, 实现尾气达标排放的目的。
1 实验部分
1.1 仪器和试剂
试剂:NaOH、Na2SO3、喹啉、CuSO4·5H2O、NaClO3、催化剂A,均为分析纯。
仪器:余氯检测仪(HD-P900X-S4)、二氧化硫检测仪(usafe 2000)、安捷伦高效液相色谱仪(HPLC-1260)(色谱柱ZORBAX RX-C8)、 原子吸收光谱仪(AA-6880)、水分测定仪。
1.2 尾气吸收实验
模拟车间生产进行实验制备尾气, 为确保实验条件平行, 系列合成实验投料量及反应条件均不变,实验编号为BD-X,其中X=1,2,3,4,5。
1)Na2SO3与NaOH 吸收液对照实验:同时进行合成实验BD-1、BD-2。 102 ℃下反应4 h 后同时接入尾气吸收, 实验BD-1 尾气用15%Na2SO3溶液吸收,实验BD-2 尾气用15%NaOH 溶液吸收。 通过流量计控制尾气流速为700 mL/min。
2)尾气流速对Na2SO3溶液吸收效果的影响:进行合成实验BD-3,102 ℃下反应4 h 后接入尾气吸收,尾气用15%Na2SO3溶液吸收,通过流量计调节尾气流速,进行400、700、1 000、1 300、1 600 mL/min等流速下吸收实验。 每个流速下均更换新的15%Na2SO3溶液,每个流速下吸收时间为0.5 h。
3)吸收液浓度对吸收效果的影响:进行合成实验BD-4,102 ℃下反应4 h 后接入尾气吸收,通过流量计调节尾气流速为1 600 mL/min。 尾气分别用10%、15%、20%、25%、30%Na2SO3溶液吸收,每个浓度下吸收时间为0.5 h。
4)Na2SO3溶液吸收能力实验: 进行合成实验BD-5,开始加热时即接入尾气吸收,调节尾气流速,氧化反应结束后,统计Na2SO3消耗,评价Na2SO3溶液吸收能力。
2 结果与讨论
2.1 Na2SO3 溶液与NaOH 溶液吸收尾气对照实验
表1 与表2 分别为Na2SO3溶液与NaOH 溶液吸收尾气记录。
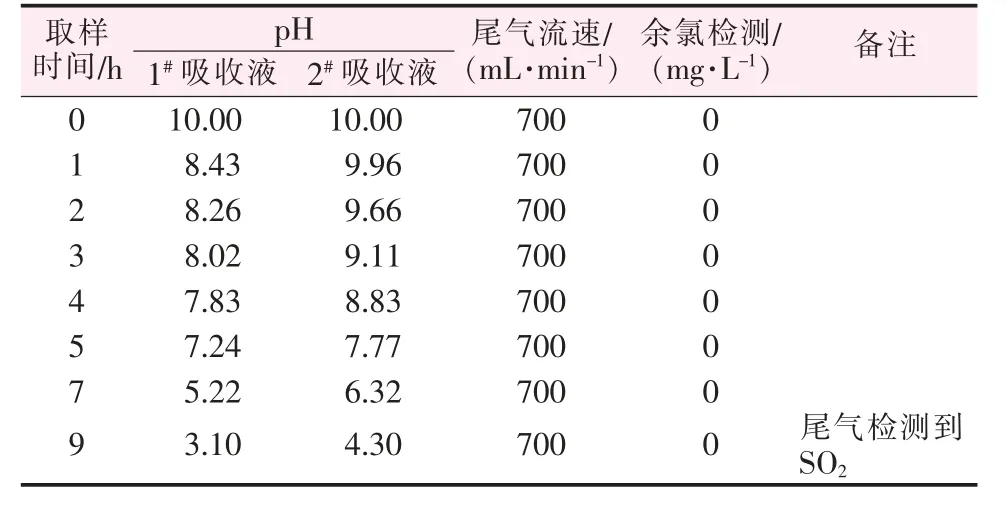
表1 Na2SO3 溶液吸收尾气记录
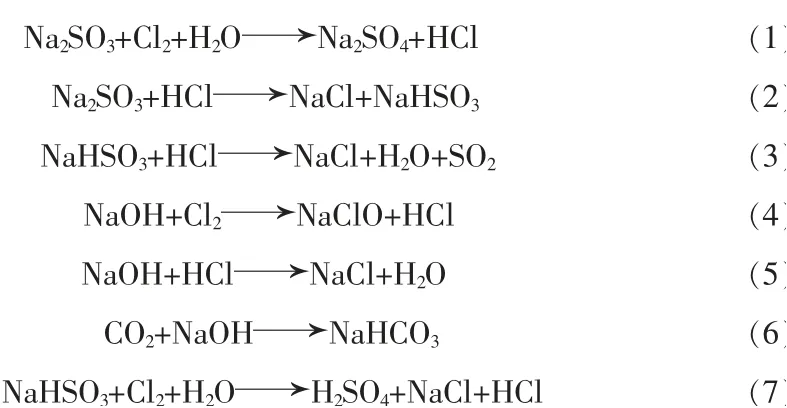
从表1 与表2 可知, 随着吸收反应的进行,两种吸收液的pH 均逐渐降低。 这是因为Na2SO3溶液在吸收尾气时同时发生(1)(2)(7)反应,反应(1)属于氧化还原反应,反应速度快于(2),所以一开始就呈现pH 下降现象, 当继续进行吸收反应, 溶液中Na2SO3含量不足时,富余的酸较多,导致后续pH 下降较快(第5 h),继续反应,pH 下降加快,在pH 为3~4 时尾气中检测出刺鼻气味的SO2,说明发生了化学反应(3);而NaOH 溶液吸收尾气的同时发生(4)、(5)反应,反应开始时NaOH 浓度较高,反应(4)生成的盐酸继续发生反应(5),所以pH 下降缓慢,3 h 内仅下降0.95,而5 h 后,pH 相对于3 h 时的pH 下降了3.7,说明此时NaOH 浓度降低,盐酸相对开始富余。 从表2 看到pH 降到10.3 时,出现沉淀,经检测为NaHCO3, 这是因为尾气中含有大量的CO2气体(见图1 方程式),会发生反应(6),当pH 降至6~10时NaHCO3就会析出,因此出现沉淀。
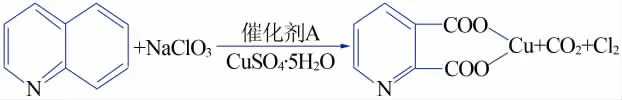
图1 吡啶酸合成涉及反应式
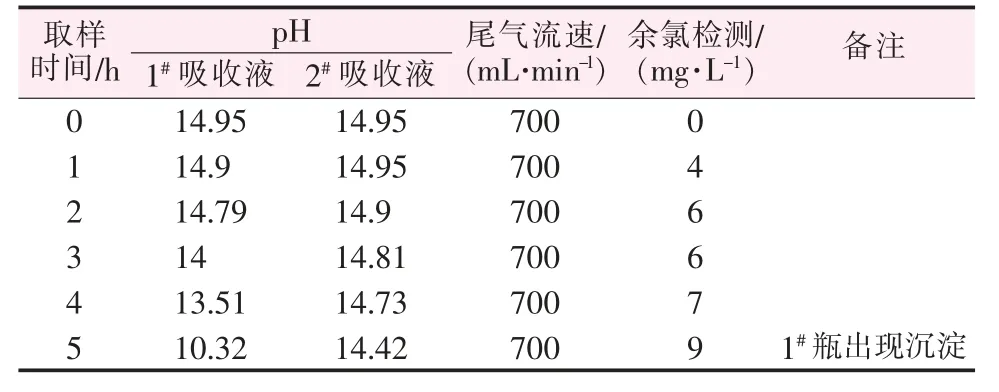
表2 NaOH 溶液吸收尾气记录
两种吸收液中2#瓶均比1#瓶pH 下降慢,说明大部分Cl2先与1#瓶中吸收液反应,残余Cl2再与2#瓶反应。 通过余氯检测发现,经Na2SO3溶液吸收后尾气中Cl2为0,而经NaOH 溶液吸收后有Cl2存在,说明Na2SO3吸收效果强于NaOH,是因为反应(1)是氧化还原反应,反应速度大于反应(4)化学反应速度。 尾气中的CO2在pH 降至10 以后会与NaOH 溶液反应生成NaHCO3沉淀,存在堵塔风险。
Cl2与NaOH 溶液反应时,先发生水解反应(8),生 成HClO 与HCl,HClO 再 与NaOH 反 应 生 成NaClO 和H2O。而Cl2与Na2SO3发生的是氧化还原反应,水解反应相对本氧化还原反应速度较慢,且Cl2与NaOH 溶液分两步反应才生成NaClO。 此外尾气中的CO2气体会与NaOH 反应生成NaHCO3沉淀,存在堵塔风险。所以用Na2SO3溶液吸收尾气要优于NaOH 溶液。

2.2 尾气流速对吸收效果的影响
表3 为尾气流速对吸收效果的影响数据。 由表3结果可见,在尾气流速达到1 600 mL/min 时,尾气中检测到Cl2,同时未检测到SO2,证明不是Na2SO3量不足而导致的吸收能力不足。 说明吸收液质量分数在15%时,尾气流量对吸收效果是有影响的,尾
气流速过快,不利于Cl2的吸收。 由于是自反应产生尾气,产气速率不变,调节尾气流速实际改变的是尾气中Cl2的浓度以及Cl2同Na2SO3接触的时间。 尾气流速加快, 使Cl2来不及与吸收瓶中的Na2SO3反应而直接排出,造成吸收能力下降。
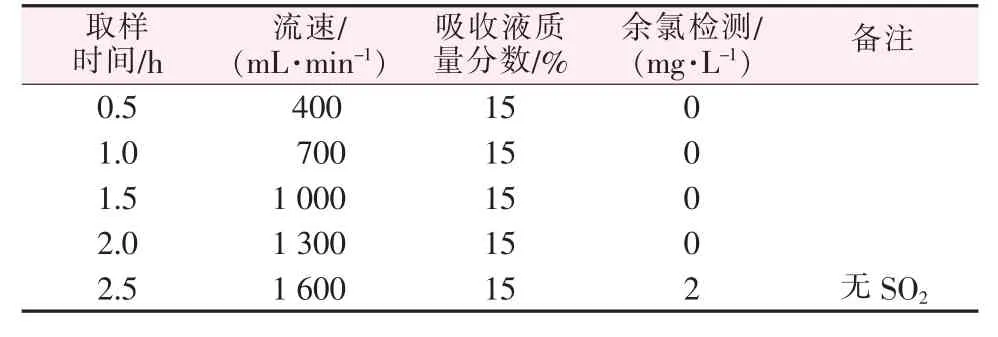
表3 尾气流速对吸收效果的影响
2.3 吸收液浓度对吸收效果的影响
表4 为吸收液浓度对吸收效果影响的数据。 常温下Na2SO3溶解度有限,且反应完后硫酸钠浓度过高后会析出堵塞管道,因此浓度最高定在30%(质量分数)。 表4 实验结果显示,在尾气流速为1 600 mL/min 不变的情况下, 吸收液质量分数在15%以下时, 尾气中检测到Cl2存在, 没有检测到SO2气体,而吸收液在20%以上时,尾气中没有Cl2存在。说明即使在较高尾气流速下,适当提高吸收液浓度可以提高对尾气中Cl2的吸收效果。

表4 吸收液浓度对吸收效果的影响
2.4 Na2SO3 吸收能力实验
表5 为Na2SO3溶液吸收能力实验数据,表6 及图2 为此次反应产品检测结果。
表5 结果显示,随着尾气吸收的进行,1#与2#吸收液pH 均不断下降,由于吸收液pH 降至3~4 时会进行反应(3),释放出空气污染物SO2,因此要限制反应(3)的发生,促进反应(7)进行,这样才能有效利用Na2SO3, 所以使用30%NaOH 溶液去中和富余的HCl,pH 过高,加入的NaOH 容易与尾气中CO2发生反应(6),所以应维持吸收液pH 在5.7~5.9。 实验结果说明,NaOH 的滴加,有效地抑制了反应(3)的进行,提高了Na2SO3利用率,反应结束时1#吸收液中剩余1%Na2SO3,2#吸收液中剩余6%Na2SO3。 每50 g喹啉反应需要300 g 20%Na2SO3与500 g 30%NaOH吸收尾气中的Cl2。 整个反应中尾气未检测到Cl2及SO2等有害气体,吸收效果较好。

表5 Na2SO3 溶液吸收能力实验

表6 产品分析结果
反应全程采用Na2SO3吸收尾气后,经后处理得到的产品吡啶酸纯度为99.9%、 收率为65%, 重金属、氯离子等指标均符合客户公司质量要求。说明用Na2SO3溶液吸收尾气后,不影响产品品质及收率。
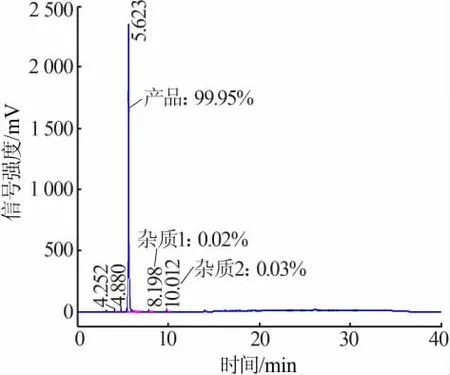
图2 BD-5 合成实验产品液相色谱图
3 结论
1)Na2SO3溶液吸收吡啶酸合成尾气效果优于用NaOH 溶液吸收。 2)吡啶酸合成尾气流速与吸收液浓度影响对尾气中Cl2的吸收效果, 适当降低流速以及提高吸收液浓度有利于吸收尾气中的Cl2。3)用30%NaOH 溶液调节吸收液pH,可最大程度地发挥Na2SO3吸收Cl2的能力,每50 g 喹啉反应对应需要300 g 20%Na2SO3与500 g 30%NaOH 吸收尾气中的Cl2。 整个反应中尾气未检测到Cl2及SO2等有害气体,吸收效果较好。
