用HPLC波长切换法同时测定甲氯霜中3种成分的含量
2020-07-08邱会苹张素娜樊晓雷王伟勤
郝 哲,邱会苹,张素娜,樊晓雷,王伟勤,屈 俊
(联勤保障部队第九八八医院药剂科,郑州 450042)
甲氯霜系联勤保障部队第九八八医院自制制剂,主要用于干性皮脂溢出症、痤疮、疱疮等症,疗效颇佳。该制剂处方以甲硝唑、氯霉素为主药,以羟苯乙酯为抑菌剂。甲硝唑为硝基咪唑衍生物,对大多数厌氧菌具有强大的抗菌作用[1],但药品不良反应(ADRs)限制了其应用。甲硝唑现多采用外用剂型,具有用量小、局部浓度高、作用持久、ADRs少、无全身给药弊端等特点,且对皮肤无刺激性[2]。氯霉素局部外用可减少或抑制痤疮棒状杆菌,减轻炎症反应[3]。羟苯乙酯为尼泊金酯类防腐剂,具有广谱抑菌作用,常用于食品、药品和化妆品中[4]。人用药物注册技术要求国际协调会议(International Conference on Harmonization of Technical Requirements for Registration of Pharmaceuticals for Human Use,ICH)明确提出应建立抑菌剂含量测定方法[5]。若药物制剂中抑菌剂用量不足,便达不到有效抑菌浓度,而用量过大,则具有一定毒性,易引起ADRs[6]。近年来,人们越来越重视制剂中羟苯乙酯的含量控制。虽已有文献[7-8]报道其他制剂中甲硝唑、氯霉素的含量测定方法,但均为单波长法。本研究首次采用HPLC波长切换法同时测定甲氯霜中甲硝唑、氯霉素及羟苯乙酯3种成分的含量,该方法简便、快速,可为甲氯霜制剂质量标准的制定提供一定的科学依据。
1 仪器和试药
1.1 仪器 岛津LC-10A高效液相色谱仪(包括SPD-10A 紫外检测器和LC-solution Lite色谱工作站,日本岛津公司);BT-125D型电子天平(精度0.01 mg/0.1 mg,称量范围41 g/120 g,德国赛多利斯有限公司);AS3120A 型超声波清洗器(天津Auto-science公司);Wondasil C18色谱柱(日本岛津公司)。
1.2 药品和试剂 甲硝唑对照品(纯度99.9%,批号100191-201507)、氯霉素对照品(纯度99.8%,批号130555-201704)、羟苯乙酯对照品(纯度99.9%,批号100847-201604,中国食品药品检定研究院)。甲氯霜(规格30 g/支,批号180911、180912、180913)和阴性样品均为本院自制;水为自制蒸馏水;甲醇(色谱纯,天津四友精细化学品有限公司);其他试剂均为分析纯。
2 方法和结果
2.1 色谱条件 Wondasil C18色谱柱(250 mm×4.6 mm,5 μm);流动相为甲醇(A)和0.5%冰乙酸溶液(B),梯度洗脱:0~8 min 35%A,8~16 min 35%~45%A,16~30 min 45%~60%A;柱温为40 ℃。检测波长:0~8 min在320 nm处检测甲硝唑,8~16 min在278 nm处检测氯霉素,16~30 min在254 nm处检测羟苯乙酯。
2.2 溶液的制备
2.2.1 混合对照品溶液 分别精密称取甲硝唑对照品9.68 mg和氯霉素对照品9.58 mg置50 ml量瓶中,加乙醇溶解并定容至刻度,摇匀,作为对照品储备液1。精密称取羟苯乙酯对照品11.72 mg置50 ml量瓶中,加乙醇溶解并稀释至刻度,摇匀,作为对照品储备液2;再精密量取1 ml对照品储备液2置25 ml量瓶中,加乙醇溶解并稀释至刻度,摇匀,作为对照品储备液3。分别精密量取对照品储备液1和对照品储备液3各3 ml置10 ml量瓶中,加乙醇稀释至刻度,摇匀,作为混合对照品溶液。
2.2.2 供试品溶液 另取甲氯霜约0.5 g,精密称定,置烧杯中,加乙醇约30 ml,置80 ℃水浴中加热2 min,振摇使溶解,转移至50 ml量瓶中,放冷至室温,用乙醇稀释至刻度,摇匀,置冰浴中冷却3 h,取出后迅速滤过,续滤液放至室温,再精密量取3 ml置10 ml量瓶中,用乙醇稀释至刻度,摇匀,过0.22 μm微孔滤膜,即得。
2.2.3 阴性样品溶液 根据处方中药物的比例,按相关工艺制备不含甲硝唑、氯霉素和羟苯乙酯的阴性样品,再按2.2.2项下方法制成阴性样品溶液。
2.3 系统适用性实验 分别取2.2项下混合对照品溶液、供试品溶液、阴性样品溶液各10 μl注入HPLC仪,按2.1项下色谱条件进样测定,记录色谱图,结果见图1。由图1可见,各主成分分离度好,阴性样品在3种成分相应位置上无吸收,表明阴性无干扰。
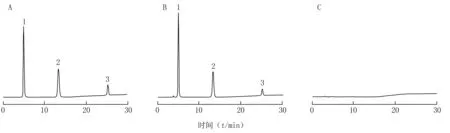
图1 甲氯霜的HPLC谱图Figure 1 HPLC chromatograms of Jialv creamA:混合对照品溶液;B:供试品溶液;C:阴性样品溶液;1:甲硝唑;2:氯霉素;3:羟苯乙酯
2.4 线性关系考察 分别精密吸取2.2.1项下对照品储备液1和对照品储备液3各2、2.5、3、3.5、4 ml置10 ml量瓶中,加乙醇稀释至刻度,分别吸取10 μl注入色谱仪,按2.1项下色谱条件测定。以对照品的质量浓度(c,单位μg/ml)为横坐标,以峰面积(A)为纵坐标,绘制标准曲线。得到甲硝唑、氯霉素及羟苯乙酯的回归方程分别为A甲硝唑=3.01×104c+3.28×103(r=0.999 9),线性范围38.68~77.36 μg/ml;A氯霉素=1.91 ×104c-6.19×103(r=0.999 9),线性范围38.24~76.49 μg/ml;A羟苯乙酯=7.86×104c+4.78×102(r=0.999 9),线性范围1.87~3.75 μg/ml。结果表明,3种成分在相应范围内线性关系良好。
2.5 精密度实验 吸取2.2.1项下混合对照品溶液,重复进样6次,每次10 μl,测定其峰面积并计算RSD值。结果甲硝唑、氯霉素及羟苯乙酯峰面积的RSD值分别为0.73%、0.97%、1.02%(n=6),表明仪器精密度良好。
2.6 重复性实验 精密称取6份样品(批号180911)各0.5 g,按2.2.2项下方法制备供试品溶液,按2.1项下色谱条件进行测定,结果甲硝唑、氯霉素及羟苯乙酯峰面积的RSD值分别为1.01%、0.93%和1.11%(n=6),表明该方法重复性良好。
2.7 稳定性实验 取2.6项下1号供试品溶液适量,分别于0、2、4、8、12 h进样10 μl,测定峰面积并计算RSD值。结果甲硝唑、氯霉素及羟苯乙酯峰面积的RSD值分别为1.03%、0.98%、1.11%(n=5),表明供试品溶液在配制后12 h内稳定。
2.8 加样回收率实验 精密称取已知含量的样品9份(批号180911),每份约0.25 g,按照样品中各成分含量的80%、100%、120%分别精密加入相应对照品(甲硝唑对照品溶液浓度为1.065 mg/ml,氯霉素对照品溶液浓度为1.004 mg/ml,羟苯乙酯对照品溶液浓度为0.234 2 mg/ml ),按2.2.2项下方法制备供试品溶液,并按2.1项下色谱条件测定,计算平均回收率。结果甲硝唑、氯霉素和羟苯乙酯的平均回收率分别为(99.4±0.4)%、(99.3±0.8)%、(98.9±0.4)%(n=9)。
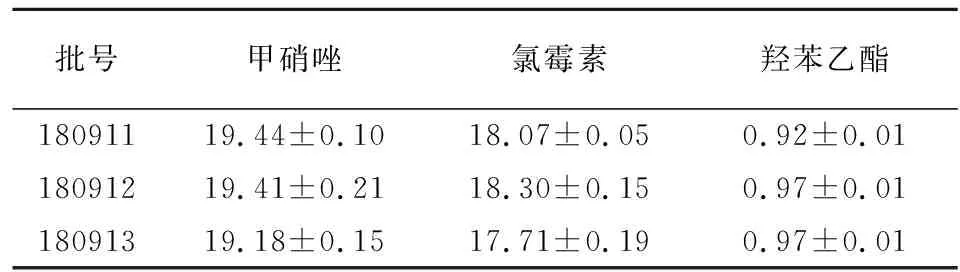
2.9 样品含量测定 分别取3批样品,每批3份,精密称定,按照2.2.2项下方法制备供试品溶液,按2.1项下色谱条件进行含量测定,以外标法计算含量,结果见表1。
表1 甲氯霜中甲硝唑、氯霉素和羟苯乙酯含量测定结果
Table 1 Determination results of the components of
metronidazole,chloramphenicol and
ethylparaben in Jialv cream
批号甲硝唑氯霉素羟苯乙酯18091119.44±0.1018.07±0.050.92±0.0118091219.41±0.2118.30±0.150.97±0.0118091319.18±0.1517.71±0.190.97±0.01
2.10 含量限度确定 本处方中甲硝唑和氯霉素的理论含量均为18.8 mg/g,羟苯乙酯理论含量为1 mg/g,取其标示量的90.0%~110.0%为含量限度,即得甲硝唑和氯霉素的含量限度均为16.9~20.6 mg/g,羟苯乙酯的含量限度为0.9~1.1 mg/g。本研究所测含量结果均在此范围内。
3 讨 论
3.1 提取溶剂的选择 作者曾比较了甲醇、乙醇两种提取溶剂,结果两者提取的样品冰浴后,基质均无明显析出,但乙醇提取的样品中3种药品含量均略高且杂质峰面积较小,故选择乙醇为提取溶剂。另在提取过程中,瓶底部有少许黄色团状物,其为升华硫,在滤过中除去,不影响含量测定。
3.2 冰浴时间的考察 预实验中曾考察了冰浴1、2、3、4 h对提取效果的影响。结果冰浴3 h与4 h药品含量基本一致,表明冰浴3 h即可将有效成分提取完全,故选择冰浴3 h。
3.3 流动相的选择 本研究曾考察甲醇-乙腈-水(50∶5∶45)[7]体系作为流动相,但羟苯乙酯峰保留时间为33 min,出峰时间较迟;又考察了甲醇-水(68∶32)[8]体系,氯霉素峰拖尾严重;后尝试甲醇-0.1%冰乙酸溶液与甲醇-0.5%冰乙酸溶液体系,结果发现甲醇-0.5%冰乙酸溶液体系比甲醇-0.1%冰乙酸溶液体系分离效果好,三者峰形尖锐,拖尾因子符合要求,且均达到基线分离,在25 min内即可完成含量测定,故选择甲醇-0.5%冰乙酸溶液体系作为流动相。
3.4 检测波长的选择 将甲硝唑、氯霉素和羟苯乙酯3种对照品储备液用流动相稀释后在200~400 nm波长范围内进行扫描,结果甲硝唑、氯霉素、羟苯乙酯的最大吸收波长分别为320、278、256 nm,三者吸收波长差异较大,因此选择波长切换法分别在各自吸收峰值处测定其含量。
3.5 柱温的选择 本研究曾比较了柱温为25 ℃、30 ℃和40 ℃条件下的样品分离情况,发现柱温为25 ℃和30 ℃时,样品分离效果不好,重现性较差,而柱温为40 ℃时,样品各成分峰形对称,均达到基线分离,且重复性好,故选择柱温为40 ℃。
