曲克芦丁及其代谢产物在大鼠体内的排泄动力学研究
2020-07-06余芳金涌
余芳,金涌
作者单位:安徽医科大学药学院,安徽 合肥230032
曲克芦丁是黄酮类化合物芦丁的半合成衍生物,可以抑制血小板凝集,防止血栓形成,具有抗氧化、抗炎、抗化学性肝损伤等一系列药理作用;是临床上用来治疗慢性静脉功能不全、毛细管出血、脑血栓等疾病的常用药物[1-6]。近年来对曲克芦丁的研究主要集中在药理作用和作用机制等方面[7-10],关于其代谢方面的研究知之甚少。曲克芦丁在大鼠和人体内的药代动力学研究表明曲克芦丁口服吸收差,生物利用度低,临床应用不良反应较多[11-12]。我们前期的研究结果表明曲克芦丁在体内主要被肠道菌群代谢脱去芸香糖成曲克芦丁苷元[13]。因此弄清曲克芦丁及其代谢产物在体内的排泄情况是研究曲克芦丁的一个非常重要的补充。本研究起止时间为2018年7月至2019年3月,针对大鼠腹腔注射曲克芦丁后其在尿液、胆汁和粪便样品中的排泄情况,以及曲克芦丁代谢产物在粪便中的生成量,探讨了曲克芦丁在体内的一般排泄规律。
1 材料与方法
1.1 仪器、试剂与实验动物 LC-20A高效液相色谱仪(日本岛津公司);Neofuge23R台式高速冷冻离心机(力康发展有限公司);KQ-500DE型医用数控超声波清洗器(昆山市超声仪器有限公司);XW-80A涡旋振荡器(上海精科实业有限公司);超纯水机(美国Millipore公司)。
曲克芦丁原料药(阿拉丁试剂有限公司,生产批号T101630);芦丁对照品(中国药品生物制品检定所,生产批号100080-201811,)、曲克芦丁对照品(中国药品生物制品检定所,生产批号100416-201607);甲醇(天津四友精细化学品公司,生产批号0113180403,色谱纯);其他试剂为分析纯。
健康雄性SD大鼠5只,体质量范围为(250±50)g,(安徽医科大学实验动物中心,动物实验合格证号:皖医实动准字第01号)。
1.2 色谱条件 色谱柱为Shim-pack ODS C18柱(250 mm×4.6 mm,5 μm);内标物为芦丁;流速为1.0 mL/min;柱温40℃;检测波长350 nm;流动相为甲醇(A)和1.7%冰醋酸(B),梯度洗脱(0~15 min,41%A;15~30 min,41%~65%A;30~40 min,65%~41%A);进样量20 μL。
1.3 实验试剂和溶液配制
1.3.1 药物溶液的配制 用0.9%的生理盐水将曲克芦丁制成5.25 mg/mL的溶液,临用前配制。
1.3.2 标准溶液的配制 精密称取芦丁、曲克芦丁、曲克芦丁苷元对照品,用甲醇配制成质量浓度为1.0 mg/mL标准储备液,4℃保存。
1.4 给药与样品采集
1.4.1 尿液和粪便 SD大鼠5只,雄性,分别置于5只代谢笼中,给药前12 h禁食,不禁水,收集空白尿液、粪便。腹腔注射曲克芦丁,剂量为52.5 mg/kg,分别收集0~2 h、2~4 h、4~8 h、8~12 h、12~24 h的尿液和粪便,测定尿液容积后置于-20℃冰箱保存。粪便烘干研碎称重后置于-20℃冰箱保存。
1.4.2 胆汁 SD大鼠5只,雄性,给药前12 h禁食,不禁水。腹腔注射10%水合氯醛(0.3 mL/100 g)麻醉后,仰卧固定于手术台上,做胆管插管引流术,见有胆汁稳定流出后,收集空白胆汁。收集一段时间后腹腔注射曲克芦丁,剂量为52.5 mg/kg,分别收集0~1 h、1~2 h、2~4 h、4~8 h、8~12 h的胆汁,测定胆汁容积后置于-20℃冰箱保存。实验中腹腔注射2 mL生理盐水以补充体液。
1.5 样品预处理
1.5.1 尿液样品预处理 分别精密吸取尿液样品、内标芦丁溶液100 μL于1.5 mL离心管中,加入100 μL甲醇,涡旋震荡1 min使之充分混匀,10 000 r/min离心10 min。精密吸取200 μL上清液于另一干净离心管中供高效液相色谱法(HPLC)检测。
1.5.2 粪便样品预处理 取大鼠粪便样品,加2倍量生理盐水,超声10 min,制成匀浆,4 000 r/min离心10 min后取上清液。粪便精密吸取粪便匀浆上清液、内标芦丁溶液100 μL于1.5 mL离心管中,加入100 μL甲醇,涡旋震荡1 min使之充分混匀,10 000 r/min离心10 min。精密吸取200 μL上清液于另一干净离心管中供HPLC检测。
1.5.3 胆汁样品预处理 分别精密吸取胆汁样品、内标芦丁溶液100 μL于1.5 mL离心管中,加入甲醇100 μL,涡旋震荡1 min使之充分混匀,10 000 r/min离心10 min。精密吸取200 μL上清液于另一干净离心管中供HPLC检测。
2 实验结果
2.1 方法学结果
2.1.1 专属性考查 分别取空白尿液、空白粪便匀浆和空白胆汁,空白尿液、空白粪便匀浆和空白胆汁加曲克芦丁和内标芦丁对照品溶液,以及给药后的样品溶液,按“1.5”项下样品预处理方法操作,进样分析,得到相应的色谱图。由图可知,内标芦丁和曲克芦丁在大鼠空白尿液、空白粪便匀浆和空白胆汁中的保留时间分别为12 min和15 min左右,曲克芦丁苷元的保留时间为35 min左右,分离度符合要求,杂质不影响测定。
2.1.2 线性关系 分别取空白尿液、空白粪便匀浆和空白胆汁,加入曲克芦丁储备液,制成0.1、0.5、1.0、5.0、10.0、100.0、500.0、1 000.0 μg/mL的尿液样品;0.1、0.5、1.0、5.0、10.0、20.0、40.0、80.0 μg/mL的粪便样品;0.1、0.5、1.0、5.0、10.0、100.0、500.0、1 500.0 μg/mL的胆汁样品;取空白粪便匀浆,加入曲克芦丁苷元储备液,制成0.1、0.5、1.0、5.0、10.0、80.0、400.0、800.0 μg/mL的粪便样品,按“1.5”项下样品预处理方法操作。横坐标为曲克芦丁和曲克芦丁苷元的浓度,纵坐标为曲克芦丁、曲克芦丁苷元与内标芦丁的峰面积比值,绘制标准曲线,得到标准曲线方程。曲克芦丁在尿液、粪便和胆汁中的标准曲线方程分别为y=0.0455x-0.0837(r=0.999 8,线性范围0.1~1 000.0 μg/mL)、y=0.057 7x-0.051 5(r=0.999 4,线性范围0.1~80.0 μg/mL)、y=0.043 3x+0.141 9(r=0.999 9,线性范围0.1~1 500.0 μg/mL);曲克芦丁苷元在粪便中的标准曲线方程为y=0.053 8x-0.076 3(r=0.999 1,线性范围 0.1~800.0 μg/mL)。
2.1.3 回收率和精密度 分别取空白尿液、空白粪便匀浆、空白胆汁,加入曲克芦丁对照品溶液,制成0.5、10.0、60.0 μg/mL的低、中、高三个浓度样品,每个浓度制备5个样品,按“1.5”项下样品预处理方法进行处理后进样,计算方法回收率。取空白粪便匀浆,加入曲克芦丁苷元对照品溶液,制成0.5、10.0、60.0 μg/mL低、中、高三个浓度样品,每个浓度制备5个样品,按“1.5”项下样品预处理方法进行处理后进样,计算方法回收率。同时制备0.5、10.0、60.0 μg/mL曲克芦丁和曲克芦丁苷元对照品溶液,直接进样。同等浓度尿液、粪便匀浆、胆汁中曲克芦丁的峰面积和曲克芦丁对照品峰面积的比值为提取回收率。同法配制低、中、浓度的尿液、粪便、胆汁样品,按“1.5”项下处理后进样,同日和连续5 d各测定5份样品。计算日内和日间精密度。结果,曲克芦丁在尿液中低中高浓度的方法回收率分别为(104.10±9.62)%,(98.05±6.29)%,(92.67±3.34)%(n=5),提取回收率分别为(84.01±11.54)%,(85.47±7.82)%,(81.93±8.38)%(n=5);日内精密度分别为9.82%,7.51%,6.13%;日间精密度分别为5.46%,9.37%,8.25%。曲克芦丁在粪便中低中高浓度的方法回收率分别为(90.0±6.67)%,(96.1±5.46)%,(93.19±7.22)%(n=5),提取回收率分别为(78.05±11.11)%,(82.64±7.08)%,(72.95±8.66)%(n=5);日内精密度分别为8.66%,10.41%,7.75%;日间精密度分别为7.94%,10.27%,9.98%。曲克芦丁在胆汁中低中高浓度的方法回收率分别为(94.15±8.51)%,(96.31±7.76)%,(96.59±3.80)%(n=5);提取回收率分别 为(74.10±10.64)% ,(83.26±8.80)%,(82.75±7.88)%;日内精密度分别为10.12%,8.53%,8.56%;日间精密度分别为8.62%,9.73%,10.64%。曲克芦丁苷元在粪便中低中浓度的方法回收率分别为(90.20±10.51)% ,(95.32±9.68)% ,(100.08±7.66)%(n=5);%,提取回收率分别为(82.07±9.23)%,(77.62±11.28)%,(80.70±11.59)%(n=5);日内精密度分别为6.09%,4.45%,3.35%;日间精密度分别为5.63%,5.17%,7.06%。
2.1.4 定量限和检测限 取曲克芦丁对照品储备液分别用尿液、粪便和胆汁稀释,曲克芦丁苷元对照品储备液用粪便稀释,按“2.1”项下方法测定,以S/N=10计算,曲克芦丁在尿液、粪便和胆汁中的定量限分别为0.17、0.11、0.14 μg/mL,曲克芦丁苷元在粪便中的定量限为0.13 μg/mL;以S/N=3计算,曲克芦丁在尿液、粪便和胆汁中的检测限分别为0.051、0.033、0.042 μg/mL,曲克芦丁苷元在粪便中的检测限为0.039 μg/mL。
2.2 排泄结果
2.2.1 尿液样品中的排泄情况 大鼠腹腔注射曲克芦丁52.5 mg/kg后,尿液中曲克芦丁的累积排泄率为(16.17±10.28)%。见图2。
2.2.2 粪便样品中的排泄情况 结果表明曲克芦丁大鼠腹腔注射曲克芦丁52.5 mg/kg后,粪便中曲克芦丁原型药物的累积排泄率为(0.54±0.47)%,见图2。曲克芦丁代谢物曲克芦丁苷元的累积生成量为(22.69±12.48)%,见图3。
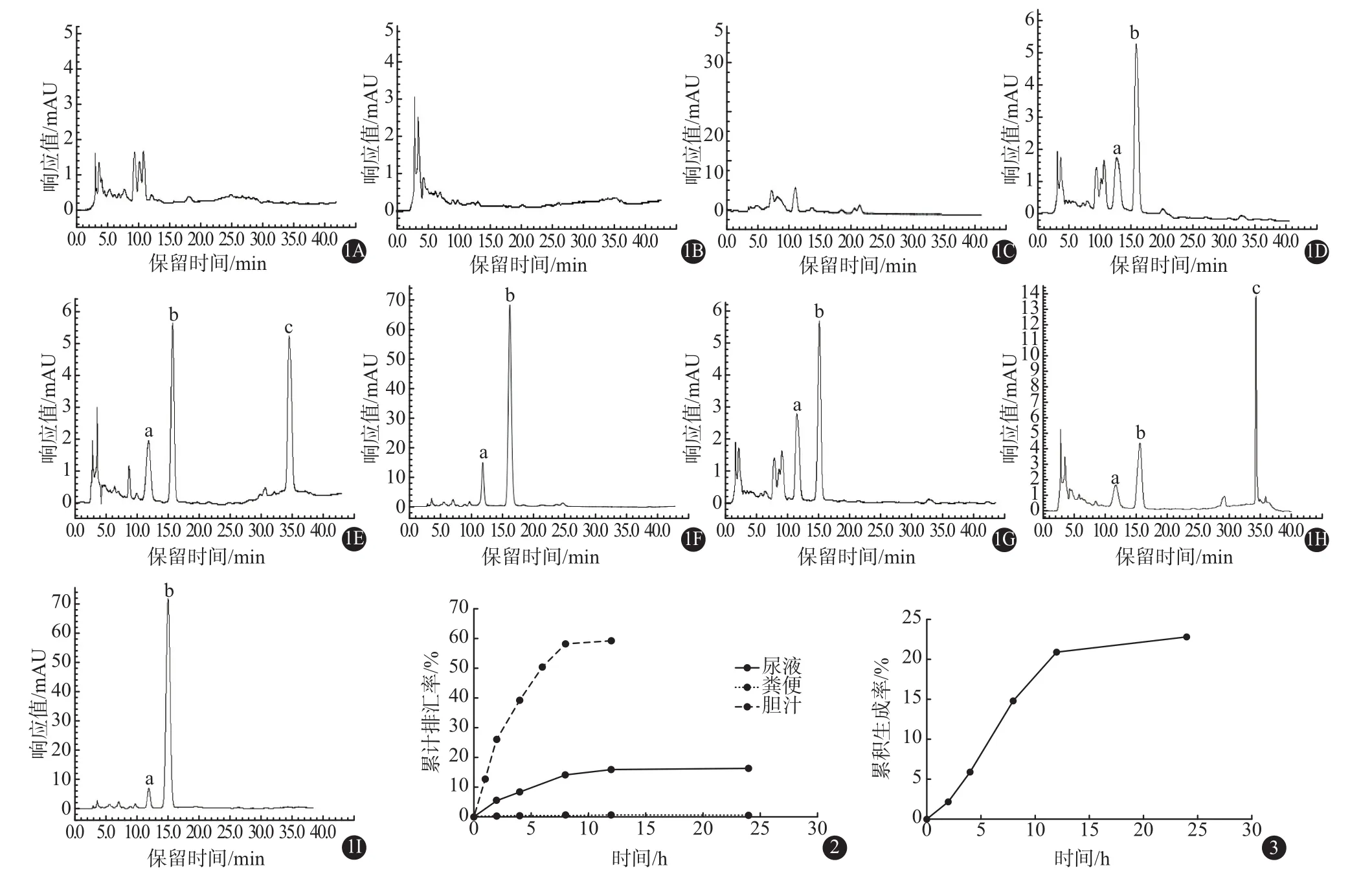
图1 曲克芦丁和曲克芦丁苷元在大鼠尿液、粪便和胆汁中的高效液相色谱图:A为空白尿液,B为空白尿液加对照品,C为给药后尿液样品,D为空白粪便,E为空白粪便加对照品,F为给药后粪便样品,G为空白胆汁,H为空白胆汁加对照品,I为给药后胆汁样品 图2 大鼠腹腔注射给药后曲克芦丁在大鼠尿液、粪便和胆汁中的累积排泄率 图3 曲克芦丁苷元在大鼠粪便中的累积生成率
2.2.3 胆汁样品中的排泄情况 大鼠腹腔注射曲克芦丁52.5 mg/kg后,胆汁中曲克芦丁的累积排泄率为(58.94±13.37)%。见图2。
3 讨论
新药开发与研究中有很多重要的环节,其中药动学研究是不可或缺的一环。影响药物的生物利用度的一个重要因素就是药物在体内的代谢情况[14]。近年来,曲克芦丁在大鼠体内的排泄动力学及组织分布已有报道[15],在人[11-12]和Beagle犬[16]体内的药代动力学也有相关研究。但曲克芦丁和其代谢产物在大鼠体内的排泄动力学尚未见相关研究。因此,本研究以大鼠为研究对象,腹腔注射曲克芦丁后,对其在大鼠尿液、粪便和胆汁中的排泄与代谢进行了研究。
本研究中大鼠腹腔注射曲克芦丁52.5 mg/kg后,曲克芦丁在大鼠尿液(24 h)、粪便(24 h)和胆汁(12 h)中的累积排泄分数分别为(16.17±10.28)%、(0.54±0.47)% 和(58.94±13.37)% ,总 量 约 为76.00%;大鼠粪便中曲克芦丁代谢产物曲克芦丁苷元的累积生成量为(22.69±12.48)%。本研究结果表明,曲克芦丁主要通过胆汁进行排泄;最后在粪便中生成代谢产物排出体外。这是因为相对分子质量大于300并且有极性基团的药物主要通过胆汁排到肠道,最后随粪便排出体外。肠道中有着种类丰富的肠道菌群[17],糖苷类化合物可被肠道中的微生物水解生成苷元[18-19]。曲克芦丁结构中存在着糖苷键,容易被肠道菌群水解释放出苷元。同时糖苷键在酸性环境下容易水解,曲克芦丁口服进入体内后在胃肠道内发生代谢转化,这可能是曲克芦丁血药浓度低的一个重要因素。因此后续的工作将围绕曲克芦丁口服后的吸收机理和在体内的转化进行展开,以期弄清曲克芦丁在体内发挥药效的作用机制。
