克唑替尼相关药物性肝损1例及文献复习
2020-07-02任长娟张瑞侠李晓红
任长娟 张瑞侠 李晓红
间变性淋巴瘤激酶(anaplasticlymphoma kinase,ALK)融合基因是肺癌常见的驱动基因之一,约3%~5%非小细胞肺癌(non-small-cell lung cancer,NSCLC)患者可携带ALK融合基因[1],其中以与棘皮动物微管相关类蛋白4(echinoderm microtubule associated protein like 4,EML4)形成的ALK-EML4融合基因最为常见[2]。克唑替尼是ALK融合基因阳性NSCLC患者一线标准治疗之一,多项研究显示克唑替尼相关肝损伤是其最常见不良反应之一[3],但对于肝损伤处理尚缺乏统一。我们回顾克唑替尼相关肝损伤文献并结合本科室1例克唑替尼相关药物性肝损伤患者治疗经过,探讨克唑替尼相关药物性肝损对克唑替尼治疗的影响和应对策略。
临床资料
患者女,60岁,无吸烟史、无慢性病毒性肝炎及其他肝病病史,平素无长期服药病史。该患者因“胸闷、间断发热1月余”于2018年6月15日入院,入院后外周血检查结果(如表1)所示,肝肾功能、血常规、凝血功能未见明显异常。胸部CT见左上肺门旁见一大小约为44mm团状软组织密度影;上腹部CT提示肝右叶约4cm大小单发转移灶。针对肺部病灶行纤维支气管镜检查,镜下见左舌支管腔开口见息肉样新生物阻塞管口,局部活检组织病理示:肺低分化恶性肿瘤、倾向低分化腺癌,送检蜡块及外周血高通量测序检测(NextSeq 550AR平台)均提示ALK-EML4融合基因阳性,类型为EML4-ALK(E6;A20),融合基因丰度为8.4%。BRAF 、EGFR、ERBB2(HER2) 、KRAS、MET、RET、ROS1均为阴性(见图1)。
患者自2018年7月3日开始口服克唑替尼 250mg bid治疗,半月后患者胸闷症状逐渐缓解,无发热,有轻度乏力,食欲正常,2018年7月19日复查肝功能正常但ALT较前有所升高,2018年7月26日再次复查肝功能示ALT 389U/L,AST 65U/L,GGT 50U/L,AKP 109U/L,停用克唑替尼,静脉使用多烯磷脂酰胆碱465mg qd、复方甘草酸苷120mg qd治疗,2018年8月6日复查肝功能示ALT 215U/L,AST 55U/L,GGT 41U/L,AKP 107U/L,2018年7月31日复查胸部CT左肺病灶明显缩小,治疗有效,于2018年8月10日开始再次服用克唑替尼 250mg bid,改口服多烯磷脂酰胆碱胶囊2粒tid、复方甘草酸苷片 2片 tid保肝治疗,2018年8月20日复查肝功能ALT 113U/L,AST 57U/L,GGT 59U/L,AKP 104U/L,仍有肝损害,将整克唑替尼调为250mg qd治疗,分别于2018年8月2日5、2018年9月4日、2018年9月11日、2018年9月18日复查肝功能,ALT在68~80U/L,AST在50~54U/L,GGT在50~69U/L,AKP在91~124U/L,2018年9月18日复查胸部CT左肺病灶消失,肝脏转移灶明显缩小,2018年10月17日复查上腹部增强CT提示肝脏转移灶消失,疗效评估达到完全缓解(complete remission,CR)。2018年10月17日恢复克唑替尼剂量为250mg bid,继续口服多烯磷脂酰胆碱胶囊2粒tid、复方甘草酸苷片 2片 tid保肝治疗,2018年10月22日复查肝功能ALT 48U/L,AST 33U/L,GGT 72U/L,AKP 126U/L;2018年11月1日复查肝功能ALT 82U/L,AST 53U/L,GGT 72U/L,AKP 112U/L,此后方案未作调整,2018年11月22日再次复查胸腹部CT,疗效评估仍为CR(见图2)。
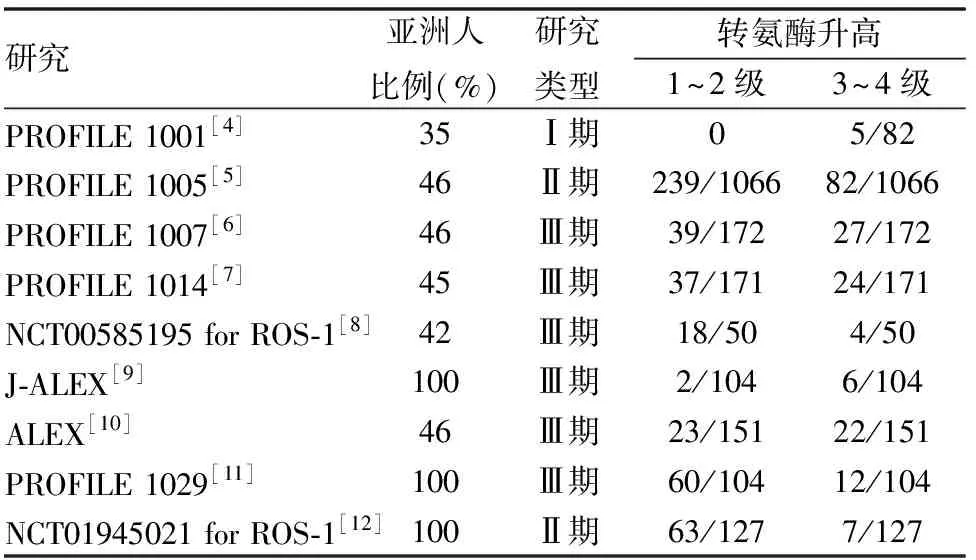
表1 克唑替尼相关前瞻性临床研究肝损伤结果列表
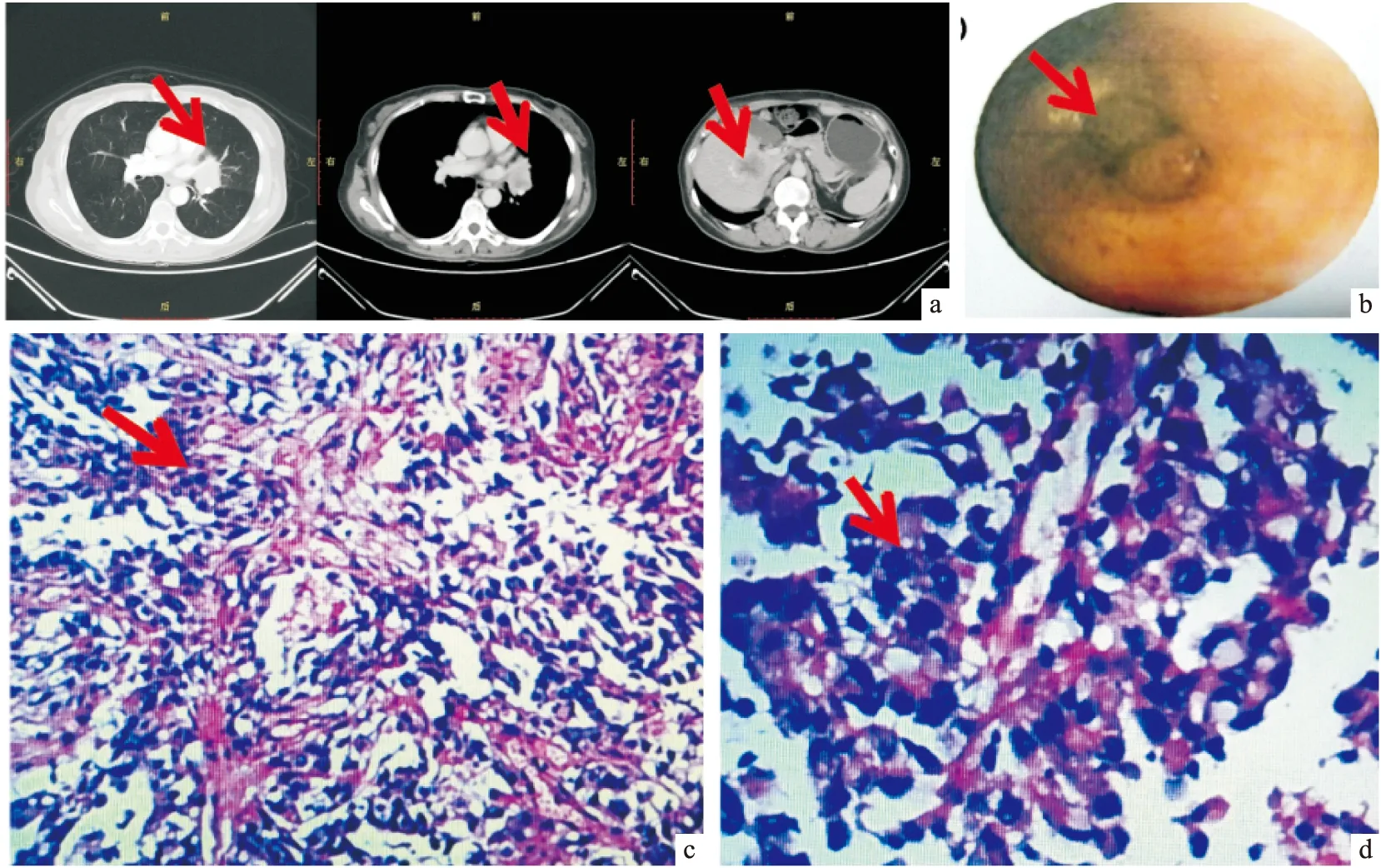
图1 患者影像学、气管镜检查及病理结果
a:初诊胸部CT及腹部CT检查结果:左上肺门旁见一大小约为33mm×44mm团状软组织密度影,远端见条片状高密度影,肿块包绕左肺门组织,相应左肺上叶舌段支气管明显变窄,增强后病变轻度强化,内见无强化坏死区;肝右叶见大小约37mm×39mm类圆形稍低密度灶,边界模糊,增强后病变呈轻度强化;b:气管镜检查是左肺舌段开口处新生物;c:气管镜活检病理HE染色(40×);d:气管镜活检病理HE染色(100×
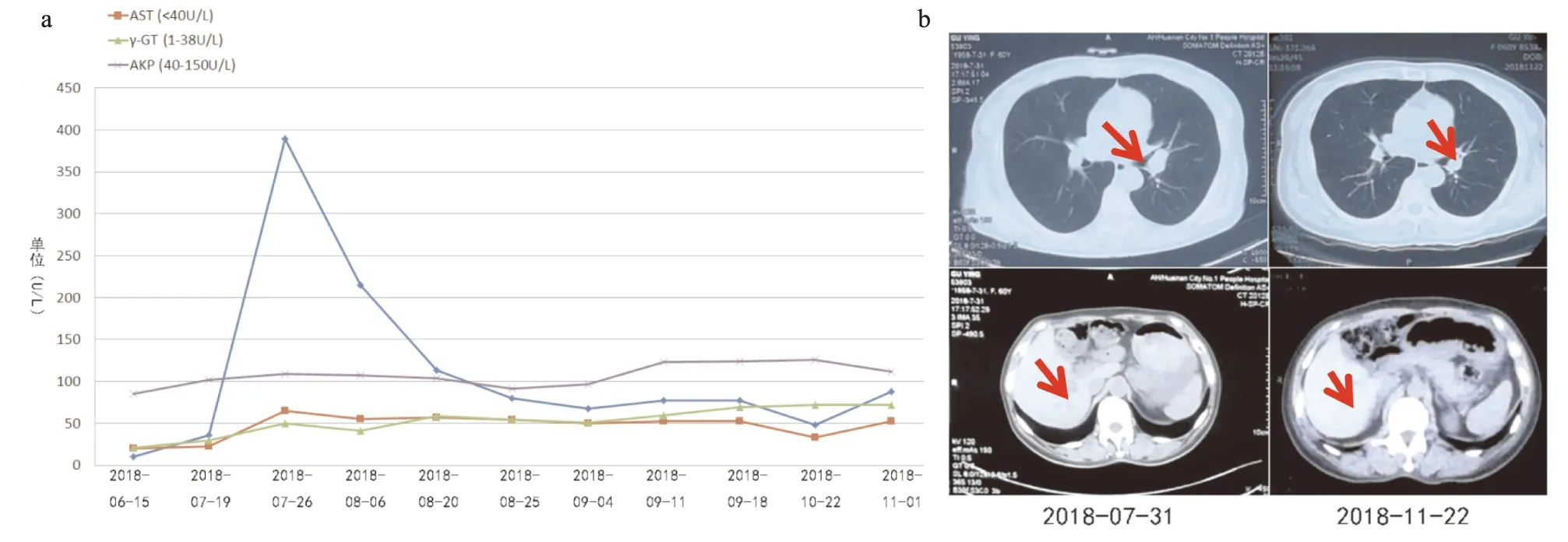
图2 患者治疗前后肝功能及病灶变化
a: 治疗过程中复查肝功能情况;b:胸部CT及腹部CT复查左肺门及肝右叶病变逐渐缩小,末次复查2018年11月22日现左上肺门旁软组织团块较前明显缩小,相应支气管壁增厚、管腔狭窄较前明显好转,阻塞性肺不张较前明显减轻;肝右叶转移灶消失。
讨 论
本文报道了一例ALK融合基因阳性的NSCLC患者一线克唑替尼治疗初期出现药物性肝损,予以停药及护肝治疗后恢复克唑替尼治疗并根据病情行剂量调整,最终患者由持续克唑替尼治疗中获益。这为临床针对克唑替尼相关药物性肝损的处理提供了依据。
克唑替尼是2011年由FDA批准上市的小分子口服酪氨酸激酶抑制剂(tyrosine kinase inhibitor,TKI)[13],对ALK、ROS-1和c-MET均有抑制活性[14]。ALK融合基因是肺癌主要的驱动基因之一,ALK融合基因大约占NSCLC患者5%左右。ROS-1基因重排也是肺癌驱动突变之一,约占NSCLC患者4%左右[15];c-MET扩增或14外显子跳跃突变约占NSCLC患者的1%左右[16]。因此,初诊的NSCLC患者中,大约10%为克唑替尼的潜在适应症对象。除此之外,部分表皮生长因子受体(epidermal growth factor receptor,EGFR)突变患者经EGFR-TKI靶向治疗后可以合并cMET扩增、ALK-EML4融合突变等导致耐药,对此类患者克唑替尼同样有效[17-18]。同时随着临床医生对临床决策前完成多种驱动突变检测意识的提高和得益于克唑替尼定价下调和进入医保等,未来克唑替尼在NSCLL患者中的使用将更为广泛,因此充分了解克唑替尼相关不良反应和应对策略十分重要。
克唑替尼相关药物性肝损是其最主要不良反应之一(如表1)所示,目前发表的前瞻性研究显示,克唑替尼相关肝损伤平均发生率为34.4%(670/1945),其中3级以上不良反应发生率为9.7%(189/1945),这其中三项针对亚洲人群的研究显示,克唑替尼在亚洲人群中肝损伤平均发生率为44.8%(150/335),其中3级以上不良反应发生率为7.5%(189/335)。国内的两项小样本回顾性临床研究则显示,克唑替尼治疗ALK融合基因阳性NSCLC患者中3级以上肝损发生率为12.8%[19]和12.0%[20],克唑替尼相关肝脏不良反应发生率显著高于化疗[21]。近期韩国研究人员开展的一项纳入了153例患者的回顾性研究显示,慢性乙型病毒性肝炎及其他慢性肝病和服用H2受体拮抗剂可显著增加克唑替尼相关肝损的发生风险,而患者年龄、性别、肝转移等其他因素并不增加克唑替尼相关肝损伤[22]。鉴于克唑替尼相关肝损发生率并不低,目前推荐对于克唑替尼治疗患者应在前两个月每两周复查肝功能[23]。本例患者口服克唑替尼治疗2周后复查肝功能基本正常但ALT较治疗前有所升高,故1周后再次复查肝功能可见ALT及AST均显著升高,此后予以停药及护肝治疗后又快速下降,这符合药物性肝损的临床表现,同时,该患者胆红素及AKP升高不明显,提示该患者以肝细胞损伤型为主。这提示对于克唑替尼治疗早期,注意复查肝功能的重要性。
克唑替尼相关肝损伤大部分经停药后可恢复,其中Charville等人报道的一例克唑替尼相关爆发性药物性肝损伤患者停药后1月左右肝功能基本恢复正常[24],而Adnlkarl等人报道的一例更为年长的克唑替尼相关爆发性药物性肝损伤患者则在入院后第18天死于多器官功能障碍[25]。近期发表的一项真实世界的研究显示,因不良反应导致停药占克唑替尼治疗患者的3.2%[26]。这些研究提示,对于克唑替尼治疗后出现肝损伤患者,早期处理十分重要。根据近年发表的、中华医学会肝病学分会药物性肝病学组制定的《药物性肝损伤诊治指南》[27],,对于出现以下任一情况患者应考虑停药:(1) 谷丙转氨酶≥5倍正常值上限;(2)碱性磷酸酶≥2 5倍正常值上限,特别是伴有5′核苷酸酶或谷氨酰转肽酶升高且排除骨病引起的碱性磷酸酶升高;(3)谷丙转氨酶≥3倍正常值上限且总胆红素≥2倍正常值上限。但对于克唑替尼停药后如何制定后续克唑替尼临床策略尚缺乏统一意见。本例患者ALT为正常值上限的9倍,因此予以停用克唑替尼并予以护肝治疗,2周后再次予以克唑替尼治疗,10日后将克唑替尼剂量减半,约2月后再次恢复克唑替尼推荐剂量,此后多次复查肝功能均提示肝酶基本稳定在正常值2倍左右。
尽管克唑替尼相关肝损伤已越来越受到临床重视,但目前对克唑替尼肝损伤发病机制尚不完全明确[28]。部分研究提示克唑替尼相关肝损伤可能与过高的血药浓度相关。克唑替尼主要通过细胞色素P450(eytoehrome P450,CYP450)家族中CYP3A途径代谢,同时克唑替尼也是是CYP3A的抑制剂[29]。研究显示,CYP3A5活性降低与克唑替尼肝损伤有一定相关性,抑制CYP3A5活性可增加克唑替尼相关肝毒性[30]。这提示对于同时服用CYP3A5抑制剂药物患者应更为关注其克唑替尼相关肝毒性。本例患者并无其他药物合并治疗,治疗过程中尽管存在半月余停药和长达2月的剂量减半,临床评估仍可达到CR,这提示该患者可能存在克唑替尼血药浓度偏高的现象,但受限于目前临床现状尚未推广克唑替尼血药浓度检测,尚不能验证这一推测。
综上所述,本文报道了一例克唑替尼相关药物性肝损的NSCLC患者,经短期停药和护肝治疗后再次恢复克唑替尼治疗,此后患者肝损伤出现反复,予以减量后好转,最终再次恢复克唑替尼推荐剂量,在该过程中病情评估显示克唑替尼疗效达到CR。这表明短期停药待肝功能好转后可再次尝试克唑替尼治疗,患者仍可从克唑替尼治疗中获益。
