聚偏氟乙烯/磷酸化纳米二氧化硅螯合金属锆杂化膜
2020-06-17孙俊芬张逸飞
孙俊芬,张逸飞,陈 龙
(东华大学 a. 材料科学与工程学院; b. 纤维材料改性国家重点实验室,上海 201620)
含磷蛋白作为蛋白质中非常重要的一个大类,其在各个领域都有非常大的发展潜力,例如卵清蛋白、酪蛋白[1]、卵黄磷蛋白[2]等都有优良的药用和生物研究价值。同时蛋白质磷酸化[3]也是当今蛋白质研究的重点之一,因为蛋白质磷酸化作为真核细胞信号转导中的核心,在生命系统中发挥着重要作用。因此,蛋白质磷酸化选择性分离是蛋白质分析中的重要任务。
固定化金属螯合亲和层析技术(immobilized metal-chelated affinity chromato-graphy,IMAC)是一种新型亲和层析技术,它主要用于分离生物大分子。1975年Paroth[4]提出这项技术,便引起了社会的广泛关注,IMAC技术具有很多独特的优点,不仅对蛋白质的分离具有选择性和特异性,以及分离得到的目标蛋白质纯度高,而且还可以用于基因工程技术、核酸的纯化与分离等生物医疗卫生领域。膜分离技术作为一种新兴交叉学科的高新技术,已经在日常生活中得到广泛的应用,而将膜分离技术与IMAC技术相结合能够很好地选择性分离含磷蛋白。
近些年来,IMAC技术的螯合配基又有了许多新的尝试,例如以磷酸基团作为新型的金属螯合剂。Zhou等[5]提出了磷酸基团作为新的金属螯合剂,同时螯合锆(Zr)与钛(Ti)金属离子,对于含磷的蛋白质有很强的特异性吸附能力。文献[6-7]研究表明,Zr与磷酸基团特异性结合对于含磷蛋白有优良的吸附效果。常用的固定金属亲和层析膜的改性方法即通过化学改性在膜表面接枝功能基团,这种方法对于膜的化学和物理性能都有很大影响,所以需要选择一种拥有更高稳定性的层析膜来试验。聚偏氟乙烯(PVDF)膜拥有优良的物理化学性能以及稳定性,是理想的膜材料。文献[8-12]通过在PVDF膜基体中添加无机粒子来制备杂化膜。利用纳米粒子表面的功能基团做进一步氨基化、磷酸化和固定螯合金属,可以达到分离含磷蛋白的目的[13-14]。
本文利用原位合成法和相转化法来制膜,同时利用改性后功能化纳米粒子对卵清蛋白的高吸附性和高分子膜的选择性分离原理,制备出了聚偏氟乙烯/氨基化纳米二氧化硅(PVDF/NH2-SiO2)杂化膜,最后通过磷酸化添加磷酸基团并螯合Zr离子,从而实现对卵清蛋白的选择性吸附。本文所采用的制膜方法比较简单,并且对卵清蛋白的分离固定时间较短,同时也在最大程度上保持了原有蛋白质的活性。
1 试 验
1.1 试验材料及仪器
试验材料:聚偏氟乙烯(PVDF,6020,苏威(上海)有限公司);正硅酸乙酯(TEOS,分析纯,国药集团化学试剂有限公司);3-氨丙基三乙氧基硅烷(APTES,高纯,国药集团化学试剂有限公司);N-甲基吡咯烷酮(NMP,分析纯,国药集团化学试剂有限公司);N,N-二甲基乙酰胺(DMAc,化学纯,国药集团化学试剂有限公司);卵清蛋白(生化试剂,上海阿拉丁生化科技股份有限公司);聚乙烯吡咯烷酮90(PVP K90,工业级,国药集团化学试剂有限公司);聚乙烯吡咯烷酮30(PVP K30,工业级,国药集团化学试剂有限公司)。
试验仪器:电子分析天平(CB603-N型,上海精密科学仪器仪表有限公司);恒温振荡器(SHZ-05型,上海申能博彩生物科技有限公司);电热真空干燥箱(ZKF-035型,上海实验仪器厂);红外光谱仪(Nicolet 8700型,美国Nicolet公司);紫外可见分光光度计(UV-1800型,岛津仪器苏州有限公司);双稳定时电泳仪(DYY-8C型,上海泰坦科技股份有限公司);扫描电子显微镜(Quanta-250型,捷克FEI);电感耦合等离子体发射光谱仪(Prodigy型,美国Leeman);X射线多晶衍射仪(Bruker D2 PHASER型,德国布鲁克AXS公司)。
1.2 磷酸化Zr+PVDF/NH2-SiO2杂化膜的制备
取质量分数为15%的PVDF颗粒于三口烧瓶中,然后加入质量分数为3%的PVP K90和质量分数为2%的PVP K30作为制孔剂,以NMP/DMAc(质量比为9∶1)为混合溶剂,分别加入质量分数为0、 4%、 8%、 10%的TEOS,再加入APTES(其与TEOS的质量比为1∶13),最后缓慢滴加几滴0.15 mol/L的稀盐酸作为催化剂,调节温度为45 ℃,转速为230 r/min,在此条件下溶胀2 h,之后温度调节为75 ℃,转速为280 r/min,溶解搅拌24 h。整个制备过程中分别加入不同质量分数的TEOS来制膜,从而可以制备出有不同TEOS含量的PVDF/NH2-SiO2杂化膜铸膜液。
将上述铸膜液趁热倒入洁净的烧杯中,并用保鲜膜封口,防止空气中水分的进入,使其在室温下静置脱泡10 h。待完全脱泡后,将铸膜液流延在洁净的不锈钢板上,用3号刮刀进行刮膜,使铸膜液展开形成具有一定厚度(300 μm)的均匀薄层,然后马上将附着有薄膜的不锈钢板放入水中凝固,使得薄膜固化,在凝固浴中浸泡1~2 d,然后测定膜的水通量,并做扫描电子显微镜(SEM)、衰减全反射傅里叶变换红外光谱(ATR-FTIR)、电感耦合等离子体(ICP)元素等分析。
磷酸化:取80 g磷酸与100 mL 二甲基甲酰胺置于400 mL烧杯中混合均匀,在100 ℃下,将所制备好的膜放入其中,进行磷酸化1 h,再用蒸馏水浸泡冲洗干净。
螯合固定Zr:取1.78 g ZrOCl2溶解于200 mL蒸馏水中,将磷酸化膜放入其中,浸泡8 h,再用蒸馏水浸泡冲洗干净,烘干后进行测试表征。磷酸化Zr+PVDF/NH2-SiO2杂化膜制备反应流程如图1所示。
1.3 膜的结构表征和性能评价
1.3.1 红外光谱测定
测试前将膜在烘箱中完全烘干,采用傅里叶变换红外光谱仪对PVDF纯膜和改性以后的PVDF/NH2-SiO2杂化膜进行ATR-FTIR分析,波数范围为4 000~400 cm-1,扫描次数为32次,精度为4 cm-1。
1.3.2 表观形态表征
测试前先将膜在30 ℃真空烘箱中干燥12 h,然后将膜放在液氮中冷冻并使其脆断,以保证其截面结构不受损伤,最后置于离子溅射喷金仪中对其截面进行喷金处理。在扫描电子显微镜下观察PVDF纯膜和磷酸化Zr+PVDF/NH2-SiO2杂化膜上表面、下表面以及膜断面处的形态结构。
1.3.3 X射线衍射光谱测定
把磷酸化Zr+PVDF/NH2-SiO2杂化膜置于60 ℃的真空烘箱中干燥24 h,然后用X射线衍射仪分析膜的物相组成,步长为0.02°,2θ测量范围为10°~60°,扫描速度为0.1(°)/s。
1.3.4 ICP元素分析
将含不同质量分数TEOS的PVDF/NH2-SiO2杂化膜在60 ℃的真空烘箱中烘干12 h,用ICP发射光谱仪测试样品中硅(Si)、磷(P)、 Zr的元素组成。
1.3.5 卵清蛋白吸附性能
分别剪取若干块1.5 cm×1.5 cm的膜,然后将它们置于真空烘箱中,设定温度为60 ℃,在此条件下烘10 h至完全干燥,然后用分析天平准确地称取各张膜的质量并做记录。取一块膜置于样品瓶中,并用移液枪在瓶中加入事先配置的5 mL 质量浓度为2 g/L的卵清蛋白溶液,盖好瓶盖,将恒温振荡器的温度设定为25 ℃,调节振动频率,振荡24 h,最后再用分光光度计在280 nm波长处测定卵清蛋白溶液的吸光度,并计算出卵清蛋白的质量浓度,根据式(1)计算膜吸附量q(mg/g)。
(1)
式中:c0为原液中卵清蛋白质量浓度,mg/mL;c1为吸附后溶液中卵清蛋白质量浓度,mg/mL;m为膜的干质量,g;V为卵清蛋白溶液的体积,mL。
取质量浓度为2 g/L的卵清蛋白吸附原液,在25 ℃下振荡吸附24 h,测试吸附前后卵清蛋白溶液的吸光度,计算膜的吸附量;然后用蒸馏水冲洗杂化膜,将膜置于10%的氨水溶液中,在25 ℃下振荡24 h,测量蛋白的解吸附率,即为第一次吸附试验;将杂化膜烘干后称其质量,重复上述步骤4次,来测定杂化膜的重复吸附率,根据式(2)计算膜的解吸附率(%)。
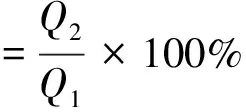
(2)
式中:Q1为膜的吸附量,mg/g;Q2为膜的解吸附量,mg/g。
2 结果与讨论
2.1 傅里叶变换红外光谱分析
纯PVDF膜、用APTES改性的PVDF/NH2-SiO2杂化膜,以及磷酸化Zr+PVDF/NH2-SiO2杂化膜的傅里叶变换红外光谱如图2所示。其中,PVDF纯膜的PVDF质量分数为15%,APTES改性的PVDF/NH2-SiO2杂化膜中TEOS质量分数为4%,磷酸化Zr+PVDF/NH2-SiO2杂化膜中TEOS质量分数为4%。由图2可知:PVDF纯膜在3 411 cm-1处没有吸收峰,当PVDF纯膜中引入氨基化SiO2后,在3 411 cm-1处出现了强烈的吸收峰,该吸收峰为N—H键的伸缩振动吸收峰,说明氨基化改性以后杂化膜内加入了NH2基团,实现了SiO2粒子的氨基化;与PVDF纯膜相比,改性后的PVDF/NH2-SiO2杂化膜在1 640 cm-1处出现了一个小的吸收峰,该吸收峰为N—H键的面内弯曲振动吸收峰,同样也说明了氨基化改性以后杂化膜内加入了NH2基团,证明实现了SiO2粒子的氨基化。对比曲线a和b可知,曲线c在1 076 cm-1处出现了一个新的吸收峰,此吸收峰为与Si和P化学键相关的吸收峰,说明磷酸化处理改性的PVDF/NH2-SiO2杂化膜中加入了含有Si和P的基团,证明PVDF/NH2-SiO2杂化膜上成功接入了磷酸基团。而固定螯合金属Zr的吸收峰在此FTIR谱图中不能显示,需用其他表征方法进一步测定。
2.2 表观形态分析
不同TEOS质量分数的PVDF/NH2-SiO2杂化膜(未经过磷酸化和螯合金属处理)的上表面与下表面的SEM图如图3所示,其放大倍数为10 000倍。从图3可以看出:杂化膜的上表面都是比较致密的形态结构,而下表面的孔洞比较多;随着TEOS质量分数的增加,杂化膜表面的孔洞也越来越多,孔径逐渐增大,且纳米粒子的团聚现象减少。因为TEOS经过水解-聚合反应形成硅氧聚合物,可以产生较长的线型硅氧键,然后随着硅氧键的伸展与链之间的相互交联,最后形成了一种交联的无规网络结构,它们能够与PVDF的大分子链互相缠绕,SiO2粒子穿插在PVDF溶液中,可以有效地阻碍PVDF大分子间的聚集,并且当PVDF铸膜液固化时,可以在无机相和有机相之间产生一定的空隙。
Fig.3 SEM images of top and bottom surfaces of PVDF/NH2-SiO2membranes with different TEOS mass fractions
2.3 X射线衍射光谱分析
由于PVDF分子链结构上含有很多氟基团(—F),因而分子链之间会形成氢键,制备得到的PVDF纯膜会具有相对比较高的结晶度。试验中采用TEOS与APTES和PVDF共混制备PVDF/NH2-SiO2杂化膜的实质是破坏了PVDF分子链之间的氢键。PVDF纯膜和不同质量分数的TEOS改性的磷酸化Zr+PVDF/NH2-SiO2杂化膜的XRD测试结果如图4所示。由图4可知,作为一种结晶型聚合物,PVDF纯膜在20°左右有一个明显的衍射峰,用TEOS和APTES共混改性后杂化膜的衍射峰相较于PVDF纯膜的衍射峰尖锐程度明显下降,衍射峰面积也减小,且随着TEOS质量分数的增加,PVDF杂化膜的结晶度呈现逐渐降低的趋势。因为TEOS和APTES的加入破坏了PVDF分子链之间的氢键,随着TEOS质量分数的增加,PVDF的结晶结构被破坏得越严重,膜的结晶度也随之降低。
2.4 元素组成分析
不同质量分数的TEOS改性制得的磷酸化Zr+PVDF/NH2-SiO2杂化膜的P、Si、Zr含量进行ICP(inductively coupled plasma)元素分析测试,结果如表1所示。

表1 磷酸化Zr+PVDF/NH2-SiO2杂化膜的ICP元素分析结果
由表1可知,在改性后的杂化膜上测到了P、 Si、 Zr 3种元素的存在,可以说明金属Zr已经成功地螯合到了PVDF/NH2-SiO2杂化膜上,并且当TEOS质量分数为8%时,PVDF/NH2-SiO2杂化膜可以负载更多的金属Zr。随着TEOS质量分数的增加,杂化膜上Si的含量也增加。这是由于TEOS的增加则导致铸膜液中硅氧聚合物增加,从而导致Si含量增加。随着TEOS质量分数的增加,杂化膜上P和Zr的含量先升高后降低。这是由于TEOS质量分数较低时,膜上固定的磷酸基团较少,所能螯合的Zr离子有限,所以Zr含量较低;当TEOS质量分数继续增加时,膜上功能基团(如NH2等)数量增加,能与更多的磷酸基团反应,进而能够固定螯合更多的Zr离子;但当TEOS质量分数继续增加,SiO2含量也随之增加,会形成团聚现象,从而导致能与硅烷偶联剂APTES反应脱水缩合的基团下降,并引起磷酸化和螯合金属的下降。
2.5 卵清蛋白吸附性能分析
2.5.1 TEOS质量分数对杂化膜吸附性能的影响
磷酸化Zr+PVDF/NH2-SiO2杂化膜对质量浓度为2 g/L的卵清蛋白的吸附量随TEOS质量分数的变化如图5所示。
从图5可以看出,随着TEOS质量分数的增加,磷酸化Zr+PVDF/NH2-SiO2杂化膜对卵清蛋白的吸附量先快速上升,然后缓慢升高到最大值,再略微降低,当TEOS质量分数为8%时,磷酸化Zr+PVDF/NH2-SiO2杂化膜对卵清蛋白的吸附量达到最大值,为150.7 mg/g。由此说明,通过在PVDF铸膜液中加入TEOS后能够有效地提高PVDF膜对卵清蛋白的吸附能力,且加入不同质量分数的TEOS改性的磷酸化Zr+PVDF/NH2-SiO2杂化膜对蛋白质的吸附能力的提高程度是不同的。这是由于加入PVDF铸膜液中的TEOS经过水解-聚合反应可以生成硅氧聚合物,并且产生了较长的线性硅氧键,由于大分子链之间的相互交联以及硅氧键的不断伸展,最后便会产生线性交联的三维无规网络结构,它们能与PVDF分子链互相缠绕,SiO2穿插在PVDF溶液中,有效地阻止了PVDF大分子间的聚集,然后通过TEOS与APTES可以引入功能基团,进而与磷酸基团反应,由于磷酸基团可以螯合Zr,而Zr对于含磷蛋白(如卵清蛋白)有很好的吸附效果。随着TEOS质量分数的增加,加入的APTES浓度也在增加(APTES和TEOS的质量比为13∶1),由于反应过程是TEOS水解成SiO2粒子,然后与APTES反应,即对SiO2粒子进行氨基化,所以在SiO2粒子上的氨基也在增加,可以引入更多的磷酸基团以及固定螯合更多的Zr,所以磷酸化Zr+PVDF/NH2-SiO2杂化膜对卵清蛋白的吸附会随着TEOS质量分数的增加而增加;当TEOS质量分数增加到8%后,由于杂化膜表面积有限,引入的磷酸基团和固定的Zr会达到一个最大值,这时磷酸化Zr+PVDF/NH2-SiO2杂化膜对卵清蛋白的吸附提供的吸附位点和吸附空间达到最大值,所以吸附量也达到最大值;继续增加TEOS质量分数,SiO2含量也增加,使得其本身发生了团聚现象,从而导致与硅烷偶联剂APTES脱水缩合的反应基团下降,P和Zr的含量也随之下降,引起吸附效果的下降。
2.5.2 磷酸化Zr+PVDF/NH2-SiO2杂化膜的重复吸附
利用磷酸化Zr+PVDF/NH2-SiO2杂化膜吸附卵清蛋白不是本文研究的最终目的,还需通过对磷酸化Zr+PVDF/NH2-SiO2杂化膜进行解吸附处理,从而将其所吸附的卵清蛋白释放出来,这样可以将释放出的卵清蛋白另作他用,同时将磷酸化Zr+PVDF/NH2-SiO2杂化膜循环使用。磷酸化Zr+PVDF/NH2-SiO2杂化膜(TEOS质量分数为8%,磷酸化处理1 h)对卵清蛋白的重复吸附率的测试结果如表2所示。
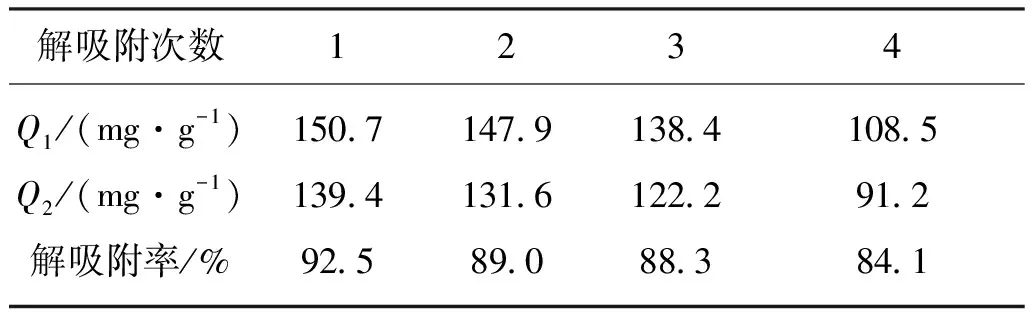
表2 磷酸化Zr+PVDF/NH2-SiO2杂化膜对卵清蛋白的重复吸附容量
试验中采用质量浓度为2 g/L的卵清蛋白溶液(用pH值为5的缓冲溶液配置)进行吸附,然后用质量分数为10%的氨水溶液对杂化膜进行解吸附处理,重复4次。由表2可知,随着重复吸附次数的增加,磷酸化Zr+PVDF/NH2-SiO2杂化膜对卵清蛋白的吸附量和解吸附量均逐渐减少。这可能由于膜在每次使用的过程中均有一部分蛋白质未被洗脱,从而造成了膜的污染。但是从整体上而言,试验中所制得的磷酸化Zr+PVDF/NH2-SiO2杂化膜对卵清蛋白具有良好的重复吸附和解吸附能力,可以循环使用。
3 结 语
本文成功地用APTES改性TEOS制备出氨基化的SiO2,并用原位合成法制备分散良好、性能优异的PVDF/NH2-SiO2杂化膜,最后成功对膜进行了磷酸化和螯合固定金属锆。研究结果表明,随着TEOS质量分数的增加,磷酸化Zr+PVDF/NH2-SiO2杂化膜对卵清蛋白的吸附量先快速上升,然后升高到最大值,稳定后再略微降低,当TEOS质量分数为8%时,杂化膜对卵清蛋白的吸附量达到最大值,为150.7 mg/g。通过将磷酸化Zr+PVDF/NH2-SiO2杂化膜循环使用,表明该杂化膜具有良好的重复吸附和解吸附能力。
