铜锰铈复合氧化物催化甲苯燃烧研究
2020-05-29左满宏郭喜文刘恩莉徐敏燕
左满宏,郭喜文,高 超*,刘恩莉,徐敏燕
(1.西安元创化工科技有限公司,陕西 西安 710061; 2.鲁西催化剂有限公司,山东 聊城 252211)
挥发性有机化合物(VOCs)通常指在常温下,沸点(50~260) ℃的各种有机化合物[1]。工业上通常以组分复杂、低浓度、高通量和大体积等特点排放到大气,这些挥发性有机化合物对人类和环境造成巨大伤害[2]。甲苯是典型的VOC,具有挥发性和易燃性。甲苯去除技术包括吸附[3]、催化燃烧[4]、光催化降解[5]和物理分离[6]。催化燃烧法是去除甲苯的最经济的策略之一,它具有更大的处理能力,更高的效率和更低的操作温度(低于550 ℃)。目前,贵金属催化剂和过渡金属氧化物催化剂已广泛应用于甲苯催化燃烧[7]。贵金属催化剂催化性能更加优异,更易活化C—H键,但是贵金属活性组分铂、钯价格高,且对氯或硫敏感,易中毒,长时间高温反应,活性组分易烧结导致性能下降。过渡金属氧化物催化剂(如CuO和MnO2)便宜并且对氯或硫有一定耐受力,不宜中毒,有时硫和氯还可以作为促进剂修饰和改善催化剂的氧化性能[8]。
近年来,具有尖晶石结构(AB2O4)的多元复合氧化物广泛应用于催化、储能、锂电池等方面,AB2O4型化合物中A、B位金属阳离子的选择多样,晶体结构的差异通常会在光、电、磁、热等激发诱导下引起物化性能的显著变化,展示出较好的应用前景。在催化领域,CuMn2O4尖晶石以离子结合方式多样性和在晶体结构中的灵活性著称。虽然CuMn2O4尖晶石在甲苯催化氧化过程中具有良好的氧化还原性能,但尖晶石的供氧能力和储氧能力不足限制了催化性能的进一步提升。CeO2表现出良好的储存-释放氧能力,CeO2与过渡金属之间独特的电子相互作用可以显著促进催化材料的氧化还原性能。Lu Hanfeng等[9]研究了用于甲苯燃烧反应的Cu-Mn,Cu-Mn-Ce和Cu-Ce混合氧化物催化剂,发现Cu-Mn-Ce三元催化活性最高。
本文通过一种简单的共沉淀方法制备了具有高比表面的Cu-Mn-Ce催化剂并将其应用于甲苯催化燃烧。新型的Cu-Mn-Ce催化剂表现出更好的催化活性,并且在很长时间里催化剂仍然具有很高的催化活性。
1 实验部分
1.1 原 料
硝酸锰、硝酸铜、硝酸铈,均为分析纯,国药集团化学试剂有限公司;石英砂,(10~20) 目,天津石英钟厂霸州市化工分厂;
1.2 催化剂制备
采用共沉淀法由前驱体盐制备Cu1-yMn2CeyOx(y=0.1、0.2、0.3):将Mn(NO3)2、Cu(NO3)2·3H2O和Ce(NO3)3·6H2O以适当的物质的量比溶解于去离子水中,得到溶液(Mn2+浓度为0.01 M作为基准)。以Cu0.9Mn2Ce0.1O4为例,将Cu(NO3)2·3H2O、50%Mn(NO3)2和Ce(NO3)3·6H2O溶于200 mL去离子水中,以 0.25 mol·L-1NaOH调节pH=10,搅拌24 h。过滤后在真空烘箱中333.15 K干燥,在马弗炉中空气气氛下423.15 K焙烧1 h除去样品中剩余的水分,马弗炉升温速率5 K·min-1,同样速率升温至823.15 K焙烧4 h即得所需催化剂。
1.3 催化剂表征
XRD表征采用荷兰PANalytical 公司X′Pert Powder 型多功能粉末衍射仪。
催化剂比表面积及孔结构表征采用美国麦克仪器公司TriStar3 000化学吸附仪,N2为吸附气体,样品在液氮温度77 K进行吸附-脱附,测定前,样品在300 ℃真空脱气3 h,根据BET公式计算样品的比表面积和孔体积。
1.4 催化剂性能评价
催化剂性能评价采用固定床反应器,石英反应管(内径11 mm)中加入(60~80) 目的催化剂200 mg。质量流量计控制含甲苯体积分数0.2%的空气为反应原料,流量120 mL·min-1,空速10 000 h-1。甲苯入口和出口浓度采用GC7900气相色谱分析,火焰离子化检测器,Carbowax 20M/Chromosorb W色谱柱,柱箱温度为423.15 K。
2 结果与讨论
2.1 表征结果
图1是Cu1-yMn2CeyO4(y=0.1、0.2、0.3)的XRD图。由图1可知,Cu0.9Mn2Ce0.1O4、Cu0.8Mn2Ce0.2O4和Cu0.7Mn2Ce0.3O4中均观察到尖晶石结构的CuMn2O4衍射峰(JCPDS-ICDD 74-2422),其中2θ=18.5o、30.4o、35.85o、37.5o、43.58o、47.7o、57.6o、63.3o为CuMn2O4特征衍射峰。CuMn2O4衍射峰尖锐,表明其晶形相对完整。与CuMn2O4相比,Cu1-yMn2CeyO4(y=0.1、0.2、0.3)的XRD图中可以观察到CeO2(JCPDS-ICDD 89-8436)的存在,2θ=28.5o、33.08o、47.5o、56.3o、59.09o为CeO2的特征衍射峰。CuMn2O4和CeO2峰位置发生红移,表明CuMn2O4和CeO2的晶面间距发生了变化。3种催化剂中均未观察到其他相,如CuO和MnOx,原因在于一方面形成了尖晶石结构,另一方随着Cu含量的降低,一些相对过量的Mn发生电子转移,Mn3+向Mn4+价态变化,以维持尖晶石的电中性,而其他的Mn则进入CeO2晶格。
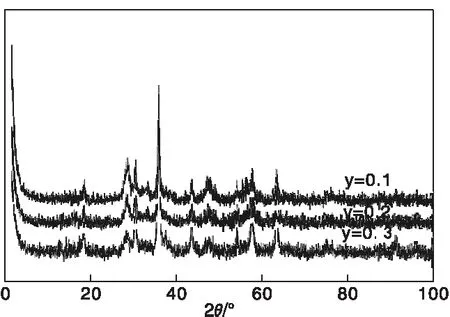
图1 Cu1-yMn2CeyO4(y=0.1、0.2、0.3)的XRD图Figure 1 XRD patterns of Cu1-yMn2CeyO4(y=0.1,0.2,0.3)
Cu1-yMn2CeyO4(y=0.1、0.2、0.3)催化剂的比表面积、孔容和孔径如表1所示。由表1可知,3种催化剂孔径(2.742~3.832) nm之间,表明Cu1-yMn2CeyO4(y=0.1、0.2、0.3)为介孔材料。甲苯分子直径为0.6 nm,催化剂可较为容易的提供甲苯有效吸附通道,为气固相反应提供大量的物理吸附位点和扩散通道,提高反应速率。
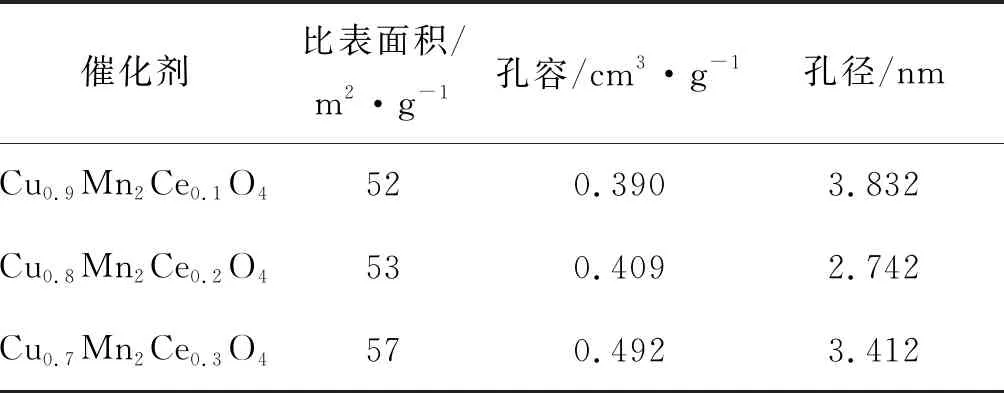
表1 Cu1-yMn2CeyO4(y=0.1、0.2、0.3)的比表面、孔容和孔径
2.2 催化剂活性
Cu0.8Mn2Ce0.2O4催化剂及文献[10-12]中铜、锰催化体系的甲苯燃烧活性如表2所示。由表2可知,同文献中报道的不同含过渡金属的催化剂相比,本文制备的Cu1-yMn2CeyO4性能较好,反应温度更低。
不同反应温度下,Cu1-yMn2CeyO4(y=0.1、0.2、0.3)催化剂上甲苯转化率如图2所示。由图2可知,Cu0.8Mn2Ce0.2O4催化剂上甲苯转化率最高,反应温度大于292 ℃时,甲苯完全降解。催化剂活性顺序为Cu0.8Mn2Ce0.2O4>Cu0.9Mn2Ce0.1O4>Cu0.7Mn2Ce0.3O4>CuMn2O4。Cu0.8Mn2Ce0.2O4催化剂寿命评价发现该催化剂稳定性良好。催化剂的性能取决活性组分的分散度,CuMn2O4尖晶石结构和CeO2的添加量。在Cu1-yMn2CeyO4催化剂中,CeO2和CuMn2O4有明显的相互作用。由于Cu含量的降低,CuMn2O4尖晶石中Mn3+向Mn4+转化,将尖晶石的Mn4+引入CeO2晶格中,产生CeO2(111)晶格面中的晶格缺陷。

表2 自制催化剂和文献中催化剂的甲苯燃烧性能
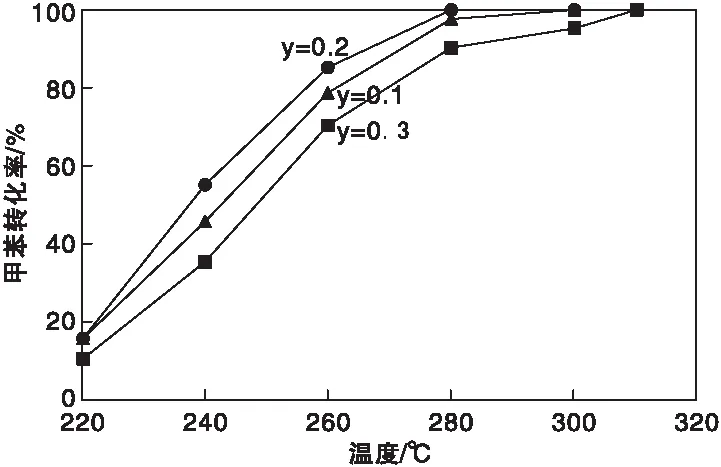
图2 Cu1-yMn2CeyO4(y=0.1、0.2、0.3)催化燃烧甲苯转化率Figure 2 Catalytic activity of Cu1-yMn2CeyO4(y=0.1、0.2、0.3) for toluene oxidation
2.3 反应机理
为进一步研究甲苯氧化反应过程,采用GC-MS分析Cu0.8Mn2Ce0.2O4催化剂上甲苯全氧化反应过程中的副产物,结果如表3所示。由表3可知,未检测到副产物苯酚和氢醌,这主要是由于这些分子反应活性较高;副产物乙炔、甲基乙炔,二甲基甲烷具有链烷烃特征,它们的存在可以通过芳环的开环和催化裂化来解释;副产物甲烷和苯可以通过甲苯的裂解来解释。通常,GC-MS观察的主要副产物如果是甲烷和苯,由于甲烷和甲苯比开环和催化裂化产物的氧化难度大,可判断催化剂性能方面表现不佳。

表3 Cu0.8Mn2Ce0.2O4催化剂质谱观察到的副产物痕迹
本研究的主要副产品是一氧化碳和甲苯的开环和催化裂化产物,Cu0.8Mn2Ce0.2O4具有较少量的副产物苯。因此,Cu0.8Mn2Ce0.2O4更容易开环和催化裂解芳环。一氧化碳的完全氧化温度在Cu0.8Mn2Ce0.2O4上较低,开环和催化裂化产物完全氧化温度也不高。总的来说,Cu0.8Mn2Ce0.2O4对甲苯氧化是非常有效的。
3 结 论
通过共沉淀法成功制备了一系列不同负载量的Cu1-yMn2CeyO4(y=0.1、0.2、0.3)催化剂。Cu0.8Mn2Ce0.2O4具有良好的甲苯降解催化稳定性,得益于CeO2-CuMn2O4与Cu0.8Mn2Ce0.2Ox高分散的相互作用。与CuMn2O4相比,Cu0.8Mn2Ce0.2O4中Cu含量的降低促进了Mn3+向Mn4+的电子转移,当尖晶石中过量的Mn被引入CeO2晶格时,Ce含量的增加产生了氧空位。
