CoMnOx/ZSM-5催化剂制备及其甲苯催化氧化性能
2020-05-29周晓东杨凳尧宋振超郭利民
周晓东,杨凳尧,张 龙,宋振超,郭利民*
(1.山西新华化工有限责任公司,山西 太原 030000;2.华中科技大学环境科学与工程学院,湖北 武汉 430074)
挥发性有机化合物(VOCs)主要来源于汽车尾气和工业排放的过程废气等[1-3],是形成光化学烟雾和雾霾的主要前体物,对生态环境和人体健康有巨大危害[4]。近年来,为了有效控制VOCs污染,发展多种VOCs治理技术[5],催化氧化可在相对较低温度下将VOCs分解成无害产物CO2和H2O[6-9],被认为是一种有效且节能的VOCs控制方法。
VOCs催化氧化技术核心是开发高催化活性、稳定性和低成本的催化剂。文献中,贵金属[7-10]、过渡金属氧化物[11-13]和沸石基催化剂[1,14-15]等已被广泛用于各种VOCs催化氧化应用与研究。近年来,多级孔结构沸石分子筛负载型催化剂对VOCs催化氧化应用研究受到广泛关注。如沸石基催化剂用于含氯挥发性有机化合物(CVOCs)的催化氧化,文献[16-18]表明,H型沸石对CVOCs有较高的催化活性和较好的HCl选择性。但在催化氧化过程中观察到催化剂表面因积炭而导致催化剂失活的现象。有研究者将介孔引入传统沸石中,发现介孔的引入有助于反应过程中底物的扩散,可有效解决因扩散效率导致积炭失活的问题。Chen Chunyu等[19-20]发现载Pt多级孔ZSM-5和β沸石催化剂对比传统ZSM-5和β沸石具有更高的活性和稳定性。Wang Yu等[21]发现,载Ru多级孔ZSM-5催化剂相比传统ZSM-5对甲苯的吸附能力明显提高,对甲苯催化氧化活性也有一定提高,并可重复多次使用。尽管沸石负载贵金属催化剂可实现VOCs催化氧化,但由于贵金属成本高而限制了这类催化剂的广泛使用。
过渡金属氧化物(如CuO[2]、MnO2[11]、Co3O4[22]、LaMnO3[2]等)在VOCs催化氧化领域被广泛研究。Zhang Qi等[23]采用水热法制备了不同形貌的三维多级孔Co3O4纳米催化剂,并用于甲苯催化氧化研究,结果表明,更多表面吸附氧及高氧化态Co物种有利于甲苯催化氧化。Cai Ting等[24]研究了Mn掺杂Co3O4对邻二氯苯(o-DCB)的催化氧化,发现Mn掺杂Co3O4对o-DCB催化氧化具有较高活性。Co-Mn催化剂因其优异的VOCs催化氧化性能而受到广泛关注。Wang Yu等[25]利用Redox-Precipitation方法制备了一系列CoMnxOy,并用于甲苯催化氧化,结果表明,Co与Mn物质的量比为3的催化剂具有最好的催化氧化甲苯活性,甲苯浓度400×10-6,空速67 500 h-1时,T50=172 ℃。
以多级孔沸石分子筛ZSM-5为载体,基于前期多金属物种间氧化还原法制备高性能复合金属氧化物催化剂工作[25],本文通过制备条件控制在多级孔沸石分子筛ZSM-5上负载非贵金属复合金属氧化物CoMnOx,制备CMZ-R1、CMZ-R2和CMZ-R3催化剂,并考察其催化氧化甲苯性能。
1 实验部分
1.1 试 剂
F127,分析纯,Sigma试剂公司;正硅酸乙酯、四丙基氢氧化铵溶液、异丙醇铝、氢氧化钠、高锰酸钾、六水合硝酸钴和氨水,分析纯,国药集团化学试剂有限公司。水为去离子水,实验室自制。
1.2 催化剂制备
多级孔沸石分子筛ZSM-5制备:参照文献[21]方法制备,具体过程:将3.2 g F127置于烧杯,再加入32 g去离子水持续搅拌至F127完全溶解。称取0.255 g异丙醇铝和10.4 g正硅酸乙酯(TEOS)放入另一个烧杯,搅拌均匀后逐滴加入上述F127水溶液中。继续剧烈搅拌2 h,逐滴加入4.1 g四丙基氢氧化铵溶液(TPAOH)。40 ℃持续搅拌至凝胶状,湿凝胶60 ℃老化8 h,随后90 ℃过夜干燥,然后将得到的干凝胶160 ℃用蒸汽辅助法处理18 h。产物经过洗涤和过滤,100 ℃干燥,最后在马弗炉中600 ℃焙烧10 h,制得多级孔沸石分子筛ZSM-5载体。
CoMnOx/ZSM-5系列催化剂制备:取1 g多级孔沸石分子筛ZSM-5粉体于研钵中,加入0.54 g六水合硝酸钴和0.295 g高锰酸钾,研磨至均匀,移至10 mL坩埚中,并置于高压反应釜,于釜内加入少量氨水,140 ℃水热处理6 h,60 ℃烘干,制得CMZ-R1催化剂。
取1 g多级孔沸石分子筛ZSM-5粉体于研钵中,加入0.54 g六水合硝酸钴和0.295 g高锰酸钾,研磨至均匀,移至10 mL坩埚中,并置于高压反应釜,于釜内加入少量去离子水,140 ℃水热处理6 h,60 ℃烘干,并将样品300 ℃焙烧3 h,制得CMZ-R2催化剂。
将0.54 g六水合硝酸钴和0.295 g高锰酸钾配成适量体积的水溶液,滴加到1 g多级孔沸石分子筛ZSM-5载体内,室温静置老化4 h,110 ℃烘干,空气中500 ℃焙烧4 h,制得CMZ-R3催化剂。
1.3 催化剂表征
XRD由荷兰帕纳科公司Empyrean型X射线粉末衍射仪测定,CuKα,工作电压40 kV,工作电流40 mA,扫描速率5o·min-1。
N2吸附-脱附由美国麦克仪器公司ASAP 3020型吸附仪在-196 ℃下测定,BET计算样品比表面,t-plot计算孔容,BJH计算孔径。
SEM采用德国卡尔·蔡司股份公司场发射扫描电镜SIGMA300观察样品的微观形貌。
TEM采用日本JOEL公司JEM-2100型透射电镜观察样品的微观结构。
XPS由日本岛津/Kratos公司AXIS-ULTRA DLD-600W型X射线光电子能谱仪测定,AlKα,C1s线校正。
1.4 催化活性测试
甲苯催化氧化活性评价在微型固定床反应器上进行,所用气体均为高纯N2和O2(纯度>99.999%)。甲苯气体通过氮气在甲苯溶液中鼓泡产生(通过调节氮气流量和水浴温度控制甲苯浓度)。反应器入口气体中甲苯浓度测定:先将入口气体通过一个装有CuMn/Al2O3催化剂的转化炉(400 ℃),其中的甲苯完全转化为CO2,再经德国Sick-Maihak红外气体分析仪S710,在线检测CO2浓度,经过碳守恒间接计算得出甲苯在气体中的浓度。实验所需各路气体流量均由质量流量计调节和控制。H2O通过恒温水浴中鼓泡引入到反应气流中。反应混合气为:400×10-6甲苯,体积分数20%O2∶质量分数1.58%H2O∶N2,总流量100 mL·min-1,75 mg催化剂,(40~60)目,气体流速(空速)80 000 mL·(g·h)-1。以50%和90%甲苯转化为CO2所对应的温度(T50和T90)来评价样品的催化活性。根据下式计算甲苯转化率:


2 结果与讨论
2.1 XRD
图1为CMZ-R1、CMZ-R2和CMZ-R3催化剂的XRD图。

图1 CMZ-R1、CMZ-R2和CMZ-R3催化剂的XRD图Figure 1 XRD patterns of CMZ-R1,CMZ-R2 and CMZ-R3 catalysts
由图1可知,CMZ-R1、CMZ-R2和CMZ-R3催化剂在2θ= 5°~35°出现衍射峰,归属于MFI结构分子筛 (JCPDS PDF#44-0003)[21],表明负载钴锰混合氧化物后,多级孔沸石分子筛ZSM-5保持了沸石结构。此外,3个样品XRD图中没有明显观察到对应于钴锰复合氧化物的衍射峰,表明钴锰复合氧化物高度分散或以弱晶化状态存在。
2.2 N2吸附-脱附
图2为CMZ-R1、CMZ-R2和CMZ-R3催化剂的N2吸附-脱附等温线和孔径分布。
根据IUPAC分类标准,制备的催化剂均具有Ⅳ型等温线和H4回滞环,在较高相对压力0.85~0.95处发生毛细凝聚和出现回滞环,表明样品中存在较大孔径的介孔。

图2 CMZ-R1、CMZ-R2和CMZ-R3催化剂的N2吸附-脱附等温线和孔径分布Figure 2 N2 adsorption-desorption isotherms and pore size distribution of CMZ-R1,CMZ-R2 and CMZ-R3 catalysts
表1为样品的结构性质。由表1结合图2可以看出,催化剂具有微孔-介孔的多级孔结构。

表1 样品的结构性质
①相对压力0.05~0.35的BET比表面积;②t-plot方法计算外比表面积;③t-plot方法计算微孔比表面积;④t-plot方法计算微孔孔容;⑤相对压力0.95时的总孔容
由表1可见,催化剂比表面积及孔容均出现相应降低,这归因于钴锰复合氧化物的负载。在催化过程中,可以借助材料的比表面积和孔径分布数据间接评估孔道扩散性能和微孔损失对催化剂活性的影响。Perez-Ramirez Javier等[26]引入多级孔因子(HF)概念,并将HF定义为Smeso/SBET和Vmicro/Vpore的乘积,提出HF越高,材料的综合性能越好。催化剂HF见表1,载体多级孔沸石分子筛ZSM-5的HF约0.07。CMZ-R1催化剂的HF最高,为0.11。CMZ-R2和CMZ-R3催化剂的HF为0.04。HF数据表明,负载活性组分后,催化剂介孔与微孔比例出现变化。其中,CMZ-R1催化剂的HF变大,表明对反应物扩散具有促进作用,而CMZ-R2和CMZ-R3催化剂的HF降低,表明负载后反应过程中的反应物扩散受到抑制。
2.3 SEM
图3为CMZ-R1、CMZ-R2和CMZ-R3催化剂的SEM照片。

图3 CMZ-R1、CMZ-R2和CMZ-R3催化剂的SEM照片Figure 3 SEM images of CMZ-R1,CMZ-R2 and CMZ-R3 catalysts
由图3可见,负载钴锰氧化物后,CMZ-R1催化剂表面可以看到较多的光滑块状表面,放大照片可以看到,片状钴锰氧化物较为均匀分布在载体表面。CMZ-R2和 CMZ-R3催化剂显示的表面粗糙程度与载体ZSM-5类似,表明钴锰复合氧化物分散于载体表面。
2.4 TEM
图4为CMZ-R1、CMZ-R2和CMZ-R3催化剂的TEM照片。由图4可见,钴锰复合氧化物较均匀地分布在载体上。CMZ-R3催化剂表面具有薄片状物质,对应于钴锰复合氧化物。CMZ-R2和CMZ-R3催化剂表面没有出现同样的条状钴锰氧化物,但可以看到较小的颗粒物在球状结构载体表层,进一步观察,发现许多短棒状颗粒在载体ZSM-5周围,表明在CMZ-R2和CMZ-R3催化剂上,负载的钴锰氧化物以纳米级颗粒堆积在载体表面。

图4 CMZ-R1、CMZ-R2和CMZ-R3催化剂的TEM照片Figure 4 TEM images of CMZ-R1,CMZ-R2 and CMZ-R3 catalysts
2.5 XPS
图5为CMZ-R1、CMZ-R2和CMZ-R3催化剂的O1s XPS谱图。

图5 CMZ-R1、CMZ-R2和CMZ-R3催化剂的O1s XPS谱图Figure 5 XPS spectra of O1s of CMZ-R1,CMZ-R2 and CMZ-R3 catalysts
由图5可以看出,结合能531.6 eV的峰对应催化剂表面吸附氧物种,结合能529.8 eV的峰对应晶格氧物种。
Co3+和Co2+在2p3/2和2p1/2能带中所属的结合能非常接近,很难区分,所以进行了分峰,分峰后Co2p XPS谱图可分为7个峰,分别是Co2+和Co3+的特征峰和3个卫星峰。图6为CMZ-R1、CMZ-R2和CMZ-R3催化剂的Co2p XPS谱图。由图6可见,第一个结合能在780.6 eV[27],2p3/2-2p1/2结合能相差15.2 eV,这归属于Co3+的特征峰。第二个结合能在782 eV[27]附近,2p3/2-2p1/2结合能相差15.5 eV,这归属于Co2+的特征峰。

图6 CMZ-R1、CMZ-R2和CMZ-R3催化剂的Co2p XPS谱图Figure 6 XPS spectra of Co2p of CMZ-R1,CMZ-R2 and CMZ-R3 catalysts
图7为CMZ-R1、CMZ-R2和CMZ-R3催化剂的Mn 2p XPS谱图。

图7 CMZ-R1、CMZ-R2和CMZ-R3催化剂的Mn2p XPS谱图Figure 7 XPS spectra of Mn2p of CMZ-R1,CMZ-R2 and CMZ-R3 catalysts
由图7可见,Mn2p3/2和Mn2p1/2峰均可分出两个次峰,催化剂表面Mn物种由Mn3+和Mn4+组成。
催化剂元素组成通过XRF测定,Oads、Olat物质的量比、Co3+、Co2+物质的量比和Mn3+、Mn4+物质的量比通过XPS测定。表2为CMZ-R1、CMZ-R2和CMZ-R3催化剂的化学组成及表面化学性质。

表2 CMZ-R1、CMZ-R2和CMZ-R3催化剂的化学组成及表面化学性质
由表2可以看出,催化剂Si、Al物质的量比均约等于22,Co、Mn物质的量比均接近3,与合成时的配比一致。催化剂表面Co3+、Co2+物质的量比顺序为CMZ-R1>CMZ-R2>CMZ-R3。催化剂CMZ-R1表面有更多的Mn3+物种。
综上所述, CMZ-R1表面吸附氧物种的比例最高,同时该催化剂表面具有更多的高氧化态Co和低氧化态Mn物种。高氧化态Co和低氧化态Mn物种增加有助于提升催化剂催化氧化甲苯的能力[8]。
2.6 甲苯催化氧化
甲苯浓度400×10-6和空速80 000 mL·(g·h)-1时,CMZ-R1、CMZ-R2和CMZ-R3催化剂上甲苯催化氧化反应性能如图8所示,催化剂的甲苯催化燃烧活性如表3所示。

图8 CMZ-R1,CMZ-R2和CMZ-R3催化剂上甲苯催化氧化性能Figure 8 Catalytic oxidation of toluene over CMZ-R1,CMZ-R2 and CMZ-R3 catalysts
由图8结合表3可以看出, CMZ-R1的甲苯催化氧化活性最高,280 ℃将甲苯完全转化,T90和T50分别是258 ℃和252 ℃。CMZ-R2和CMZ-R3的甲苯催化活性明显低于CMZ-R1,T90和T50分别是288 ℃、319 ℃和281 ℃、310 ℃。结果表明,制备方法对催化剂表面活性物种有很大影响,最终影响催化剂活性。结合催化剂表征数据,发现甲苯催化氧化活性最好的催化剂CMZ-R1具有以下特征:(1) 催化剂表面CoMnOx为片状复合氧化物,可以暴露更多的反应位点。(2) XPS分析表明,CMZ-R1表面晶格氧丰富,表面活性氧物种在氧化反应中起重要作用,这些吸附氧物种能促进氧化反应发生[27]。(3) XPS分析表明,CMZ-R1表面相对于CMZ-R2和CMZ-R3,具有更多的氧化数为3的Co物种和氧化数为3的Mn物种,有助于提升CMZ-R1的催化活性[8]。

表3 催化剂的甲苯催化燃烧活性
甲苯催化氧化在O2过量条件下,反应对甲苯浓度服从一级反应[22]。CMZ-R1、CMZ-R2和CMZ-R3催化剂上甲苯催化氧化的阿伦尼乌斯曲线如图9所示。为了消除扩散因素的干扰,阿伦尼乌斯曲线数据仅来自甲苯催化氧化转化率低于20%的数据。基于阿伦尼乌斯曲线斜率可以计算得到每个催化剂的表观活化能(见表3)。可以看出,表观活化能为CMZ-R1 图9 CMZ-R1、CMZ-R2和CMZ-R3催化剂上甲苯催化氧化的阿伦尼乌斯曲线Figure 9 Arrhenius plots for the catalytic combustion of toluene over CMZ-R1,CMZ-R2 and CMZ-R3 catalysts 采用不同制备方法在多级孔沸石分子筛ZSM-5上负载非贵金属复合氧化物CoMnOx,制备得到CMZ-R1、CMZ-R2和CMZ-R3催化剂,用于催化氧化甲苯性能研究。结果表明,采用氧化还原法制备的CMZ-R1催化剂具有最好的甲苯催化氧化活性,甲苯浓度400×10-6和空速80 000 mL·(g·h)-1时,T90和T50分别为258 ℃和252 ℃,表观活化能为120.3 kJ·mol-1。结构及表面分析表明, CMZ-R1负载CoMnOx的片状结构和相对更多的高氧化态Co物种和低氧化态Mn物种,促进了甲苯催化氧化性能的提高。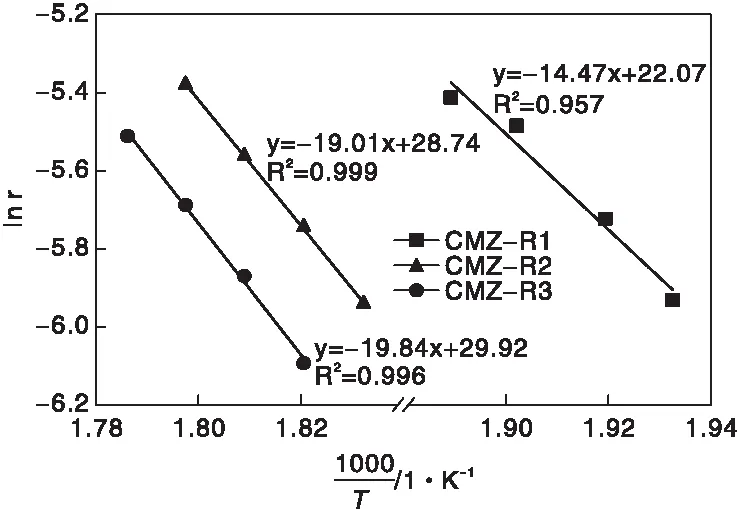
3 结 论
