肝硬化并发门静脉血栓患者临床特征及其危险因素分析*
2020-05-28热那特克力木吐尔干艾力阿吉邵英梅
热那特·克力木,吐尔干艾力·阿吉,邵英梅
血流动力学的改变、血管壁的损伤、血液高凝状态的形成是静脉血栓发生机制的三要素[1]。肝脏是凝血因子合成的主要器官。肝硬化患者肝功能损伤后,肝脏合成和灭活凝血因子的能力出现异常,造成凝血功能障碍[2]。肝硬化患者门静脉血栓形成(portal vein thrombosis, PVT)的机制尚不明确。本研究分析了肝硬化并发PVT患者的临床特征,并分析了PVT形成的危险因素,旨在为临床能够早期采取措施预防PVT的发生提供依据。
1 资料与方法
1.1 一般资料 2015年2月~2019年2月我院肝胆包虫科收治的肝硬化患者160例,男性109例,女性51例;年龄42~68岁,平均年龄为(56.78±11.35)岁;病程2~8年,平均病程为(5.61±1.77)年。符合肝硬化诊断标准[3],经彩超或CT等影像学检查诊断PVT形成。有吸烟史者64例,体质指数(body mass index, BMI)为19~28 kg/m2,平均为(24.32±2.17)kg/m2。肝硬化病因包括乙型肝炎、丙型肝炎和酒精性肝炎肝硬化等。排除标准:布加综合征[4]、由其他非肝脏疾病引起的PVT[5]、近期服用过抗凝药物、伴有精神性疾病无法配合治疗或检查、孕妇或哺乳期妇女。本组发生PVT患者80例。患者签署知情同意书,本研究通过我院医学伦理委员会批准同意。
1.2 研究方法 对入选病例进行回顾性分析,记录一般资料、临床症状和实验室检查结果。使用西门子公司生产的ADVIA2120全自动生化分析仪检测血生化指标;使用日本Sysmex公司生产的CA6000全自动凝血分析仪检测凝血功能指标。
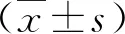
2 结果
2.1 两组临床资料比较 80例PVT患者腹痛、腹水和消化道出血发生率、血小板(PLT)和白细胞(WBC)计数显著高于80例未发生PVT组(P<0.05)。
2.2 一般资料比较 两组患者年龄、性别构成、吸烟史差异均无统计学意义(P>0.05);PVT患者高血压史、糖尿病史、脾切除史所占比例显著高于无PVT组,差异有统计学意义(P<0.05,表1)。
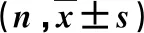
表1 两组一般资料比较
2.3 肝硬化并发门静脉血栓危险因素的多因素分析 将单因素分析具有统计学意义的腹水、消化道出血、HGB、PLT、WBC、高血压病史、糖尿病史和脾切除史进行多因素Logistic 回归分析,结果显示PLT、糖尿病史和脾切除史为肝硬化并发门静脉血栓的独立危险因素(P<0.05,表2)。
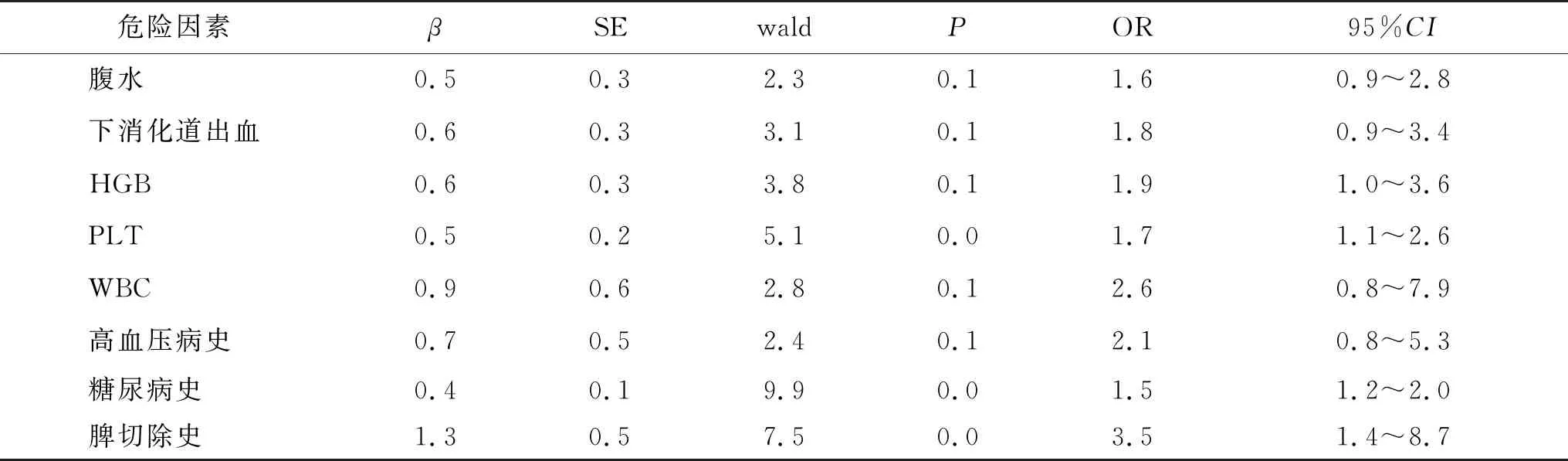
表2 肝硬化并发门静脉血栓危险因素的多因素分析
3 讨论
PVT是发生在门静脉主干和肝内门静脉分支的深部血管栓塞性疾病,是肝硬化患者失代偿期发生的一种严重并发症,可造成患者发生消化道出血、顽固性腹水,严重危害患者生命,影响患者预后[6,7]。 因此,临床在对肝硬化并发PVT患者进行及时治疗的同时,也要对易发PVT的肝硬化患者进行早期预防性处理和密切观察。
随肝硬化病情的发展和加重,再生性结节、增生的结缔组织和纤维隔的形成导致门静脉和中央静脉血管受到挤压,导致门静脉血管阻力增加,脾静脉压力随门静脉高压而升高[8,9],血液淤滞逆流导致脾脏出现淤血性增大,且脾肿大程度随血流量的增加而增加,脾脏内储藏的血容量增加,脾功能亢进导致大量滞留脾内的HGB、PLT和WBC等血细胞和血液成分受到破坏,其水平降低[10,11],但同时门静脉高压形成后,肠道回流至门静脉的血液流变学发生改变,出现血流速度缓慢、双向性甚至逆向血流,最终发展成为离肝性血流[12]。门静脉高压导致门静脉血管出现损伤,刺激内皮素等促进血管收缩因子的表达和分泌,导致血管发生痉挛,加重血管的损伤,暴露胶原纤维,激发炎性反应,促进了WBC等炎性细胞因子的产生[13],PLT的沉积、聚集形成止血栓以修补损伤的血管内壁,PLT水平升高,而PLT及其活性物质能够介导并释放凝血因子及促炎因子,加重患者血液的高凝状态和血管内皮细胞的炎症反应,进一步促进了PVT形成和WBC等炎性因子水平的升高[14,15]。在本研究结果中也发现PVT患者HGB水平显著低于无PVT组,PLT和WBC水平均显著高于无PVT组,差异具有统计学意义。本研究对两组患者临床症状进行统计和分析发现两组患者均以腹水、消化道出血、肝功能异常为主要临床表现,其中PVT组腹痛、腹水和消化道出血发生率显著高于无PVT组,差异具有统计学意义。肝硬化是肝细胞长期反复的坏死、再生的结果[16],患者出现肝功能减退,当疾病进展进入失代偿期,门脉高压的发生可导致肠系膜上静脉代偿性增宽、肠道静脉回流受阻,引发静脉曲张。当受到粗糙食物、化学物质或腹内压升高等因素刺激时,曲张的血管极易破裂,发生消化道大出血[17]。肝功能损伤造成肝细胞合成ALB的能力减弱,导致腹水的形成[18],而门静脉高压造成内脏血管压力的升高,导致淋巴液回流受阻,血浆胶体渗透压降低导致钠水潴留的发生,加重腹水的形成[19]。在PVT发生后,造成门静脉和内脏毛细血管压力进一步的升高,导致患者更易发生腹水和消化道出血[20]。疼痛是血栓形成的特点之一[21],且门静脉没有静脉瓣,在发生PVT后,栓子随血液循环扩散,加重门静脉高压,从而加重PVT,导致严重的腹痛[22]。但肠梗阻也可出现腹痛、腹水、消化道出血等相似的临床症状,易与肝硬化并发PVT发生误诊,故临床疾病鉴别时采取症状结合实验室检查指标,及时正确的诊断和治疗,避免患者病情继续发展,出现死亡[23]。
将两组患者的一般资料及实验室指标进行对比分析,本研究发现高血压史、糖尿病史、脾切除史为肝硬化并发PVT的影响因素。PLT、糖尿病史和脾切除史为肝硬化并发PVT的独立危险因素。高血压造成血管湍流增多、剪切应力增高导致血管内皮损伤,刺激PLT的活化,且高血压病患者凝血酶及纤维蛋白含量更高,凝血系统和纤溶系统的失衡导致患者更易发生静脉血栓[24],但在既往肝硬化PVT形成的危险因素研究分析中,高血压对PVT的形成无显著影响,与本研究所得结果相悖,仍需设立研究进行进一步的探讨[25]。糖尿病患者持续慢性的高糖状态使多种蛋白发生糖化,在现有研究中已经提出发生糖化的蛋白可刺激凝血因子Ⅴ、Ⅷ的表达,增加了血液的凝固性,促进了血栓形成[26]。糖尿病患者糖、脂质的代谢紊乱,易产生活性氧自由基,导致血管内皮细胞出现损伤,为血栓形成提供条件[27]。脾切除术是门静脉高压、脾功能亢进的重要治疗方式[28]:(1) 脾切除术对血管进行机械结扎可导致血管内膜损伤,激活凝血系统,术后患者造血功能活跃,PLT等血细胞的水平升高,增加患者血液粘稠度[29];(2)术后脾静脉一端闭合,回流门静脉的血流量减少,门静脉压力降低,血流速度相对较慢,易形成涡流,而PLT在涡流中滞留时间长,在血液循环中相互碰撞并激活成为聚集体,即涡流为血栓形成提供场所。PLT能够释放抗纤溶因子及其他促凝物质,促进不溶性纤维蛋白的合成,使PLT聚集附着与损伤的血管内皮以达到修复损伤的作用,使受损的血管管腔变窄,导致血液流速减慢、流量减少。通过抑制纤溶系统的活化,使PLT聚集体不溶解。
综上所述,肝硬化并发PVT患者以腹水、消化道出血和肝功能异常为主要临床症状。PLT、糖尿病史和脾切除史为肝硬化并发门静脉血栓的独立危险因素。
