QuEChERS/超高效液相色谱-串联质谱法测定土壤中31种磺酰脲类除草剂残留
2020-05-08邱世婷雷绍荣郭灵安
李 莹,韩 梅,邱世婷,雷绍荣,郭灵安,侯 雪
(四川省农业科学院分析测试中心,农业部农产品质量安全风险评估实验室(成都),四川 成都 610066)
自1982年美国杜邦公司报道第一个磺酰脲类除草剂品种氯磺隆后,磺酰脲类除草剂正式走进人们的视野[1]。由于磺酰脲类除草剂具有高效、低用量、低成本、高选择性等特点,自开发以来得到了广泛应用和快速发展[2-3]。目前,已被广泛应用于防治水稻、麦类、大豆、玉米、油菜、草坪和其他非耕地的杂草。研究表明,磺酰脲类除草剂在土壤中的降解方式主要有化学水解和生物降解,但其降解速度受化合物结构、土壤pH值、温湿度、土壤类别、土壤有机物含量等影响较大[4]。不同磺酰脲类除草剂具有不同的残效期,一些残效期较长的除草剂(如甲磺隆、绿磺隆、氯嘧磺隆、嘧磺隆等),即使在土壤中微量残留,也会对后茬敏感农作物、环境以及人体健康造成较大的影响[5-7]。土壤中磺酰脲类除草剂的消解及暴露风险评估研究表明:除草剂的原始残留量和施药量成正相关,而除草剂的残留量直接影响致癌风险值的大小[6]。目前,已有50多种磺酰脲类除草剂被大量推向市场。2008年,苯磺隆等除草剂被列入美国环境保护署(EPA)公布的171种对人体具有潜在致癌作用的农药目录中[6,8-9]。因此,建立一种简便、快速、灵敏、高效的土壤中磺酰脲类除草剂残留的分析方法具有重要意义。
磺酰脲类除草剂的分析方法主要有毛细管电泳法(CE)[10-11]、高效液相色谱法(HPLC)[12-13]、高效液相色谱-质谱联用法(HPLC-MS或HPLC-MS/MS)[14-15]与酶联免疫吸附法(ELISA)[16]等,其中HPLC-MS/MS法因具有较高的选择性和灵敏度,比较适合环境中痕量磺酰脲类除草剂的分析检测。但土壤样品基体比较复杂,含有不同大小的矿物颗粒,不同分解程度的有机残体、腐殖质及生物活体、各种养分、水分、空气等。同时,磺酰脲类除草剂在土壤中的残留量通常较低,因此选择一种高效、快速、稳定的样品前处理方法,对于实现目标分析物的提取和分析至关重要。本研究参考美国AOAC 2007.01 QuEChERS标准方法[17],对提取溶剂、净化材料等加以优化,并结合超高效液相色谱-三重四极杆质谱联用法,对土壤中31种磺酰脲类除草剂进行分析,建立了一种快速、简便、高灵敏度的磺酰脲类除草剂的多残留分析方法。
1 实验部分
1.1 仪器与试剂
LC-30AD超高效液相色谱仪与LC MS-8060三重四极杆质谱仪联用系统(日本岛津公司);Multi Reax多位试管涡旋振荡器(德国海道夫公司);Neofuge 18R台式高速冷冻离心机(上海力申科学仪器有限公司)。31种磺酰脲类除草剂标准品(纯度≥97%,德国Dr.Ehrenstorfer公司);乙腈、甲醇(色谱纯,美国Fisher公司);甲酸、乙酸、乙酸铵、甲酸铵、氨水(色谱纯,上海安谱实验科技股份有限公司);NaCl(分析纯,四川西陇科学有限公司);无水MgSO4(≥98%,德国CNW科技公司);N-丙基乙二胺(PSA)、C18、石墨化碳黑(GCB)(上海安谱实验科技股份有限公司);实验用水为纯净水(由Milli-Q超纯水仪制备)。
1.2 色谱与质谱条件
色谱条件:Shim-pack XR-ODS ⅢPKA-C18色谱柱(2.0 mm×150 mm,2.2 μm);流动相:A为0.1%甲酸+5 mmol/L乙酸铵,B为甲醇;总流速:0.3 mL/min;柱温:40 ℃;进样体积:1 μL。梯度洗脱程序:0~2 min,10%~50%B;2~8 min,50%~85%B;8~9 min;85%~95%B;9~10 min,95%B;10~10.1 min,95%~10%B;10.1~12 min,10%B。
质谱条件:ESI源;正、负离子模式同时扫描;接口电压:4 000 V;多反应监测(MRM)模式;雾化气(N2)流速:3.0 L/min;干燥气(N2)流速:10.0 L/min;加热气(空气)流速:10.0 L/min;接口温度:300 ℃;脱溶剂管温度:250 ℃;加热模块温度:400 ℃;碰撞气(Ar)压力:270 kPa。
1.3 标准溶液配制
称取适量各标准品,分别用甲醇配制成1 000 μg/mL储备液,储存于-20 ℃冰箱。分别准确量取一定体积的不同磺酰脲类除草剂储备液,用乙腈定容配成20 μg/mL的混合标准溶液,保存于-4 ℃冰箱。根据实验需要,用乙腈或土壤空白基质溶液稀释混合标准溶液,配成不同质量浓度的标准工作溶液。
1.4 样品前处理
1.4.1 样品制备取土壤样品500 g,人工除去石块、树枝等杂物,捣碎、研磨、混匀,过60目样品筛,备用。
1.4.2 提取与净化称取5.0 g土壤样品于50 mL离心管中,加3.0 mL水,常温静置10 min。加入20.0 mL 1%乙酸-乙腈、4 g无水硫酸镁和1 g氯化钠,涡旋1 min,以10 000 r/min离心5 min;取6.0 mL上层有机相于10 mL离心管中,加入900 mg无水硫酸镁和150 mg C18,涡旋1 min,8 000 r/min离心5 min,取2 mL上清液,过0.22 μm滤膜后,装瓶待测。
2 结果与讨论
2.1 色谱条件的优化
磺酰脲类除草剂由芳环、磺酰脲桥和氮杂环组成[18],在ESI源的正离子模式下易形成[M+H]+母离子[19]。在流动相中加入甲酸有助于提高化合物的正离子化效率[14],进而提高目标分析物的灵敏度,加入甲酸铵和乙酸铵可改善色谱峰峰形。分别考察了以甲醇-0.1%甲酸、甲醇-0.1%甲酸+5 mmol/L乙酸铵、甲醇-0.1%甲酸+3 mmol/L甲酸铵、乙腈-0.1%甲酸、乙腈-0.1%甲酸+5 mmol/L乙酸铵为流动相时,对各待测化合物的峰形、分离效果以及离子化效率的影响。
结果表明:以甲醇-0.1%甲酸和乙腈-0.1%甲酸为流动相时,待测物的响应度较低,氯嘧磺隆在乙腈-0.1%甲酸体系中受杂质干扰严重。以甲醇-0.1%甲酸+3 mmol/L甲酸铵为流动相时,甲酰胺磺隆的峰拖尾,酰嘧磺隆和玉嘧磺隆的峰形较差。以乙腈-0.1%甲酸+5 mmol/L乙酸铵为流动相时,唑吡嘧磺隆和氯嘧磺隆与杂质的分离效果差,三氟啶磺隆钠、苯磺隆、乙氧磺隆等的响应低。而甲醇-0.1%甲酸+5 mmol/L乙酸铵体系中,待测物的峰形、响应度及受干扰程度均有改善,因此最终选择甲醇-0.1%甲酸+5 mmol/L乙酸铵为流动相。
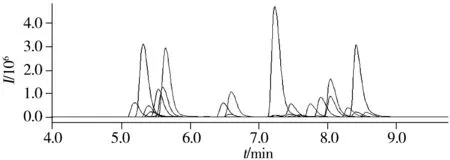
图1 MRM模式下31种除草剂混合标准溶液(0.1 μg/mL)的总离子流色谱图Fig.1 Total ion chromatogram of 31 herbicides’ mixed standard solution(0.1 μg/mL) in MRM mode
2.2 质谱条件的优化
采用正负离子同时扫描模式,对31种磺酰脲类除草剂的单标准溶液进行一级全扫描,得到稳定的母离子,大多数待测物均得到[M+H]+母离子,氯吡嘧磺隆得到[M-H]-母离子。经仪器自动优化,筛选出碰撞能量(CE)和信号较强的二级碎片离子作为子离子,确定最优质谱条件,使各待测物的离子化效率最佳。31种磺酰脲类除草剂的MRM参数见表1,0.1 μg/mL混合标准溶液的MRM色谱图见图1。

表1 31种磺酰脲类除草剂的质谱参数Table 1 MS/MS parameters of 31 sulfonylurea herbicides
(续表1)
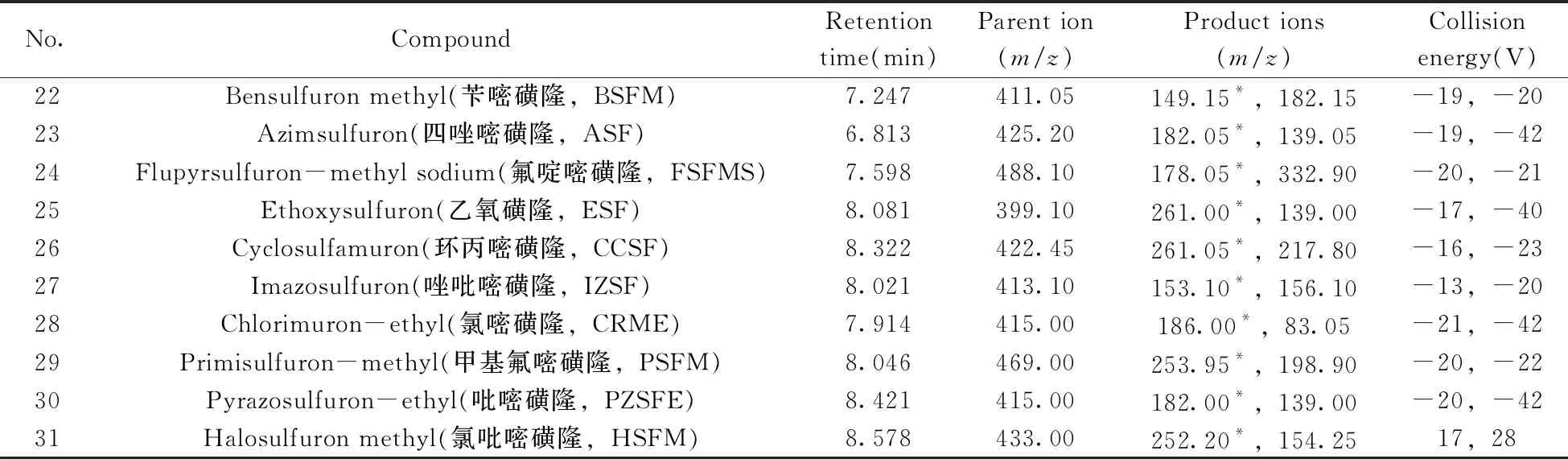
No.CompoundRetention time(min)Parent ion(m/z)Product ions(m/z)Collision energy(V)22Bensulfuron methyl(苄嘧磺隆,BSFM)7.247411.05149.15*,182.15-19,-2023Azimsulfuron(四唑嘧磺隆,ASF)6.813425.20182.05*,139.05-19,-4224Flupyrsulfuron-methyl sodium(氟啶嘧磺隆,FSFMS)7.598488.10178.05*,332.90-20,-2125Ethoxysulfuron(乙氧磺隆,ESF)8.081399.10261.00*,139.00-17,-4026Cyclosulfamuron(环丙嘧磺隆,CCSF)8.322422.45261.05*,217.80-16,-2327Imazosulfuron(唑吡嘧磺隆,IZSF)8.021413.10153.10*,156.10-13,-2028Chlorimuron-ethyl(氯嘧磺隆,CRME)7.914415.00186.00*,83.05-21,-4229Primisulfuron-methyl(甲基氟嘧磺隆,PSFM)8.046469.00253.95*,198.90-20,-2230Pyrazosulfuron-ethyl(吡嘧磺隆,PZSFE)8.421415.00182.00*,139.00-20,-4231Halosulfuron methyl(氯吡嘧磺隆,HSFM)8.578433.00252.20*,154.2517,28
*quantitative ion
2.3 提取溶剂的优化
磺酰脲类化合物易受结构和体系pH值的影响而发生水解,尤其是苯磺隆受pH值的影响非常大[20]。为提高易水解化合物的稳定性,分别考察了乙腈、甲醇、0.1%乙酸-乙腈、1%乙酸-乙腈、1%氨水-乙腈作为提取溶剂的提取效果(图2)。结果表明,采用1%氨水-乙腈提取时,烟嘧磺隆、甲酰胺磺隆、玉嘧磺隆的回收率仅为24.0%、27.5%、38.5%。采用0.1%乙酸-乙腈、甲醇、乙腈提取时,31种待测物的回收率分别为58.5%~98.0%、68.5%~101%、61.5%~105%。而采用1%乙酸-乙腈提取时,31种待测物的提取效果总体较好,回收率为68.0%~117%,各待测物的回收率在100%附近波动。因此,本实验选择1%乙酸-乙腈为提取溶剂。

图2 31种除草剂在不同提取溶剂中的平均回收率(加标400 μg/kg)Fig.2 Average recoveries of 31 herbicides spiked with 400 μg/kg in different extraction solvents
2.4 净化剂种类及用量的优化
土壤样品基体较复杂,需采用净化剂对样品进行净化,以避免土壤中有机质等对除草剂残留量分析的影响。参考美国AOAC 2007.01 QuEChERS标准方法[17],对净化材料的种类(C18、PSA、GCB)和用量加以优化。
考察了分别以C18(25.00 mg/mL)、PSA(25.00 mg/mL)和GCB(5.00 mg/mL)为净化剂时的净化效果(图3),结果表明,C18的净化效果相对较好,各待测物的回收率在70%~120%范围内,PSA的净化效果次之。GCB对各待测物的净化效果差异较大,烟嘧磺隆(52.5%)、玉嘧磺隆(49.5%)、氟胺磺隆(56.0%)、苄嘧磺隆(40.5%)、乙氧磺隆(14.0%)、环丙嘧磺隆(46.0%)的回收率偏低。

图3 31种除草剂在不同净化剂下的平均回收率(加标400 μg/kg)Fig.3 Average recoveries of 31 herbicides spiked with 400 μg/kg under different purificants
进一步对C18用量(8.33、16.67、25.00、33.33 mg/mL)进行优化。结果表明,C18用量对各待测物的回收率影响不大,不同用量C18净化后的回收率均为87.5%~114%。但在8.33、16.67、33.33 mg/mL C18用量下,环丙嘧磺隆、啶嘧磺隆回收率的相对标准偏差(RSD)大于15%。因此,最终选择C18用量为25.00 mg/mL。
2.5 定容溶剂与定容方式的影响
实验对定容溶剂及定容方式进行了考察。按照“1.4.2”的提取净化过程,取2 mL上清液,A组溶液过0.22 μm微孔滤膜后装瓶;B组溶液于40 ℃氮吹至近干,再用2 mL甲醇-水(1∶1,体积比)定容,过0.22 μm微孔滤膜后装瓶;C组溶液取出1 mL上清液,用1 mL甲醇-水(1∶1)稀释,过0.22 μm微孔滤膜后装瓶。分别测定其回收率,结果表明:A组各待测物的回收率为83.5%~120%,C组和A组的回收率基本一致,但C组中氟酮磺隆钠的回收率偏低;B组的回收率为56.5%~98.0%,尤其是玉嘧磺隆和乙氧磺隆在氮吹后受影响较大,可能是由于氮吹导致部分待测物损失,同时乙氧磺隆在甲醇中的溶解度较低所致。考虑到实验的简便性和各待测物回收率的稳定性,最终采用A方案,即取上清液直接过0.22 μm微孔滤膜后装瓶测定。
2.6 基质效应
基质效应(ME)是指由于共洗脱杂质的干扰导致分析物信号的增强和减弱现象[19]。在复杂样品的分析中,基质效应会影响离子的电离程度,进而对目标化合物的定量结果造成影响[7]。本实验按照“1.3”配制基质匹配标准溶液,并以1%乙酸-乙腈配制相同质量浓度的各待测物标准溶液,采用本方法进行样品前处理和测定,分别以峰面积和质量浓度绘制标准曲线,通过比较两条标准曲线的斜率判断基质效应的强弱。当|ME|<20%时为弱基质效应;当20%≤|ME|<50%时为中等强度基质效应;当|ME|≥50%时为强基质效应[21],计算公式如下:ME(%)=(Sm/Ss-1)×100,式中:Sm和Ss分别表示基质标准曲线和溶剂标准曲线的斜率。
结果表明:除烟嘧磺隆、三氟啶磺隆钠、玉嘧磺隆、啶嘧磺隆、氯吡嘧磺隆表现为中等强度基质效应外,其余待测物表现为弱基质效应,可忽略基质效应的影响(见表2),说明QuEChERS法的净化效果较好。对于烟嘧磺隆等5种中等基质效应的待测物,需配制基质匹配标准溶液进行定量分析,其余待测物则采用试剂标准溶液进行定量。
2.7 方法学考察
2.7.1 方法的线性与定量下限按照“1.3”配制质量浓度为0.001~0.5 μg/mL的31种磺酰脲类除草剂混合基质标准溶液,采用本方法进行样品前处理和测定。以各待测物的质量浓度(x,μg/mL)为横坐标,对应峰面积(y)为纵坐标绘制校准曲线,结果显示,31种除草剂的线性关系良好,相关系数(r2)均不小于0.998 0。按10倍信噪比(S/N=10)计算定量下限(LOQ),31种除草剂的LOQ为0.012~2.321 μg/kg(表2),方法灵敏度可满足土壤中目标物的检测要求。

表2 31种除草剂的线性范围、线性方程、相关系数、基质效应、定量下限和标准定量下限Table 2 Linear ranges,linear equations,correlation coefficients(r2),matrix effects,limits of quantitation(LOQ) and limits of quantitation in NY/T 2067-2011 of 31 herbicides
*no data
2.7.2 方法准确度与精密度在空白土壤样品中添加10、100、400 μg/kg的31种除草剂混合标准溶液进行回收率实验,每个加标浓度重复测定6次。由表3可知,31种除草剂的平均回收率为71.8%~119%,相对标准偏差(RSD)为0.62%~13%,表明所建立的方法具有较好的准确度和精密度,能够满足实际样品分析的需求。
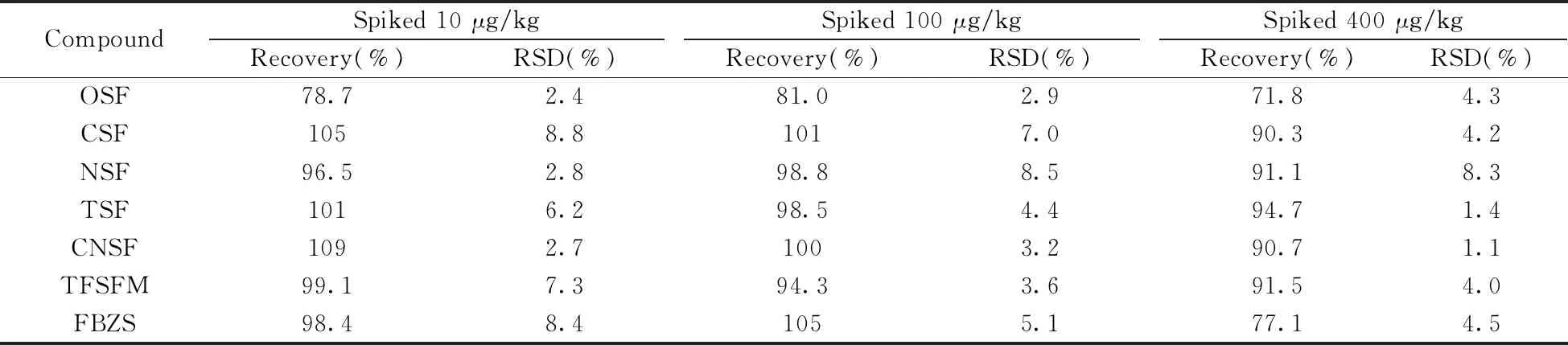
表3 31种除草剂在土壤中的加标回收率及相对标准偏差(RSD)(n=6)Table 3 Spiked recoveries and relative standard deviations(RSD) of 31 herbicides in soil(n=6)
(续表3)
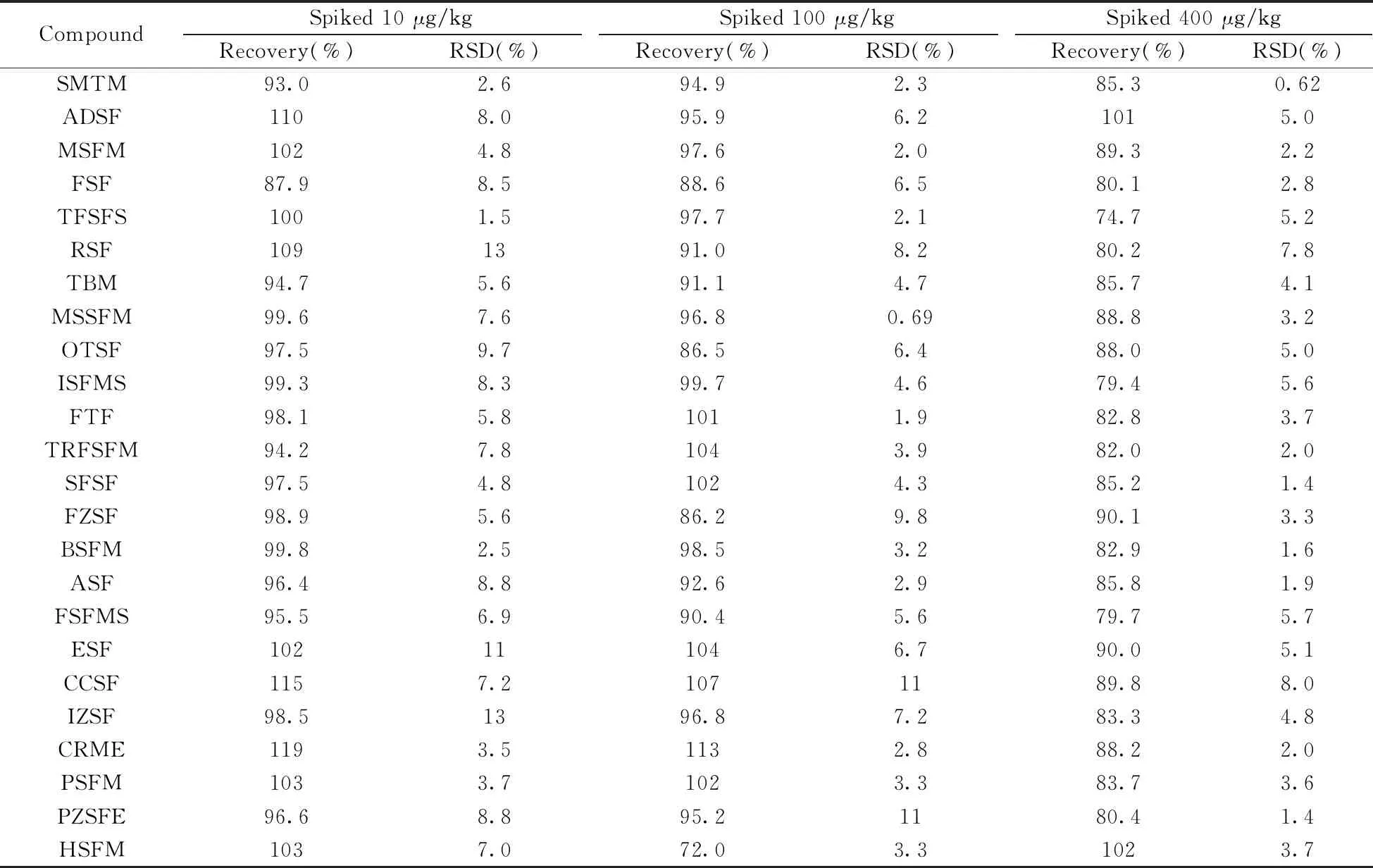
CompoundSpiked 10 μg/kgSpiked 100 μg/kgSpiked 400 μg/kgRecovery(%)RSD(%)Recovery(%)RSD(%)Recovery(%)RSD(%)SMTM93.02.694.92.385.30.62ADSF1108.095.96.21015.0MSFM1024.897.62.089.32.2FSF87.98.588.66.580.12.8TFSFS1001.597.72.174.75.2RSF1091391.08.280.27.8TBM94.75.691.14.785.74.1MSSFM99.67.696.80.6988.83.2OTSF97.59.786.56.488.05.0ISFMS99.38.399.74.679.45.6FTF98.15.81011.982.83.7TRFSFM94.27.81043.982.02.0SFSF97.54.81024.385.21.4FZSF98.95.686.29.890.13.3BSFM99.82.598.53.282.91.6ASF96.48.892.62.985.81.9FSFMS95.56.990.45.679.75.7ESF102111046.790.05.1CCSF1157.21071189.88.0IZSF98.51396.87.283.34.8CRME1193.51132.888.22.0PSFM1033.71023.383.73.6PZSFE96.68.895.21180.41.4HSFM1037.072.03.31023.7
2.8 实际样品的测定
采用本方法对随机选取的200份土壤样品进行测定,结果显示:共有6个样品有检出,其中4个样品检出烟嘧磺隆,检出值分别为3.04、1.64、2.64、2.64 μg/kg;1个样品检出噻吩磺隆(3.92 μg/kg),1个样品检出苄嘧磺隆(8.44 μg/kg)。土壤空白基质添加0.1 μg/mL的混合标准溶液,按照本方法进行前处理和测定,加标回收率为73.4%~103%,其中烟嘧磺隆、噻吩磺隆、苄嘧磺隆的回收率分别为103%、91.2%、95.4%。分析表明:烟嘧磺隆、噻吩磺隆、苄嘧磺隆的检出值均大于本方法的LOQ,且该方法的LOQ低于目前标准规定的LOQ,表明该方法具有较高的灵敏度。
3 结 论
本文建立了一种结合QuEChERS前处理技术和UHPLC-MS/MS测定土壤中31种磺酰脲类除草剂残留的分析方法。该方法前处理简单,样品用量少,分析速度快,线性范围宽,准确度、精密度及灵敏度好,适用于大批量土壤中磺酰脲类除草剂残留的筛查和风险监测。
