基于证据推理与模型认知素养的氧化还原知识构建探讨
2020-05-06黎旭阳
黎旭阳
【摘要】氧化还原反应是中学化学的核心概念,它分散在学生化学学习的全过程。常用的教学方法中,学生短时间内难以认识其本质,进而无法建立相关的知识模型。在教学中不断改进若由化合价变化切入,运用证据推理建立模型认知的方式,能使学生迅速了解氧化还原反应的特征与本质,并体会到证据推理与模型认知在学习中的重要作用。
【关键词】化合价;电子偏移;氧化还原反应
胡久华教授指出氧化还原反应是高中化学核心概念[1],氧化还原反应的思想贯穿了学生化学学习的全阶段,氧化还原反应知识还是解释相关生产生活事件和现象的有效工具。
普通高中化学课程标准(2017年版)提出要以发展化学学科核心素养为主旨,五大素养中包含了证据推理与模型认知素养。基于证据推理与模型认知素养开展氧化还原反应教学能够有效地解决常用的教学方式中存在的不足,取得更好的教学效果。
一、氧化还原教学中常见的教学方式
1.讲授式
奥苏贝尔指出,学生需要花好几小时才能收集到的信息,如果通过教师的有效讲解,可以大大缩短他们的学习时间。有效的讲授式教学能够充分地传递知识信息,引发学生思考、理解与记忆,并掌握科学的思维方法。
讲授式的模式通常由以下几个环节构成。环节一,根据学生已有的知识列出氧化反应的代表:Cu+O2CuO,以及还原反应的代表:CuO+H2Cu+H2O,由此引导学生从氧元素的得失角度进行分析。环节二,建立起氧化反应。还原反应不是孤立发生的,氧化反应与还原反应是同时进行的反应,要构建氧化还原反应的概念。环节三,进一步分析反应中各元素化合价,得出氧化还原反应都有化合价的升降,并利用该特征分析不含氧元素的反应如Fe+CuSO4=FeSO4+Cu。环节四,形成有化合价升降的反应都是氧化还原反应的概念,掌握通过化合价判断反应是否为氧化还原反应的方法。
2.探究式
杜威强调科学教学不仅仅是教给学生探究的结论,而且需要学生形成探究的思维,掌握探究的操作程序,即让学生像科学家搞科学研究工作那样去探索和获取知识。这种思想后来就发展为科学教学的一种方法,即探究式教学。
在氧化还原的探究式教学中,探究式教学的主要思路是“①展示氧化反应或还原反应→②通过标识化合价,探究化合价变化情况→③得出结论:氧化还原反应都有化合价变化→④运用结论分析无氧元素的反应→⑤建立起通过化合价判断反应类型的知识体系→……”在教学的过程中,教师设计问题,让学生讨论发现氧化还原反应的特征是化合价的变化,然后利用这一特征去解决相应的问题。
3.讲授式和探究式的特点与局限
讲授式和探究式在教学设计的总体路线上是一致的,都是利用学生已经掌握的氧化反应、还原反应的定义去认识、评判化学反应,并由此引发认知冲突,使学生感受到已有知识的局限性,然后换一个角度重新分析找到氧化还原反应所隐含的、共同的外部特征,从而建立对氧化还原反应的新认识。
在实际教学中发现,这两种教学方式在从含有氧的氧化还原反应过渡到无氧参与的氧化还原反应的过程中,有较大的思维跳跃,对于基础知识牢固、思维活跃、理解能力强的学生来说,不会产生太大困难;但是对于化学基础薄弱、思维不太活跃的学困生而言,这样的推导分析让他们如坠云雾,无法真正掌握知识重点,更不会运用氧化还原知识解决相关问题。
二、基于证据推理与模型建构的氧化还原反应教学案例
学生化学学科核心素养的发展是一个自我构建、不断提升的过程,可以通过引导学生开展分类与概括、证据与推理、模型与解释、符号与表征等具有学科特质的学习活动,结合小组合作、实验探究、谈论交流等多样化方式促进学生学习方式的转变。
以任务驱动为方法,在课堂中为学生设立相应的任务,学生在完成相关任务的过程中不断地梳理凌乱的知识,逐步建构相关的知识体系,掌握运用知识解决问题的技能,内化知识原理,在学习过程中逐渐形成相关的学科素养。
1.环节一:分类与概括——建立证据意识
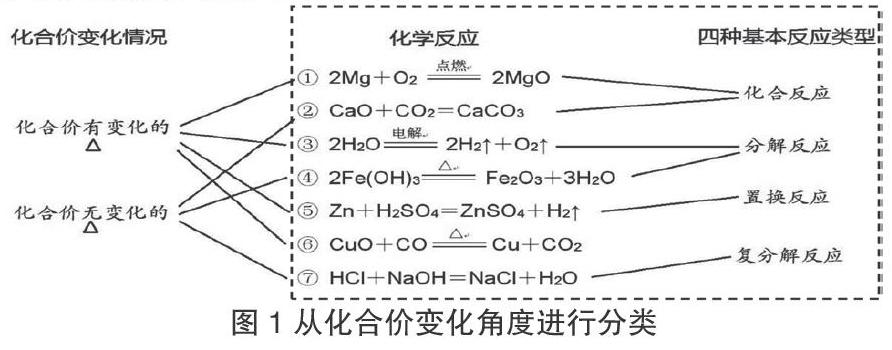
任务一:运用分类知识仔细观察教师提供的反应方程式,选择合适的分类方法对反应进行分类,然后向组员阐述自己的分类依据并获得他们的支持。学生作答情况如图1中右侧虚线框部分。
设计意图:在对提供的反应进行分类的过程中,大部分学生都能够依据四大基本反应类型的分类标准进行分类,但是对于反应⑥的归属产生了争议:一部分同学依据置换反应表面特征认为属于置换反应;另一部分同学认为依据置换反应的原理不属于置换反应。在争论中,学生能够逐渐建立证据意识,掌握利用证据进行分析的技巧。
2.环节二:标注化合价——建构新认知模型
任务二:换个角度认识世界。在前面的任务中归纳发现,同学们在初中掌握的知识是非常牢固的,都是从反应物和生成物的类型,以四大基本反应类型的特征为依据进行分类。但是,大家还掌握了化合价的标注,尝试一下如果从化合价的角度重新看这些反应会不会有新的发现。学生作答情况见图1。
设计意图:通过对化合价进行标注,找到在一部分化学反应中某一元素的化合价在反应前后的变化情况,另一部分化学反应中的所有元素的化合价在反应后并无变化,由此构建了化学反应的新的认知模型——化合价发生改变。
在学生掌握了利用化合价对反应进行分类的方法后,建立关于氧化还原反应的判断流程,提炼成形成口诀:同元素,前减后,不为零,定氧还。
至此,经过两个环节的学习活动,学生建立了在不同证据观点的支撑下可以得到不同的结论的认知。
3.环节三:微观表征——建立认知图式
任務三:原子非常小,无法用肉眼观察,但是科学家为我们提供了微观与宏观联系的工具——原子结构示意图。下面让我们带上原子结构示意图这个工具,阅读教材图2-11氯化钠形成示意图,找出反应①化合价升降的原因,模仿画出形成示意图。
设计意图:利用化合价对化学反应进行分类的方法仅仅是对化学反应分类的方法,还未能完整建构氧化还原反应的认知模型。通过引导学生阅读教材,观察镁原子、氧原子的原子结构示意图,运用教材提供信息分析在反应中电子的得失情况,自主画出氧化镁形成示意图,自主构建氧化还原反应中元素化合价变化的原因。
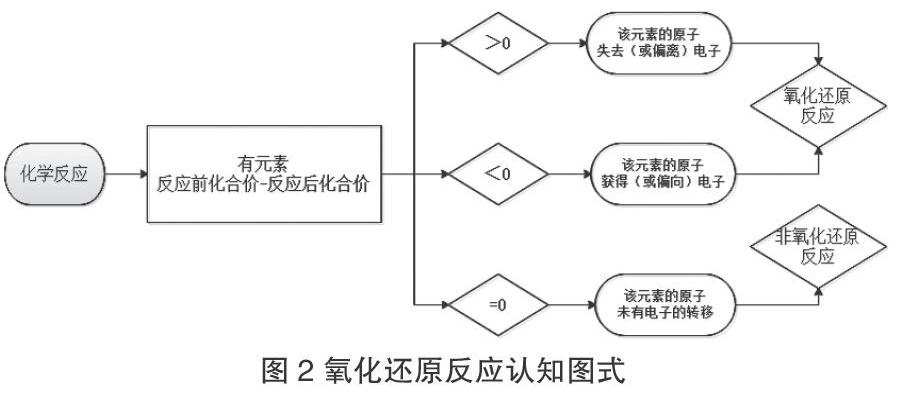
在此基础之上与学生共同提炼生成氧化还原反应的认知图式,见图2。
4.环节四:归纳整理——概念内化
任务四:经过前面的体验,我们逐渐明确了有的化学反应会有化合价的变化,有的化学反应没有化合价的变化,导致化合价变化的原因是由于原子的电子发生了得失或偏移。下面我们从知识的本质出发,以电子是否发生转移为标准,将化学反应分成两类(即氧化还原反应和非氧化还原反应)。之前我們掌握的四大基本反应类型与氧化还原反应和非氧化还原反应之间存在怎样的联系?请用集合的观点完成关系图。
设计意图:四大基本反应类型与氧化还原反应是由于分类角度不同而产生的不同的结论,通过对代表反应的分析,引导学生形成多角度思维的习惯,培养学生根据信息正确选择模型的能力。
5.环节五:整理联系——技巧培养
任务五:按要求写化学方程式,找出规律,总结判断氧化还原反应的技巧。
(1)一种单质还原一种化合物。
(2)一种单质氧化另一种单质。
(3)一种非金属单质还原一种氧化物。
(4)同一种物质中一种元素氧化另一种元素。
学生提炼心得:有单质出现的化学反应基本上都是氧化还原反应。
设计意图:在实际解决问题中,学生需要有一个简单易行的方式与方法,运用这些方式方法,既能够提高解决问题的效率,也能够增强解决问题的信心。
三、课后反思
在解决实际问题的时候通常需要从储备知识中准确筛选出有助于解决问题的知识。化学的知识点多而且分布较为零散,这个特点会在学生运用化学知识解决问题的过程中会造成不小的障碍。要顺利突破这个障碍,不仅需要有扎实的知识储备,而且需要有科学的思维方式。新课标中明确提出证据推理与模型认知素养就是学生需要养成的科学的思维方式。科学的思维方式不是一朝一夕能够养成的,需要在日常有意识地渗透到教学的各个环节中,引导学生在分析问题时不要跟着感觉走,而是要有理有据。
【参考文献】
胡久华,陈欣,支瑶.不同教学处理方式对高中生化学核心概念建构的影响[J].中国教育学刊,2007(07):61-64.
