TiO2纳米管阵列粗糙度调控及其与蛋白相互作用
2020-04-06吴娜董依慧吉晓燕皇甫长安陆小华
吴娜,董依慧,吉晓燕,皇甫长安,陆小华
(1 南京工业大学材料化学工程国家重点实验室,江苏南京210009; 2吕勒奥工业大学能源工程系,瑞典吕勒奥97187)
引 言
蛋白分子与载体材料表面之间的相互作用具有高度的复杂性,涉及到工程学、材料学、生物学等跨学科研究领域[1],推动着如人造器官的抗污染特性[2],液相色谱柱分离蛋白[3],以及电化学生物传感和药物运输中酶的固定化[4]等领域的发展。一系列不同应用和现象背后的本质在于蛋白分子与载体材料表面之间的相互作用的大小不同,因此,调控两者之间的相互作用对于控制生物分子的作用行为至关重要[1,5]。
当生物材料进入到生理体系中,材料的表面结构性质对蛋白分子在表面的相互作用有着重要的影响。材料结构性质,主要包括形状、孔结构和表面粗糙度。例如Tang 等[6]通过调整硅前驱体和表面活性剂的摩尔比,进而控制二氧化硅颗粒形貌,从球形、棒状到蠕虫状结构,不同形状颗粒比表面积不同,药物运输的能力也不同。Bayne 等[7]分析孔材料孔隙直径和酶负荷值之间的关系,发现当孔径小于10 nm,由于酶在进入孔时受到物理限制,载量较小,当孔径大于100 nm,由于可用表面积减少,酶载量也会下降,在10~100 nm 的孔径范围内,随着孔径的增大,酶载量水平会降低。Huang等[8]通过对钛片表面喷砂处理,再采用强酸腐蚀,得到具有纳米粗糙度的结构,并在界面上培养细菌,发现具有纳米粗糙结构的表面具有很强的抗细菌功能。这些不同结构的本质主要是固体材料与蛋白分子的有效接触面积的不同,接触面积不同进而产生不同的相互作用及性能。因此,调节材料表面结构可以实现蛋白分子与固体表面相互作用的调控。
在一系列载体材料中,TiO2纳米管(TiO2nanotube arrays,TNAs)在具有TiO2材料的优点,如优异的生物相容性、机械稳定性好的同时[9-12],还具有纳米形貌可调、形貌高度规整有序等特点,成功运用到如光电催化[13-14]、电化学生物传感[15-16]、抗菌涂层[17]、医学植入材料[18]等领域。目前制备TNAs 的方法有多种[19-21],其中阳极氧化法由于方法简单,过程简练,而受到广泛关注。当氧化电压越大时,制备得到的TNAs 管径越大[22]。然而,随着电压的增加,TNAs的粗糙度也大大增加,粗糙度主要来源于制备过程形成的大范围裂纹以及管径的高低不均匀性,导致高电压下制备得到的纳米管性能降低[23]。因此如何合理有效地调控纳米管表面的粗糙度,进而实现其表面结构性能的有效提高尤为重要。文献[24]报道阳极氧化法利用电解液腐蚀生成TNAs,电解液组分包括氟化铵、乙二醇和水,其中氟离子作为主要腐蚀剂,能有效定向调节TNAs 的表面结构,包括孔径、壁厚,有望作为调控纳米管表面粗糙度的一种手段。
通常情况下,判断生物蛋白在载体表面的吸附强弱主要通过宏观吸附量的大小[25-27],然而宏观吸附量只是一种简单的定性分析相互作用强弱的手段,需要借助其他一些高效实验手段来表征生物蛋白与载体表面的相互作用。表征蛋白与固体表面相互作用的手段有多种,如液相色谱[28]、电化学传感[29]、表面拉曼增强[30]等,而原子力显微镜(atomic force microscopy,AFM)作为表征材料表面三维结构以及表面力学性质的有效仪器[31],可以通过自组装将蛋白分子固定在AFM 探针上直接用来表征蛋白分子与复杂固体表面相互作用力的大小[32-33]。本课题组前期采用AFM 定量研究了介孔TiO2与不同蛋白相互作用,并获得了单个蛋白分子与介孔TiO2表面在复杂条件下的作用力[22,34-36],奠定了利用AFM定量研究蛋白与固体表面相互作用的基础。基于此,本文的工作主要通过调节电解液中氟离子的浓度来制备不同粗糙度的TNAs,进一步采用AFM 表征其形貌及粗糙度,并基于AFM 的力学表征特性,研究纳米管表面力学性能。同时,将蛋白自组装修饰到探针针尖,形成蛋白团簇,测试该团簇与材料表面黏附力,研究粗糙度对生物分子与TNAs 表面相互作用影响。
1 实验部分
1.1 材料
金属钛片(0.25 mm),99.7%,Sigma-Aldrich;砂纸,50 μm;氟化铵(NH4F),ACS,98%;乙二醇(C2H6O2),分析纯,上海试四赫维化学有限公司;无水乙醇(C2H6O),分析纯,上海凌峰化学试剂有限公司;商业可用纯净水;细胞色素C(Cytochrome C,Cyt C,尺寸:2.6 nm×3.2 nm×3.3 nm,分子量:12400),北京拜尔迪生物有限公司;巯基十六烷基酸(HS(CH2)15COOH, 90%),上海Sigma-Aldrich Trading Co.Ltd.公司;二甲基甲酰胺(DMF,无水),三乙胺(C6H15N,99%),三氟乙酸酐(C4F6O3,98%)均购于上海J&K Scientific 公司;二氯甲烷(CH2Cl),分析纯,国药集团化学试剂有限公司。
1.2 TNAs的制备
TNAs 的制备方法采用Grimes[20]提出的恒电位阳极氧化法,具体过程如下:金属钛片作为基底,将钛片裁剪成1 cm×3 cm 的长方形,用砂纸打磨掉表面的TiO2层,在纯净水和无水乙醇中分别超声清洗15 min,重复交替3 次后,常温下用氮气吹干密封保存,作为阳极基底备用。电解液采用乙二醇作溶剂,0.4%(质量)氟化铵作腐蚀剂,并含有1%(质量)的纯净水。电解池中盛放75 ml 上述电解液,预处理后的钛片做阳极,铂片做阴极。采用两步阳极氧化法,先在8 V 电压下反应12 h,后分别在15、25、35、45 V 下反应12 h,将制得物在乙二醇中超声清洗45 min,再用无水乙醇冲洗两次,于60℃烘箱中烘干,再采用高温退火处理,马弗炉于初始温度20℃下以2℃·min-1速度升高到500℃,焙烧2 h 后自然冷却,密封干燥保存。
本文通过改变电解液中氟离子的浓度来调节TNAs 表面的粗糙度,因此,同时制备了不同氟离子浓度下的TNAs,制备方法同上,仅将氟化铵的浓度分别变为0.3%、0.2%(质量)。因此,基于不同氟离子浓度下制备得到的样品命名为:0.4-TNA-15V、0.4-TNA-25V、0.4-TNA-35V、0.4-TNA-45V、0.3-TNA-15V、0.3-TNA-25V、0.3-TNA-35V、0.3-TNA-45V、0.2-TNA-15V、0.2-TNA-25V、0.2-TNA-35V、0.2-TNA-45V。
1.3 材料表征
X 射线粉末衍射(XRD,Bruker D8 Adavance)用于表征材料晶体结构,工作电流、电压分别为40 mA和40 kV,扫描速度为0.02(°)·min-1,范围为10°~60°;扫 描 电 子 显 微 镜(FESEM,Hitachi S-4800,Japan)用于表征材料的表面结构形貌,放大倍数1000~200000,加速电压5 kV;原子力显微镜(atomic force microscopy,AFM,Bruker ICON)用于表征材料表面三维形貌(轻敲模式)及力学测试(接触模式);激光拉曼光谱(Raman,Horiba Labram HR800)用于表征材料表面组成信息,采用He-Cd 激光,激光波长为514 nm,激光功率为10 mW,扫描范围100~800 cm-1。
1.4 Cyt C修饰AFM探针
AFM 探针选为表面覆盖Au 的氮化硅探针(NPG-10,弹性系数在0.05~0.5 N·m-1,针尖曲率半径约为20 nm),将探针浸泡在溶剂为50%(体积)的无水乙醇溶液的1 mmol·L-1巯基十六烷基酸溶液中,于37℃的烘箱中避光放置12 h。随后取出探针,用无水乙醇清洗表面3~4 次,自然风干。随后将探针放置在0.28 ml 三乙胺、0.14 ml 三氟酸酐和9.58 ml二甲基甲酰胺的混合溶液中,室温下浸泡20 min[37]。然后取出探针,用二氯甲烷清洗3次,自然风干。最后,配制pH 为7.2 的磷酸缓冲盐(phosphate buffer saline,PBS)溶液体系下的2 mg·ml-1的Cyt C溶液,将探针浸泡到上述PBS 缓冲体系下的蛋白溶液中12 h,随后用缓冲溶液清洗,自然风干,即可得到修饰Cyt C的探针。
1.5 AFM黏附力测试
在室温、大气状态下,使用接触模式进行AFM黏附力的测试,主要包括采用AFM 探针(SNL-10,弹性系数在0.06~0.35 N·m-1)直接测试材料表面黏附力,以及采用Cyt C 修饰后AFM 探针测试Cyt C 与材料表面黏附力。测试步骤分两步,第一步矫正探针弹性系数,首先选择蓝宝石为基底,在扫描速率为1.0 Hz 下扫完一张图,获得偏转灵敏度(deflection sensitivity),接着进行热调(thermal tune),获得矫正后的探针的弹性系数,最后可将电压信号(V)转换为力的单位(N)。第二步将蓝宝石换为待测样品,在扫描速率为1.0 Hz,扫描范围为2 μm×2 μm 下扫完一张图,黏附力的测得主要根据力曲线获得[37]。在扫描图中选取100 个点做100 个力曲线用于获得平均黏附力。
2 结果与讨论
2.1 TNAs的组成分析
采用XRD 表征三种不同氟离子浓度下制备得到的四种外加电压下(15、25、35、45 V)的TNAs 的晶相。图1(a)~(c)分别是0.4%、0.3%、0.2%(质量)氟离子浓度下TNAs 的XRD 谱图,其中在25.3°、37.7°和48.0°均出现了明显的衍射峰,分别对应的是TiO2的101、004 和200 晶面,为典型锐钛矿相。同时,可以发现锐钛矿相峰的强度随着外加电压的升高逐渐增强,说明样品中锐钛矿相的含量逐渐增加,无定形的含量逐渐减少。另外,由于TNAs 的制备基底为Ti基底,因此,在TNAs的XRD谱图上还会存在少许Ti的峰,随着电压的增加,制备的管越长,XRD 谱图上Ti的峰越来越弱,这是由于XRD在Ti上的衍射穿透深度越来越弱所导致[22]。
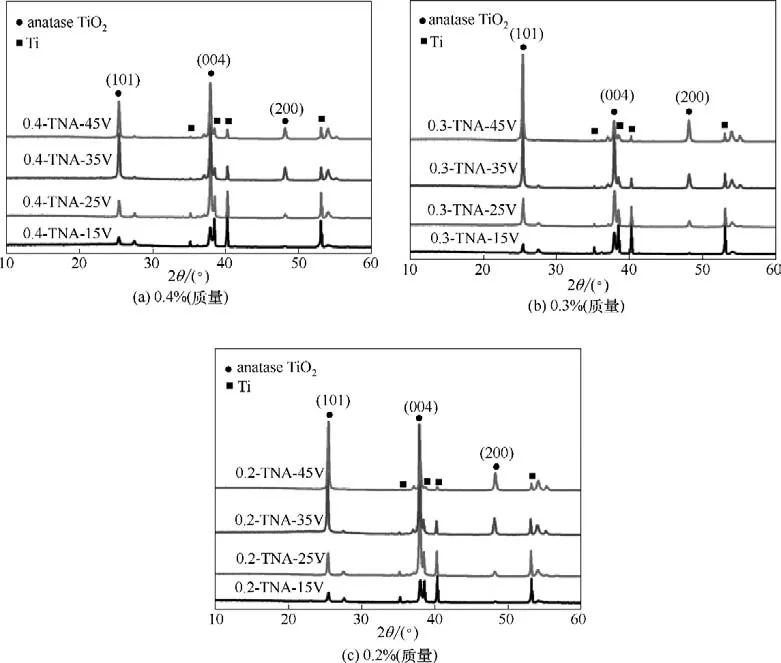
图1 不同氟离子浓度和电压下制备TNAs的XRD谱图Fig.1 XRD patterns of TNAs prepared at different F-concentrations and voltages
图2(a)~(c)分别是0.4%、0.3%、0.2%(质量)氟离子浓度下TNAs 的Raman 谱图。由图中可以发现,峰出现的 位 置分别在145.2、398.1、519.6、641.7 cm-1,进一步说明制备得到的TNAs 均是稳定的锐钛矿晶型,同时发现锐钛矿相峰的强度随着外加电压的增大逐渐增强,说明样品中锐钛矿相的含量逐渐增加,与XRD谱图中的结果一致。
采用AFM 对TNAs 表面形貌及粗糙度进行表征。图3 是0.4%(质量)氟离子浓度下的四个外加电压(15、25、35、45 V)下的TNAs 的2D 以及表面高度图。从2D 图可以发现,随着阳极氧化电压的增加,TNAs 的管径增加。另外,随着氧化电压的增加,TNAs 的粗糙度增加,通过均方根(root-mean-square,RMS)处理得到15、25、35、45 V 电压下制备得到的TNAs 粗糙度分别约为23.2、47.5、61.4、85.2 nm(表1)。同时,发现表面高度图的起伏程度也随着电压的增大而增大,波谷深度从约90 nm到350 nm,即裂纹导致的起伏越来越明显,这也是粗糙度逐渐增加的原因。
图4 是0.3%(质量)氟离子浓度下的四个外加电压下的TNAs 的2 D 以及表面高度图。可以发现,TNAs的管径随着阳极氧化电压的增加而增大,粗糙度也增加,处理得到四个电压下的TNAs 粗糙度分别约为21.4、44.9、55.1、65.3 nm(表1)。同时,表面高度图的起伏程度同样随着电压的增大而增大,波谷深度从约50 nm 到200 nm。另外,和图3 比较,在同一电压下,0.3%(质量)氟离子浓度下的TNAs 表面粗糙度值降低,同时高度图的起伏程度比0.4%(质量)氟离子浓度下的小,说明通过降低氟离子浓度可以减小纳米管表面粗糙度以及高低起伏程度。这是因为TNAs 的生成分为三个阶段:TiO2氧化膜的形成,多孔氧化膜的形成,纳米管的形成,氟离子主要作用在多孔氧化膜的形成阶段,能刻蚀钛基底表面和溶解生成的TiO2阻挡层,将表面由点蚀坑形貌逐渐变为蜂窝状结构[38],因此氟离子浓度减小,表面腐蚀程度降低,从而影响TNAs表面的粗糙结构。
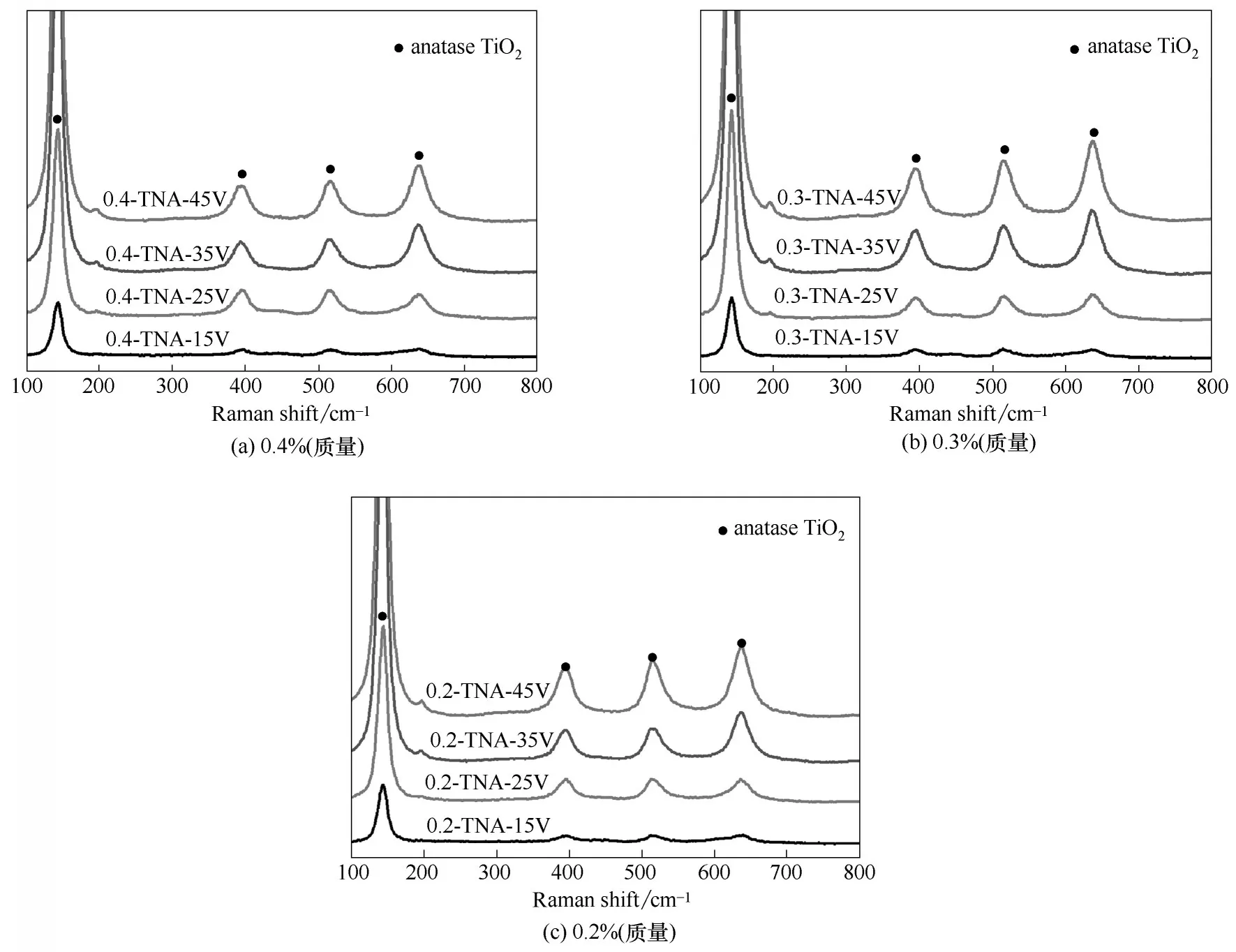
图2 不同氟离子浓度和电压下制备TNAs的Raman谱图Fig.2 Raman spectra of TNAs prepared at different F-concentrations and voltages
图5 是0.2%(质量)氟离子浓度下的四个外加电压下的TNAs 的2 D 以及表面高度图。同样发现,TNAs的管径随着阳极氧化电压的增加而增大,粗糙度同样增加,处理得到四个电压下的TNAs 粗糙度分别约为14.4、36.7、37.0、63.8 nm(表1),粗糙度值相比0.3%(质量)氟离子浓度下的TNAs 明显降低。同时,表面高度图的起伏程度虽随着电压的增大而增大,但在同一电压下,0.2%(质量)氟离子浓度下的TNAs 表面高度图的起伏程度最小,波谷深度从约20 nm 到150 nm 左右,明显发现纳米管的高低起伏的不均匀性得到改善,进一步验证了采用氟离子浓度的调控可以实现纳米管表面粗糙度以及高低起伏平整度的调控。
将不同氟离子浓度下制备得到的TNAs 粗糙度值汇总在表1 中,可以发现,当氟离子浓度一定时,随着氧化电压增大,制备得到的TNAs 粗糙度增大;同时,在外加电压一定的情况下,降低氟离子浓度,TNAs表面粗糙度有所降低。进一步分析,在氧化电压较低的情况下(如15 V 和25 V),氟离子浓度的改变对粗糙度的影响不及高电压下(如35 V 和45V)的明显,尤其在35 V时,氟离子浓度从0.4%(质量)降到0.2%(质量),TNAs 粗糙度降低了将近一半。由此可见,通过调控电解液中氟离子的浓度,可以实现TNAs的表面粗糙度的有效调控。
采用FESEM 对TNAs 进行形貌表征。图6 是0.4%(质量)氟离子浓度下的TNAs 的FESEM 图(500 nm 和5 μm 扫描范围)。通过FESEM 图(500 nm 扫描范围)可以发现,随着氧化电压增加,制备得到的TNAs 的管径增加,15、25、35、45 V 电压制备得到的TNAs 的管径分别约为24.7、51.1、65.7、91.6 nm(表2)。同时,通过FESEM 图(5 μm 扫描范围)可以发现,随着外加电压增大,TNAs表面平整度变差,这和AFM表征的粗糙度结果一致。
图7 是0.3%(质量)氟离子浓度下的TNAs 的FESEM 图(500 nm 和5 μm 扫描范围)。通过FESEM图(500 nm 扫描范围)发现,随着氧化电压增加,制备得到的TNAs 的管径增加,15、25、35、45 V 电压下制备得到的TNAs 的管径分别约为23.1、49.9、65.0、87.2 nm(表2)。同时,通过比较FESEM 图(5 μm 扫描范围),外加电压增大,TNAs 表面平整度变差。另外,和图6相比较,在同一电压下,0.3%(质量)氟离子浓度下的TNAs 的管径与0.4%(质量)氟离子浓度下的相比变化不大,但是表面平整度变好,与AFM 表征的粗糙度结果一致。
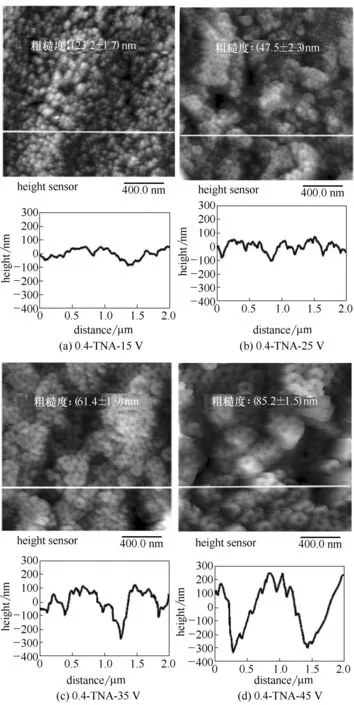
图3 0.4%(质量)氟离子浓度下不同电压制备TNAs的AFM 2D以及高度图Fig.3 AFM topographical and corresponding height images of TNAs prepared with different voltages at 0.4%(mass)F-concentration
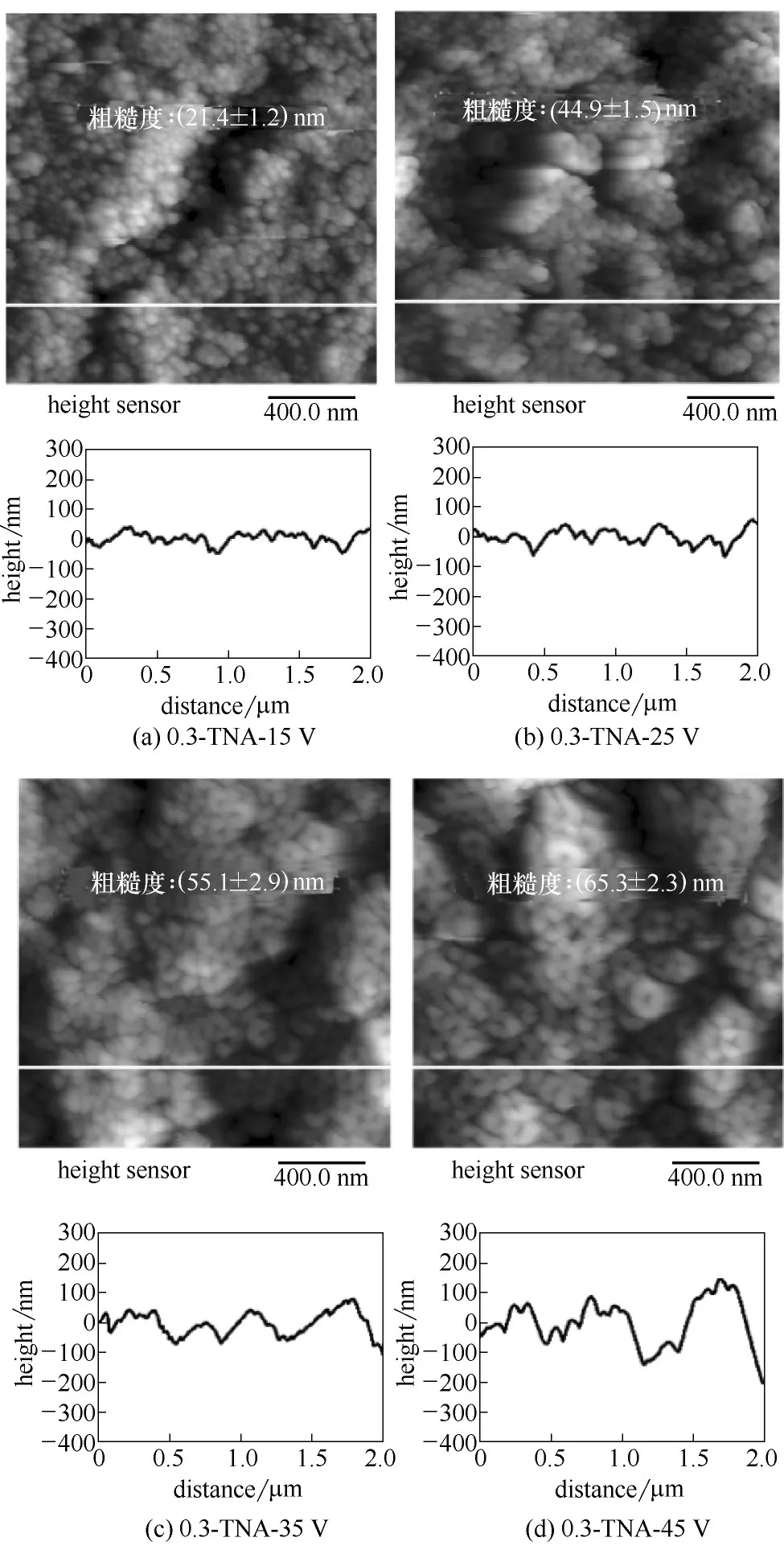
图4 0.3%(质量)氟离子浓度下不同电压制备TNAs的AFM 2D以及高度图Fig.4 AFM topographical and corresponding height images of TNAs prepared with different voltages at 0.3%(mass)F-concentration
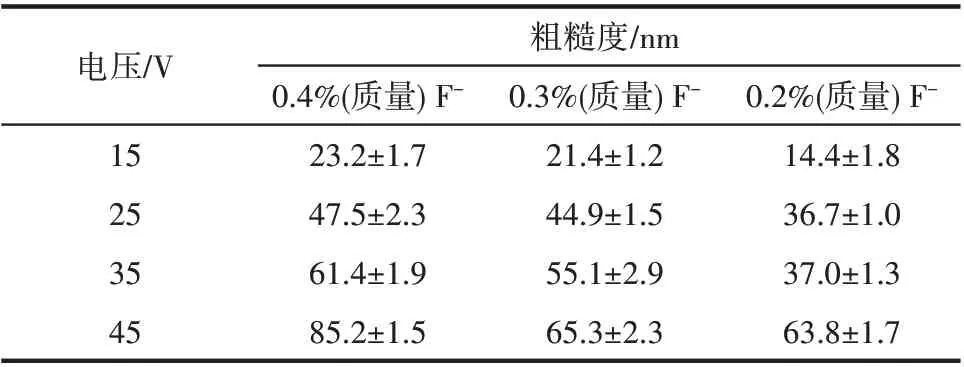
表1 不同外加电压以及氟离子浓度下TNAs粗糙度Table 1 Roughness of TNAs under different applied voltages and F-concentrations
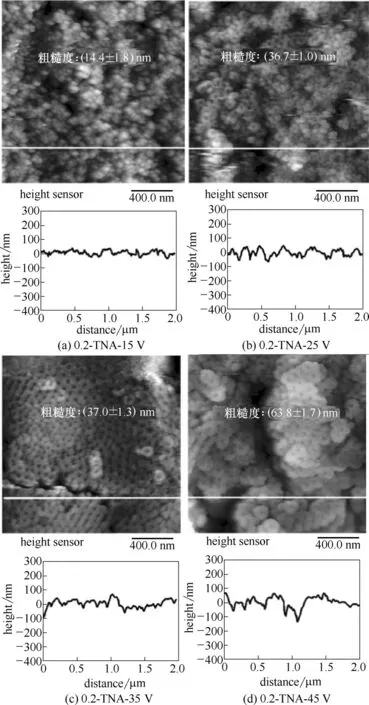
图5 0.2%(质量)氟离子浓度下不同电压制备TNAs的AFM 2D以及高度图Fig.5 AFM topographical and corresponding height images of TNAs prepared with different voltages at 0.2%(mass)F-concentration
图8 是0.2%(质量)氟离子浓度下的TNAs 的FESEM 图(500 nm 和5 μm 扫描范围)。通过FESEM图(500 nm 扫描范围)发现,随着氧化电压增加,制备得到的TNAs 的管径增加,15、25、35、45 V 电压下制备得到的TNAs 的管径分别约为21.5、48.7、62.3、78.8 nm(表2)。同时,通过比较FESEM 图(5 μm 扫描范围),外加电压增大,TNAs 表面平整度也变差。另外,和图7相比较,在同一电压下,0.2%(质量)氟离子浓度下的TNAs 的管径在电压较小的情况下变化不大,但表面平整度得到改善,裂纹明显减少,和前面AFM表征的粗糙度结果一致。
将不同氟离子浓度以及电压下的TNAs 的壁厚、管径列于表2中。结果发现,当氟离子浓度相同时,TNAs 的管壁随外加电压的增大而变薄;当制备电压一定时,随着氟离子浓度的降低,TNAs 的壁厚增加。说明氟离子浓度的降低在减小表面粗糙度的同时,增加了壁厚。当电压固定时,随着氟离子浓度的降低,管径减小,但是变化较小,其主要由于壁厚的增加导致管径有所减小。
TNAs 的管长对其性能也有一定影响,因此,同时采用FESEM 对TNAs 管长进行表征,测得不同外加电压以及氟离子浓度下TNAs 管长,结果汇总于表3。可以发现,同一氟离子浓度下,管长随着电压增大而增大;而同一电压下,不同氟离子浓度下制备的TNAs 管长几乎相等,说明改变氟离子浓度对管长的影响可忽略。
2.2 AFM测试探针与TNAs黏附力
黏附力测试在AFM接触模式下进行,AFM测得的黏附力的大小与针尖和样品之间的接触面积相关,接触面积越大,探针脱离表面所需要克服的力就增加,因此获得的黏附力也增加。为了获得统计学意义,探针与每个样品之间的黏附力测试了100个位置的力曲线,获得100个黏附力,并做成统计分布图。
将探针在不同氟离子浓度和外加电压下制备得到的TNAs表面(2 μm×2 μm)黏附力分布图通过高斯方程拟合,以35 V 的数据处理为例,如图9 所示。使用拟合得到的峰位置和半峰宽分别作为平均黏附力和误差值,将结果列于表4 中。表4 同时列出了处理得到的壁面积比率。结果发现,同一氟离子浓度下,35 V 下TNAs 表面黏附力皆最大,这是由于此时壁面积比率最大,探针与TNAs 有效接触面积达到最大;而外加电压一定时,随着氟离子浓度降低,纳米管表面粗糙度减小,壁面积比率值增加,探针与TNAs 有效接触面积增大,因而黏附力也增大。

表2 不同外加电压以及氟离子浓度条件下TNAs壁厚及管径Table 2 Wall thickness and diameter of TNAs under different applied voltages and F-concentrations

图6 0.4%(质量)氟离子浓度下不同电压制备得到TNAs的FESEM 图像Fig.6 FESEM images of TNAs prepared with different voltages at 0.4%(mass)F-concentration

图7 0.3%(质量)氟离子浓度下不同电压制备TNAs的FESEM图像Fig.7 FESEM images of TNAs prepared with different voltages at 0.3%(mass)F-concentration
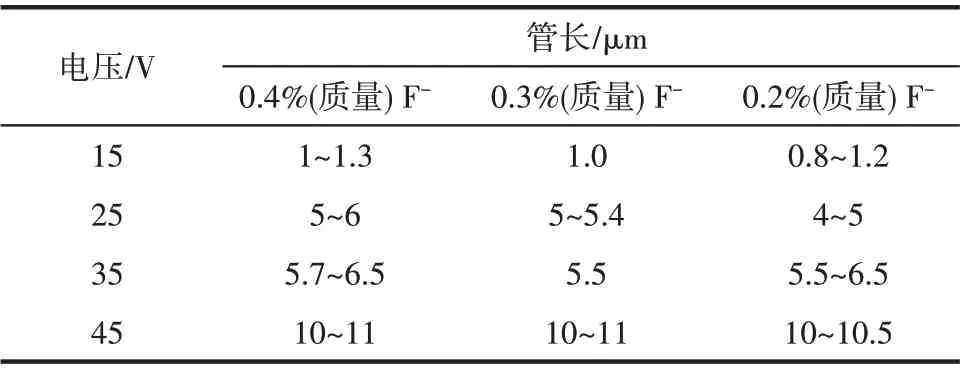
表3 不同外加电压以及氟离子浓度下TNAs管长Table 3 Tube length of TNAs under different applied voltages and F-concentrations

图8 0.2%(质量)氟离子浓度下不同电压下制备TNAs的FESEM图像Fig.8 FESEM images of TNAs prepared with different voltages at 0.2%(mass)F-concentration
2.3 AFM测试Cyt C与TNAs黏附力
Cyt C 是一种在生物氧化过程中具有电子传递能力的蛋白,进而在生物传感以及表面拉曼增强等领域被广泛用作模型研究蛋白[22,39]。将Cyt C 自组装修饰到探针针尖,形成蛋白团簇,测试该团簇与材料表面黏附力。和AFM 测试探针与材料表面黏附力相同,组装蛋白的针尖脱离样品表面的力为蛋白与其表面黏附力。同样地,为了获得统计学意义,Cyt C 与每个样品之间的黏附力测试了100 个位置的力曲线,获得100 个黏附力,并做成统计分布图。
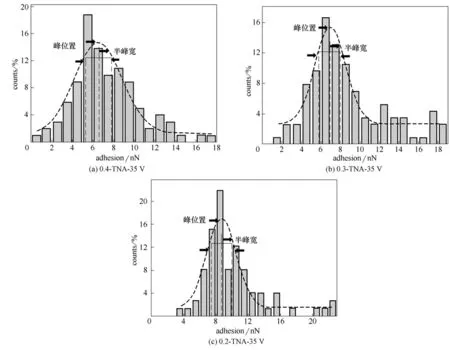
图9 不同氟离子浓度35 V下制备TNAs的表面黏附力分布Fig.9 Histogram of adhesion forces measured for TNAs prepared with 35 V at different F-concentrations
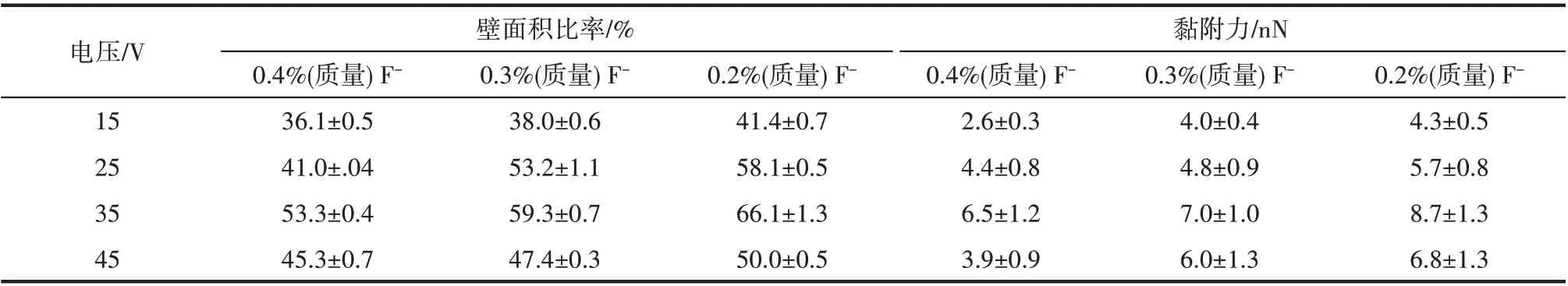
表4 不同外加电压以及氟离子浓度条件下TNAs壁面积比率以及表面黏附力Table 4 Wall area ratio and adhesion force of TNAs under different applied voltages and F-concentrations
将Cyt C 在不同氟离子浓度和外加电压下制备得到的TNAs表面(2 μm×2 μm)黏附力分布图通过高斯方程拟合,以35 V的数据处理为例,如图10所示。使用拟合得到的峰位置和半峰宽分别作为平均黏附力和误差值,将结果列于表5中。可以发现探针-TNAs 表面黏附力随电压和氟离子浓度的变化趋势相同,即同一氟离子浓度下,35 V 下黏附力皆最大;而当外加电压一定,随着氟离子浓度降低,纳米管表面粗糙度减小,黏附力增大。结果说明通过调控电解液中氟离子浓度能够有效控制TNAs 表面粗糙度,进一步改变蛋白与其表面相互作用大小。
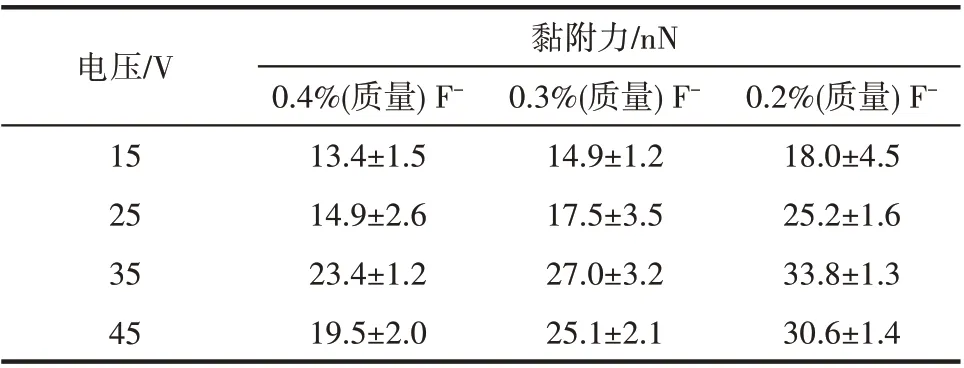
表5 不同外加电压以及氟离子浓度条件下Cyt C-TNAs表面黏附力Table 5 Adhesion force of Cyt C-TNAs under different applied voltages and F-concentrations
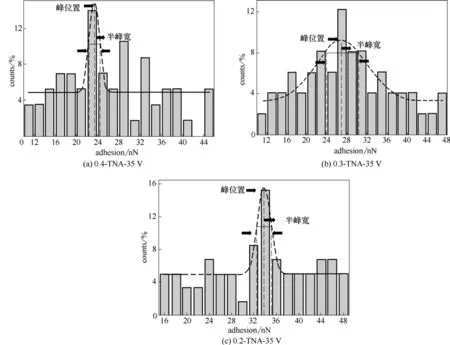
图10 Cyt C与不同氟离子浓度35 V下制备TNAs的表面黏附力分布Fig.10 Histogram of adhesion forces measured for Cyt C with TNAs prepared with 35 V at different F-concentrations
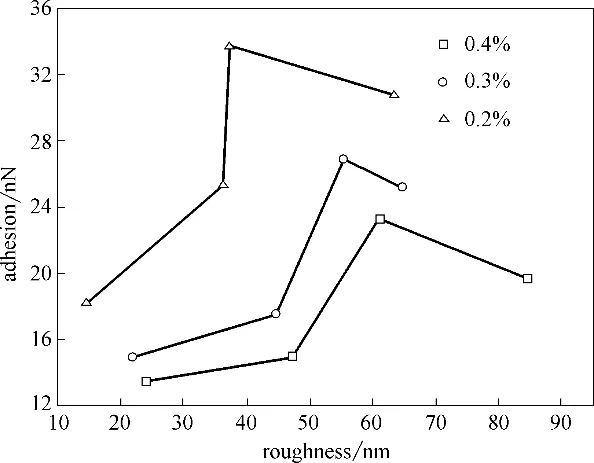
图11 黏附力与粗糙度的关联Fig.11 Association between adhesion and roughness
图11 为黏附力与粗糙度的关联,可以发现,同一氟离子浓度下,Cyt C 与不同电压制备下的TNAs之间的黏附力先增加后减小,在35V 下制备得到的TNAs 与蛋白之间的黏附力均最大,主要原因在于TNAs 壁面积比率最大,蛋白团簇与TNAs 表面有效接触面积最大;而同一电压下,氟离子浓度降低,黏附力增大,也是由于TNAs 平整度变好,壁面积比率变大,蛋白团簇与TNAs 有效接触面积增大。电解液中氟离子浓度以及外加电压对粗糙度的影响,本质上是对Cyt C 与TNAs 有效接触面积的改变,进一步实现对两者之间的黏附力的调控。
3 结 论
采用电化学阳极氧化法,电解液以乙二醇为溶剂,分别以0.4%、0.3%、0.2%(质量)氟化铵为腐蚀剂,不同电压下制备得到一系列不同粗糙度和孔径大小的TNAs,以AFM 表征其形貌粗糙度以及进行力学测试,并将蛋白修饰到针尖,进一步研究粗糙度对生物分子与TNAs 表面相互作用影响。研究发现,当固定外加电压,氟化铵质量分数从0.4%(质量)降到0.2%(质量),制备得到的TNAs 表面粗糙度降低,壁厚增加,TNAs管径变化较小,导致壁面积比率增加,蛋白分子与TNAs 有效接触面积增大,进一步导致黏附力增加。综上所述,通过调节电解液里氟化铵的质量分数可改变TNAs 表面粗糙度,从而增大蛋白分子与其表面接触面积,进一步增加其表面黏附力,这对TNAs 在生物电极固定化领域具有一定的指导意义。
