多酚与玉米淀粉相互作用研究
2020-03-23任顺成李林政潘天义
肖 遥,曹 悦,任顺成*,李林政,潘天义
1.河南工业大学 河南省天然色素制备重点实验室,河南 郑州 450001 2.河南中大恒源生物科技股份有限公司,河南 漯河 462600
淀粉作为人类食物的主要成分可提供生命活动所需的能量,且由于其独特的性质,在食品、化学、化工中的应用日趋广泛。淀粉由线性的直链淀粉和具有高分支结构的支链淀粉构成,根据二者比例的不同主要分为高直链淀粉、普通淀粉和蜡质淀粉[1]。天然淀粉存在一些不足,如冻融稳定性差、易老化、冷水溶解性差等,因此常通过改性或改变加工、贮藏方式等使其理化性质得到改善。
植物多酚是广泛存在于植物体内的一类天然产物,具有芳香环结构并在环上结合一个或多个羟基[2]。按照多酚的化学结构可分为水解单宁类与缩合单宁类,另外,根据多酚的分子结构中碳原子骨架结构的异同,将其分为酚酸类、类黄酮类、香豆素类、木酚素类、芪类、醌类和单宁酸类[3-5]。酚酸类在植物中含量极为丰富,常见的有阿魏酸、香豆酸、没食子酸、咖啡酸和绿原酸以及芥子酸等。类黄酮类是人类日常膳食中含量最多的多酚类物质,如常见的儿茶素属于黄烷醇类、原花青素属于分子量相对较大的原花色素类多酚。单宁酸是一类由单体聚合而成的结构比较复杂的多聚体,分子结构上存在大量的羟基,可以与食物中的多糖、蛋白质和生物碱发生反应,影响食物品质[6-8]。食源多酚在食品领域中越来越受重视,其功能特性逐渐为人们所熟知[9]。
国内外学者将多酚作为一种添加剂加入淀粉中,利用多酚与淀粉分子之间的相互作用,改变淀粉分子的结构特征,使淀粉特性向人们期望的方向改变,达到改善淀粉类食品品质的目的[10]。何财安等[11]报道,苦荞多酚与两种淀粉的共糊化显著降低了淀粉的透明度和沉降体积,凝沉和老化速率加快,糊化温度和糊化焓显著下降,淀粉更易糊化。Xiao等[12-13]报道,茶多酚能抑制玉米淀粉、米粉和马铃薯淀粉的老化。胡柏等[14]报道,红米麸皮多酚的主要成分为原花青素,对α-淀粉酶、α-葡萄糖苷酶、麦芽糖酶、蔗糖酶活性均有抑制作用。Wokadala等[15]报道,直链淀粉可以包裹相对较小的客体分子形成左手单螺旋的V型结晶复合物,而对于那些比较大的多酚分子,大多数在直链淀粉外部通过氢键与其结合形成复合物[16]。有研究表明茶多酚与淀粉形成非共价复合物的主要作用力是氢键[17]。目前对茶多酚的研究较多,对其他多酚的研究相对较少。作者采用膳食中常见的7种多酚单体化合物,分别添加到高直链玉米淀粉和蜡质玉米淀粉中,通过测定多酚淀粉络合物的淀粉-碘结合力和粒径,以及淀粉-多酚复合物的红外(FT-TR)和X-射线衍射(XRD)分析来研究它们间的相互作用,为新型功能食品的开发奠定基础。
1 材料与方法
1.1 材料
高直链玉米淀粉(HACS)、蜡质玉米淀粉(WCS):上海权旺科技有限公司;原花青素(单聚体)、儿茶素、咖啡酸、单宁酸、没食子酸、绿原酸、阿魏酸:南京龙源天然多酚合成厂,纯度均大于96%。
1.2 仪器与设备
UV-752紫外可见分光光度计:上海菁华科技仪器有限公司;LGJ-10C型冷冻干燥机:北京四环科学仪器厂有限公司;X-Pert PRO X-射线衍射仪:荷兰PA Nalytical公司;BT-9300S型粒度分布仪:丹东百特仪器有限公司;WQF-510傅立叶变换红外光谱仪:北京北分瑞利分析仪器公司。
1.3 方法
1.3.1 食源多酚对玉米淀粉粒径的影响
将7种多酚按质量比2.1%(g/g)与淀粉混合(高直链玉米淀粉和蜡质玉米淀粉)制样,并做空白对照样品,将其配成1%淀粉溶液,置于室温,每隔5 min搅拌1次,30 min后测定粒度。
1.3.2 食源多酚对玉米淀粉与碘结合力的影响
根据柴艳伟[18]的方法并稍做改动,按照1.3.1的方法配制1%的淀粉乳溶液,沸水浴加热15 min,冷却至室温,在溶液中添加适量碘溶液(2%KI,0.2%I2),搅拌均匀,放置30 min后淀粉溶液显色,在680 nm处测定吸光度。
1.3.3 食源多酚与玉米淀粉复合物的红外分析
按照1.3.1的方法配制淀粉样品,准确称取12.00 g,溶于100 mL去离子水中,搅拌均匀,在水浴锅中(95 ℃)糊化20 min,冷冻干燥后制成透明的KBr压片,用傅立叶红外光谱仪进行定性分析[19]。
1.3.4 食源多酚与玉米淀粉复合物的X-射线衍射分析
分别配制含多酚2.1%的7种淀粉样品(包括高直链玉米淀粉和蜡质玉米淀粉)和不含多酚的空白样品,准确称取12.00 g,溶于100 mL去离子水中,搅拌均匀,分别对样品糊化30 min,取出冷却至室温,在冰箱中4 ℃放置7 d,然后在冰箱中(-20 ℃)预冻4 h,冷冻干燥,并用研钵研磨粉碎,过100目筛,样品放置在干燥皿中备用。将制备好的食源多酚与玉米淀粉复合物粉末进行X-射线衍射分析。
1.3.5 数据处理
试验数据采用Origin 9.0软件和Peakfit 4.5软件进行分析。
2 结果与讨论
2.1 食源多酚对玉米淀粉粒径的影响
如表1所示,在高直链玉米淀粉中分别添加7种食源多酚后,其D10、D50和D90均有所增加,其中单宁酸影响最明显;7种食源多酚均增加了淀粉的平均粒径,单宁酸和原花青素对其影响最为明显,说明多酚与高直链玉米淀粉发生了较强的相互作用。有研究表明,直链淀粉可以与许多物质发生相互作用,主要有两种方式:外来物质嵌入到直链淀粉内部,与之复合;外来配体插入到两条直链淀粉的螺旋之间,连接两条直链淀粉[20]。由于多酚分子上存在着大量羟基,为两者相互作用提供了条件,小分子的多酚,如儿茶素、咖啡酸、没食子酸、绿原酸和阿魏酸等,主要是通过氢键、范德华力和疏水相互作用等进入直链淀粉内部形成V型复合物;而大分子的原花青素和单宁酸进入直链淀粉内部的可能性不大,它们可能是通过非共价作用插入到两条直链淀粉的螺旋之间,连接两条直链淀粉,试验结果证明了这一推断,原花青素、单宁酸对D50和D90影响较为显著。
如表2所示,7种多酚对蜡质玉米淀粉的D10、D50和D90影响各不相同,除儿茶素和阿魏酸外,其他5种多酚均增加了淀粉的D10,绿原酸影响最大;咖啡酸和绿原酸减小了蜡质玉米淀粉的D50,且除单宁酸外,其他6种多酚均减小了蜡质玉米淀粉的D90;咖啡酸和绿原酸较为明显地减小了蜡质玉米淀粉的平均粒径,说明咖啡酸和绿原酸可以与支链淀粉分子发生相互作用,但是作用方式尚不明确。

表1 7种食源多酚对高直链玉米淀粉粒径的影响Table 1 Effects of 7 kinds of food-borne polyphenols on the particle size of high amylose corn starch μm
注:D10指颗粒粒径小于该直径的颗粒占10%;D50指颗粒粒径小于该直径的颗粒占50%;D90指颗粒粒径小于该直径的颗粒占90%,表2同。

表2 7种食源多酚对蜡质玉米淀粉粒径的影响Table 2 Effects of 7 kinds of food-borne polyphenols on the particle size of waxy corn starch μm
2.2 食源多酚对玉米淀粉与碘结合力的影响
淀粉可以与碘发生相互作用,支链淀粉与碘形成紫红色复合物,而直链淀粉与碘则形成蓝色复合物,故常用淀粉与碘复合物的比色法来测定淀粉中直链淀粉含量和鉴定直链淀粉纯度[21]。如图1所示,7种多酚与高直链玉米淀粉相互作用后,淀粉与碘结合力显著下降,其中,咖啡酸和阿魏酸影响最为显著,它们发生相互作用后,碘离子嵌入到直链淀粉螺旋内腔的数量显著减少,其中小分子的多酚(儿茶素、咖啡酸、没食子酸、绿原酸和阿魏酸)对其影响较为明显,进一步说明多酚有效阻止了直链淀粉与碘的结合,并且小分子的多酚可以进入直链淀粉螺旋内腔,这与粒径分析结果较为一致。

注:不同小写字母表示差异显著(P<0.05),图2同。图1 7种食源多酚对高直链玉米淀粉与碘结合力的影响Fig.1 Effects of 7 kinds of food-borne polyphenols on the iodine binding force of high amylose corn starch

图2 7种食源多酚对蜡质玉米淀粉与碘结合力的影响Fig.2 Effects of 7 kinds of food-borne polyphenols on the iodine binding force of waxy corn starch
如图2所示,除单宁酸外,其他6种多酚均显著减小了蜡质玉米淀粉与碘的结合力,其中咖啡酸和绿原酸影响比较显著。碘离子也可以与支链淀粉形成复合物,可能是由于7种多酚在氢键、范德华力、离子相互作用和疏水相互作用等作用力下,与支链淀粉的侧链结合在一起,从而阻止了碘离子与支链淀粉的结合。
2.3 食源多酚与玉米淀粉复合物红外分析
从图3可以看出,将添加了多酚的试验组与空白组进行比较,发现在波谱图中并没有新峰出现,说明高直链玉米淀粉与多酚发生相互作用后,并没有产生新的共价键,即淀粉与多酚是通过非共价相互作用(氢键)而连接到一起。据报道,淀粉在3 197~3 428 cm-1、3 515 cm-1处会出现吸收峰,并且当淀粉中羟基形成分子内或者分子间氢键时该波段向低波段平移,并且波形变得平滑[22-25]。高直链玉米淀粉分别添加食源多酚后, 在3 515 cm-1处有向低波段平移的趋势,阿魏酸、咖啡酸和绿源酸较为明显,说明食源多酚与直链淀粉或者支链淀粉形成分子内或者分子间氢键。

注:1—8分别为HACS、原花青素+HACS、儿茶素+HACS、咖啡酸+HACS、单宁酸+HACS、没食子酸+HACS、绿原酸+HACS、阿魏酸+HACS。图3 7种食源多酚与高直链玉米淀粉复合物红外分析Fig.3 Infrared analysis of complexes of 7 kinds of food-borne polyphenols and high amylose corn starch
从表3可以看出,几种食源多酚均明显减小了高直链玉米淀粉在1 162 cm-1波峰处的拟合面积,咖啡酸和阿魏酸影响最为明显;几种食源多酚均明显减小了高直链玉米淀粉在1 082 cm-1的波峰处的拟合面积,降低了淀粉的结晶度,咖啡酸、绿原酸和阿魏酸影响最为明显。

表3 7种食源多酚与高直链玉米淀粉复合物在λ1 000、λ1 082和λ1 162的峰拟合面积Table 3 Peak fitting area of complexes of 7 kinds of food-borne polyphenols and high amylose corn starch at λ1 000, λ1 082 and λ1 162
注:λ1 000、λ1 082和λ1 162分别代表在波数1 000、1 082和1 162 cm-1处的拟合面积,表4同。
从图4可以看出,蜡质玉米淀粉与多酚发生相互作用后,并没有产生新的共价键,即支链淀粉与多酚是通过非共价相互作用结合到一起。蜡质玉米淀粉分别添加一定比例的食源多酚后,在3 515 cm-1处的波峰向小波段平移了一小段距离,其中,咖啡酸、绿原酸和阿魏酸平移最为明显,说明这7种多酚可以与支链淀粉形成分子间氢键,咖啡酸、绿原酸和阿魏酸与其作用最强。

注:A—H分别为蜡质玉米淀粉(WCS)、原花青素+WCS、儿茶素+WCS、咖啡酸+WCS、单宁酸+WCS、没食子酸+WCS、绿原酸+WCS、阿魏酸+WCS。图4 7种食源多酚与蜡质玉米淀粉复合物红外分析Fig.4 Infrared analysis of complexes of 7 kinds of polyphenols and waxy corn starch
从表4可以看出,原花青素和阿魏酸均明显减小蜡质玉米淀粉在1 162 cm-1波峰处的拟合面积,原花青素和阿魏酸影响最为显著;7种食源多酚对蜡质玉米淀粉在1 082 cm-1的波峰有影响,儿茶素和阿魏酸显著减小了其波峰面积,说明它们减少了淀粉的结晶度,而单宁酸和原花青素增加了其结晶度;7种食源多酚对蜡质玉米淀粉在1 000 cm-1的波峰没有影响,说明食源多酚对淀粉的无定形区域没有影响。在7种多酚中,原花青素、单宁酸、阿魏酸和支链淀粉发生相互作用,但是作用程度很小。
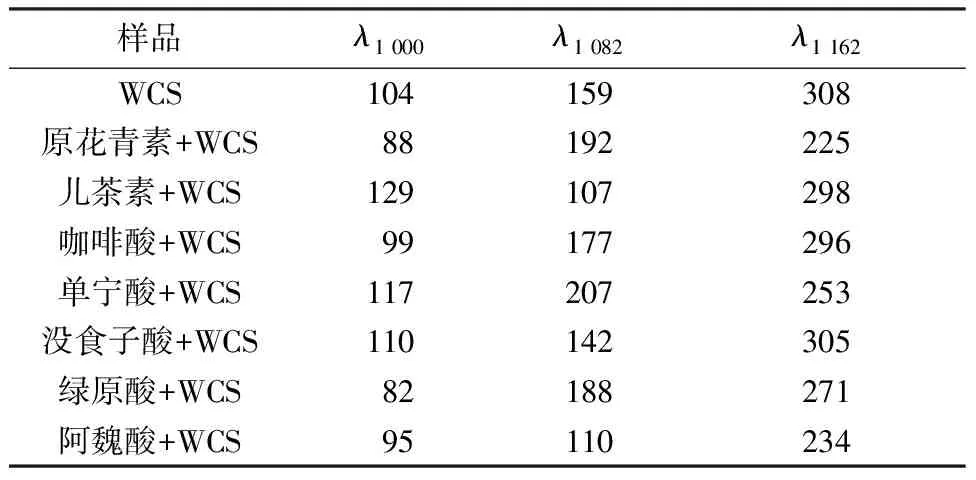
表4 7种食源多酚与蜡质玉米淀粉复合物在λ1 000、λ1 082和λ1 162的峰拟合面积Table 4 Peak fitting area of complexes of 7 kinds of food-borne polyphenols and waxy corn starch at λ1 000, λ 1 082 and λ 1 162
2.4 多酚-淀粉复合物的X-射线衍射分析
对高直链玉米淀粉与食源多酚的混合物进行XRD分析,如图5所示,空白组在17.1°处出现典型的B型结晶峰,说明高直链玉米淀粉经过7 d老化后具有B型结晶结构,与空白组相比,添加食源多酚的淀粉组特征峰较多,并出现了新的峰,具体如下:原花青素组出峰位置,17.1°、26.9°;儿茶素组出峰位置,7.3°、13.1°、17.1°、20.1°、26.9°;咖啡酸组出峰位置,7.3°、15.3°、17.1°、20.1°、26.3°;单宁酸组出峰位置,17.0°、32.4°;没食子酸组出峰位置,10.2°、13.1°、17.1°、20.1°、24.3°、32.4°;绿原酸组出峰位置,10.2°、13.1°、17.1°、20.1°、26.3°;阿魏酸组出峰位置,7.3°、10.2°、13.1°、17.1°、20.1°、26.3°、32.4°。
当淀粉与脂肪酸、碘以及其他物质结合形成V型结晶后,会在7.0°、13.1°及20.0°形成X-射线衍射特征峰[26]。结果表明,分别在7.0°、13.1°
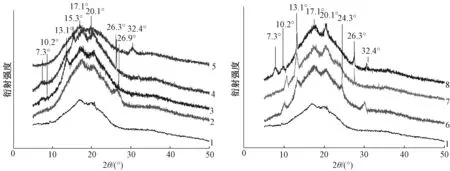
注:1—8分别为HACS、原花青素+HACS、儿茶素+HACS、咖啡酸+HACS、单宁酸+HACS、没食子酸+HACS、绿原酸+HACS、阿魏酸+HACS。图5 食源多酚-淀粉复合物(高直链玉米淀粉)的XRD图谱Fig.5 XRD patterns of food-borne polyphenol-high amylose corn starch complexes
及20.0°出现特征峰的有儿茶素、咖啡酸、没食子酸、绿原酸和阿魏酸,说明可以与高直链玉米淀粉形成V型结晶,而分子量相对较大的原花青素和单宁酸在这3处并没有出现特征峰,没有与淀粉形成V型结晶。这可能是因为分子量相对较小的食源多酚分子在非共价作用下,进入直链淀粉的螺旋内腔,从而形成了V型复合物。
如图6所示,蜡质玉米淀粉老化7 d后也呈现B型结晶结构,在分别添加7种多酚后,除阿魏酸外,其他6种多酚在7.0°、13.1°、20.0°均没有新峰出现。阿魏酸在13.1°出现了新峰,说明它可以与蜡质玉米淀粉形成V型结晶,这可能是因为阿魏酸在疏水、氢键等相互作用下进入支链淀粉的C链中从而形成了复合物。阿魏酸可以通过非共价作用与蜡质玉米淀粉形成V型复合物,而其他6种多酚则与淀粉形成不了V型复合物,这可能是由多酚分子的结构、羟基的数量及位置造成的。

注:A—H分别为WCS、原花青素+WCS、儿茶素+WCS、咖啡酸+WCS、单宁酸+WCS、没食子酸+WCS、绿原酸+WCS、阿魏酸+WCS。图6 食源多酚-淀粉复合物(蜡质玉米淀粉)的XRD图谱Fig.6 XRD patterns of food-borne polyphenol-waxy corn starch complexes
3 结论
7种食源多酚均增加了高直链玉米淀粉的平均粒径,单宁酸对其影响最为明显。多酚能够阻止淀粉与碘的结合,其中多酚对高直链淀粉作用更为显著,小分子的多酚可以进入到直链淀粉螺旋内腔。多酚与淀粉通过非共价相互作用结合,与直链淀粉或者支链淀粉形成分子内或者分子间氢键,其中阿魏酸、咖啡酸和绿原酸与直链淀粉作用最强,原花青素、单宁酸、阿魏酸和支链淀粉也发生相互作用,但作用程度较弱。除原花青素和单宁酸外,其他5种多酚均能与高直链玉米淀粉形成V型复合物,但能与蜡质玉米淀粉形成V型复合物的只有阿魏酸。
