不同直接抗病毒药物方案对基因1b型慢性丙型肝炎及代偿期丙型肝炎肝硬化临床结局的影响
2020-02-09侯艺辉刘腾飞赵晓青张缭云
侯艺辉,刘腾飞,赵晓青,张缭云
1 山西医科大学,太原 030001; 2 山西医科大学第一医院 感染病科,太原 030001
慢性丙型肝炎(CHC)是由一种HCV感染引起的慢性肝病,传播方式主要有血液或血制品、性接触及母婴传播[1]。CHC临床症状一般较轻微,常被患者忽视,导致病情被延误,进展为肝硬化和肝癌,严重威胁人类健康。直接抗病毒药物 (DAAs)的上市,使CHC治疗发生了划时代的改变,我国DAAs获批上市较晚,药物应用于临床时间短,临床数据有限,有些潜在不良反应尚未发现。本研究旨在观察不同DAAs联合方案对1b型HCV感染者及丙型肝炎代偿期肝硬化患者临床结局的影响,为后续抗病毒治疗提供参考。
1 资料与方法
1.1 研究对象 纳入2018年1月-2018年12月在山西医科大学第一医院感染科就诊的CHC患者及丙型肝炎代偿期肝硬化(compensatory liver cirrhosis,CLC)患者。纳入标准:(1)所有患者的诊断均符合《丙型肝炎防治指南(2015年更新版)》[2],即抗-HCV及HCV RNA 阳性;(2)HCV基因分型为1b型;(3)接受 DAAs 抗病毒治疗。排除标准:(1)DAAs治疗前确诊为失代偿期肝硬化、肝癌或合并有其他恶性肿瘤的患者;(2)有心脏疾病尤其是伴有心律失常并应用胺碘酮的患者;(3)半年内有干扰素治疗史;(4)同时应用与DAAs有相互作用并影响DAAs代谢的药物,例如抗结核药、抗癫痫药。该研究方案经由山西医科大学第一医院伦理委员会审批[批号:(2013)伦审字(62)号],患者均签署知情同意书。
1.2 DAAs方案选择原则 根据患者治疗前肝功能、肾功能及并发症所用药物,注意药物间相互作用(drug-drug interactions,DDIs)而选择相应抗病毒方案进行治疗。(1)DAAs方案:基于当时已获批DAAs药物的可选方案,1b型患者可选方案有索磷布韦联合维帕他韦(SOF+VEL),艾尔巴韦格拉瑞韦片(EBR+GZR),奥比帕利联合达塞布韦(OBV+DSV),索磷布韦联合达拉他韦(SOF+DCV),索磷布韦联合利巴韦林(SOF+RBV)方案;(2)肝功能:在肝功能正常或代偿期肝硬化患者中应用含蛋白酶抑制剂(proteasome inhibitor,PI)的药物,需密切监测ALT、TBil等指标变化,注意药物引起肝硬化失代偿风险;(3)肾功能:由于SOF及其主要代谢物通过肾脏代谢,肾功能不全时会引起血药浓度的改变,故对肾功能不全者,在慢性肾脏病4期、5期以及尿毒症患者中,避免使用含SOF的方案[3-4];(4)DDIs:对于因合并症同时用药的患者,查找HCV药物相互作用表,选用较合理的方案,因SOF与RBV均不经细胞色素P450酶类代谢,故SOF+RBV方案潜在DDIs风险较小;如合并用药复杂或病史、用药史不明确时,应谨慎使用OBV+DSV方案[5]。
根据上述方案选择原则,该研究共纳入基因1b型HCV感染者115例,其中CHC患者91例,28例采用SOF+VEL方案,21例采用EBR+GZR方案,16例采用OBV+DSV方案,13例采用SOF+DCV方案,13例采用SOF+RBV方案;CLC患者24例,15例采用SOF+VEL方案,4例采用EBR+GZR方案,5例采用SOF+DCV方案,(SOF+RBV方案疗程24周,其余方案疗程均为12周)。
1.3 观察指标 患者治疗前进行HCV基因分型(采用PCR-测序法,试剂购自中山大学达安基因股份有限公司,检测仪器:基因测序仪ABI3500-DX,性能指标:(1)检测范围5×103IU/ml~5×108IU/ml;(2)最低检出量:5×103IU/ml,按说明书操作)。收集入选患者治疗过程中血清 HCV RNA(采用实时荧光定量PCR法,试剂购自苏州天隆生物科技有限公司,检测下限50 IU/ml)、血常规、肝功能、甲胎蛋白、血脂血糖、肾功能等相关实验室检查结果。
1.4 疗效判断标准 主要疗效指标:超快速病毒学应答率(super rapid virological response,SRVR):抗病毒治疗1周HCV RNA不可测;快速病毒学应答率(rapid virological response,RVR):抗病毒治疗4周时HCV RNA不可测;完全早期病毒学应答(complete early virological response,cEVR):治疗第12周时HCV RNA不可测;持续病毒学应答率(sustained virological response,SVR):治疗结束后12周时HCV RNA不可测,表示为SVR12。次要疗效指标:ALT/AST复常率。
1.5 DAAs不良反应 询问并记录患者治疗过程中是否有头痛、腹泻、恶心呕吐等不良事件的发生,并详细记录其发生的频率和程度。
1.6 统计学方法 采用SPSS19.0软件进行统计分析,符合正态分布的计量资料以±s表示,2组间比较采用t检验;不符合正态分布的计量资料以M(P25~P75)表示。计数资料组间比较采用χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 一般资料 91例CHC患者中14例患者合并高血压(5例服用硝苯地平缓释片、7例服用苯磺酸左旋氨氯地平片、2例服用依那普利),1例患者合并轻度肾功能不全,1例患者合并产后抑郁症[同时服用喹硫平50 mg(1次/d)]和盐酸氟西汀分散片20 mg(1次/d),根据药理作用,之后减喹硫平至25 mg]。24例CLC患者中4例患者合并高血压(1例服用苯磺酸左旋氨氯地平片、1例服用依那普利、2例服用氢氯噻嗪片),3例患者合并轻度肾功能不全。115例患者基线特征见表1。
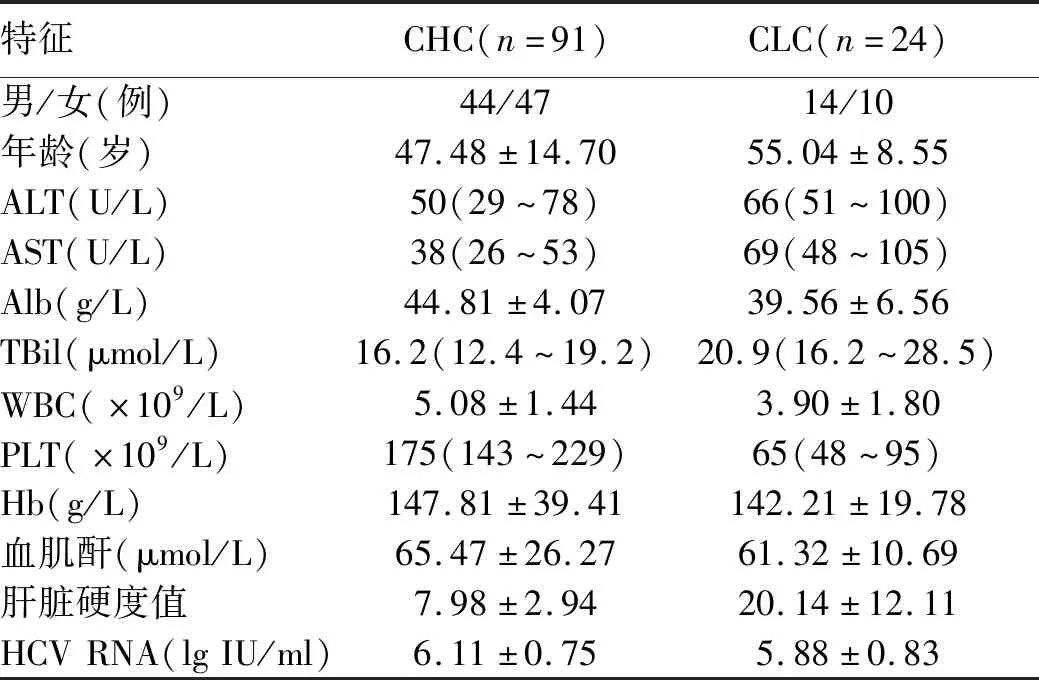
表1 患者基线特征
2.2 病毒学应答情况 115例患者无论HCV RNA的基线水平、采用何种DAAs抗病毒方案,总疗效为:在DAAs治疗1周时患者获得SRVR达90.4%,治疗4周时RVR率达98.2%,治疗12周时cEVR率达100%,治疗结束后12周SVR12达100%。不同抗病毒治疗方案在治疗1周及4周时HCV RNA阴转率差异均无统计学意义(P值均>0.05)(表2)。
2.3 生化学应答
2.3.1 DAAs治疗对肝功能的影响 115例患者经DAAs抗病毒治疗12周,109例(94.8%)肝功能指标恢复正常,未见有异常升高。不同抗病毒方案均可明显改善患者肝功能,不同抗病毒方案组间疗效差异无统计学意义(P值均>0.05)(表3) 。
进一步分析显示,对于使用较多的SOF+VEL抗病毒方案(CHC组28例,CLC组15例),2组患者治疗前后的肝功能(ALT)复常率分别为89.3%(25例)、80.0%(12例),差异无统计学意义(χ2=0.14,P>0.05)。
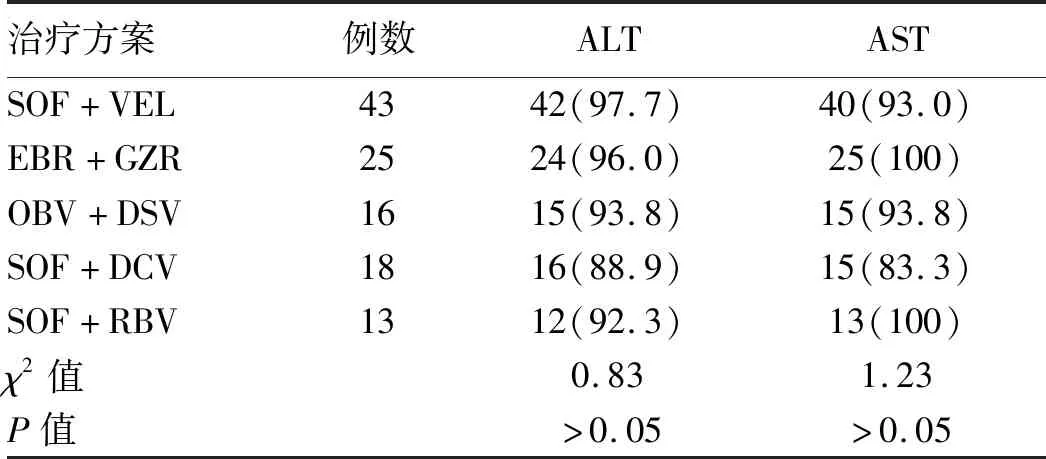
表3 不同抗病毒方案治疗12周肝功能复常率比较[例(%)]
对含PI方案的患者(n=37)治疗前后的肝功能水平进行统计,患者治疗前ALT为(73.19±24.44)U/L,AST为(45.48±15.36)U/L,治疗12周时ALT为(27.22±8.56)U/L,AST为(21.48±6.60)U/L,结果显示治疗前后ALT、AST差异均有统计学意义(t值分别为5.80、5.37,P值均<0.05)。
2.3.2 DAAs治疗对肾功能的影响 经DAAs抗病毒治疗12周,CHC患者血肌酐为(69.38±19.27)μmol/L,CLC患者血肌酐为(60.13±9.45)μmol/L,与治疗前相比未见有明显升高或降低,差异均无统计学意义(t值分别为1.32、0.56,P值均>0.05)。
2.4 DAAs治疗期间不良反应事件的发生情况 1例患者采用SOF+RBV治疗1个月时,因发生溶血而出现全身皮肤、巩膜黄染,后改用SOF+DCV;1例患者服用OBV+DSV时出现全身皮疹而改用EBR+GZR;其余不良反应轻微,出现2例恶心,1例头晕,1例心悸,所有患者没有因不良反应而退出治疗。
3 讨论
HCV感染影响了全世界1.3~1.5亿人,是肝硬化和肝癌的主要病因[6],抗病毒治疗清除HCV是治疗的关键措施[7]。自2017年DAAs在我国上市以来,口服抗病毒以其方便、副作用小、短疗程等优点,广泛应用。丙型肝炎基因分为6型[8],在我国,除4型外,其余基因型病毒感染均有分布,且有明显地域差异,全国感染HCV的基因型以1b型(56.8%)与2型(24.1%)为主,山西省丙型肝炎基因型分布与国内大致相同,以基因1b型为主[9]。
本研究结果显示,无论何种抗病毒方案,均可获得快速病毒学应答,其SRVR为76.9%~95.3%,SVR12均为100%。SOF+RBV疗程24周,虽然统计12周时HCV RNA已经阴转,但为了巩固疗效,患者仍按指南完成24周疗程,并计算其SVR12,与其他组别进行统计分析。此外,本研究结果与诸多相关真实世界研究[10-12]结果相符,例如来自我国香港地区一项94例基因1b型CHC患者应用SOF联合DCV方案的真实世界数据[12]显示,其SVR12达100%,并无严重不良事件发生。
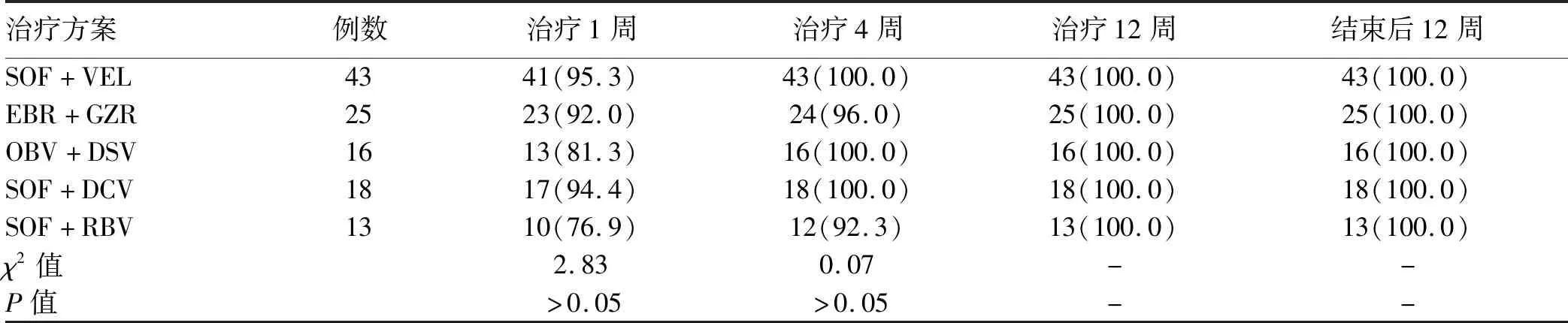
表2 不同抗病毒方案治疗1周、4周、12周及结束后12周时HCV RNA阴转率比较[例(%)]
注:“-”表示无相关数据。
丙型肝炎慢性化率高,很多未经抗病毒治疗的患者出现肝病进展甚至发生肝硬化或肝癌。许多患者除患丙型肝炎外,还同时患有其他疾病,导致用DAAs抗病毒治疗时合并用药的机会增加,DDIs发生风险增加。相关研究[5]指出,复合制剂发生DDIs的概率明显高于单药治疗;单药中,SOF发生DDIs的风险最低,而3D方案中包含P-gp和(或)细胞色素P450 3A4的酶底物及抑制剂,最易发生DDIs;其次是Daclatasvir以及Ledipasvir[13]。本研究中在治疗前充分评估DDIs,尽量规避已知的DDIs,治疗过程中未出现DDIs。
丙型肝炎治疗经常遇到的问题是药物对肝、肾功能的影响。个别DAAs会对肝、肾功能产生不同程度的影响[6,14],本研究分别分析了含PI方案和SOF方案的DAAs治疗前后肝肾功能指标的变化,结果显示DAAs抗HCV疗效显著,治疗后患者肝功能指标明显改善,也没有发生肝功能恶化的情况,而对患者肾功能指标的分析显示,DAAs治疗后对肾功能正常的患者无明显影响。
本研究结果显示,DAAs治疗过程中不良事件较少且轻微,但选择方案时应注意到PI对肝损伤的副作用、SOF对肾功能的要求以及DDIs,避免临床不良反应的发生,在此提醒医师在治疗过程中仍应给予更多的关注,尤其是发生需要改变原治疗方案的不良事件,如溶血等。
本研究所有患者均未发生病毒学或病情反弹,虽留取了患者治疗前的标本,因没有出现疗效不佳或复发患者,故均未做基线耐药监测。
综上所述,本研究根据患者病情、经济承受能力、个性化选择不同DAAs治疗方案,对基因1b型CHC及CLC患者的治疗均可获得满意的SVR,并且能显著改善患者肝功能,不良反应少且轻微、可逆。提示上述几种DAAs治疗在我国基因1b型CHC患者均可获得满意的病毒学应答及生化指标的改善。鉴于本文为随机对照试验研究,基于有限的样本量,结论仍需临床真实世界研究进一步验证。
