WO3(001)表面活性氧物种的理论研究
2019-12-06金华
金 华
(宜春学院 化学与生物工程学院,宜春 336000)
1 引 言
三氧化钨(WO3)是一种重要的n型多功能半导体材料,因具有独特的物理和化学性质而受到科研工作者们的关注,并广泛应用于电致/光致变色[1,2]、气体传感[3,4]、化学催化[5,6]等领域.尤其在传感器方面,大部分反应在材料的表面或界面进行,气体吸附质分子在WO3表面发生的氧化还原反应往往是传感器表面电信号变化的主导因素,而表面活性位点种类及其数量对于该氧化还原过程又起到关键的作用,并且会影响表面的传感性能.探究WO3表面可能存在的活性氧物种,将有助于加深对其气体传感和氧化性能及反应机理的理解,为研发和制备性能更加优越的三氧化钨基半导体材料有重要的理论指导意义.
目前对于WO3传感材料的应用研究不论在实验还是理论方面都有较多报道,Hübner等[7]人对不同氧分压条件下CO在WO3表面的传感机理进行了探究,指出CO与WO3表面氧原子直接作用,发生氧化还原反应形成表面缺陷是造成表面电导率增大的最可能原因;并且发现随着表面氧分压增大,缺陷表面又会被重新氧化导致表面电导率减小,且传感器电导率与表面氧缺陷的存在与否有较大关联.随后Ahsan[8]研究小组采用热蒸发法制备了Fe掺杂的WO3薄膜传感器,他们的实验研究进一步证实了Hübner等人的结论,即CO被WO3纳米表面氧化为CO2造成表面电导率的变化,并指出催化CO氧化的表面活性物种为O2-.近期,Zappa课题组[9]合成了一种新型的三氧化钨纳米线进行CO探测,他们将传感器电阻信号的变化归结于表面吸附的活性氧物种(O2-、O-或者O2-)的得失平衡.理论方面,Oison等[10]和Tian等人[11]分别采用第一性原理计算对WO3表面传感机理进行了探究,计算结果与实验结论一致,表面缺陷态的形成以及表面氧物种类型的变化是表面电导率变化的主导因素.
综上可知,作为一种表面控制型半导体材料,WO3表面存在多种活性位点,吸附在表面的氧物种很可能成为催化氧化反应的活性位,表面缺陷的存在对于表面活性位点数量及种类又有着显著影响.但是表面可能存在的活性氧物种有哪些,不同的氧物种在WO3表面催化氧化过程中是如何起作用的,以及表面缺陷对WO3表面活性位以及其催化氧化性能又有什么影响,这些重要问题目前尚未见报道,仍需要进一步研究.鉴于此,本文采用基于密度泛函理论的第一性原理结合周期性平板模型的方法,对WO3(001)表面可能存在的氧物种进行了系统的研究,通过计算O2分子在WO3(001)完整和缺陷表面吸附构型和电子性质的分析,确定可能存在的氧空位和氧物种,以期为深入认识WO3表面传感及催化氧化性能,寻求化学反应规律提供有益的理论支持.
2 计算细节
2.1 计算模型
以室温下最稳定单斜相γ-WO3作为基本的构造单元,创建了如图1所示的c(2×2)的WO3(001)完整表面,并采用周期性重复平板模型进行表面模拟.图中 W6f和W5f分别表示表层六配位和五配位的W原子,Ot表示表层单配位的O原子.经过能量收敛测试,选取平板厚度为5层,每层包含三个O-WO2-O原子层.构型优化和性质计算过程中,固定底部两层原子描述体相的性质,放开上面三层的原子描述表面反应特点.
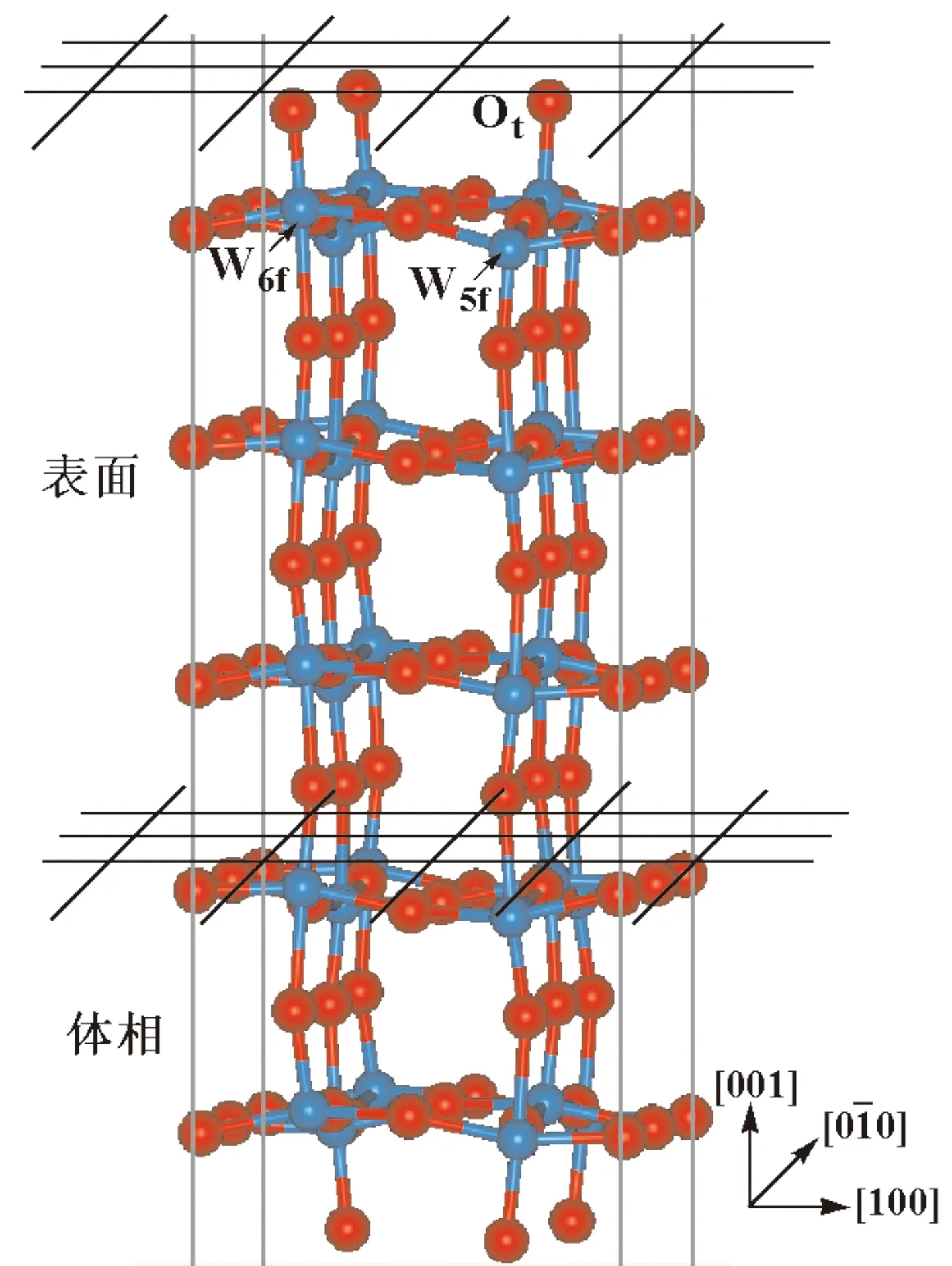
图1 WO3(001)完整表面结构图Fig. 1 Structure of perfect WO3(001) surface
2.2 计算方法
所有计算均采用基于密度泛函理论的VASP(Vienna ab initio simulation package)程序包[12-15]进行.电子-离子之间的相互作用采用超软赝势(US)[16,17]描述,电子交换关联势采用广义梯度近似法(GGA)的PW1[18]来描述.Kohn-Sham采用平面波基组展开,截止能设置为400eV.自洽场能量收敛标准为10-4eV,原子净余力小于0.03 eV/Å.布里渊区采用Monkhorst-Pack[19]方法对k点进行取样,k网格的大小设置为5×5×1.真空层厚度设置为10 Å,以消除平板间的相互作用.
对于吸附质O2在WO3(001)表面的吸附能(Eads)定义如下:
Eads=Eslab+EO2-Etotal
(1)
其中Etotal表示吸附后体系的总能量,Eslab和EO2分别表示O2吸附前WO3(001)清洁表面的能量和自由O2分子的能量.对于O2分子,基态为三重态.Eads越正表示吸附体系越稳定.
对于缺陷形成能(Evac)定义如下:
(2)
其中,Eperf和Edef分别表示完整和缺陷WO3(001)表面的能量,EO2为自由O2分子的能量,n代表表面缺失氧原子的数目,缺陷形成能Evac的值越负表示失去表面氧原子的体系越稳定.
3 结果与讨论
为了更好的探究WO3(001)表面可能存在的活性氧物种,首先对表面可能存在表面缺陷类型进行探讨,随后对O2分子在WO3(001)完整和缺陷表面的吸附行为展开讨论.
3.1 WO3(001)缺陷表面的结构和电子性质
实验中发现,在WO3晶体形成的过程中经常伴随着各种缺陷的存在,而且随着氧缺陷浓度的增加,半导体的WO3呈现金属性.由于反应一般在表面进行,本文仅考虑了表层端氧原子(Ot)缺失的缺陷型表面,包括两种缺陷类型,M1和M2,表面氧缺陷位置用Wv表示(见图2).其中M1表示表层半数端氧原子缺失的WO3(001)缺陷表面,M2表示表层所有端氧原子缺失的WO3(001)缺陷表面,即形成以WO2为终端的极性表面.图2为两种缺陷体系的构型图,仅给出了表面三个原子层的键长参数.为了更直观的比较氧缺陷前后表面几何结构变化情况,完整表面的相关数据在表中也一并标出.

图2 WO3(001)缺陷表面(左)俯视和(右)侧视图Fig. 2 Top (left) and side view (right) of (a) M1- and (b) M2-type WO3(001) defective surfaces


按式(2)得到了两种缺陷体系(M1和M2)的缺陷形成能分别为1.94 eV和2.34 eV.缺陷形成能为正值,表明表面缺陷态的形成为热力学非自发过程,尤其对于M2模型,表面失去全部Ot原子更加困难.本文在后续讨论O2分子在缺陷表面吸附行为的过程中,仅考虑M1构型.
表面端氧原子(Ot)的缺失对表面电子态也会造成较大的影响,图3为WO3(001)完整表面和M1缺陷表面的能带结构图.由图3 a可以看出,完整WO3表面的带隙虽然较小,但是仍然保留了体相的半导体性质.但当表面失去了部分Ot原子之后,费米能级处有能带占据,出现了新的电子态(即缺陷态),导致缺陷后体系呈现金属性.由此可以推论,当吸附质分子与完整表面的端氧原子(Ot)相互作用发生氧化还原反应之后,表面形成缺陷态,进而表面电导率增大,这与实验结果和其他理论结论一致.

图3 完整和M1型缺陷WO3(001)表面的能带结构图Fig. 3 Band structures of (a) perfect WO3(001) surface and (b) M1-type defective WO3(001) surface
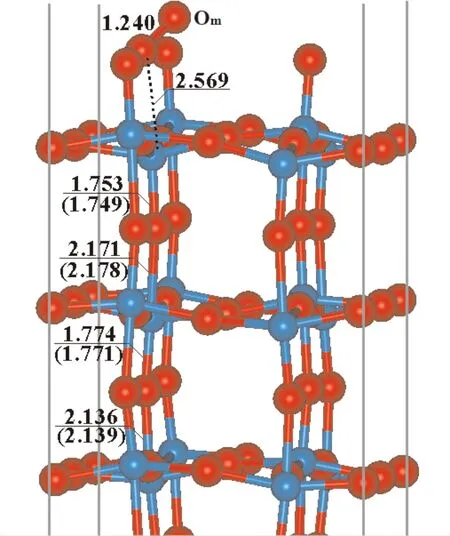
图4 O2在WO3(001)完整表面的吸附构型Fig. 4 Adsorption structure of O2 on the perfect WO3(001) surface
3.2 O2在WO3(001)完整表面的吸附及可能存在的活性氧物种
图4给出了优化后O2分子在WO3(001)完整表面吸附的最稳定构型,即O2分子与表层五配位的W原子(W5f)作用成键.相应的键长信息已在图中标出,括号内数据为完整表面的键长大小.由图中键长数据可知,距表面较近的氧气分子中的一个氧原子(Om)与表面的W5f原子之间键长为2.569 Å,较正常的W-O键(约为1.9 ~ 2.0 Å)要长,与此同时,吸附后氧气分子中的O-O键键长为1.240 Å,接近于O2自由分子的键长(1.237 Å).另外,O2吸附后表面上各个W-O键较未吸附的完整表面来说,键长变化较小(< 0.01 Å),说明O2在WO3(001)完整表面为一种弱的物理吸附作用.进一步计算显示该体系的吸附能仅为-0.419 eV,表明O2在WO3(001)完整表面的吸附为热力学非自发过程.上述结果说明WO3完整表面上吸附态的O2分子不易成为表面活性氧物种,则对于WO3(001)完整表面来说,表面活性氧物种仅有一种,即表面晶格氧(Ot),吸附质分子在表面形成物理吸附后,优先与表面Ot原子结合,进而完整表面转变为缺陷表面(M1),表面由半导体转变为导体,体系电导率增大.
3.3 O2在WO3(001)缺陷表面的吸附及可能存在的活性氧物种
对于O2在WO3(001)缺陷表面的吸附行为考察了五种可能构型,图5和表1分别给出了相应的优化构型、键长参数和吸附能数据.从各优化构型的吸附能可知,type1的吸附能最大,为1.11 eV,O2水平吸附在缺失了端氧的W原子(Wv)处.从图5 a中可以观察到来自O2分子中的两个O原子(Om)都与表面Wv原子成键,形成的W-O键长分别为1.923 Å和1.926 Å,接近体相W-O键水平.正是因为这两个原子的强相互作用,使得氧气分子中两个氧原子之间的成键(Om-Om)被削弱,吸附前后的O=O键长增加0.215 Å,由基态的1.237 Å变为吸附后的1.452 Å.Bader电荷布居分析结果显示,约有0.7e电子从表面转移到吸附的O2分子上,吸附在WO3(001)缺陷表面的O2分子被活化,形成了类似O2-的物种,该活性氧物种对于表面的催化氧化反应起到了非常重要的作用.另外,O2与Wv的作用也引起吸附位附近其他原子的电子转移以及W-O键长的较大变化,详见图5 a.

图5 O2分子在M1型WO3(001)缺陷表面的吸附构型Fig. 5 Various adsorption structures of O2 on the M1-type WO3(001) defective surface
对于type 2构型来说,即O2竖直吸附在缺失端氧的W原子处(图5 b),该构型与type 1的吸附位相同,只是吸附方式不同.而此吸附构型中的O=O较自由分子仅有0.04 Å的变化,其吸附能为0.45 eV,比type 2构型高出0.66 eV.由此可见,O2更倾向于缺失了端氧的钨原子成键,O2的两个原子都与缺失端氧的W作用得到的吸附构型更稳定. 当选取表层没有缺失端氧的W5f作为吸附位时,得到的吸附构型type 3和type 4均不稳定,吸附能为负值.对应的优化构型中形成的W-O键长也都大于2.0 Å(见图5 c和图5 d).
此外还考察了将O2放在两个相邻的五配位W原子之间的吸附情况,优化得到的吸附能为0.378 eV.由图5 e给出的键长数据可以看出,未缺失端氧的W5f处W-O键长为2.202 Å,而缺失端氧的Wv处W-O键长为1.914 Å;且该原子下方对应的W-O键长变化较大,均大于0.15 Å,而W5f处的W-O键长变化都小于0.05 Å.这表明O2更倾向于吸附在缺陷位置Wv.
综合上述分析可知,暴露在空气中的WO3(001)缺陷表面容易被空气中的O2氧化,导致表面电导率的降低.此时体系的活性氧物种除了表面晶格氧(Ot)以外,还有新氧物种O2-的生成,而且这种活化的O2-可能在WO3表面催化氧化过程中比晶格氧(Ot)表现出更加优越的氧化性能.
表1 O2在M1型WO3(001)缺陷表面吸附构型的吸附能
Table 1 Adsorption energy of O2on the M1-type WO3(001) defective surface

吸附类型type1type2type3type4type5吸附能(eV)1.110.45-0.63-0.600.38
4 结 论
通过第一性原理计算结合周期性重复平板模型的方法对WO3(001)完整和缺陷表面的结构、电子性质以及氧气分子在这两类表面上的吸附行为进行了详细研究.计算结果如下:
(1)考察了半数表面端氧原子(M1)和全部端氧原子(M2)缺失的WO3(001)缺陷表面,缺陷形成能的计算结果表明M1构型较M2构型更为稳定.
(2)O2在WO3(001)完整表面的吸附为弱物理吸附,且吸附态的O2不易成为表面催化氧化反应的活性物种.当吸附质在WO3完整表面上发生氧化反应时,优先与表面晶格氧Ot作用,费米能级处出现缺陷态,体系呈现金属性,电导率增大.
(3)O2在WO3(001)缺陷表面的吸附倾向于与表面缺陷位的Wv成键,氧气分子中的两个O原子均与Wv作用,形成O2-活性氧物种,吸附表面被氧化,电导率降低.
