睾丸去分化脂肪肉瘤1例报道并文献复习
2019-11-26彭洁王卫张仁亚崔文
彭洁,王卫,张仁亚,崔文
0 引言
去分化脂肪肉瘤(dedifferentiated liposarcoma,DDLPS)定义为非典型脂肪瘤样肿瘤/高分化脂肪肉瘤在原发或复发部位向各种组织学级别的非脂肪源性肉瘤转化的情况。10%的各种亚型高分化脂肪肉瘤,好发于中老年人肢体深部、腹膜后、睾丸旁区,一般病史较长,近期迅速生长,其特征是具有强侵袭性[1-3]。本文将结合文献对1例去分化脂肪肉瘤的临床病理学特征及免疫表型进行分析,旨在提高对其诊断水平。
1 临床资料
1.1 资料
患者,男,78岁,因“右腹股沟肿物待查”入院。该患者3月前发现右腹股沟处肿物,未进行任何治疗,自感肿物逐渐增大。体检:右侧腹股沟区可触及肿物,大小约3 cm×4 cm ×5 cm,质韧、活动期欠佳、无压痛、余体检未见明显异常。手术行右腹股沟肿物切除术+右侧单侧睾丸切除术+腹壁补片修补术,肿物全部切除并送病理检查。
1.2 方法
(1)标本常规制片;(2)苏木精-伊红染色法(HE染色法);(3)免疫组织化学(Immunohistochemistry,IHC),染色所用IHC抗体为迈新公司即用型抗体;(4)FISH技术。
病理检查:大体观:睾丸一个,大小7 cm×4 cm×3.5 cm,睾丸旁区见一肿物,大小3.8 cm×4 cm×5 cm,呈多结节状、切面灰白质稍韧,界不清。镜检:本例高分化成分约占肿瘤10%,去分化成分约占肿瘤90%,高分化成分呈脂肪瘤样脂肪肉瘤形态:具有分化好、近乎成熟的脂肪细胞,可见核大、深染、异型的脂肪母细胞(图1),去分化成分可见异型增生的梭形细胞排列成显著stori-form结构,梭形细胞可见核周空晕及病理性核分裂相(图2),少部分区域可见多形性肉瘤成分(图3),部分呈黏液纤维肉瘤形态(图4),另外,高级别成分与低级别成分由胶原纤维分隔开(图5)。免疫表型:P16(+)(图6)、CDK4(+)(图7)、CD34(-)、CD117(-)、Dog-1(-)、Vimentin(+)、SMA(-)、CD68(-)、Ki-67增殖指数约5%(图8),各免疫组织化学标志物在高、低分化区域无明显差异。FISH检测:MDM2基因扩增且在高、低分化区域无明显差异(图9)。
病理诊断:去分化脂肪肉瘤。
2 讨论
脂肪肉瘤(liposarcoma,LPS)是一种恶性间充质肿瘤,约占软组织肉瘤的20%[4],LPS最常见于四肢,但也可能涉及罕见部位,如胸部、颈部、腹膜后[5]和皮下组织。最新WHO脂肪肉瘤分类:非典型脂肪瘤(ALT)/良好分化的脂肪肉瘤(WDLS)、黏液样脂肪肉瘤、多形性脂肪肉瘤、去分化脂肪肉瘤(DDLS)和混合型脂肪肉瘤[6]。其中去分化脂肪肉瘤具有高度恶性,其复发和转移率高于其他类型[4,7],可以转移到腹膜后或肝脏、肺部和软组织部位,包括睾丸周围区域、背部和大腿[2]。本例高分化部分包括脂肪瘤样型:具有分化好、近乎成熟的脂肪细胞,可见核大、深染、异型的脂肪母细胞;炎性反应型:在脂肪瘤样型中出现淋巴细胞。去分化成分大多为不典型非脂肪源性肉瘤样形态:低级别黏液纤维肉瘤样;低度恶性纤维肉瘤样:轻度异型、束状排列的成纤维细胞,似高分化纤维肉瘤;少部分为多形性脂肪肉瘤样。

图1 去分化脂肪肉瘤呈梭形细胞脂肪肉瘤样Figure1 Dedifferentiated liposarcoma arranged as spindle cell liposarcoma

图2 去分化脂肪肉瘤呈低度恶性纤维肉瘤样Figure2 Dedifferentiated liposarcoma arranged as low-grade malignant fibrosarcoma
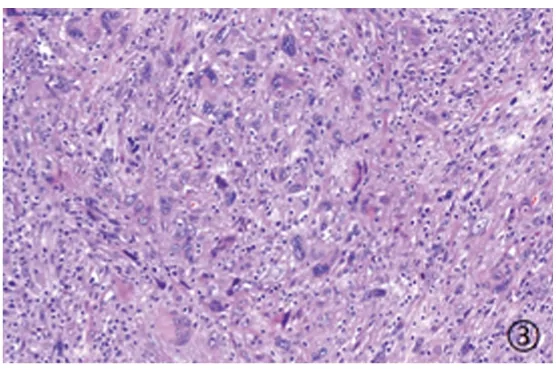
图3 去分化脂肪肉瘤呈多形性脂肪肉瘤样Figure3 Dedifferentiated liposarcoma arranged as polymorphic liposarcoma

图4 去分化脂肪肉瘤呈黏液纤维肉瘤样Figure4 Dedifferentiated liposarcoma arranged as mucinous fibrosarcoma
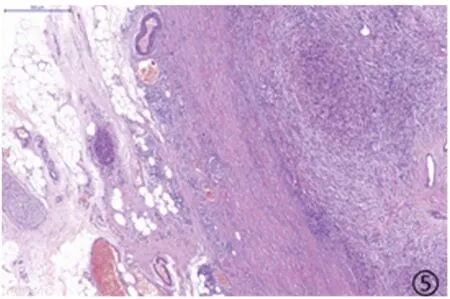
图5 高级别成分与低级别成分由胶原纤维分隔开Figure5 High-level and low-grade components were separated by collagen fibers
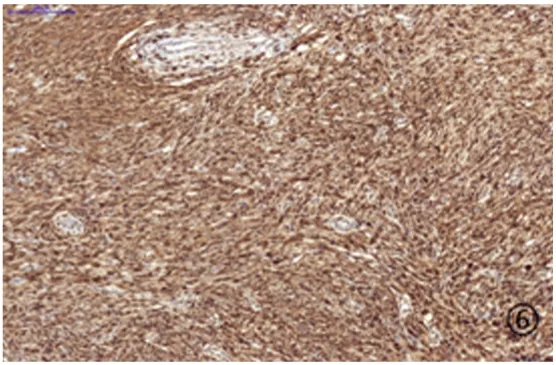
图6 免疫组织化学染色P16强阳性Figure6 Immunohistochemical staining showed P16 positive
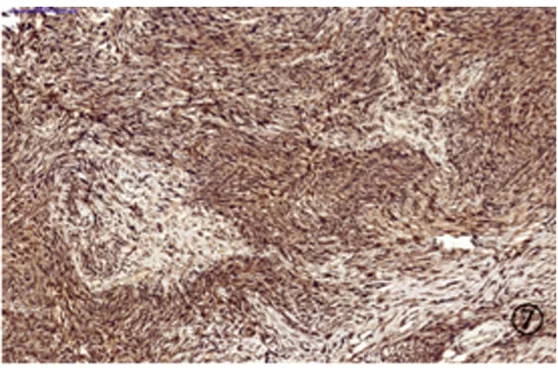
图7 免疫组织化学染色CDK4阳性Figure7 Immunohistochemical staining showed CDK4 positive
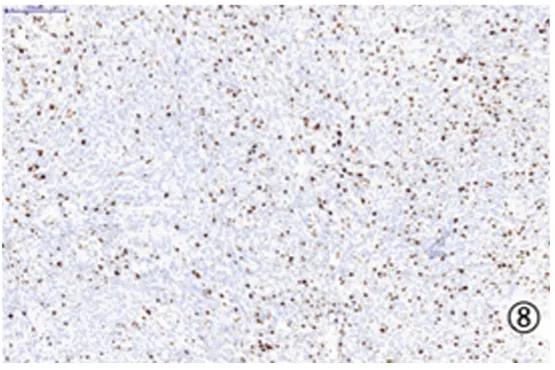
图8 免疫组织化学染色Ki67阳性Figure8 Immunohistochemical staining showed Ki67 positive

图9 FISH检测:红色信号显示MDM2基因簇状扩增,其中绿色信号为内参Figure9 FISH detection:red signal showed clustering of MDM2 gene,green signal was internal reference
DDLPS需与以下疾病进行鉴别:(1)梭形细胞脂肪瘤:常表现为单个无痛性结节,由梭形细胞及成熟脂肪细胞构成,没有脂肪母细胞,关键是无细胞核非典型性,有粗糙折光的胶原纤维,MDM2基因无扩增可与DDLPS鉴别。(2)平滑肌肉瘤:多见于老年人,常表现为单个或多个质硬结节。肿瘤由多形性梭形细胞构成,具有嗜酸性胞质和两端钝圆的细胞核,SMA、desmin阳性,MDM2阴性。(3)脂肪瘤:多呈叶状,有完整薄层纤维性包膜,瘤细胞主要为成熟的脂肪细胞,缺乏细胞核的异型性。(4)胃肠道间质瘤:好发于胃肠道,由梭形细胞和上皮样细胞构成,可有囊性变和坏死,免疫组织化学CD117、CD34和Dog-1阳性,可与DDLPS鉴别。
在遗传学上,DDLPS 12q13-15区域的基因扩增,包括MDM2、CDK4、DDIT3、HMGA2[8],并对其预后具有重要临床意义[9]。因CDK4特异性高、MDM2敏感度高,常联合使用CDK4和MDM2以提高诊断准确性。另外,DDIT3在33%的去分化脂肪肉瘤病例中得到了扩增,DDIT3过表达可能干扰脂肪细胞分化而诱导DDLPS形成[1]。
DDLPS具有复发率高的特点,切除边缘的根治性手术是主要的推荐治疗方法[10]。虽然手术切除是目前主要治疗方法,但对于复发或转移的DDLPS患者效果十分有限,现正在研究针对12号染色体基因产物的新型靶向治疗[2]。另外,在复发性DDLPS中,术前放射治疗可以将不可切除的肿瘤转变为可切除的形式[11]。另外,全血miRNA表达分析显示miR-3613-3p是DDLPS的潜在生物标志物[12]。miR-133a在DDLPS患者组织中显著下调从而导致机体代谢的转变,可能是DDLPS的潜在靶标。
DDLPS预后较差,具有位点依赖性,观察155例DDLPS患者发现,腹膜后DDLPS的预后明显差于其他部位的DDLPS[13]。目前,此患者已进行手术治疗,未进行术后放化疗,身体状况尚可。
