不同方法检测丹参多酚酸对血小板功能影响的比较
2019-11-04华晓东税凤春
华晓东,侯 娟,徐 琳,税凤春
(天津市药品检验研究院,天津 300070)
血小板功能检测最经典的方法是血小板聚集试验,由于该方法需要制备富血小板血浆(PRP)和贫血小板血浆(PPP),影响因素较多,试验者的操作经验对结果的影响较大,因此试验的可靠性较差。CD62p又名血小板活化依赖性颗粒表面膜蛋白,是血小板活化的特异性生物标志物。降低血小板的CD62p表达是临床活血化瘀方剂抗血小板治疗效果监测的高特异性指标,与其临床效应密切相关。采用流式细胞术检测CD62p的表达,进而评价血小板的功能[1],方法快速稳定,简单可靠,影响因素少,灵敏度也高于血小板聚集试验。本研究拟通过比较这两种血小板功能的评价方法,为在临床前研究中综合评价血小板功能提供一种新途径。
1 材料与方法
1.1药品 注射用丹参多酚酸:浅棕色疏松块状物, 规格:100 mg/支,批号20180501,试验时分别采用氯化钠注射液按丹参多酚酸含量计算稀释至试验所需浓度备用。单抗 anti-mouse/rat CD62p-PE/Cy7(藻红蛋白-青花素7标记的抗大/小鼠CD62p抗体,批号B223759)、anti-mouse/rat CD61-PE(藻红蛋白标记的抗大/小鼠CD61抗体,批号B216420),均由美国Biolegend公司生产;同型对照 Rat IgG2a-PE/Cy7(藻红蛋白-青花素7标记的大鼠IgG2a,批号4290714)、Rat IgG-PE(藻红蛋白标记的大鼠IgG,批号 4281135),美国eBioscience公司生产。ADP(批号SLBP6247V,SIGMA公司生产)。
1.2仪器 ACEA流式细胞仪,ACEA Bioscience,Inc;LBY-NJ4血小板聚集仪,北京生化仪器厂生产;XS-205DU电子天平,精度0.1 mg,试剂称量用;XP2001S电子天平,精度1 g,动物称量用。
1.3动物 SD大鼠,体重 220~250 g,雌雄各半,雌鼠应无孕,斯贝福(北京)生物技术有限公司,SCXK(京)2016-0002。
1.4方法
1.4.1注射用丹参多酚酸对大鼠体外血小板聚集功能的影响 取SD大鼠8只,雌雄各半,体重230~250 g,大鼠腹腔注射20%乌拉坦5 ml/kg麻醉。以注射器自大鼠腹主动脉采血,每只约5~6 ml,置硅化离心管中,以3.2%柠檬酸钠溶液9∶1抗凝,1 000 r/min离心5 min,制成富血小板血浆(PRP),以2 000 r/min离心10 min,制成贫血小板血浆(PPP),按比浊法采用血小板聚集仪测定血小板的最大聚集率。注射用丹参多酚酸配制成不同浓度(4、1、0.4、0.1和0.04 mg/ml),将对照管取0.18 ml PPP加入0.02 ml氯化钠注射液校正100%透过率值,每个测定管取0.18 ml PRP加入0.02 ml氯化钠注射液(基础值)或不同浓度的药液,预先将测定管在血小板聚集仪中温育5 min,再加入 200 μmol ADP溶液10 μl(终浓度为10 μmol/ml),随即记录5 min内血小板最大聚集率,对照组与各给药组平行检测。以各组的血小板最大聚集率进行组间比较(t测验),并计算出血小板聚集抑制率。采用SPSS 21.0进行统计,受试物作用前后进行配对资料的t检验。血小板聚集抑制率(%)=(对照组聚集率-给药组聚集率)/对照组聚集率。
1.4.2注射用丹参多酚酸对大鼠体外血小板活化的影响 上述大鼠麻醉后眼眶取血0.5 ml,以3.2%柠檬酸钠溶液9∶1抗凝。每只动物取1份50 μl抗凝血加入氯化钠注射液50 μl,37 ℃作用5 min,加入50 μl终浓度为10 μmol的ADP激活,用于测定经ADP激活血小板活化率基础值;另分别取50 μl抗凝血加入不同浓度(4、1、0.4、0.1和0.04 mg/ml)的丹参多酚酸溶液50 μl,37 ℃作用5 min,再用终浓度为10 μmol的ADP激活。上述2种抗凝血分别加入CD62p PE/Cy7和CD61 PE各1.0~1.5 μl双标,以CD61标记所有血小板,CD62p标记活化血小板。以上各管4 ℃避光孵育20 min;再加入0.5 ml 4%多聚甲醛固定10 min。取固定后的血样50 μl,加入1 ml稀释液稀释后上机分析。在CD61 PE/侧向角光散射(SSC)双参数散点图中划定血小板细胞群,计数5 000个血小板,进一步在CD61/CD62p散点图中计数CD61及CD62p阳性表达的细胞数,并以CD62p阳性表达率占CD61表达率的百分比反映血小板的活化率(%)。处理后上机检测与受试物作用后经ADP激活的血小板活化率。并采用SPSS 21.0进行统计,受试物作用前后进行配对资料的t检验。
2 结果
2.1对大鼠体外血小板聚集功能的影响 在采用血小板聚集仪进行的血小板聚集检测中,0.4 mg/ml以上的丹参多酚酸能够明显抑制血小板的聚集作用。而0.1 mg/ml剂量已无明显的血小板聚集抑制作用。由于每只动物的采血量不足以支持全部的检测样本,因此未进行0.1 mg/ml以下剂量的检测。见表1。

表1 注射用丹参多酚酸对大鼠体外血小板聚集作用的影响
2.2对大鼠体外血小板活化的影响 在采用流式细胞仪进行的血小板活化检测中,0.04 mg/ml以上的丹参多酚酸均可明显抑制CD62p的表达,对血小板表现出明显的活化抑制作用。见表2。
2.3方法一致性的比较 不同浓度药物对血小板聚集抑制率与血小板活化抑制率的相关分析,给药后不同浓度药物对血小板聚集抑制率与血小板膜糖蛋白CD62p活化抑制率均成正相关,按抑制率计算,两种方法的相关性为0.982。表明两种方法有较好的一致性,而血小板活化检测的灵敏度明显高于聚集率检测。见图 1 。

表2 注射用丹参多酚酸对大鼠体外血小板活化作用的影响
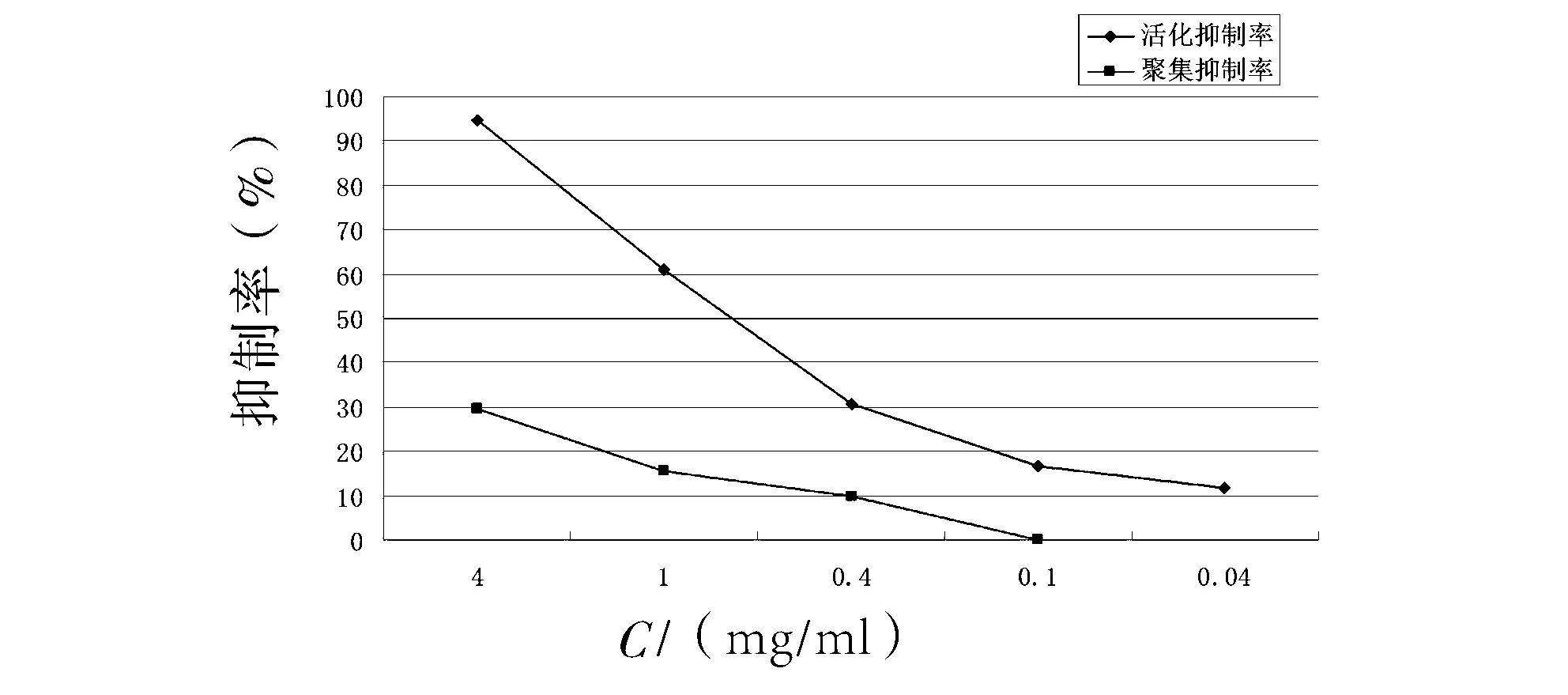
图1 丹参多酚酸对血小板活化抑制率和聚集抑制率影响的比较
3 讨论
心肌梗死、脑栓塞和肺栓塞等血栓性疾病在我国发病率很高,活血化瘀是主要的治疗手段,活血化瘀药物应用非常广泛。而评价活血化瘀药物功效的主要手段就是检测药物对血小板功能的影响。血小板活化、血小板聚集是血栓形成的病理基础,也是评价血小板功能的最重要指标[2]。
血小板功能的传统检测方法为比浊法检测血小板聚集,即采用血小板聚集仪测定血小板聚集情况的经典方法,该方法应用广泛,是目前较为经典的血小板功能检测方法,但该方法也存在一些固有的不足。例如去除红细胞不能完全反映体内血细胞之间的相互作用;如测定时间较长,可致血小板功能降低;需要制备的富血小板血浆(PRP)和贫血小板血浆(PPP)没有严格规范化标准,影响因素较多,个人操作习惯对结果影响较大,结果的稳定性和可重复性较差。需要较多的血液量,不适合用于高通量筛选。
CD62p(P-选择素,GMP-140)又名血小板活化依赖性颗粒表面膜蛋白或P-选择素,是一种膜糖蛋白颗粒,在静息血小板中仅分布在血小板内部, 当血小板被激活时, 随着血小板脱颗粒与释放反应, CD62p 重新分布至血小板膜表面, 且其只能在脱颗粒的血小板表面表达。由于只在已活化的血小板上有表达,其表达程度与血小板活化有很强的相关性,因而CD62p被认为是血小板活化检测的高特异性指标,与药物的临床效应密切相关。临床研究显示在冠心病的不同类型患者(稳定型心绞痛及急性冠脉综合征)中均观察到 CD62p 显著升高的现象, 即血小板的异常活化;同时CD62p水平与冠心病血瘀证呈正相关,因此降低血小板的 CD62p 表达也成为临床活血化瘀方剂抗血小板治疗的重要监测指标之一[3,4]。
采用流式细胞术检测血小板活化时血小板表面糖蛋白CD62p的表达,只需取少量外周血,经单克隆抗体标记后就可快速、稳定地检测。随着流式细胞仪检测手段的完善,其检测的敏感性和特异性也大大提高。因此,完全可以通过建立一种相对简单的流式细胞仪检测外周血中CD62p含量或百分率的模型,达到检测抗血小板活化类活血化瘀药物生物活性的目的。即将一定量的受试物(注射用丹参多酚酸)与大鼠抗凝血混合,作用一定时间后,用流式细胞术检测生物标志物(CD62p)的方法,测定并比较给药前后经ADP激活的血小板活化率,判定该受试物是否对ADP诱导的血小板活化具有抑制作用,从而评价药物是否具有活血化瘀作用。与传统血小板聚集测定法相比[5,6],全血法流式细胞术(FCM)有许多明显优点,采用全血进行检测,标本处理的简化能避免血小板体外激活,并防止血小板影响因子的丢失,不干扰循环中的红细胞、白细胞对血小板活化的影响,因此能在最接近真实体内环境的条件下测定血小板功能;由于使用了血小板生物标志物(单抗),检测的仅是血小板,而不会受其他种类细胞或碎片的干扰,保证了检测的特异性;检测仅需极少量全血,一次取血可进行多批样品检测,可减少动物用量,符合动物伦理;检测速度快,在接收样品后24 h内即可同时完成多批样品的检测;操作简单,影响因素较少,同时灵敏度高,方法稳定可靠,尤其适合进行大量样品的筛选。
注射用丹参多酚酸是一种新型的中药注射剂,具有明确的活血化瘀功效。在本研究中,不同剂量的丹参多酚酸可以明显地抑制ADP诱导的血小板活化和血小板聚集,而且采用流式细胞仪进行的血小板活化检测的灵敏度明显高于采用比浊法进行的血小板聚集检测。由于血小板活化是血小板聚集的必经步骤,二者的检测结果有很好的正相关性,而血小板活化检测的诸多优点提示该方法可以作为血小板聚集检测的替代方法用于血小板的功能评价。
中药成分复杂,单一地通过理化检测控制少数指标性成分难以全面控制药物的安全性和有效性,因此利用生物活性测定法对于中药进行质量控制已是一种必然的趋势。相较于影响因素较多的整体试验,通过选择一种公认的、特异性良好的生物标记物作为检测指标来反映药物的生物活性,能够从作用机制角度更好地体现其有效性,检测指标更易量化,也更适合作为质量标准引入具体品种项下。
