用数字传感器测定混合碱中碳酸钠的含量
2019-10-10陈大为
陈大为

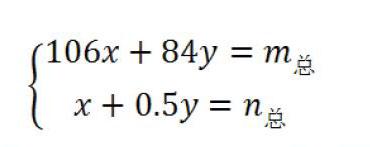

摘 要 碳酸钠与碳酸氢钠混合物的测定有多种方法,其中滴定法的误差较小。为了进一步缩小误差,简化滴定过程,提高滴定过程中的精确度,在实验中引入数字传感器,详细介绍在实验过程中使用传感器的方法。最后分析此实验引入传感器的优缺点。
关键词 化学;滴定实验;数字实验系统;pH传感器;滴数传感
器;数字采集器;碳酸钠;碳酸氢钠
中图分类号:G633.8 文献标识码:B
文章编号:1671-489X(2019)03-0124-03
1 实验背景
碳酸钠与碳酸氢钠混合物的测定的相关内容位于上海科学技术出版社出版的高三《化学拓展型课程(试用本)》“定量实验”一节[1]。在书中介绍的课堂实验是“测定含有少量氯化钠的碳酸钠的含量”,而学生实验则是“测定含有氯化钠杂质的碳酸氢钠的含量”。测定碳酸钠与碳酸氢钠混合物含量的实验虽然在教材中没有直接体现,但是这个实验可以作为上述二者实验练习的一种延伸,帮助学生强化学习三种混合物的定量测定方法——滴定法、沉淀法和热重法。其中滴定法操作简单,耗时较短,且在相同条件下相比于其他方法,误差较小。因此,选择滴定法测定混合碱的含量最为合理。
然而传统滴定法中也存在一些缺陷,如学生操作不熟练、不规范,对滴定管读数、指示剂颜色判断会有偏差,对滴定管液体“悬而不落”的现象不进行校正。这些偏常操作都会造成实验结果不准确。如何改进实验,避免读数带来的误差,是迫切需要解决的问题。本文介绍如何使用数字传感器和数字采集器对滴定实验进行优化和改造。
2 实验原理
数字实验的基本组成部分 在本实验中将使用各类传感器组成一套简单的数字实验系统,各种功能不同的数字传感器会收集到实验仪器中各项指标的变化,并将其转化为电信号传输到数据采集器中,采集器将收集、归纳数据,并转化为直观图像呈现在屏幕上。根据功能不同,传感器有许多类型,如氧气传感器、电导率传感器、pH传感器、滴数传感器等,这些传感器在测定实验中产生的各个变量的变化时起到关键性作用。在本实验中,运用到滴数传感器和pH传感器,数据采集器会采集实验过程中二者收集到的数据,并绘制成一张曲线图。
本实验的反应原理 在碳酸钠和碳酸氢钠的混合溶液中滴加硫酸至反应完全后,计算硫酸消耗的体积,通过一元二次方程组进行求解,即可得出碳酸钠与碳酸氢钠混合物的含量。在碳酸钠和碳酸氢钠的混合溶液中滴加稀硫酸,先发生的离子反应是:
即第一阶段,溶液的pH值会缓慢下降,至第一化学计量点pH=8.3,此时溶液中全部为碳酸氢钠。继续加入硫酸,发生的离子反应为:
此时溶液的pH迅速下降,理论上在反应结束时,溶液中只存在硫酸钠,二氧化碳会逸出,溶液呈中性,pH=7为滴定终点。但实际上二氧化碳会溶解在溶液中,导致溶液提前呈酸性,若将此时定为滴定终点,可能有一部分碳酸氢钠没有反应完,溶液中形成(NaHCO3—H2CO3)二元体系,使溶液可能呈中性。因此,此时需要继续滴加稀硫酸。
随着稀硫酸的不断加入,溶液的pH先呈现缓慢下降趋势,在第二化学计量点pH=3.89时,再一次迅速下降,二氧化碳逸出。这是因为随着溶液酸性的增强:
②式的平衡不断逆向移动,使c(H2CO3)增大,导致①式也逆向移动,二氧化碳逸出,达到滴定的终点。在实际操作中,也观察到溶液呈酸性时,产生气泡的速率明显加快。
综上所述,在本实验中借助pH传感器和滴数传感器,当pH传感器测定溶液的pH为3.89及以下时,停止滴定,读取滴数传感器测量得到的溶液体积,即可对混合物含量进行测定,计算方法如下。
设混合物中碳酸钠为xmol,碳酸氢钠为ymol。根据反应方程式:
可列出一元二次方程组:
其中,m总为混合物的总质量,n总为消耗稀硫酸的总体积。
n总=c(稀硫酸)×V(滴数传感器读取体积)×稀释放大倍数
本实验中配制了250 mL的混合碱溶液,取出10 mL,稀释至100 mL进行滴定,因此放大倍数为25。进一步解得x,即可计算碳酸钠的质量,从而得出碳酸钠在混合碱中的质量分数。
3 实验仪器和试剂
配制溶液阶段需要的实验仪器:250 mL容量瓶2个,烧杯2个,玻璃棒2根,胶头滴管2个,10 mL量筒1个,电子天平,蒸馏水洗瓶。
滴定阶段需要的实验仪器:数据采集器、滴数传感器、pH传感器、500 mL烧杯(反应容器)、250 mL烧杯(调试用)、洗瓶、磁力搅拌站、10.00 mL移液管(2支)、洗耳球。其中,数据采集器、滴数传感器、pH传感器、磁力搅拌站均为Vernier公司生产,数据采集器型号为LabQuest?2-LE,滴数传感器型号为VDC-BTD,pH传感器型号为FPH-BTA。
实验试剂:碳酸钠固体(AR)、碳酸氢钠固体(AR)、浓硫酸、蒸馏水。
实验装置如图1所示。
4 实验步骤
实验溶液的配制
1)0.5 mol/L稀硫酸的配制。量取6.7 mL浓硫酸注入水中,待冷却至室温后,转移至250 mL溶液瓶中;并洗涤烧杯和玻璃棒3~4次,将洗涤液也注入容量瓶中,定容至250 mL,摇匀,贴好标签备用。
2)稱取混合碱的总质量,记录m总。
3)混合碱溶于水中,不断搅拌,至完全溶解后,转移至250 mL容量瓶中;并洗涤烧杯和玻璃棒3~4次,将洗涤液也注入容量瓶中,定容至250 mL,摇匀,贴好标签备用。
4)用配制好的稀硫酸对塑料滴定管(滴数传感器附件)进行润洗。用配制好的混合碱对移液管进行润洗。
滴定过程
1)稀硫酸的标定。取配制好的稀硫酸溶液10 mL,加入2~3滴甲基橙,用标准碳酸钠溶液进行标定。
2)滴数传感器的校正。根据数据采集器预设的操作步骤,校正滴数传感器每滴滴出液体的体积,在本实验中校正值为23.10滴/毫升。具体操作:用10.00 mL移液管向塑料滴定管中注入10.00 mL标定好的硫酸溶液,打开数据采集器的校准界面,逐滴放完10.00 mL溶液,采集器会自动记录滴数;输入准确的溶液体积值之后,采集器会自动计算每毫升溶液的滴数,即完成校准过程。
3)pH传感器的校正。用pH=4.00的缓冲溶液对pH传感器进行校正,并使用蒸馏水对pH传感器进行归零;用滤纸擦干表面溶液后,放置待用。
4)滴定过程。用配制完成的混合碱溶液对移液管进行润洗,然后用移液管吸取10.00 mL混合碱溶液,加水稀释至100 mL左右。本实验中加水稀释量对实验结果没有影响,加水的量根据磁力搅拌子和pH传感器的位置来定,以磁力搅拌子不会撞击到pH传感器且能形成小的涡流为宜。
用稀硫酸润洗塑料滴定管并注入一定量的硫酸,由于滴数传感器可以直接记录消耗溶液的体积,因此无须记录初读数和末读数。缓慢打开塑料滴定管的活塞,使硫酸逐滴滴下,检查滴数传感器是否正常工作。
将稀释后的混合液放在磁力搅拌站上,打开调速器至7档左右,然后按下数据采集器的“开始采集”按钮;缓慢旋开塑料滴定管的活塞,目测使稀硫酸下落的速率基本为1滴/秒。观察数据采集器采集的体积-pH变化图。
待溶液pH下降至3.89及以下时,关闭活塞,按下“停止采集”按钮。读取数据采集器采集的数据,选择溶液pH接近3.89的体积值。在实际操作中,取数原则为向下取,即选择pH值≤3.89时的体积数据,记录在数据表中。
平行实验三次,取平均值,进行计算。若某一次的数据出现偏常,则需要在数据采集器上按“放弃记录”,以删除偏常数据。
5 数据记录和处理
在本实验中,数据记录和图像的生成都由数据采集器自动完成,表1为某一次实验中记录的数据表。
当有液体经过滴数传感器的红外感应门后,传感器就会记录一次pH和体积的数据,并在图像上绘制一个点。图2是某次实验结束后,所有数据绘制成的曲线图,其中纵坐标为pH值,横坐标为体积。在选择数据时,选择(3.85,6.821)
的点,即pH=3.85,此时消耗硫酸6.821 mL,即V(滴数传感器读取体积)=6.821 mL。根据图像的变化,证明本文中实验原理的解释是正确的。
6 注意事项
滴数传感器使用注意事项 使用滴数传感器之前,一定要进行体积的校准,否则会带来较大的误差。
稀硫酸的滴速一定要慢,保证滴数传感器能逐滴感应到每一滴液体的滴落,使溶液体积更准确。由于本实验不存在等待指示剂30 s不褪色的情况,因此,滴速慢可以保证反应的充分进行,且更容易捕捉到滴定突跃时溶液pH值接近3.89的数据点;若滴落速度过快,则会导致滴定突跃时pH值剧烈变化,难以捕捉终点。观察每一组之间消耗硫酸的体积,若体积读数偏差太大,则舍弃数据。
pH传感器使用注意事项 若pH传感器记录的pH值发生波动,在图像上呈现“锯齿状”时,暂停滴定,待pH值稳定后滴定。
不可将pH传感器做玻璃棒搅拌使用,pH传感器每次转移前都要用滤纸擦干表面的溶液,防止形成误差。
实验过程中的注意事项 磁力搅拌的速度不可过大,否则会导致溶液飞溅,黏附在烧杯壁上。在滴定过程中也需要不断用蒸馏水将烧杯壁上的液滴冲入溶液中。
一定要先按“开始采集”,再进行滴定,否则滴入的液滴不会被采集到,使得实验数据不准确。
7 本实验的优缺点与意义
本实验的优点
1)相比传统滴定法,在滴定读数和终点判断上更精准。传统滴定法的精准体现在两处:第一处是在终点时对指示剂颜色进行判定;第二处是读取滴定管的初读数和末读数。由于滴定时只使用了少量溶液,一旦出现误差,呈现在结果中将被放大很多倍。减小误差的方法是反复练习,熟悉操作,減少在操作和读数上带来的误差。但是由于高二学生刚接触滴定实验,无法像化学教师一样熟练进行,难免会出现滴定过量,指示剂颜色判断不准确的情况。因此,引入数字实验的好处在于可以消除由学生操作不熟练带来的误差,实验者可以直接通过传感器传输到采集器的数据进行摘录和分析。因此,对传感器的校正是非常重要的,只有传感器校正后,才能减小误差。
与此同时,滴数传感器可以保留三位小数,读数上比滴定管更加准确。pH传感器的读数可以保留两位小数,且有具体数值,相比酸碱指示剂没有滞后性。
2)滴定过程更加轻松,实验时间更短。传统滴定法操作过程要求实验者必须全神贯注,手眼联动,眼睛注视锥形瓶颜色变化,手部转动锥形瓶和控制滴定管的活塞。实验者一旦分心,就会导致实验出现误差。运用数字化传感器可以实现实验过程的自动化,滴定和体积的读取由滴数传感器完成,全程数据记录,即便滴定过量也无须重新实验。因此,实验者无须全程保持紧张,有助于降低实验过程中出现误操作的概率。
本实验的缺点
1)降低了学生的操作体验。正如上文所述,滴定过程由各式仪器自动化完成,降低了学生对滴定的操作体验,不利于学生对滴定过程的理解。
2)弱化了学生的实验观察能力。由于滴定终点是依靠pH传感器读数来判断的,因此不需要学生通过观察指示剂的颜色变化来判断终点。这样一来,虽然操作变得简单,但不利于培养学生的实验观察能力。
3)传感器存在不稳定性。传感器在每次实验前都需要进行调试,否则会导致每一组平行实验的误差很大,在无形中使实验变得烦琐。另外,传感器可能在实验过程中出现故障与问题,这是实验者无法预估的。因此,若要使数字实验变得更加成熟和稳定,需要不断对传感器进行调试,同时要注意在平时对传感器进行维护。
本实验的意义 化学实验是化学学科的灵魂,对实验不断进行改进、优化、简化,是化学学习者和化学教学者不断追求的目标。让经典实验焕发生机,需要结合时下的新科技和新技术来进行。本实验就是利用时下热门的传感器技术对传统的滴定实验进行改进。本次改进遵循的一大原则就是“基于课本,高于课本”,即完全保留了滴定实验的所有因素,对实验的核心问题进行改进与优化——提高滴定过程中读数的准确度。通过这次改进,也让学生体会到定量实验中“准确”二字的重要性。如在若干次平行实验中,虽然体积的读数仅相差0.1 mL甚至0.05 mL,但是由于在最后的计算中需要放大25倍,因此出现“差之毫厘,谬以千里”的现象。
通过本次实验的改进,希望有越来越多的学生和化学教师体会到数字传感器的方便之处,也希望越来越多的人尝试使用数字传感器对化学实验进行设计和改进,从而不断提高教学质量。■
参考文献
[1]姚子鹏,陈基福,洪东府.化学拓展型课程(试用本)[M].上海科学出版社,2007:209-211.
[2]武汉大学.分析化学实验[M].5版.北京:高等教育出版社,2011.
[3]王晓江.用数字化传感器解决化学教学中的疑难点问题[J].中国教育技术装备,2014(11):49-50.
