常压下DDQ/TBN催化的苄醇有氧氧化
2019-09-23
(浙江工业大学 化学工程学院,浙江 杭州 310014)
将伯醇和仲醇氧化成相应的羰基化合物是有机化学中重要的官能团转化反应[1-2],传统使用的氧化方法需要使用化学计量的氧化剂,从而产生大量的副产物,不仅浪费试剂、成本高,并且严重污染环境。分子氧价格低廉、来源丰富,反应生成的副产物是水,清洁无污染。从经济性和环境方面来考虑,分子氧是一种理想的终端氧化剂[3-5]。然而,由于分子氧和有机化合物之间存在高能量势垒,在氧化反应中,直接用分子氧氧化有机化合物是很困难的。因此,针对温和条件下分子氧如何活化及其在醇氧化反应中的应用已经展开了大量的研究[6]。
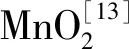
1 实验部分
1.1 实验试剂及仪器
采用Agilent 7890A气相色谱仪对产物进行分析,色谱柱为FFAP(30 m×0.25 mm×0.33 μm),采用FID检测器。进样口温度为230 ℃,载气为氮气,其流量为1 mL/min。所选用的测试条件:柱温120 ℃,保持2 min,20 ℃/min程序升温至230 ℃,恒温20 min,分流比为30∶1。另外,笔者所使用的试剂若无特别说明,均为市售CP或AR级,不经特别处理,直接使用。
1.2 实验方法
苯甲醇的氧化典型操作步骤:在25 mL的双口反应瓶中,加入0.216 0 g苯甲醇(2 mmol),0.022 7 g DDQ(0.1 mmol)和10.3 mg TBN(0.1 mmol),5 mL乙二醇二乙醚,将冷凝管置于反应瓶上,冷凝管另一端连接氧气球。然后开通氧气球,置换装置内的气体,置换完后用橡皮塞密封反应瓶另一端。随后,将反应瓶放入油浴(油浴已预热至100 ℃)中加热,开启磁力搅拌器。反应过程中通过取样针进行取样检测,直至原料反应完全。原料转化率和产物选择性由面积归一化法确定,部分产物表征数据如下:
对甲基苯甲醛:1H NMR (500 MHz, CDCl3)δ为9.98 (s, 1H), 7.79 (d,J=8.1 Hz, 2H), 7.35 (d,J=8.0 Hz, 2H), 2.46 (s, 3H); MS (EI),m/z为120.06 [M+]。
间氯苯甲醛:1H NMR (500 MHz, CDCl3)δ为9.99 (s, 1H), 7.87 (t,J=1.7 Hz, 1H), 7.785 (d,J=7.6 Hz, 1H), 7.61~7.63 (m, 1H), 7.50 (t,J=7.8 Hz, 1H); MS (EI),m/z为140.01 [M+]。
对甲硫基苯甲醛:1H NMR (500 MHz, CDCl3)δ为9.92 (s, 1H), 7.77~7.79 (m, 2H), 7.27~7.34 (m, 2H), 2.54 (s, 3H); MS (EI),m/z为152.03 [M+]。
1-对甲苯基乙酮:1H NMR (500 MHz, CDCl3)δ为7.85~7.87 (m, 2H), 7.25~7.27 (m, 2H), 2.58 (s, 3H), 2.41 (s, 3H); MS (EI),m/z为135.06 [M+]。
2-羟基-1,2-二苯乙酮:1H NMR (500 MHz, CDCl3)δ为7.91~7.92 (m, 2H), 7.50~7.53 (m, 1H), 7.38~7.41 (m, 2H), 7.26~7.35 (m, 5H), 5.95 (s, 1H), 4.57 (s, br, 1H); MS (EI),m/z为212.09 [M+]。
2-(2,6-二甲基-1-氧-1,2-二氢异喹啉-3-基)苯甲醛(1):1H NMR (500 MHz, CDCl3)δ为10.00 (s, 1H), 8.36 (d,J=8.2 Hz, 1H), 8.06 (m, 1H), 7.73 (m, 1H), 7.65 (t,J=7.5 Hz, 1H), 7.46 (m, 1H), 7.35 (m, 1H), 7.27 (s, 1H), 6.38 (s, 1H), 3.30 (s, 3H), 2.48 (s, 3H).
2 结果与讨论
2.1 反应条件优化
为了确定最佳反应条件,以苯甲醇作为模型底物,分别考察了溶剂、温度和DDQ/TBN用量对反应的影响。
2.1.1 溶剂对反应的影响
在催化氧化反应中,溶剂对反应体系具有重要影响,在不同溶剂中,催化剂会表现出不同的反应活性,因此,考察了一些常用的溶剂对该反应的影响,结果见表1。从表1可以看出不同的溶剂对反应的影响显著。当以四氯乙烷和乙二醇二乙醚作为溶剂时,原料苯甲醇的转化率较高,分别为95%和100%;当反应溶剂分别为乙二醇和正丁醇时,原料苯甲醇的转化率比较低。在产物的选择性方面,选用正丁醇、甲苯、三氟甲苯、氯苯、四氯乙烷和乙二醇二乙醚为溶剂,产物选择性均大于95%,而在乙二醇和乙二醇单乙醚中产物选择性比较差。综上所述,选用乙二醇二乙醚为溶剂时,原料苯甲醇能完全转化,产物选择性也大于99%,所以,最终选用乙二醇二乙醚作为最佳反应溶剂,并在此基础上对其他反应条件进行筛选。

表1 不同的溶剂对反应的影响Table 1 The effect of different solvents on the reaction
注:苯甲醇2 mmol,5 mL表中所列溶剂,反应温度(油浴)100 ℃,氧气球,反应结束后GC检测,转化率和选择性由面积归一化法确定。
2.1.2 温度对反应的影响
反应温度对化学反应的影响很大,需要选择一个合适的反应温度,因此,对不同的温度进行了考察,结果见表2。从表2中可以看出:当反应温度为100 ℃时,反应5 h后,原料已完全转化,产物选择性也大于99%,反应效果最好;当温度为80 ℃时,5 h后转化率仅为67%,虽然选择性也很高,但反应速率过慢;当温度升高到120 ℃时,虽然反应时间缩短了,但产物选择性却降低为90%。综上所述,最终选择以100 ℃作为最佳反应温度。
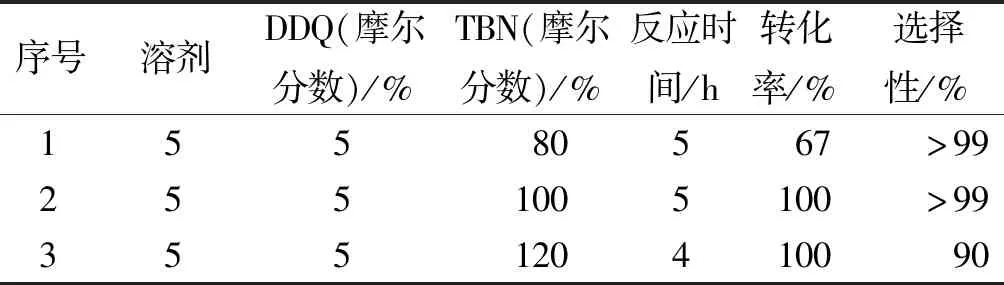
表2 温度对反应的影响Table 2 The effect of different temperature on the reaction
注:苯甲醇2 mmol,5 mL乙二醇二乙醚,油浴加热,氧气球,反应结束后GC检测,转化率和选择性由面积归一化法确定。
2.1.3 DDQ/TBN用量对反应的影响
同时,试图减少催化剂DDQ和TBN的用量,研究是否能达到相同的实验结果,结果见表3。从表3中可以看出:当DDQ和TBN的摩尔分数小于5%时,原料都无法完全转化;而当两者均为5%时,原料能完全转化;当继续增加催化剂量时,所需的反应时间越来越短。在实验范围内,产物的选择性没有显著变化,苯甲醇几乎都定量地被氧化成苯甲醛。由于增加催化剂的用量只是减短了反应时间,产物选择性与催化剂摩尔分数为5%时没有很大区别,所以DDQ和TBN的摩尔分数均为5%。
经过上述实验的对比分析,最终确定最佳反应条件:苯甲醇 (2 mmol),DDQ (0.1 mmol),TBN (0.1 mmol),乙二醇二乙醚为溶剂,100 ℃下氧气氛围中反应5 h。

表3 DDQ/TBN用量对反应的影响Table 3 The effect of the amount of DDQ/TBN on the reaction
注:苯甲醇2 mmol,5 mL乙二醇二乙醚,反应温度(油浴)100 ℃,氧气球,反应结束后GC检测,转化率和选择性由面积归一化法确定。
2.2 底物拓展
各类苄醇有氧氧化反应的反应方程式为

在2.1节的最优反应条件下,对反应的普适性进行了考察,反应结果如表4所示。从表4中可以看出:苄醇类化合物苯环上取代基不同或取代基位置不同时,其在该氧化体系下的氧化效果有明显的差异(Entries 1~10)。无任何取代基的苯甲醇(Entry 1)可以定量高选择性地转化成相应产物苯甲醛。当底物苯环上的间位或对位有供电子基团(甲基或甲氧基)取代时,都能被定量高选择性地氧化生成相应的醛(Entries 2,3,5)。然而当底物苯环上有吸电子基团取代时,除了间氯苯甲醇和对氯苯甲醇在增加一倍催化剂量下能够完全转化外(Entries 9,10),其他底物的氧化效果不是很理想(Entries 8,11)。当底物醇中含有O,S杂原子时(Entries 12,13),底物能在较短的时间内氧化成相应的醛。当底物对位有甲硫基取代时,也能在较短的时间内氧化成4-甲硫基苯甲醛(Entry 14)。
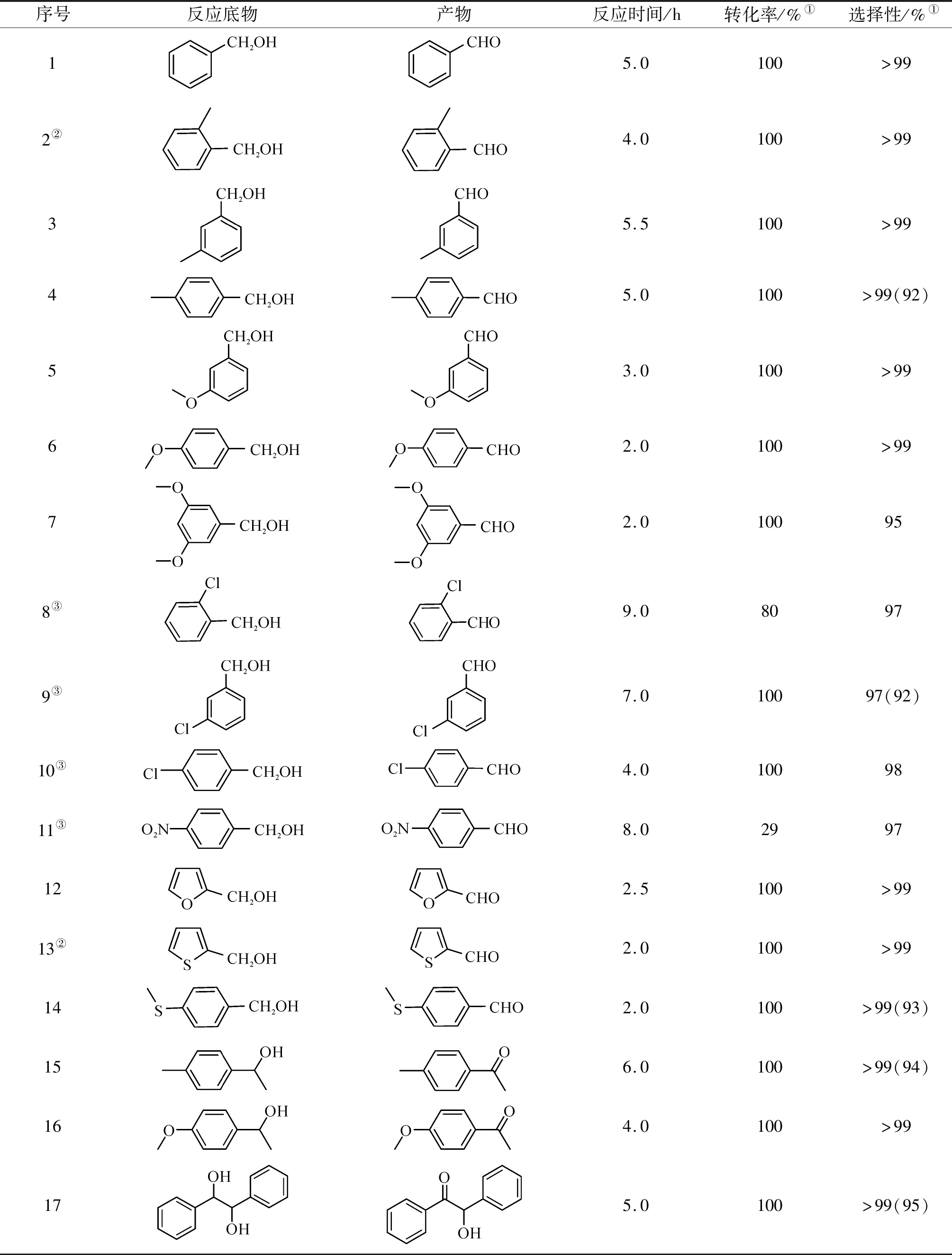
表4 各类苄醇的有氧氧化Table 4 The aerobic oxidation of different benzylic alcohols
注:反应条件为2 mmol底物,0.10 mmol DDQ,0.10 mmol TBN,5 mL乙二醇二乙醚,氧气球, 100 ℃,转化率和选择性由面积归一化法确定。
① 括号中数据为分离收率;② DDQ (0.16 mmol),TBN (0.16 mmol);③ DDQ (0.2 mmol),TBN (0.2 mmol)。
而在芳香族仲醇的氧化中,当底物为1,2-苯基乙二醇(Entry 17)时,也能定量高效地转化成相应的酮类物质,而没有发生C—C键的断裂生成苯甲醛。
通过对一系列底物的实验结果的分析,发现常压下DDQ/TBN催化的有氧氧化体系适用于能够在反应中形成稳定碳正离子的底物,如带供电子基团的底物;当带强吸电子基团底物的氧化时,由于无法生成稳定的碳正离子,所以反应比较困难;同时底物取代基的空间位阻对反应也有一定的影响。
茚并[1,2-c]异喹啉类化合物具有很高的生物活性,2-(2,6-二甲基-1-氧-1,2-二氢异喹啉-3-基)苯甲醛(1)是合成茚并[1,2-c]异喹啉类化合物的关键中间体[23]。使用笔者所提供的方法,3-(2-(羟甲基)苯基)-2,6-二甲基异喹啉-1(2H)-酮(2)可以顺利地被氧化为1,分离收率达到83%。DDQ/TBN/O2催化氧化化合物2为化合物1的反应方程式为

2.3 反应机理
结合文献[15-16,18],笔者推测了可能的反应机理:在该体系中,TBN热裂解释放出NO,NO迅速与氧气反应生成NO2。DDQ把苄醇氧化为醛或酮,本身被还原为DDHQ,DDHQ可以被NO2氧化DDQ,使得DDQ不断循环,而NO2的还原产物NO又马上被氧气氧化为NO2。DDQ/TBN催化苄醇的有氧氧化机理为

3 结 论
笔者成功开发了一种简单、高效的DDQ/TBN催化苄醇的有氧氧化方法,此方法以有机小分子DDQ为催化剂,另一有机小分子TBN为助催化剂,绿色氧化剂氧气为终端氧化剂。DDQ/TBN这一组合催化体系能有效地催化苄醇类、杂芳香苄醇类和取代α-苯乙醇类底物有氧氧化得到相对应的醛或酮。该方法不需要加压,操作简单安全,反应条件温和,无需过渡金属催化剂参与且所用催化剂廉价易得,具有绿色环保的特点。
