蔗糖共溶质对琼脂-魔芋胶共混体系溶胶-凝胶转变过程流变学性质及结构形成动力学的影响
2019-07-05朱建华邹秀容丘秀珍刘日斌
朱建华,邹秀容,丘秀珍,刘日斌,单 斌
(1.韶关学院英东食品科学与工程学院,广东 韶关 512005;2.韶关学院化学与环境与工程学院,广东 韶关 512005)
从材料科学视角而言,食品产品是将营养、感官和控释等功能赋予到由各种食用成分经过相应工艺处理(压力、剪切及温度场等)而获得的具一定微结构(如凝胶、乳液及泡沫等)的软物质,与其他软物质不同的是其能被摄食且可被感知到质构和风味[1-4]。食品工业所囊括的各式食品种类中,半固体凝胶态食品占据极为广泛的市场份额,对食品产业经济推动和满足民众消费意义重大。果冻类凝胶产品为由较低浓度的单一或多种食品高分子(多糖等亲水胶体)、高浓度低分子共溶质(蔗糖、淀粉糖浆等)及溶剂水构成,为典型半固体软物质凝胶材料[5-7]。果冻类凝胶产品工业制备成型在蔗糖等共溶质场中完成溶胶-凝胶转变过程,此过程溶胶、调配、灌装及杀菌工序都保持较高温度,体系呈溶胶状态,杀菌后的冷却工序体系发生溶胶-凝胶相转变,由流动态转变为凝胶态[8-10]。
共溶质场指食品高分子材料溶胶-凝胶过程所处的环境并非理想状态下的仅含高分子组分的水溶液环境,同时溶液中溶解有蔗糖、淀粉糖浆、聚葡萄糖、盐分、乳化剂等单一或多元低分子共溶物(即共溶质)[11-12]。此类共溶物的分子质量小于食品高分子分子质量,共溶质的存在可改变食品高分子在溶液中的折叠和缠结,并影响到溶胶-凝胶过程流变性质演变规律,进而影响到产品质构、风味及贮藏性能的体现[13-15]。果冻类产品制备成型溶胶-凝胶转变过程的流变学性质直接影响到原料泵送、产品成型及质构形成等重要性质形成。目前食品学术和产业界相关研究人员多从工艺及配方优化角度来研究果冻类凝胶体系[16-17],关于共溶质场中食品高分子共混体系的溶胶-凝胶转变过程流变性质及凝胶形成动力学研究鲜见报道。
本实验以琼脂-魔芋胶为双组分共混模拟工业生产果冻用二元复配体系,采用流变测试、质构分析、扫描电镜及红外分析等技术,研究蔗糖共溶质浓度对琼脂-魔芋胶共混体系溶胶-凝胶转变过程流变学性质变化趋势、凝胶化速度及动力学的影响,以期为果冻类凝胶产品的物性设计和规避产品质量缺陷提供应用理论基础参考。
1 材料与方法
1.1 材料、试剂与仪器
LV-Q2琼脂 福建省緑麟食品胶体有限公司;魔芋胶(型号KJ30) 湖北强森魔芋科技有限公司;蔗糖(一级,含量>99.6%) 市售。试剂均为食品级。
MCR92旋转流变仪 奥地利Anton Paar公司;FTIR-8400S傅里叶变换红外光谱仪 日本岛津公司;TMS-Pro型质构仪 美国FTC公司;TM3030型台式扫描电子显微镜 日本Hitachi公司。
1.2 方法
1.2.1 琼脂-魔芋胶共混体系相图测定
按相应比例混合蔗糖和魔芋胶粉,然后于60 ℃用纯水溶胀15 min配制获得魔芋胶储备液。用纯水及琼脂粉按预先预设比例配制悬浮液,并于室温预先进行8 h溶胀得琼脂储备液。按一定比例共混琼脂储备液及魔芋胶储备液得琼脂-魔芋胶共混液,配制后用锡箔纸密封烧杯口并放入水浴锅中于80 ℃恒温30 min,恒温阶段结束后迅速取出自然冷却至室温,通过目测法观察琼脂-魔芋胶溶液共混体系相图形态并绘制相图。
1.2.2 流变学性质测试
含有不同质量分数蔗糖的琼脂-魔芋胶共混溶液于80 ℃水浴锅中恒温30 min后,转移至保温桶中进行保温,然后将1 mL样品,快速转移到预先加热到70 ℃的流变仪平行板(上下板直径45 mm,狭缝1 mm),除去过量样品并在样品外缘加一层轻质硅油防止样品中的水分蒸发。在线性黏弹区范围内(0.5%应变),进行小振幅应变扫描考察体系黏弹性质。测试程序如下:先从70 ℃以2 ℃/min降温至10 ℃,然后在10 ℃保温10 min,此过程频率恒定为6.28 rad/s,记录G’、G”及损耗系数(tanδ);然后进行频率扫描,频率范围为0.1~100 rad/s。
1.2.3 琼脂-魔芋胶共混体系凝胶结构形成速度测定
非等温或等温过程特定时间阶段共混凝胶形成相对快慢常用凝胶结构平均形成速度(structure developing rate average,SDRa)及即时凝胶化速度进行表征[18-20],如公式(1)、(2)所示:

式中:G’ini为G’end特定时间阶段对应的起始及终点弹性模量值/Pa;tini、tend为对应阶段起始及终点测定时间/min。对G’-t曲线求一阶导数得:

式中:vg为即时凝胶化速度/(Pa/min)。
SDRa及vg分别可用于表征时间段及时间点的凝胶化相对快慢,但尚难以定量表征vg改变的快慢,为此引入即时凝胶化加速度参数,如公式(3)所示:

式中:αg为对G’-t曲线求二阶导数获得即时凝胶化加速度/(Pa/min2)。
αg的正负性具有物理意义,正值表示凝胶化处于加速阶段,而负值则反之视为凝胶化处于减速阶段,正负性相同的αg可以其绝对值(加速率)进行相对大小比较,其值越大,凝胶结构化速度改变越快。αg可用于辅助分析凝胶化加速过程特征。
1.2.4 琼脂-魔芋胶共混凝胶质构特性测定
质构测定用凝胶样品制备过程采用内空腔为圆台体的模具,相应圆台体尺寸为:下底面Ф1为(23±1.0)mm,上底面Ф2为(20±1.0)mm,高度H为(7±0.5)mm。将琼脂-魔芋胶共混溶液于80 ℃水浴恒温30 min后注入模具中,室温条件下2 h后脱模待测。测试条件及参数:P/36R探头,测前速率为1.0 mm/s,测试速率为0.5 mm/s,返回速率为1.0 mm/s,压缩变形程度为20%,触发力为0.10 N。
1.2.5 琼脂-魔芋胶共混凝胶析水性测定
琼脂-魔芋胶共混凝胶制备程序同1.2.4节,于室温条件放置2 h脱模后,移入20 ℃恒温箱中并开始计时,测定样品保温3、6、9、21、24 h及27 h后的析水率,按公式(4)计算:
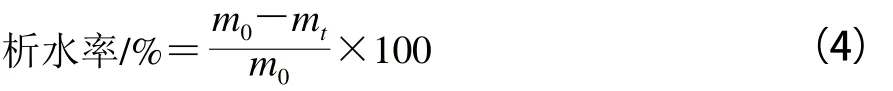
式中:m0为初始凝胶质量/g;mt为静置t小时后凝胶的质量/g。
1.2.6 扫描电镜测试
琼脂-魔芋胶共混凝胶样品制备程序同1.2.4节,切成10 mm×10 mm×10 mm薄片状,放入超低温冰箱冻结,随后置于冻干机冻干后转移至干燥器中密封保存。扫描电镜观察前用薄刀片将样品切片,并选择低真空模式后在15 kV加速电压下观察横切断面微观结构。
1.2.7 傅里叶变换红外光谱测试
测试前琼脂-魔芋胶共混凝胶样品烘干至恒质量,采用常规溴化钾压片法制备红外扫描用样品,扫描波数范围选取4 000~400 cm-1,分辨率为0.5 cm-1,记录样品的红外光谱。
1.3 数据分析
所有实验均重复3 次,利用Origin 9.0软件进行绘图,采用SPSS 21.0软件进行质构、析水性数据统计分析,通过单因素方差分析(one-way ANOVA)比较组间数据,结果以 ±s表示,P<0.05,差异显著。
2 结果与分析
2.1 琼脂-魔芋胶溶液共混体系相图分析
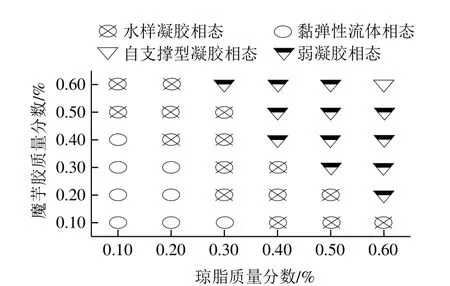
图1 琼脂-魔芋胶共混体系相图Fig. 1 Phase diagram of agar/konjac blends
未添加蔗糖条件下,图1中琼脂质量分数和魔芋胶质量分数网格线的交点为1 个样品的琼脂质量分数和魔芋胶质量分数的组合。琼脂-魔芋胶共混体系的相图形态共分为黏弹性流体态、水样凝胶态、弱凝胶态及自支撑型凝胶态。盛放样品的烧杯倾斜45°后,自杯缘可流出的样品相态为黏弹性流体态、样品上层可发生较大位移蠕动且自杯缘不可流出的样品相态为水样凝胶态、样品可轻微蠕动但烧杯垂直倒置后可从烧杯中跌落的样品相态为弱凝胶态;盛放样品的烧杯垂直倒置后样品发生轻微蠕动但不会从烧杯中跌落的样品相态为自支撑型凝胶态。由图1可知,2 种多糖质量分数均较低时,即琼脂质量分数不大于0.20%,且魔芋胶质量分数不大于0.30%,该区域内共混体系尚未形成三维网络凝胶结构,共混体系的相态为黏弹性流体态,该相态占据相图的左下角区域。在较高琼脂浓度或魔芋胶浓度区域(琼脂质量分数大于0.30%或魔芋胶质量分数大于0.40%),单独增加魔芋胶或琼脂质量分数均可观察到共混体系的相态均发生由黏弹性流体态逐渐向凝胶态转变趋势。基于相图分析及实际工业生产果冻体系多糖配料浓度范围,后续流变、析水、质构、电镜及红外性质分析选择质量分数组合为0.60%琼脂-0.60%魔芋胶的共混体系为研究对象进行考察。
2.2 琼脂-魔芋胶共混体系溶胶-凝胶转变过程流变性质分析
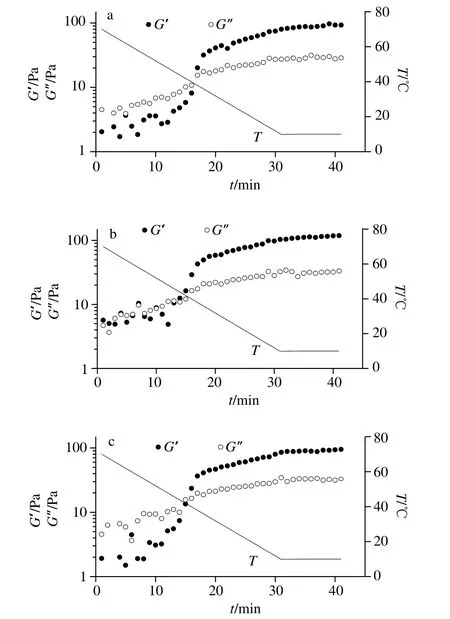
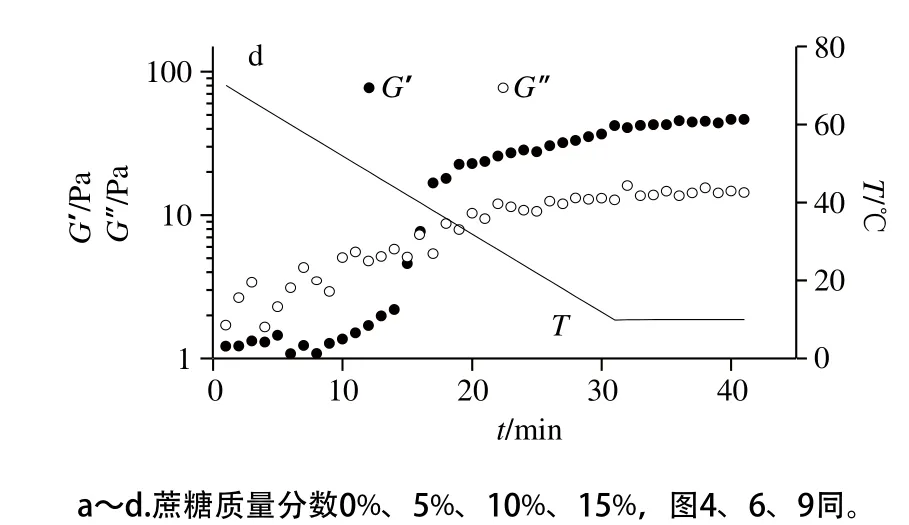
图2 琼脂-魔芋胶共混体系G’和G”随t变化曲线Fig. 2 G’-t and G”-t cures of agar/konjac blends
含不同蔗糖共溶质的琼脂-魔芋胶共混体系降温及恒温过程黏弹性模量随时间变化如图2所示。降温起始阶段(约70~55 ℃),G’及G”值均低于10 Pa且G”>G’,表明共混体系处于可流动态。降温过程随温度进一步降低(约55~40 ℃),G’、G”逐渐增加,G’增幅显著高于G”增幅,G’和G”相对大小仍呈G”>G’,但两者差值渐小,直至达到传统意义上凝胶点(gel point temperature,GPT,G’=G”时,温度值约40 ℃左右)。GPT的意义在于整个体系形成三维凝胶网络结构,共混溶液体系由溶胶转变为凝胶,不能再流动,但受外力作用时可以变形。GPT以下随温度降低直至降温末温度点,G’呈增加趋势,黏弹性模量值相对大小保持G’>G”,且二者差值呈“剪刀差”增加趋势。最后恒温阶段G’呈缓慢增加趋势,表明凝胶网络结构得到进一步巩固。相同控温程序条件下,预实验研究了纯琼脂和纯魔芋胶黏弹模量随时间变化趋势(实验数据未示出),发现控温过程琼脂溶液发生了明显的溶胶-凝胶相转变,而魔芋胶溶液G’、G”变化非常小且未出现溶胶-凝胶转变,表明琼脂-魔芋胶共混体系溶胶-凝胶转变主要由琼脂组分引起。
琼脂-魔芋胶共混体系凝胶过程特征参数结果(表1)显示,随蔗糖质量分数增加,凝胶点温度、同温度点G’、SDRa值均呈先增加而后降低趋势,表明蔗糖共溶质存在可以调节溶胶-凝胶转变进程及改变凝胶的强度。低质量分数蔗糖存在时,蔗糖与多糖分子之间的相互作用主要通过蔗糖的平伏羟基与多糖分子间形成氢键,并促进交联点出现和凝胶化[21]。此种促进凝胶形成的效应可能主要与蔗糖在水溶液体系中具备强的水合作用相关,而水合作用可将水分子从琼脂及魔芋胶高分子周围排斥出来,降低了琼脂分子周围的水分子数,削弱了琼脂分子与水分子之间的相互作用,从而促进琼脂多糖分子形成双螺旋结构。过量的蔗糖共溶质存在却因蔗糖与自由水分子间氢键分子作用加强阻碍了琼脂多糖螺旋结构的发生和弱化凝胶形成。研究人员在考察卡拉胶、结冷胶等单一多糖凝胶证实了蔗糖浓度低于临界值时可以稳定凝胶结构,而高于临界值时促使凝胶失稳的现象[22-24]。
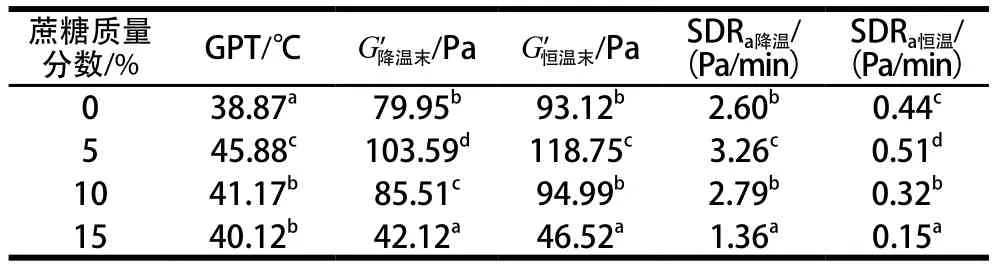
表1 琼脂-魔芋胶共混体系溶胶-凝胶转变过程流变学特征参数Table 1Rheological characteristic parameters of agar/konjac blends during sol-gel transition
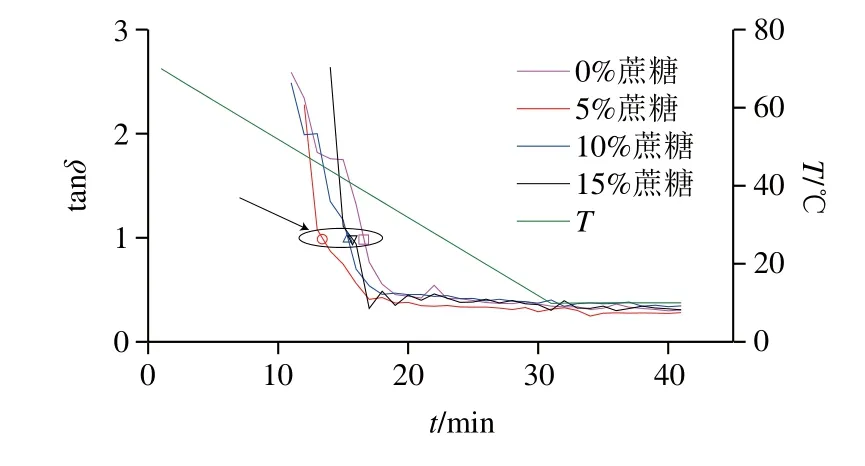
图3 琼脂-魔芋胶共混体系tanδ-t关系曲线Fig. 3 tanδ-t cures of agar/konjac blends
tanδ-t作为G’-t,G”-t曲线的补充,表征琼脂-魔芋胶共混体系溶胶-凝胶相转变时具有参考意义,图3显示琼脂-魔芋胶共混体系经历了从溶胶态过渡到凝胶态的过程,随温度降低,凝胶化开始后,tanδ不断减小,历经tanδ为1后,tanδ值最终介于0.25~0.31之间,为典型弱凝胶结构[25]。随蔗糖质量分数增加,与对照相比,添加5%蔗糖样品tanδ为1所在温度值要高于对照样,添加10%及15%蔗糖样品对应温度值介于对照样和添加5%蔗糖样品之间,进一步证实了蔗糖小分子共溶质质量分数可影响到琼脂-魔芋胶的溶胶-凝胶转变历程。
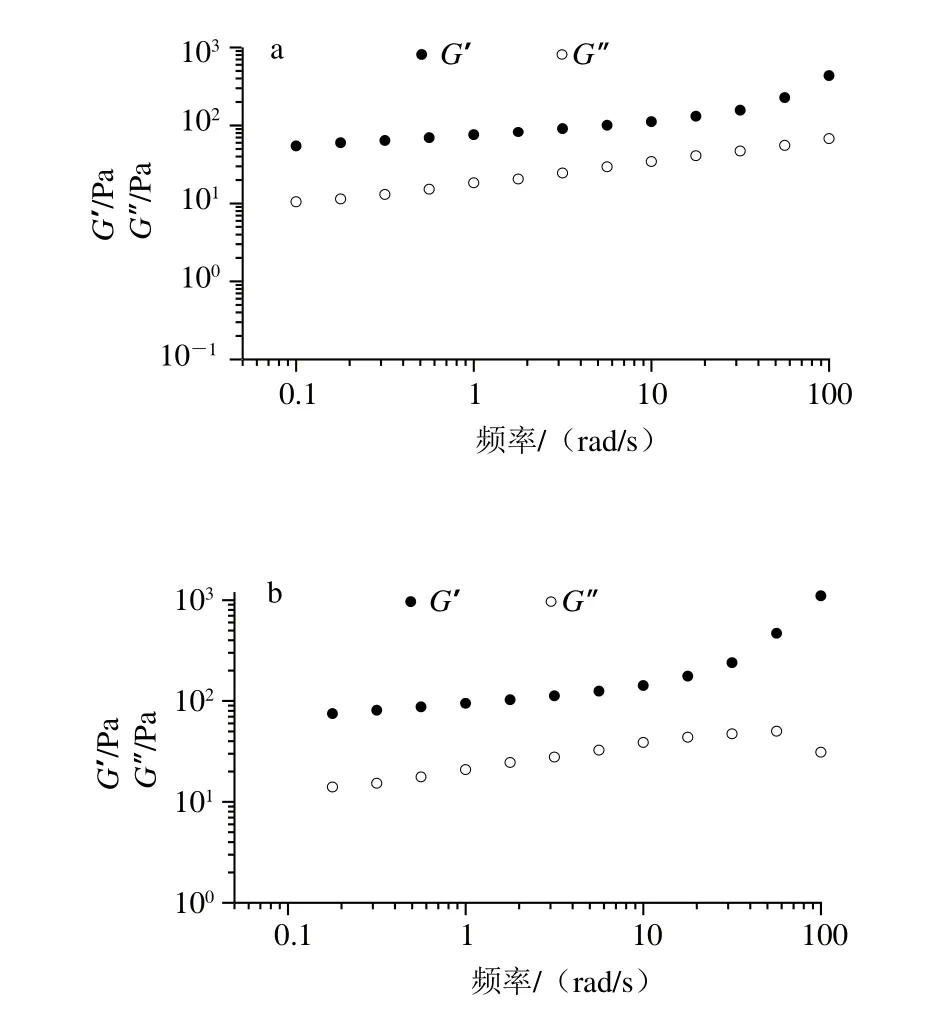
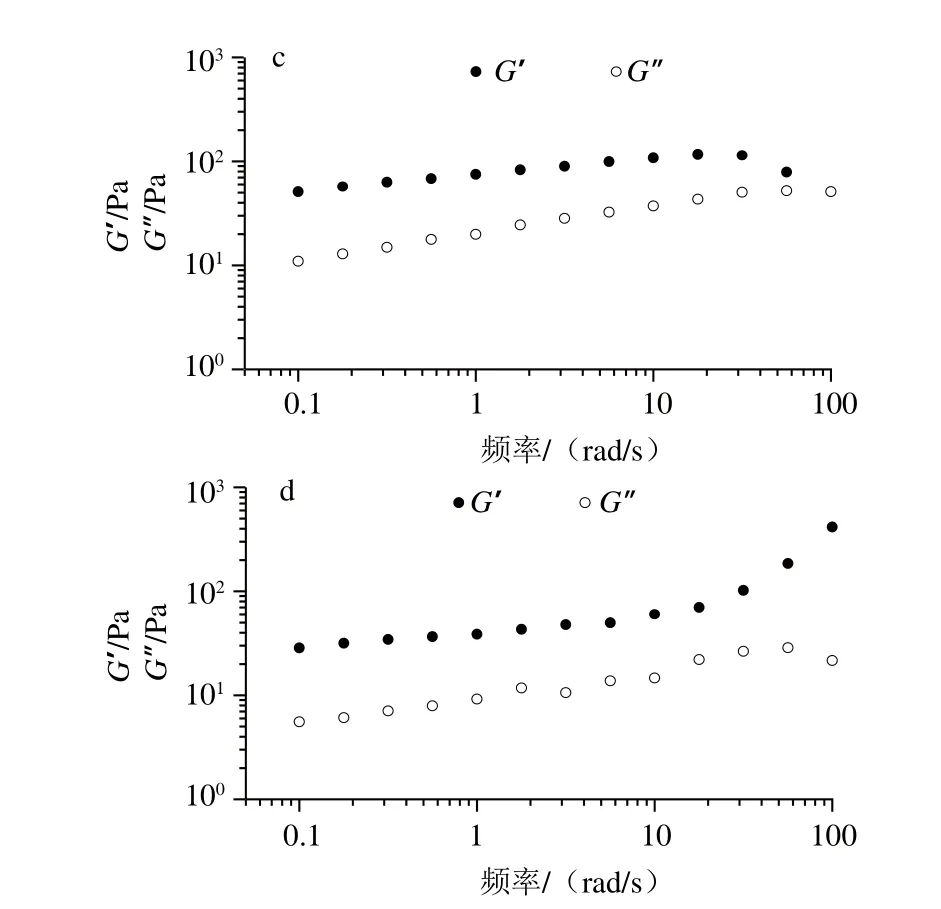
图4 琼脂-魔芋胶共混体系控温程序末频率扫描曲线Fig. 4 G’-ω and G”-ω cures of agar/konjac blends at the end of the constant temperature procedure
由图4可知,频率扫描范围内G’>G”,表明样品均能形成凝胶结构。低频范围,随频率增加模量增加缓慢,但高频区,随频率增加,弹性模量出现陡增或陡降,表明高频区共混体系凝胶结构容易被破坏。相同角频率条件下,随着蔗糖质量分数的增大,共混凝胶G’值呈先增加而后降低趋势,进一步说明低质量分数蔗糖共溶质的存在,强化了琼脂-魔芋胶共混凝胶结构,而高质量分数蔗糖共存时又使共混凝胶结构遭到破坏[26]。
2.3 琼脂-魔芋胶共混体系溶胶-凝胶相转变速度分析
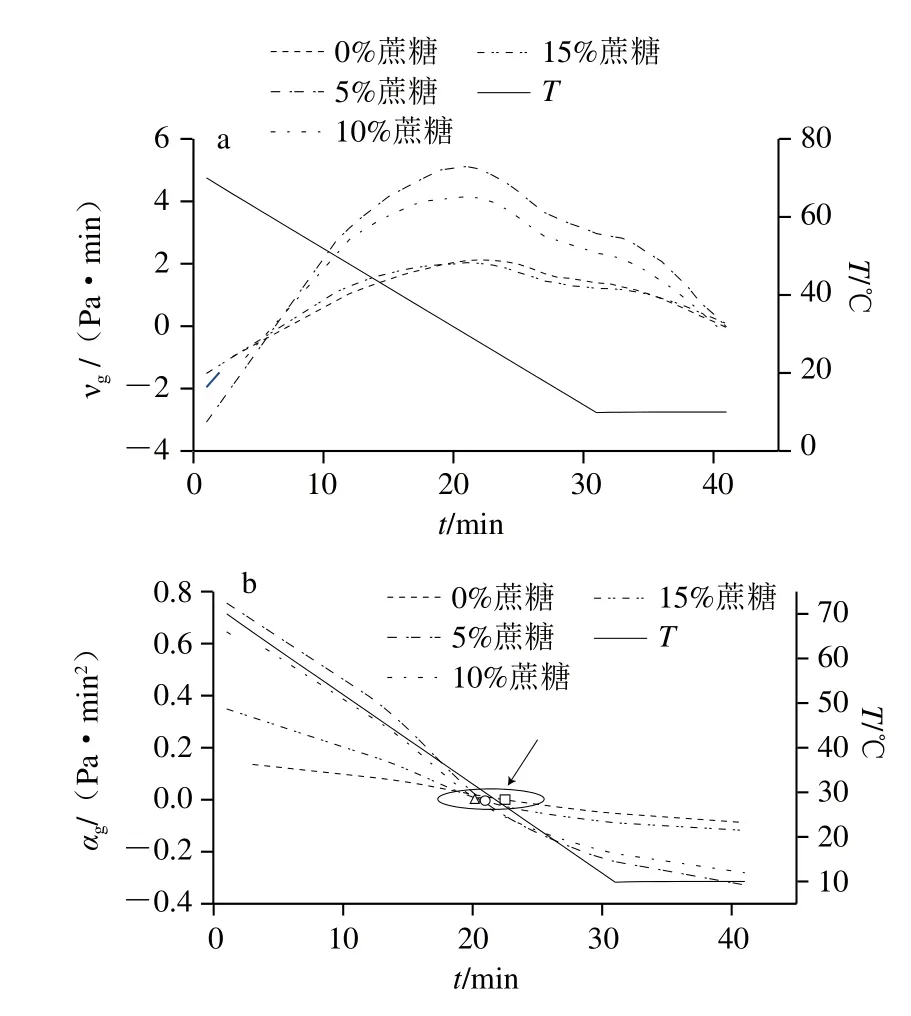
图5 琼脂-魔芋胶共混体系vg(a)及αg(b)随时间变化曲线Fig. 5 vg-t (a) and αg-t (b) cures of agar/konjac blends
高分子体系溶胶-凝胶转变存在多种判定方法,其中一种方法认为溶胶-凝胶转变时发生G’=G”,此种凝胶点的判定方法因简单直观而被广泛用于食品高分子体系凝胶研究[27-28]。但此种方法的局限性在于无法探知溶液体系中交联点的首次出现点温度及交联点生成量最大时的温度,也不能定量考察溶胶-凝胶化过程的速度及加速度情况,因此有研究人员提出对G’-t关系求导并提出vg概念对溶胶-凝胶化速度进行分析[18],本实验对该方法进行了小幅改进,提出vg参数概念表征溶胶-凝胶化进程。对G’-t关系曲线分别取一阶及二阶导数,相应得到vg及αg。
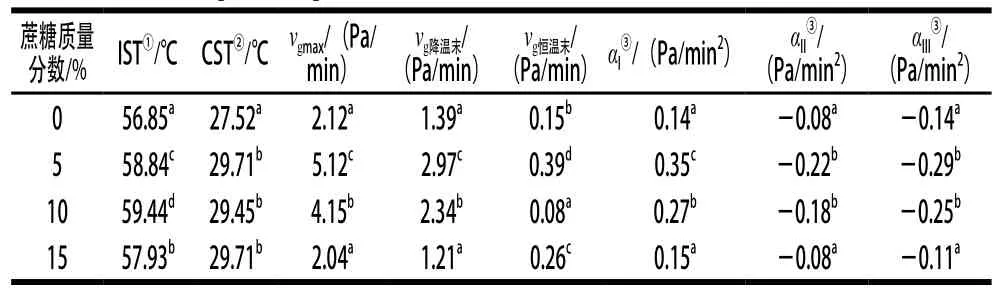
表2 琼脂-魔芋胶共混体系溶胶-凝胶过程凝胶化节点温度、速度及加速度参数Table 2 T, vg and αg of agar/konjac blends during sol-gel transition
由图5a可知,随温度降低,vg均呈先自零线(纵坐标为零的水平界限线)下方升高经过零线而后升高达到峰值,继而降低的趋势。vg为0处对应的温度点为凝胶化起始点温度(initial structure formation temperature,IST),介于55~60 ℃之间,IST可视为仪器设备感知阈值内首次感应到共混体系中多糖的螺旋结构分子链形成,此后随温度降低琼脂双螺旋结构分子链数量和长度增加引起G’增加,直至vg达最大值时温度点(critical structure formation temperature,CST),CST值约为30 ℃,此温度点琼脂双螺旋结构分子链生成量最大;温度点低于CST后,G’进一步增加,vg值从峰值回落,主要因为琼脂双螺旋结构分子链增量逐渐降低所致,恒温过程vg继续呈下降趋势,但均因出现转折点而改变了降温过程vg原有下降趋势,原因在于相同时间内恒温过程形成的琼脂双螺旋分子链相比降温而言增量更小,但凝胶网络结构得到进一步巩固。从图5a及表2特征参数可知,与对照相比,添加5%蔗糖后共混体系vg明显增加,但添加10%与添加5%蔗糖共混体系样品相比vg得到降低,但仍高于对照样,添加15%蔗糖共混体系的vg与对照样相比无显著性差别。
图5b显示所有蔗糖添加范围αg随温度降低呈逐渐降低趋势。αg曲线分布在零线两侧,零线上侧,为凝胶化正向加速阶段,其值排序依次为αg0%蔗糖<αg15%蔗糖<αg10%蔗糖<αg5%蔗糖,表明琼脂-魔芋胶共混体系凝胶化加速均在降温起始阶段,此阶段vg增加,G’亦增加。零线下侧凝胶加速度值为负值,表明凝胶化驱动力变为反相力,随温度降低凝胶形成速度递减,G’仍增加。含不同蔗糖共溶质共混体系凝胶加速率大小依次排序与零线上侧相同,同温度点含5%蔗糖共混体系凝胶结构化加速率值最高。与对照样相比,含5%蔗糖共混体系在零线两侧同温度点凝胶化加速率值均增加,且温度点距离CST越远,两者加速率差值越大,表明添加5%蔗糖后共混体系凝胶化加速快、减速也快。当蔗糖质量分数增加至10%时,共混体系零线两侧凝胶化加速率值均从峰值下降,添加15%蔗糖后,凝胶化加速率值进一步回落,但仍高于对照样。此结果可能主要因为蔗糖在水溶液环境中与琼脂亲水胶体分子竞争键合水分子,较低质量分数蔗糖利于琼脂分子链之间形成双螺旋结构,从而对凝胶结构起到稳态化作用。较低共溶质质量分数蔗糖使琼脂多糖分子链形成双螺旋结构的速率更快,达到峰值后大部分琼脂分子链形成双螺旋结构并参与凝胶结构,因而共混体系溶液中的琼脂双螺旋结构形成速度减缓从而导致凝胶化速率降低也快。
2.4 凝胶化反应动力学分析
非等温动力学模型常用于降温过程溶胶-凝胶转变动力学分析[29],此种方法主要结合经典非等温化学分解反应动力学速率方程、阿伦尼乌斯方程、时温关系及凝胶与橡胶物理体系的近似处理四方面而获得。经典的非等温化学分解反应动力学可按方程(5)表征[30]:
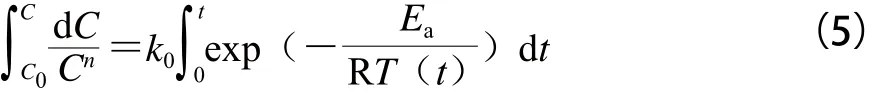
式中:C为质量分数/%;C0为初始质量分数/%;t为反应时间/min;k0为指前因子;Ea为反应活化能/(J/mol);T为t时刻对应的绝对温度值/K;R为气体常数(8.314 J/(mol·K))。
变温速率为线性速率的前提下的,基于实验实证和回归分析进行推导此表达式可获得:
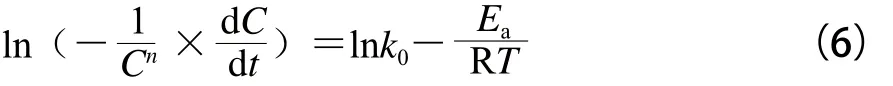
非等温条件下的经典化学反应动力学模型能与流变测试黏弹性模量关联起来,关键是借鉴橡胶弹性理论进行转换,具体就凝胶体系而言,因弹性模量值通常与高分子交联结构数量或质量分数成比例,因此质量分数改变效应可通过同步改变的弹性模量值来研究,对方程(6)而言C与弹性模量G’的改变具有等效性,因此其质量分数C和质量分数变化值(dC)可分别用模量值G’及模量变化值(dG’)予以替代[31],并得到直接用流变学参数表征凝胶过程的动力学方程:
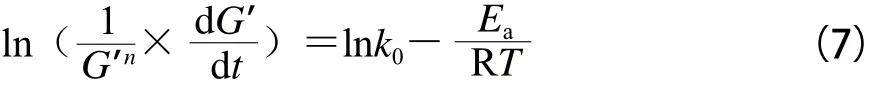
与公式(6)相比,公式(7)中因为凝胶形成过程弹性模量值增量为正,此公式中负号转换为正号,此一点与分解反应过程反应物质量分数增量为负正好相反。多糖非等温动力学分析过程常见现象是降温阶段实验结果通常会显示溶胶-凝胶转变过程具备2 个特征区域,对应2 个不同温度范围并分成2 个不同阶段的反应[32-33]。为研究蔗糖质量分数对共混体系凝胶动力学参数影响,因此进行归一化比较,利用方程(7)对琼脂-魔芋胶共混体系溶胶-凝胶形成过程进行动力学分析,参照已有亲水胶体体系凝胶过程n值亦取值为2[34-35]。图6为不同蔗糖质量分数条件下琼脂-魔芋胶共混体系的作图结果,结果表明温度大于50 ℃时,G’及G”值都很小,且黏弹性模量值存在上下波动状态,在拟合曲线上显示为噪音信号,见图6中椭圆虚线标示出区域。选定第I阶段温度范围为50~35 ℃,第II阶段温度范围为35~10 ℃,以最小二乘法拟合后求得2 个阶段的Ea值(表3),分段拟合直线的R2值均大于0.90,表明拟合过程具有较高置信度并具备可比性。
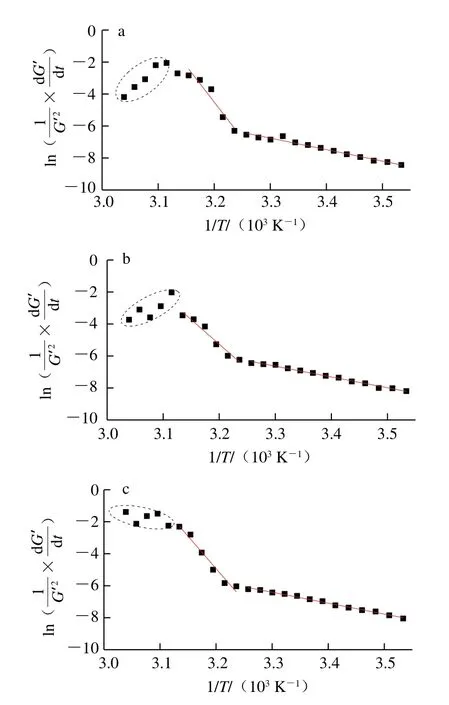
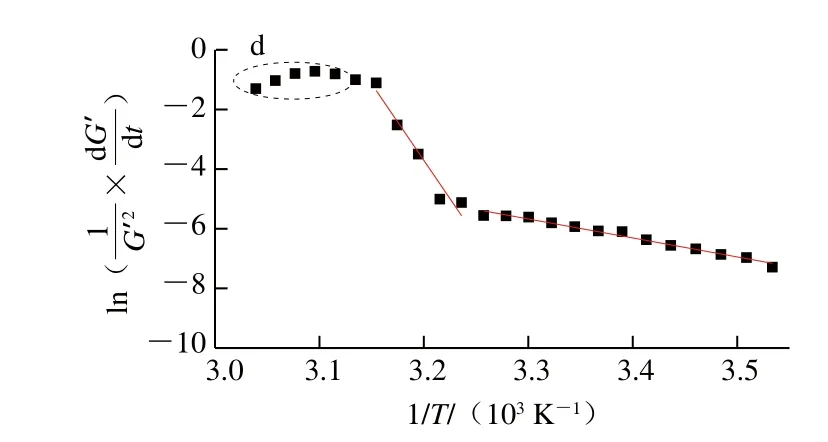
图6 琼脂-魔芋胶共混体系弹性模量随温度变化的Arrhenius拟合曲线Fig. 6 Arrhenius fitting of G’-T cures of agar/konjac blends

表3 琼脂-魔芋胶共混体系溶胶-凝胶转变过程凝胶活化能及相关系数特征参数Table 3 Characteristic parameters of Ea and R2during sol-gel transition
高温范围内所有样品的Ea介于250~430 kJ/mol,均显著高于低温区相应值(介于50~60 kJ/mol),高温范围内活化能相对比较高,表明琼脂-魔芋胶共混体系溶胶转变成凝胶三维网络需要克服能垒越高,而低温范围,琼脂分子形成双螺旋结构相对容易,能垒显著降低,凝胶形成速度大大加速。当添加蔗糖质量分数为5%时,高温区能垒被显著降低,进一步增加蔗糖质量分数到10%或15%时,能垒重新得到提高,尤其添加15%质量分数蔗糖时,能垒甚至超过对照样,弱化了形成网络结构,此结果与G’-t、G”-t曲线表现出的蔗糖质量分数改变效应趋势是一致的,主要因为低质量分数蔗糖有助于高分子间的网络结构形成,降低了形成凝胶网络所需要的能量,而高质量分数蔗糖因为蔗糖自身束缚水能力的增强弱化了多糖分子水化溶胀,最终导致形成网络结构需要消耗更多的能量。与高温区域蔗糖质量分数对活化能具备显著影响效应相比,改变蔗糖质量分数对低温区域的Ea没有显著性差别影响,原因可能在于第II阶段发生在凝胶化增强过程,琼脂双螺旋分子链结构形成相对容易。研究人员考察低甲氧基果胶、低酰基结冷胶/酪蛋白酸钠及刺槐豆胶/黄原胶共混体系单一或共混亲水胶体体系凝胶活化能随温度变化时发现了类似结果[27,29,31]。
2.5 琼脂-魔芋胶共混体系凝胶析水性质分析
由图7可知,添加5%蔗糖琼脂-魔芋胶共混体系凝胶在27 h后的析水率是1.45%,未添加共溶质对照样相应值是1.50%,略有降低,进一步增加蔗糖质量分数至10%,析水率显著降低到1.17%,表明添加蔗糖质量分数越高,琼脂-魔芋胶共混凝胶的析水率越低,蔗糖加入后,能明显提高共混凝胶的持水能力。蔗糖分子中的平伏羟基基团能够与邻近水分子相互作用,形成分子间氢键,蔗糖质量分数增加,此类氢键数也相应增加,导致持水能力增加,文献报道蔗糖共溶质质量分数对琼脂及黄原胶共混凝胶弹性模量及持水性质具类似影响趋势,并归因于蔗糖因富含羟基比亲水胶体分子具更强的水合能力所致[35-36]。
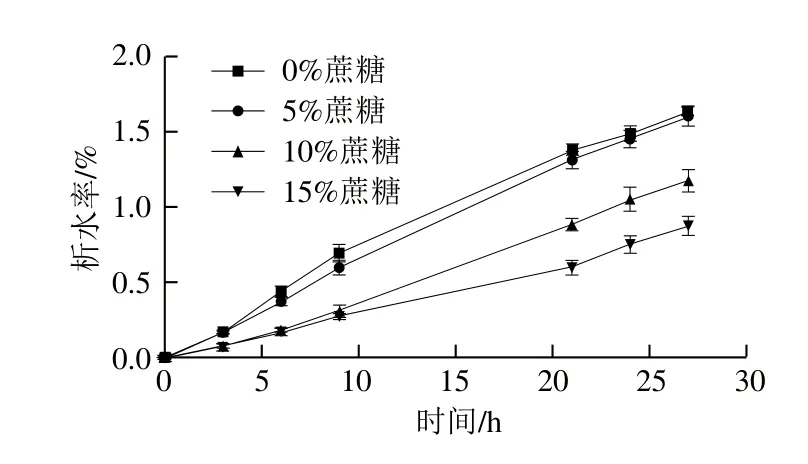
图7 蔗糖质量分数对琼脂-魔芋胶共混体系凝胶析水性影响Fig. 7 Effects of sucrose concentration on the syneresis of agar/konjac blend gels
2.6 琼脂-魔芋胶共混体系凝胶质构性质分析
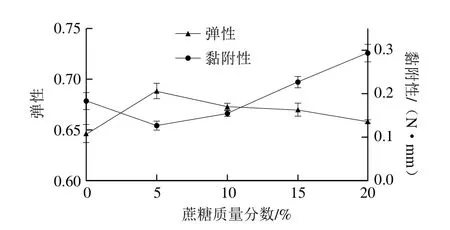
图8 蔗糖质量分数对琼脂-魔芋胶共混体系凝胶质构参数的影响Fig. 8 Effects of sucrose concentration on textural properties of agar/konjac blend gels
由图8可知,随蔗糖质量分数增加,与对照相比共混凝胶弹性值呈先增加后降低趋势,说明添加蔗糖量较少时,利于多糖分子形成双螺旋结构并促进凝胶形成,与蔗糖质量分数影响共混凝胶G’趋势结果一致。黏附性则呈先降低后增加趋势,表明较高质量分数蔗糖存在时,小分子共溶质蔗糖与水分子形成水合作用后利于对多糖分子链塑化作用,使分子链展延,不利于多糖分子链聚集并产生较强黏附作用。
2.7 琼脂-魔芋胶共混体系凝胶微观结构分析
如图9所示,与对照样相比,随蔗糖质量分数增加共混凝胶基质愈发细密化,断面区域更加平整,共混凝胶孔隙呈降低趋势,此现象可能是由于蔗糖存在因氢键作用更多的水分是以毛细水分存在,导致冻干过程,从凝胶表面逸散出去的凹洞明细减小,此与析水率的结果相一致。添加10%及15%蔗糖的共混凝胶断面微观结构呈现不规则点状白色斑点,主要是冻干过程因局部区域小分子共溶质蔗糖溶质过饱和后形成结晶所致。Maurer等[36]在考察琼脂及黄原胶体系时发现了较高质量分数蔗糖与水分子亲水胶体竞争结合时出现了类似蔗糖结晶析出现象。

图9 琼脂-魔芋胶共混体系凝胶扫描电镜图Fig. 9 SEM images of agar/konjac blend gels
2.8 琼脂-魔芋胶共混凝胶体系红外光谱分析
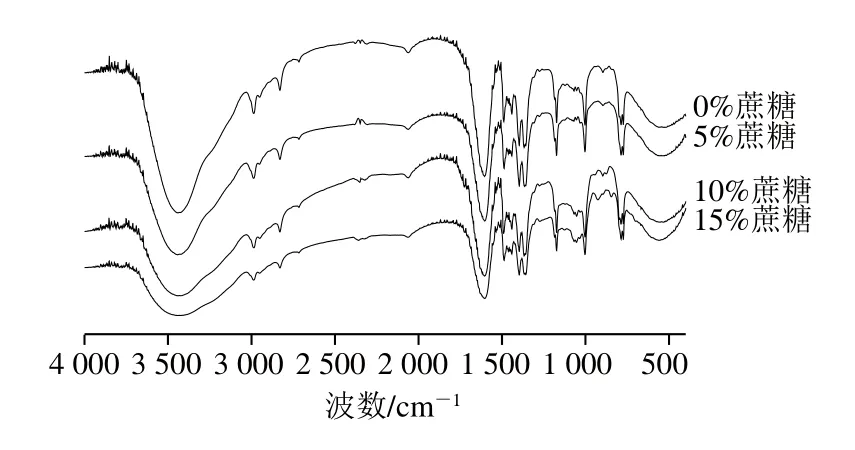
图10 琼脂-魔芋胶共混体系凝胶傅里叶红外光谱图Fig. 10 FTIR spectra of agar/konjac blend gels
FTIR是解析分子结构的有效方法,小分子共溶质与高分子体系相互作用的强弱亦可以通过振动谱带峰位置、宽度及强度的改变来确定[37]。如图10所示,4 种样品的峰形比较相似,共混凝胶在3 400 cm-1附近存在羟基伸缩振动。与对照相比,添加5%、10%及15%蔗糖后,伴随羟基振动峰的位置依次为3 445.68、3 439.71、3 427.58、3 419.08 cm-1,随蔗糖质量分数增加羟基伸缩振动峰增强并向低波数方向偏移,表明共混体系中形成氢键数更多,主要因为蔗糖与水分子结合形成了更多的氢键所致。低质量分数蔗糖的添加增强了琼脂-魔芋胶共混体系中琼脂分子间作用力,利于琼脂分子间形成螺旋结构并缠结形成三维网络结构,网络结构的稳定作用主要由氢键作用维系。但高质量分数(10%~15%)蔗糖条件下,蔗糖分子除与水分子形成氢键外,与多糖分子亦能形成氢键作用,蔗糖分子束缚水能力增强,一定程度限制了水分子运动,给多糖分子链运动提供了障碍,从而不利于琼脂双螺旋分子链结构的形成并导致凝胶网络结构弱化。
3 结 论
与对照相比,添加5%蔗糖后共混体系凝胶点温度值升高,vg明显增大,但蔗糖质量分数超过10%后,SDRa、vg均降低,但仍高于对照样,表明低质量分数蔗糖存在时可促进凝胶化,高于临界质量分数值后,弱化了凝胶形成。蔗糖共溶质质量分数对凝胶加速率的影响在零线两侧均呈先增加后降低趋势,并在添加5%蔗糖时达到最高值,表明较低质量分数蔗糖共溶质在凝胶化起始阶段可促进琼脂-魔芋胶共混体系形成网络结构,从而促进体系凝胶。蔗糖共溶质质量分数仅对高温区Ea产生显著影响(P<0.05),与对照相比,添加5%蔗糖后,Ea值由377.12 kJ/mol降低为255.49 kJ/mol,蔗糖添加量超过5%后,Ea值被升高。随蔗糖质量分数增加,共混凝胶的析水率越低,质构弹性值呈先增加后降低趋势,但黏附性则呈相反趋势,凝胶微观结构愈发细密化,断面区域更加平整,FTIR结果表明添加蔗糖可改变琼脂-魔芋胶共混体系中蔗糖分子与水分子及多糖分子间的氢键作用力,从而改变凝胶化行为。综合上述在果冻类凝胶产品实际溶胶-凝胶转变制备过程,通过选择合适共溶质质量分数来调适凝胶工序速度及优化最终制品质构、保水性等品质特性是一种潜在可用的有效方法。
