羧甲基壳聚糖对聚氨酯泡沫的改性及其对亚甲基蓝的吸附研究
2019-07-04任龙芳杜瑾瑶郗盼毅强涛涛
任龙芳, 杜瑾瑶, 郗盼毅, 强涛涛
(陕西科技大学 轻工科学与工程学院 轻化工程国家级实验教学示范中心, 陕西 西安 710021)
0 引言
合成染料广泛应用于纺织品[1]、纸张、皮革鞣制[2]、塑料、化妆品、橡胶、印染制造等行业[3,4].大量染料被排放到环境中,这对人类及水生生物产生极大的危害[5].最常见的染料去除方法有化学氧化法,吸附法和生物处理法.生物吸附法具有高效率、易操作、可重复利用、低成本等优点,是染料脱色的最佳选择[6].很多生物材料被用于开发具有高结合能力和高选择性的生物吸附剂[7].
壳聚糖及其衍生物资源丰富、可再生,聚合物链上羟基、氨基、乙酰基等官能团的存在使其易于化学改性,是性能优良的生物吸附剂[8,9].羧甲基壳聚糖是壳聚糖经羧甲基化反应后得到的一类衍生物,羧基的引入使其结合活性染料的能力大大提高[10-12].但是,羧甲基壳聚糖在水处理上的应用仍存在易聚集、分离难等缺陷,解决这些问题的方法就是将羧甲基壳聚糖嵌入聚合物基质中,使得吸附剂能够与活性染料自由的相互作用且易于与污水分离.这种聚合物基质应具有高比表面积的多孔结构及在不同环境条件下的高机械强度和稳定性,聚氨酯泡沫作为固定各种吸附剂的基质材料可以满足这些要求,因此被用作固定活性炭[13]、生物质[14]、粘土[15]等各种吸附剂的基质材料.然而将羧甲基壳聚糖嵌入聚氨酯泡沫中以除去水溶液中的亚甲基蓝的应用非常少[16].
本文以羧甲基壳聚糖(CMCTS)和端异氰酸酯基聚氨酯预聚体(PPU)为原料,根据逐步加成聚合原理制备了一种新型羧甲基壳聚糖改性聚氨酯泡沫(CMCTS-PUF),其表面含有大量的羧甲基,对阳离子染料具有较强的吸附作用,并且通过调节pH实现CMCTS-PUF的再生.通过单因素实验优化出了CMCTS-PUF的最佳合成条件,同时研究了其对亚甲基蓝(MB)的吸附性能.
1 实验部分
1.1 试剂与仪器
1.1.1 主要试剂
羧甲基壳聚糖(CMCTS),取代度:≥80%,上海麦克林生化科技有限公司;端异氰酸酯基的聚氨酯预聚物(PPU),工业品,陶氏化学公司;亚甲基蓝(MB),AR,天津市天力化学试剂有限公司;氢氧化钠(NaOH),AR,天津市河东区红岩试剂厂;浓盐酸(HCl);AR,陕西泾阳县崇文化工厂.
1.1.2 主要仪器
UV 9100型紫外可见分光光度计,莱伯泰科有限公司;SHA-C型恒温振荡器(数显),常州国华电器有限公司;TDL-50B低速台式离心机,上海安亭科学仪器厂;Vertex70型傅里叶变换红外光谱仪,德国布鲁克公司;Vega 3 SBH扫描电子显微镜,捷克TESCAN公司.
1.2 制备方法
1.2.1 聚氨酯泡沫(PUF)的制备
将10 g PPU和30 g去离子水按质量比1∶3加入反应釜中,在室温下剧烈搅拌混合60 s,得到混合溶液.然后将上述混合溶液迅速倒入托盘中,由于预聚物中异氰酸酯基(-NCO)与水反应释放出CO2气体,使得聚氨酯泡沫形成了多孔结构.在室温下干燥10 min后得到PUF.
1.2.2 羧甲基壳聚糖改性的聚氨酯泡沫(CMCTS-PUF)的制备
将10 g PPU加入反应釜中,然后称取1%、2%、3%、4%和5%的CMCTS(以PPU的质量为基准),分别溶于30 g去离子水中,再分别加入到上述反应釜中,在室温下剧烈搅拌混合60 s,得到混合溶液.然后将上述混合溶液迅速倒入托盘中,在室温下干燥10 min后得到不同CMCTS含量的CMCTS-PUF(CMCTS-PUF-1、CMCTS-PUF-2、CMCTS-PUF-3、CMCTS-PUF-4、CMCTS-PUF-5).
将托盘中的CMCTS-PUF用去离子水洗涤3次,于60 ℃下烘8 h.烘干后将其切成约0.2 g的矩形块状用于吸附实验.
1.3 标准曲线的绘制
先将吸附后的MB染料用紫外分光光度计对其吸收峰值进行扫描,扫描范围为200~800 nm,在最大吸收峰处根据峰面积估算待测样浓度范围在1~10 mg/L.
将浓度分别为1 mg/L、2 mg/L、4 mg/L、6 mg/L、8 mg/L、10 mg/L 的亚甲基蓝染料倒入比色皿中,用紫外分光光度计对其吸收峰值进行扫描,扫描范围为200~800 nm,范围内出现的最大吸收峰对应的波长即为亚甲基蓝的最大吸收波长.配制浓度分别为1 mg/L、2 mg/L、3 mg/L、4 mg/L、5 mg/L、6 mg/L、7 mg/L、8 mg/L、9 mg/L、10 mg/L的MB溶液,以蒸馏水为参比,在最大吸收波长的条件下对染料溶液进行吸光度测试,得出亚甲基蓝溶液浓度与吸光度的关系,绘制亚甲基蓝溶液标准曲线.
1.4 吸附实验
称取不同CMCTS含量的矩形CMCTS-PUF样品各0.2 g置于不同的250 mL锥形瓶中,量取浓度为100 mg/L的MB溶液50 mL于装有吸附剂的锥形瓶中,在25 ℃下恒温震荡至达到吸附平衡.取吸附后的溶液置于15 mL离心管中进行离心分离,用分光光度计于664 nm处测其上清液的吸光度值,利用MB标准曲线计算溶液中剩余MB的浓度.根据公式(1)和(2)分别计算出MB去除率与吸附容量.
qe=(C0-C)·V/m
(1)
R=(C0-C)/C0×100
(2)
式(1)、(2)中:qe为MB的平衡吸附量,mg/g;C0和C分别为吸附前后MB溶液的质量浓度,mg/L;V为MB溶液的体积,L;m为CMCTS-PUF的质量,g;R为去除率,%.
1.5 测试与表征
1.5.1 FTIR
采用薄膜法制样,取相同厚度样品,在60 ℃烘24 h后进行测试以排除样品质量、含水量对测试的影响,扫描波长范围400~4 000 cm-1,扫描次数32次.
1.5.2 SEM
在复合泡沫干燥前,取小块横截面,在真空冷冻干燥机中干燥12 h.通过扫描电子显微镜观察复合材料的表面形态和孔道结构,放大倍数为100倍.
2 结果与讨论
2.1 FTIR分析
图1为PUF和CMCTS-PUF的红外光谱图.由PUF的红外谱图可以看出,3 310 cm-1、1 652 cm-1和1 537 cm-1处分别为N-H、CO-NH和NH2的振动吸收峰,说明PUF中存在氨基甲酸酯基.1 610 cm-1和830 cm-1处为苯环的骨架振动和面外弯曲振动.2 860 cm-1、1 710 cm-1和1 222 cm-1分别对应于CMCTS-PUF中羧基的O-H伸缩振动、C=O伸缩振动和C-O伸缩振动.虽然PUF和CMCNS-PUF的大多数吸收峰相同,但是CMCTS-PUF由于受到分子间氢键的强烈影响,3 300 cm-1处N-H的伸缩振动吸收峰强度高于PUF的吸收峰.
2.2 SEM分析
图2是PUF与CMCTS-PUF的截面SEM图.从图2可以看出,所制备的泡沫均具有良好的通孔结构,这些通孔结构为复合泡沫吸附溶液中的MB染料提供了更快的交换通道,使得MB染料被更快吸附.图2(a)中PUF的泡孔大小较为均匀,孔表面光滑致密.而图2(b)中CMCTS-PUF的泡孔大小不均,表面有明显褶皱,因为有少量CMCTS聚集粘结在PUF表面,出现褶皱可以降低物质表面能而使其处于稳定状态.与PUF相比,CMCTS-PUF的孔径较小,数量较多,这说明CMCTS-PUF具有更大的表面积及更多的离子通道.这可能是因为CMCNF的加入增加了泡孔形成过程的成核位点数.无法看到CMCTS团聚体,表明CMCTS很好地融入PUF基质中.
2.3 标准曲线
图3为MB染料的全波长扫描图与标准曲线图.由图3可以得出,MB的最大吸收波长为664 nm,MB染料浓度与吸光度的关系为:y=0.025 77+0.102 42*x(R2=0.999 03).由此说明该曲线的拟合效果较好,后续可根据此标准曲线计算MB的去除率与吸附容量.
2.4 单因素实验
2.4.1 吸附时间
分别选取吸附时间为10 min、20 min、30 min、40 min、50 min、1 h、1.5 h、2 h、3 h、5 h进行实验,计算MB去除率,其结果如图4所示.
从图4可以看出,当吸附时间少于30 min时,CMCTS-PUF对MB染料的去除率明显增大,去除率达到80.6%.随着吸附时间的延长,去除率增加缓慢,吸附效率降低,在2 h时基本达到吸附平衡,去除率达到了97.1%.继续延长吸附时间至5 h后发现去除率仅增加到98.7%.整个吸附过程类似于典型的生物吸附过程,前期MB染料通过物理及化学作用快速结合到吸附剂的表面,之后,缓慢转移到吸附剂的隐蔽位置,最终由于泡沫中起吸附作用的活性位点的稳定而达到平衡[17].综合考虑,设定最佳吸附时间为2 h.
2.4.2 吸附剂用量
分别称取0.1 g、0.2 g、0.3 g、0.4 g、0.5 g CMCTS-PUF用于吸附体积为50 mL、质量浓度为100 mg/L的MB溶液,在恒温水浴震荡仪中25 ℃恒温震荡2 h后,取样、离心、测吸光度,计算去除率,其结果如图5所示.
吸附剂用量是确定吸附剂在一定吸附容量下评价吸附能力的一个重要工艺参数[18].由图5可知,CMCTS-PUF对MB优异的吸附性能,当吸附剂用量为0.2 g时,吸附容量为24.2 mg/g,去除率为97.1%,此时再增加吸附剂用量,吸附容量便大幅度降低,而去除率增加缓慢,到吸附剂用量为0.5 g时,去除率达到98.9%,而吸附容量仅为9.9 mg/g.原因是吸附剂表面上吸附位点的量随着吸附剂的量而增加,使更多的MB染料被吸附在吸附点上,因而去除率提高.而当MB的质量浓度不变时,随吸附剂用量增加,单位质量吸附剂所吸附的MB量必然降低,所以吸附容量快速下降.综合考虑吸附容量与去除率,选择吸附剂的最佳用量为0.2 g.
2.4.3 CMCTS含量
复合泡沫中CMCTS含量是影响溶液中MB染料去除率最重要的因素之一.图6为PUF及不同CMCTS含量CMCTS-PUF对MB的吸附效果.由图6可知,随着CMCTS含量的增加,CMCTS-PUF对MB的去除率逐渐升高.PUF对MB的去除率很低,仅为18.9%,这表明PUF中的氨基不能作为吸附MB的活性位点[19];当CMCTS含量增加至2%时,样品对MB的去除率达到96.5%;继续增加CMCTS含量至5%时,去除率达到97.1%,这是因为具有较高CMCTS含量的复合材料为MB染料提供了更多的吸附位点,使样品获得最大吸收效率.
在吸附相同浓度、体积的亚甲基蓝溶液时,CMCTS-PUF-5比CMCTS-PUF-2能更快达到吸附平衡.且在吸附更高浓度的亚甲基蓝溶液时,CMCTS-PUF-5的吸附容量与去除率均优于CMCTS-PUF-2.因此,综合考虑,选择CMCTS含量为5%的吸附剂.
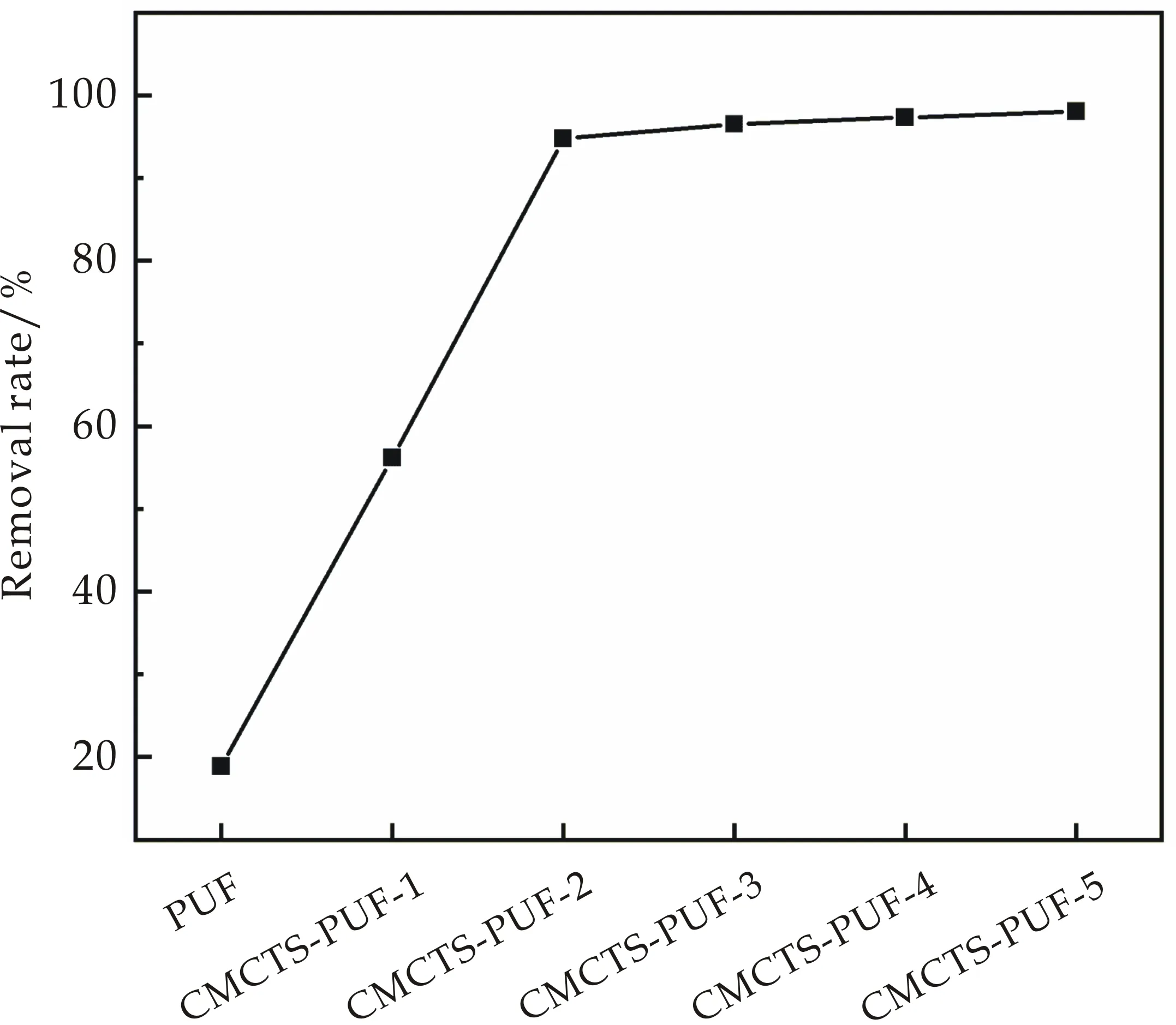
图6 CMCTS含量对吸附效果的影响
2.4.4 pH值
染料溶液的pH值对吸附过程起着重要的作用,pH值不仅影响吸附剂的表面电荷,溶液中染料的电离度和吸附剂活性位点上官能团的解离,还影响溶液中染料的化学性质[20].图7为不同pH条件下,CMCTS-PUF对染料的去除率.
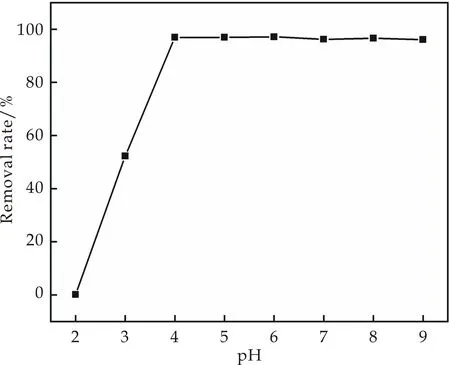
图7 pH值对吸附效果的影响
从图7可以看出,复合泡沫对pH较为敏感,当pH<4时,CMCTS-PUF对MB的去除率随pH的增大而逐渐升高;pH为4~9时对MB的去除率均在97%左右波动,说明合成的泡沫材料能在较宽的pH范围内去除MB染料.在pH=2时对染料吸附微弱归因于H+与阳离子MB分子对羧酸盐活性位点的竞争性吸附;随着pH值的增加,染料溶液的电荷密度降低,从而导致带正电的染料分子与表面带负电的吸附剂之间的电子引力增大,使吸附效果增加.
3 结论
(1)以羧甲基壳聚糖(CMCTS)和端异氰酸酯基聚氨酯预聚体(PPU)为原料,成功制备了一种表面含有大量羧甲基的新型羧甲基壳聚糖改性聚氨酯泡沫(CMCTS-PUF).
(2)本文研究结果证实,CMCTS对阳离子染料MB有很好的吸附效果.在25 ℃、不调节溶液pH的条件下,100 mg/L、50 mL MB染液的最佳吸附剂用量为0.2 g.当吸附平衡时间2 h,CMCTS含量为5%时,对MB去除率可达97.1%.
