早期肝癌射频消融术后复发时间的影响因素
2019-05-07邓俊周颜杨美蓉吴晓霞张英朱宏英陈卫
邓俊 周颜 杨美蓉 吴晓霞 张英 朱宏英 陈卫
原发性肝癌的射频消融(radio frequency ablation,RFA)治疗因其微创、不良反应小、疗效确切、费用低,而广泛应用于临床。其已被国内外多项指南推荐使用于早期肝癌的根治治疗,但临床上仍有一定的复发率。如何降低RFA术后肝癌的复发率是近年研究的热点,包括多种局部治疗的联合以及与药物的联合使用等。本研究以经皮超声引导RFA治疗早期单发肝癌75例为研究对象,回顾分析影响早期单发肝癌RFA术后复发的相关影响因素,现将结果报道如下。
资料与方法
一、病例选择
2012年7月至2016年6月原发性肝癌住院患者75例,全部病例均符合《2017版原发性肝癌诊疗规范》诊断和分期标准,其中通过动态增强CT、MRI、超声造影以及AFP等临床诊断58例,穿刺活检病理诊断17例。男性56例,女性19例,年龄29~75岁,平均(56.3±11.0)岁。纳入标准:(1)临床或病理符合原发性肝癌诊断标准;(2)因肝硬化、糖尿病、高龄、其他器官疾病、肝功能损害等因素不宜及拒绝手术治疗;(3)全部病例均为单个病灶,肿瘤最大径≤5 cm;(4)排除经皮RFA禁忌证;(5)术后1个月内经增强CT及超声造影两项影像学检查均证实消融完全;(6)1个月内经检查若有存活病灶,经再次消融或肝动脉化疗栓塞术达到完全缓解;(7)无明显腹水及黄疸(总胆红素≤51.0 μmol/L);(8)肿瘤位于特殊部位,是指肿瘤边缘距离膈顶、胆囊、下腔静脉、肝静脉主干、门静脉主干及一级分支、胃、右肾、肝包膜等结构小于0.5 cm;(9)均取得患者知情同意。排除标准:(1)既往接受过手术、放化疗及介入治疗;(2)肝功能Child-Pugh分级C级;(3)术前半年内使用影响免疫机制的药物;(4)严重凝血功能异常;(5)合并身体其他部位肿瘤性疾病;(6)合并心肺功能异常。
二、治疗方法
75例患者均在我院接受超声引导下经皮RFA,其中有38例同时接受联合胸腺肽α1治疗。
(一)RFA手术 RFA系统采用迈德医疗科技(上海)有限公司出产迈德S-1 500肿瘤射频治疗仪,射频消融针为迈德公司配套的各种型号射频消融针。术前B超确认肿瘤位置,选择合适的穿刺方向及进针深度。常规消毒铺巾后,2%利多卡因局麻后在穿刺点局部切开约0.3 cm切口,在B超引导下将射频电极针准确插至靶点部位后,推出电极子针,要求电极子针覆盖肿瘤周围0.5~1.0 cm正常肝组织。连接肿瘤射频治疗仪,B超再次确认针尖位置后进行射频消融治疗,设定为瓦控模式,输出功率100 W,当阻抗超限热凝自动停止,若病灶较大或一次消融未完全,可调节射频电极针方向和深度再次射频消融治疗。术后均给予常规保肝止血对症治疗。
(二)胸腺肽α1治疗 38例患者在经皮RFA术同时给予胸腺肽α1(日达仙,意大利蒙莎Patheon ltalia SPA.培森药厂),具体用法:术前3 d起每日皮下注射胸腺肽α1 1.6 mg,连续1周,以后隔日1次,连续2周,疗程共3周。
三、疗效评估及随访方案
(一)RFA术后的近期疗效评估 通过增强CT及超声造影两种影像学检查进行,完全消融是指原病灶坏死完全,肝内无存活病灶。术后复发判断标准:增强CT及超声造影两种影像学检查中有一项证实新生肝癌特点的结节、活动性病灶或者肝内外转移病灶。
(二)随访时间和内容 术后前3月每月、3月后每3个月随访1次检查生化及肿瘤标志物,包括肝肾功能、血常规、AFP、异常凝血酶原(DCP)等;术后1个月内复查肝脏增强CT及超声造影以确认近期疗效,以后每1~2月复查肝脏B超,每3~4月复查肝脏增强CT。随访期问,达到术后复发标准患者中止随访,采取相应治疗措施,其余患者按上述随访内容随访,直至36个月本研究随访结束。将所有患者分为早期复发组(24个月内复发)和非早期复发组(24个月后复发及至36月随访结束未复发者)。
四、统计学分析

结 果
一、肿瘤治疗及复发情况
(一)75例患者中68例术后1个月内经增强CT以及超声造影检查均证实达到完全消融,其他7例未达完全消融,其中5例经再次消融达到完全缓解,2例经肝动脉化疗栓塞术达到完全缓解。所有患者术后均未发生出血、感染、胸水等严重并发症。
(二)随访24个月内肿瘤复发31例,24个月后至36个月随访结束复发15例,随访结束时未复发29例。最短随访时间4个月,最长随访时间36个月。中位复发时间为28个月。1、2、3年肿瘤复发率分别为16.0%(12/75)、41.3%(31/75)、61.3%(46/75)。
二、影响术后复发时间的相关因素分析
在分析复发时间影响因素时,将可能的影响因素进行单因素分析,显示性别、年龄、是否合并肝硬化、甲胎蛋白、肝功能Child-Pugh分级、外周血白细胞、血小板、丙氨酸转氨酶、总胆红素、白蛋白、是否合并乙型肝炎、HBV DNA及HBsAg水平等方面,差异无统计学意义(P>0.05)。发现肿瘤大小、病灶是否属于特殊部位、是否联合胸腺肽ɑ1治疗、DCP水平是影响RFA术后复发时间因素,差异有统计学意义(P<0.05),见表1及图1-4。
三、 影响术后复发时间的多因素分析
进一步将肿瘤大小、病灶是否属于特殊部位、是否联合胸腺肽α1治疗、DCP四个因素纳入Cox回归模型进行多因素分析,结果显示肿瘤较大、病灶属于特殊部位、DCP高水平是影响复发时间的独立危险因素,联合胸腺肽α1治疗是影响复发时间的保护因素,见表2。

表1 影响射频术后复发时间的影响因素 (n=75)

图1 不同肿瘤大小患者复发曲线

图2 不同肿瘤部位患者复发曲线

图3 联合使用胸腺肽α1与否患者复发曲线
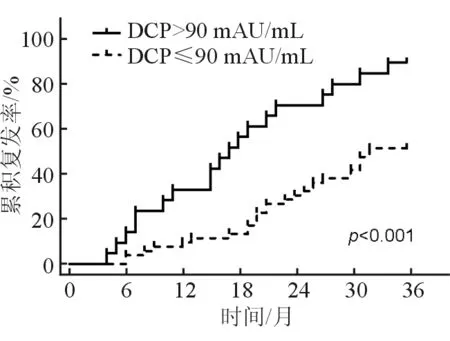
图4 不同水平DCP患者复发曲线

表2 影响单个小肝癌RFA术后复发时间的多因素分析
讨 论
目前对于手术与RFA治疗小肝癌的疗效对比研究均提示两者在术后复发率和远期生存率方面均无明显差异[1]。本文回顾性分析75例单个≤5 cm早期肝癌经皮RFA术的近期疗效及复发随访情况,完全消融率达到90.7%,中位复发时间为28个月,1、2、3年复发率分别为16.0%、41.3%、61.3%,与相关文献报道基本一致。
本研究多因素分析显示肿瘤长径>3.0 cm、特殊部位的肿瘤是术后早期复发的独立危险因素。在肿瘤亚组的分析中,肿瘤长径≤3.0 cm的1、 2、 3年累积复发率分别为13.3%、24.4%、46.7%,明显优于肿瘤长径>3.0 cm组(P=0.015);25例特殊部位肿瘤早期复发率明显高于非特殊部位(P=0.004)。分析原因可能因为直径较大的肿瘤,RFA往往很难达到一步根治的疗效;特殊部位的肿瘤往往影响布针以及消融范围,也容易出现肝包膜下出血、血气胸、胆汁瘤以及胃肠道甚至心脏损伤等并发症[2]。本研究中,术者在术前均进行超声造影等影像学充分评估,尤其对特殊部位肿瘤病灶均事先设计进针路线,评估可能发生的风险,因此未发生1例相关并发症。
DCP作为肝细胞癌的特异性肿瘤标志物已经广泛应用于肝癌的早期诊断[3-4]。Pote等[5]认为DCP水平DCP>90 mAU/mL是肝癌微血管侵犯的独立预测因子。Toyoda等[6]研究发现肝癌细胞是否有转移或治疗后是否有复发可以通过血清DCP水平变化监测。本研究提示术前DCP≤90 mAU/mL组早期复发率明显低于DCP>90 mAU/mL组(P=0.005),其52例患者中,1、2、3年复发率分别为7.7%、28.8%、50.0%。回归多因素分析同样显示,术前DCP高水平为术后早期复发的独立影响因素。对于术前DCP较高的患者,在治疗方案的选择以及术后的随访方面应引起更多的重视,以期达到满意的临床结果。
在如何提高RFA疗效、降低复发率方面,国内外研究大多主张与其他治疗手段的联合。本研究中术后1个月内影像学评估有7例患者病灶未达到完全消融,其中4例位于特殊部位,3例病灶长径≥4 cm,随后5例进行再消融、2例进行肝动脉化疗栓塞术达到完全缓解。研究表明[7-8]肝癌经手术、介入等局部治疗后联合胸腺肽α1治疗能不同程度的提高疗效、预防复发。因此,本研究也尝试在RFA治疗前后联合使用胸腺肽α1增强机体抗肿瘤免疫能力,以期提高疗效、减少复发。共有38例患者自RFA术前3 d起开始使用,共三周疗程,该亚组中1、2、3年复发率分别为8.5%、28.6%、48.6%,显著低于未使用组(P=0.027),Cox回归模型多因素分析显示为独立影响因素(P=0.012),说明联合使用胸腺肽α1治疗是RFA术后复发的保护性因素,但如何最大限度的提升其作用以及治疗方案如何进一步优化,尚需进一步深入研究。
本研究显示肿瘤较大、肿瘤位于肝脏特殊部位、术前DCP高水平是肿瘤早期复发的危险因素,联合使用胸腺肽α1是肿瘤复发的保护因素。然而本研究仅为单中心小样本研究,在相关因素中也未能涵盖肿瘤的病理学特征等,因此有较大的局限性,尚需开展更多更深入的研究。
