血清维生素K2、补体C1q肿瘤坏死因子相关蛋白3和核心结合因子a1与冠状动脉钙化的相关性研究
2019-04-23刘海玲徐炳柱郭兆文冯景辉
刘海玲 徐炳柱 郭兆文 冯景辉
151100 肇东市人民医院心血管内科(刘海玲、徐炳柱、郭兆文);150007 哈尔滨医科大学附属第一医院干部二病房(冯景辉)
血管钙化发生机制复杂,近年认为主要归因于血管平滑肌细胞(vascular smooth muscle cell,VSMC)表型的转化[1]。维生素K2(vitamin K2,VK2)与血管钙化的关系已成为研究的热点,其可通过多种维生素K依赖蛋白限制钙磷晶体生长、抑制VSMC凋亡,从而抑制血管钙化形成。而补体C1q肿瘤坏死因子相关蛋白3(complement C1q tumor necrosis factor related protein 3,CTRP3)是15种CTRP中的1种,可通过激活ERK1/2途径上调骨钙蛋白(osteopontin,OPN)、骨形态蛋白2(bone morphogenetic protein-2,BMP-2)和核心结合因子a1(core binding factor a1,Cbfa1)等成骨标记物的表达,降低收缩表型标记物sm22a和SM-α-actin的表达而促进VSMC分化[2]。此外,Cbfa1是成骨细胞的调控因子,被认为是成骨细胞分化的早期标志,在致钙化因素作用下分化的VSMC可增加Cbfa1的表达从而促进VSMC成骨样分化[3]。而Otani等[4]的动物实验表明,分化的VSMC表达的CRTP3可增加Cbfa1的表达。本研究旨在探讨人血清中VK2、CTRP3和Cbfa1水平与冠状动脉钙化(coronary artery calcification,CAC)的关系,为今后预测和防治血管钙化提供参考依据。
1 对象和方法
1.1 研究对象
本研究为病例对照研究。选取2016年6~12月就诊于哈尔滨医科大学附属第一医院并因胸痛行冠状动脉64排CT造影(coronary computed tomography angiography,CCTA)检查的患者100例,其中男性50例,女性50例,年龄35~86岁,平均(59.4±10.4)岁。排除肝肾功能不全、血液系统疾病、心肌病、心脏瓣膜病、恶性肿瘤、甲状腺及甲状旁腺疾病、感染性疾病、自身免疫性疾病、既往有过冠状动脉支架置入和旁路移植的患者。本研究方案经医院伦理委员会批准,所有入选患者均签署知情同意书。
1.2 研究方法
所有入选患者均于入院次日清晨空腹采集肘静脉血5 ml,以3 000 r/min离心10 min,取上清液速冻-80℃保存,采用酶联免疫吸附法(ELISA)测定血清CTRP3、 Cbfa1和VK2水平,试剂盒购自上海博研生化试剂有限公司。收集患者病例资料包括姓名、性别、吸烟史、高血压和糖尿病病史、总胆固醇(TC)、三酰甘油(TG)、低密度脂蛋白胆固醇(LDL-C)、高密度脂蛋白胆固醇(HDL-C)、同型半胱氨酸(Hcy)、载脂蛋白A(ApoA)、载脂蛋白B(ApoB)、钙离子(Ca2+)和磷离子(P+)等。
采用双源CT行CCTA并计算冠状动脉钙化积分(coronary artery calcium score,CACS)。检查前将患者心率控制在90次/min以下。钙化积分由钙化面积、体积及血管分布决定,采用Agatston及其修正方法计算,钙化积分=钙化灶CT峰值×钙化面积,130~199 Hu记为1分,200~299 Hu记为2分,300~399 Hu记为3分,≥400 Hu记为4分。一支冠状动脉血管的钙化总积分等于该支血管各钙化灶积分的总和,冠状动脉主要分支包括左主干、左前降支、左回旋支和右冠状动脉等,该过程由智能积分软件参与完成。
根据CCTA结果将入选患者分为CAC组60例和非冠状动脉钙化组(NCAC组)40例。其中,CAC组患者根据CACS又分为3组:轻度组(CACS<10分)23例,其中男性12例,女性11例,平均年龄(59.6±9.8)岁;中度组(CACS 11~400分)19例,其中男性10例,女性9例,平均年龄(62.2±12.1)岁;重度组(CACS>400分)18例,其中男性11例,女性7例,平均年龄(64.0±10.2)岁。
1.3 统计学方法
2 结果
2.1 两组临床资料比较
与NCAC组比较,CAC组患者年龄偏大、合并高血压和糖尿病更多,血清TC、空腹血糖、Ca2+、Hcy和ApoB/ApoA明显升高,而ApoA、HDL-C和VK2水平显著降低(均为P<0.05),见表1。
2.2 不同程度CAC组间血清VK2水平比较
NCAC组、轻度和中度CAC组的血清VK2水平明显高于重度CAC组[(3.57 ±0.59)μg/L、(3.67 ±0.40)μg/L和(3.28 ±0.80)μg/L 比 (2.40 ±0.54)μg/L],差异有统计学意义(均为P<0.05)。
2.3 VK2、CTRP3和Cbfa1之间以及与其他变量的相关分析
相关分析显示,血清VK2水平与糖尿病呈负相关,血清CTRP3水平与空腹血糖呈负相关,血清Cbfa1与ALP呈负相关(均为P<0.05),见表2。
2.4 多因素logistic回归分析CAC的独立预测因素
Logistic回归分析显示,VK2为CAC的独立影响因素,可作为CAC的一个预测因子(OR:0.251,95%CI:0.074~0.844,P=0.025),见表3。

表1 CAC组和NCAC组临床资料比较
注:ALP:碱性磷酸酶;TC:总胆固醇;TG:三酰甘油;HDL-C:高密度脂蛋白胆固醇;LDL-C:低密度脂蛋白胆固醇;ApoA:载脂蛋白A;ApoB:载脂蛋白B;ApoB/ApoA:载脂蛋白B/载脂蛋白A;FBG:空腹血糖;Ca2+:钙离子;P+:磷离子;Hcy:同型半胱氨酸;VK2:维生素K2;CTRP3:C1q肿瘤坏死因子相关蛋白3;Cbfa1:核心结合因子a1

表2 CTRP3、Cbfa1和VK2之间及与其他变量的相关分析
注:TC:总胆固醇;HDL-C:高密度脂蛋白胆固醇;FBG:空腹血糖;ALP:碱性磷酸酶;Ca2+:钙离子;P+:磷离子;VK2:维生素K2;CTRP3:C1q肿瘤坏死因子相关蛋白3;Cbfa1:核心结合因子a1
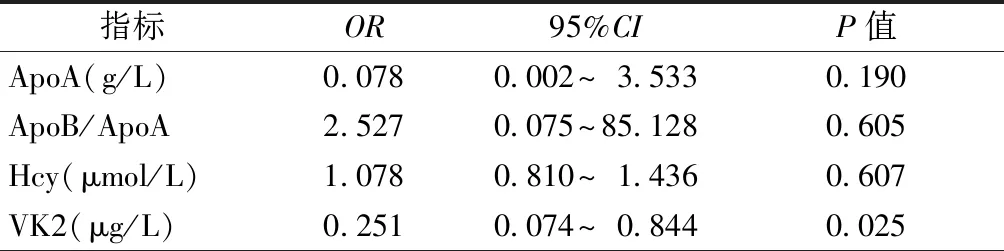
表3 多因素logistic回归分析CAC的独立预测因素
注:ApoA:载脂蛋白A;ApoB/ApoA:载脂蛋白B/载脂蛋白A;Hcy:同型半胱氨酸;VK2:维生素K2
3 讨论
CAC可使血管壁僵硬度和脆性增加,进而引起血管壁破裂、出血及血栓形成,最终导致不良心血管事件的发生。目前,有关CAC的形成机制越来越受到关注,无论是基础实验还是临床试验也越来越多。生物标记物与CAC之间的联系,已成为人们研究的热点话题。
维生素K是一种脂溶性维生素,主要有两种形式:VK1和VK2。近年在骨组织及血管中以VK2研究较多,其可通过促进成骨细胞分化和骨钙素(osteocalcin,OCN)磷酸化以及增加ALP活性和胰岛素样生长因子1而刺激成骨形成[5]。近期发现,维生素K依赖蛋白除凝血因子Ⅱ、Ⅶ、Ⅸ、Ⅹ和OCN外,还包括基质Gla蛋白、富含Gla蛋白和生长停滞特异基因6等,它们的γ羧化均需要VK2的参与[6]。基质Gla蛋白可通过与钙磷晶体结合而限制其生长,也可通过抑制BMP-2和BMP-4途径进而抑制血管钙化形成[7];生长停滞特异基因6可通过γ羧化刺激抗凋亡蛋白B细胞淋巴瘤/白血病-2的活性从而抑制VSMC凋亡;富含Gla蛋白含有大量的Gla残基,与羟磷灰石结合可调节细胞外Ca2+代谢[8]。另有实验发现,VK2通过抗氧化应激作用可减少活性氧的产生从而抑制血管钙化[9]。在本研究中,血清VK2水平在CAC组明显降低,与CAC呈负相关。相关分析显示,血清VK2水平与糖尿病呈负相关,然而糖尿病患者易伴有血管钙化,糖尿病患者中低水平的VK2又进一步加重了CAC的形成。Logistic回归分析显示,血清VK2水平降低可独立预测CAC。Scheiber等[10]实验表明,补充VK2(甲萘醌-7)可抑制小鼠主动脉钙化的发展,因此给予机体补充VK2有可能延缓血管钙化进展、减少血管钙化发生,可能成为未来防治血管钙化的一线用药。
CTRP3又称为CORS-26、Cartonectin、Cartducin和CIATNF3。VSMC可诱导CTRP3 mRNA表达,表达的CTRP3又可通过自分泌和旁分泌激活ERK1/2和P38MAPK信号通路促进VSMC增殖,最终参与血管钙化[11]。Yoo等[12]研究表明,循环中CTRP3水平与TC、TG、空腹血糖和舒张压等呈负相关。此外,Zhou等[13]体内外实验均发现,CTRP3可直接上调VSMC表达BMP-2、OPN和Cbfa1等成骨表型标记物,还可促进小鼠主动脉VSMC产生活性氧,反之又可激活ERK1/2-Runx2信号通路进一步增强VSMC成骨样分化。截至目前,尚未有研究报道循环中CTRP3水平与血管钙化的相关性,本研究分析了人血清中CTRP3水平与CAC的关系,发现CAC组和NCAC组血清CTRP3水平无显著差异,表明循环中CTRP3水平并不等同于血管钙化部位VSMC表达的CTRP3水平,血清CTRP3水平与CAC无明显关系,尚不能成为CAC的一种影响因素。
Cbfa1又称为Pebp2αA或Aml3,最近被命名为Runx2,被认为是VSMC向成骨细胞/软骨细胞表型分化的早期调控因子之一,其可通过增加OPN、OCN、核因子κB受体活化因子配基和ALP等物质表达来促进VSMC表型分化,分化的VSMC又可增加Runx2的表达进一步促进血管钙化[14]。动物研究发现,β-甘油磷酸诱导VSMC发生钙化后,Cbfα1的表达于第10天为对照组的5~6倍[15]。迄今为止,在动物钙化模型上证实了Cbfa1促进VSMC表型转化,发生表型转化的VSMC又可增加Cbfa1的表达进一步促进血管钙化,而且钙化越严重VSMC表达Cbfa1越多。本研究首次检测了血清Cbfa1水平,并分析其与CAC的关系,发现CAC组血清Cbfa1水平较NCAC组无明显降低,表明循环中Cbfa1水平并不代表血管钙化部位Cbfa1表达的水平,血清Cbfa1水平不能作为CAC的一个标记物。
血脂异常促进动脉粥样硬化的发生、发展[16]。近年来,有关ApoA、ApoB和ApoB/ApoA与冠心病的关系越来越受到关注。乔丽[17]研究发现,ApoA与CAC的严重程度呈负相关,ApoB与CAC的严重程度呈正相关。本研究发现,ApoB在CAC和NCAC两组间无显著差异,而ApoA在CAC组显著降低。目前,关于ApoB/ApoA与CAC的相关性还未有报道,本研究发现CAC组ApoB/ApoA显著升高,但回归分析显示ApoA和ApoB/ApoA不能作为CAC的独立预测因素,可能与纳入者入院前已经服用降脂药物而影响了载脂蛋白的水平有关,还可能与样本量少有关。
CAC是多因素共同作用的结果,其钙化程度严重影响患者的预后和生活质量。然而,截至目前,尚未有针对CAC的有效治疗方案。因此,研究和探索靶向物质与CAC的关系,可能成为未来防治CAC的一个新介入点。本研究为病例对照研究,不可避免会存在入选对象的选择上偏倚,且样本量也相对较少,一定程度上会影响研究结果。因此,为了进一步确定以上结论,尚需要更大样本量进行验证,并需要更深入的探讨和研究。
利益冲突:无
