治疗自身免疫病药物研究进展
2019-02-15张玲玲
张玲玲,魏 伟
(安徽医科大学临床药理研究所,抗炎免疫药物教育部重点实验室,安徽省高校抗炎免疫药物协同创新中心,安徽省高校抗炎免疫药物创新团队,安徽 合肥 230032)
自身免疫病(类风湿关节炎、系统性红斑狼疮、炎症性肠病、干燥综合征、强直性脊柱炎、慢性活动性肝炎、支气管哮喘等)是一类以局部或全身性异常炎症免疫反应为特征的炎症免疫性疾病。自身免疫病的治疗包括两个目标,第一是症状缓解和功能维持,第二是延缓组织损害进程。目前,治疗自身免疫病药物主要分为非甾体抗炎药(nonsteroid anti-inflammatory drugs,NSAIDs)、甾体抗炎药(steroid anti-inflammatory drugs,SAIDs)和改善病情抗风湿药(disease modifying anti-rheumatic drugs,DMARDs)三类。NSAIDs通过抑制环氧合酶(cyclooxygenase,COX)活性,减少前列腺素(prostaglandin,PG)生成,抑制多种细胞因子分泌而发挥抗炎、解热和镇痛作用,可改善疾病症状和体征,主要用于自身免疫病的对症治疗。SAIDs具有较强抗炎作用和免疫抑制作用,阻止炎症细胞向炎症部位聚集,抑制炎性因子释放,抑制T、B淋巴细胞增殖和分泌。DMARDs包括化学药物、天然药物以及生物制剂等,能够抑制炎症、改善症状、延缓组织破坏。DMARDs起效缓慢,用药数周或数月后,症状和体征才逐渐减轻,需长时间连续用药方可获得比较稳定的疗效。
炎症细胞因子(TNF-α、IL-1、IL-6、IL-17、IL-12、IL-23等)、细胞表面分子(CD20、CD80/86等)及其介导的信号通路(MAPKs、PI3K、NF-κB、JAK/STAT等)参与免疫细胞功能紊乱和自身免疫病的病理进程。以细胞因子、受体和信号分子为治疗靶点的靶向生物制剂,近年来获得较快发展。细胞因子和生长因子与细胞表面受体结合,触发JAK家族蛋白(JAK1、JAK2、JAK3、Tyk2)磷酸化,进一步活化STAT,启动JAK/STAT信号通路,参与炎症免疫应答。靶向JAK/STAT信号通路的多个小分子药物近年来研究活跃,已用于临床或临床试验[1]。炎症免疫反应软调节(soft regulation of inflammatory immune responses,SRIIR)药物是一类选择性调控机体组织细胞功能、基因和蛋白异常变化所致病理状态恢复至生理水平的药物。芍药苷-6-氧-苯磺酸酯(代号CP-25)是具有抗炎免疫调节作用的SRIIR药物,在治疗自身免疫病中具有潜在前景[2]。本文综述了治疗自身免疫病药物的研究进展。
1 NSAIDs
NSAIDs是治疗类风湿关节炎(rheumatoid arthritis,RA)和强直性脊柱炎(ankylosing spondylitis,AS)等自身免疫病常用药物,能有效减轻患者临床症状和体征,消除关节局部炎症反应,但是该类药只能治标,不能治本,不能控制疾病的活动及进展。NSAIDs共有的不良反应包括中枢神经系统症状(疼痛、眩晕、耳鸣等)、心血管损害(高血压、浮肿、心肌梗死、心衰等)、胃肠道症状(上腹痛、纳差、呕吐、溃疡、出血等)、造血系统改变(血小板减少)、肝肾功能不全、哮喘和皮肤药疹等。继阿司匹林之后,众多NSAIDs被研发用于临床[3],见Tab 1。
2 传统DMARDs
目前,临床常用的传统DMARDs主要包括甲氨蝶呤(methotrexate,MTX)、来氟米特(leflunomide,LEF)、环磷酰胺(cyclophosphamide,CTX)、硫唑嘌呤(azathioprine,AZA)、环孢素A(cyclosporin A,CsA)、吗替麦考酚酯(mycophenolate mofetil,MMF)、他克莫司(FK506)、柳氮磺吡啶等[4]。该类药物广泛应用于自身免疫病、慢性肾病、移植排斥反应、肿瘤等的治疗。虽然传统DMARDs化学结构和药理作用机制不尽相同,但临床药理学特征相似,即起效慢,用药数周或数月后,症状和体征逐渐减轻,长时间连续服药可获得比较稳定的疗效。如MTX抑制二氢叶酸还原酶而降低四氢叶酸形成,阻断DNA合成,能延缓关节破坏并修复骨破坏,适用于活动期RA。MTX也可治疗银屑病关节炎(psoriasis arthritis,PsA)[5]。LEF主要抑制二氢乳清酸脱氢酶活性,影响淋巴细胞嘧啶合成,可改善RA患者临床症状和实验室指标。LEF联合激素治疗狼疮肾炎(lupus nephritis,LN),疗效明显[6]。传统DMARDs的药理作用特点、临床适应症及不良反应见Tab 2[7-8]。
3 生物制剂
生物制剂通过阻断关键炎症细胞因子或细胞表面分子而发挥治疗作用,如靶向IL-1、IL-6、TNF-α和IL-17的单克隆抗体,抗CD20单抗、B淋巴细胞刺激因子(B cell activating factor,BAFF)抑制剂、T 细胞抑制剂、整合素单克隆抗体、选择性黏附分子抑制剂等[6]。
3.1细胞因子、受体及信号分子抑制剂
3.1.1TNF-α抑制剂 TNF-α抑制剂包括英夫利昔单抗(Infliximab)、阿达木单抗(Adalimumab)、依那西普(Etanercept)、戈利木单抗(Golimumab)等。Infliximab 是人鼠嵌合性TNF-α单克隆抗体,对MTX等治疗无效的RA患者具有满意疗效,早期应用的效果更好。Etanercept是人重组TNF受体p75和IgGFc段的融合蛋白,治疗RA耐受性较好。Adalimumab是针对TNF-α的全人源化单克隆抗体。通过皮下注射给药,用于治疗RA疗效确切。Adalimumab、Infliximab、Etanercept也常用于治疗银屑病。Adalimumab可用于治疗难治性重型银屑病。Infliximab对于中重度银屑病疗效较佳。Etanercept可减轻银屑病患者的疲劳感,并且对患者的烦躁、抑郁情绪予以有效缓解。Infliximab、Adalimumab和Golimumab均被美国食品药品监督管理局(Food and Drug Administration,FDA)批准用于临床治疗溃疡性结肠炎(ulcerative colitis,UC)。Infliximab是最早被FDA 批准用于治疗炎症性肠病(inflammatory bowel disease,IBD)的生物制剂,对免疫抑制剂及激素不能耐受或无效的中、重度UC 患者均有效,目前常作为UC的二线治疗药物。Adalimumab于2012年被FDA 批准用于治疗UC,可明显降低中、重度UC 患者的住院率及死亡率。Etanercept、Adalimumab有时也用于治疗AS等脊柱关节疾病。TNF-α 抑制剂主要不良反应是注射部位反应、感染、肿瘤发生风险等。其他靶向TNF-α的抑制剂见Tab 3。
3.1.2IL-6 抑制剂 托珠单抗(Tocilizumab)是抗IL-6 受体单克隆抗体,可以通过结合IL-6 跨膜受体来抑制IL-6介导的信号转导,抑制自身抗体,如类风湿因子(rheumatoid factor,RF)和抗瓜氨酸蛋白抗体(anti-citrulline protein antibody,ACPA)产生。主要用于治疗中、重度RA,也用于治疗幼年特发性关节炎(juvenile idiopathic arthritis,JIA)。随着Tocilizumab 研发成功,以IL-6信号通路作为靶点的多个生物制剂也正在研发用于治疗RA。IL-6抑制剂主要不良反应包括输液反应、感染、肿瘤发生风险、消化道溃疡、血脂检查异常、肝转氨酶升高、中性粒细胞减少等[9]。靶向IL-6的其他抑制剂见Tab 3。

Tab 1 The pharmacological mechanisms, indications in autoimmune diseases and adverse reactions of NSAIDs

Tab 2 The pharmacological mechanisms, indications in autoimmune diseases and adverse reactions of DMARDs
CD: Crohn’s disease; JIA: juvenile idiopathic arthritis; LN: lupus nephritis; MS: multiple sclerosis; PsA: psoriasis arthritis; SLE: systemic lupus erythematosus; UC: ulcerative colitis.

Tab 3 Biological agents targeting cytokines and receptors of cytokines
AS: ankylosing spondilitis; IBD: inflammatory bowel disease.
3.1.3IL-17 单克隆抗体 苏金单抗(Secukinumab)是2015年美国FDA批准用于治疗成人中、重度斑块型银屑病的IL-17单克隆抗体,对银屑病具有良好疗效。Brodalumab是人IL-17 A受体(IL-17AR)拮抗剂。2017年,美国FDA 批准治疗成人中、重度斑块性银屑病[10]。其他IL-17单克隆抗体见Tab 3。
3.1.4抗IL-12/23单克隆抗体 目前应用较广的抗IL-12/23抗体为优特克单抗(Ustekinumab),美国FDA于2009年批准用于银屑病的治疗,临床疗效明显优于其他生物制剂[11]。其他抗IL-12/23单克隆抗体见Tab 3。
3.2抗CD20单抗利妥昔单抗(Rituximab)是靶向B细胞CD20的嵌合鼠/人单克隆抗体,该抗体与CD20特异性结合,通过补体依赖性细胞毒性和抗体依赖性细胞介导的细胞毒性,诱导B细胞凋亡。2005年,Rituximab获得批准用于治疗TNF-α拮抗剂疗效不佳的RA患者,与MTX联用适用于治疗成年中度严重活动性RA,也可与CsA联合用药。Rituximab可明显改善SLE患者蛋白尿、血清白蛋白,并可减少维持阶段激素的剂量,对活动期LN诱导治疗,缓解率升高,系统性红斑狼疮(systemic lupus erythematosus,SLE)活动度评分明显降低。不良反应表现为1 000 mg首次治疗,30%病人出现皮疹,滴注部位反应、原有心脏病加重、轻微和可逆性出血以及真菌、细菌、病毒感染等。严重或活动性感染禁用,可导致B细胞耗竭[12]。其他抗CD20单抗见Tab 4。
3.3BAFF抑制剂
3.3.1贝利木单抗(Belimumab) Belimumab是抗可溶性BAFF人源化IgG1型单克隆抗体。Belimumab是近50多年来获批用于治疗SLE的首个生物制剂,2011年获得美国和欧盟批准,用于自身抗体阳性的成年SLE治疗。Belimumab能抑制BAFF的生物活性,从而降低SLE抗体水平,控制病情发展,可降低SLE治疗对激素的依赖性,抑制疾病活动性。2016年,美国风湿病学会报道,75.6%的患者可获得临床缓解,而且躯体疼痛、总体健康、生理功能、生理职能、社会功能、生命活力6项健康相关生活质量功能评分均明显改善。在激素和免疫抑制剂基础上加用Belimumab,能够降低LN的复发率。Belimumab适用于治疗活动性、自身抗体阳性的正在接受标准治疗的SLE成年患者[13]。有重要器官受累的SLE患者接受Belimumab治疗可取得明显疗效。Belimumab治疗RA处于Ⅱ期临床试验阶段,ACR20 应答率为34%。Belimumab常见不良反应包括恶心、腹泻、发热、鼻咽炎、支气管炎、失眠、肢体疼痛、抑郁、偏头痛等。
3.3.2阿塞西普(Atacicept) Atacicept是BAFF受体TACI胞外区和人IgG1的Fc片段构建而成的TACI-Ig融合蛋白。动物实验中,TACI-Ig融合蛋白能明显抑制关节炎症反应,并能抑制骨和软骨的破坏以及疾病的发展。Ⅰb期临床试验结果表明,TACI-Ig能降低血清免疫球蛋白、RF及抗ACPA抗体水平。治疗12 周后,32%的患者达到ACR20应答。IgM、IgG、IgA及RF水平明显降低。TACI-Ig治疗SLE患者,可减少红斑样皮损发生率,防止复发,提高生活质量。目前,TACI-Ig 已进入非肾炎SLE患者的II/Ⅲ期临床试验[14]。
3.4T细胞抑制剂阿贝西普(Abatacept)是由免疫球蛋白IgG1的Fc区和细胞毒T淋巴细胞抗原4(cytotoxic T lymphocyte-associated antigen 4,CTLA4)细胞外结构域组成的融合蛋白,是选择性T细胞共刺激抑制剂。Abatacept通过与抗原递呈细胞上的CD80和CD86结合,抑制T细胞激活,从而抑制炎性因子如TNF-α、IFN-γ和IL-2 的产生。临床适用于经1种或多种传统DMARDs应答不足的中、重度活动性RA患者,也可用于JIA。Abatacept可降低血清lL-6、RF、C-反应蛋白、MMP-3及TNF-α水平,延缓组织结构性破坏进程,减轻症状和体征。不良反应为上呼吸道和泌尿道感染、恶性肿瘤等。另外,Abatacept治疗干燥综合征(Sjogren syndrome,SS)目前处于Ⅲ期临床试验阶段。Abatacept能够明显降低SS疾病活动度,改善疼痛和疲劳等症状。Abatacept也用于治疗PsA[15]。
3.5整合素单克隆抗体
3.5.1那他珠单抗(Natalizumab) Natalizumab是重组α4-整合素单克隆抗体,能阻止激活的T淋巴细胞通过血脑屏障。2004年通过FDA快速通道审批,临床上用于治疗复发性多发性硬化症(multiple sclerosis,MS)和CD。MS复发率可降低68%。常见不良事件包括头痛、呼吸道感染和疲劳。由于发生罕见不良反应“进行性多灶性白质脑病(progressive multifocal leukoencephalopathy,PML)”,于2005年撤市。后因疾病治疗的迫切需求,2006年6月,FDA同意其在风险最小化计划方案下重新上市[16]。
3.5.2维多珠单抗(Vedolizumab) Vedolizumab是一种全人源化IgG单克隆抗体,能够特异性拮抗α4β7整合素。2014年,FDA批准用于对TNF拮抗剂或免疫抑制剂疗效不佳或不能耐受的中、重度UC治疗。相比于抗TNF-α 制剂,Vedolizumab起效较慢,治疗6周后效果才明显。不良反应有上呼吸道感染、鼻咽炎、腹痛、恶心、发热、关节痛等,严重不良事件报道包括严重感染、恶性肿瘤等[1]。
其他单克隆抗体生物制剂见Tab 4。
4 JAK靶向小分子抑制剂
许多促炎症细胞因子信号通过不同途径,激活JAK/STAT信号通路,JAK/STAT进一步介导下游信号,参与自身免疫病细胞增殖、活化、抗体和细胞因子产生等病理过程。特异性抑制JAK/STAT信号通路,可阻断细胞因子的级联放大作用,从而改善自身免疫病的病理和临床表现[17]。JAK抑制剂(Tofacitinib、Baricitinib、Upatacitinib、Filgotinib等)通过抑制细胞因子和生长因子的信号转导,进而抑制免疫细胞功能,包括T细胞、B细胞、巨噬细胞、树突细胞等。
4.1托法替尼(Tofacitinib) Tofacitinib为靶向JAK3的抑制剂,也有相对弱的JAK1活性,于2012 年被FDA 批准治疗RA。Tofacitinib能够在TNF单抗耐药或不应答的患者中产生良好应答,可以缓解和降低疾病活动性。Tofacitinib可治疗SLE、MS、AS、UC、CD、皮肌炎等自身免疫病,目前处于临床试验阶段[18]。Tofacitinib说明书上有严重感染和恶性肿瘤风险增加的黑框警告。
4.2BaricitinibBaricitinib是JAK1/2选择性抑制剂,具有轻度抗酪氨酸激酶2(tyrosine kinase 2,TYK2)活性和极少抗JAK3活性,治疗对传统DMARs无应答或不耐受的中、重度成人RA,可降低健康问卷评分和关节X线进程,显示较高的ACR 20/50/70应答率和良好耐受性。Baricitinib治疗银屑病、糖尿病肾病、过敏性皮炎正在临床试验阶段。
4.3FilgotinibFilgotinib为JAK1选择性抑制剂,在临床中显示出与Tofacitinib类似的疗效,但安全性有所提高,特别是淋巴细胞减少的症状大大缓解。Filgotinib治疗RA、SLE、MS、AS、UC、CD、银屑病关节炎等自身免疫病,目前处于临床试验阶段。近期研发的其他小分子JAK 抑制剂见Tab 5。
5 天然药物
用于治疗自身免疫病的天然药物包括苷类和生物碱,苷类药物如白芍总苷、人参总苷、绞股蓝总苷、黄芪甲苷、雷公藤总苷、三七总皂苷等,生物碱类如青藤碱、川乌总碱、槐果碱、雷公藤新碱等。
5.1雷公藤总苷(tripterygiumglycosides,TG) TG是雷公藤根部提取物,为雷公藤的主要有效成分,可抑制T细胞增殖、自身抗体产生及炎症细胞因子IL-1、IL-6、IL-8、TNF-α和PGE2产生,具有较强抗炎和免疫抑制作用。临床上,TG常联合小剂量MTX治疗RA。TG改善SLE临床症状,能降低γ-球蛋白,使抗核抗体ANA转阴或滴度下降。TG联合泼尼松治疗LN远期疗效较好。TG也用于治疗银屑病,改善局部微循环。TG不良反应主要有皮肤过敏反应及心血管、消化、造血、神经、生殖系统不良反应等,还可引起脱发、色素沉着、腰痛等。TG引起月经紊乱及精子活力降低,数量减少,停药可恢复正常。孕妇忌服,老年患者及严重心血管病的患者慎用[19]。
5.2白芍总苷(totalglucosidesofpaeony,TGP) TGP是从白芍中提取的有效部位,其成分包括芍药苷、羟基芍药苷、芍药花苷、芍药内酯苷、苯甲酰芍药苷等,其中芍药苷是TGP的主要活性成分。TGP具有抗炎免疫调节作用,抑制PGE2、 IL-1、LTB4、TNF-α等细胞因子产生,调节免疫细胞信号转导。TGP作为天然药物来源的Ⅱ类化学药品被批准上市治疗RA,可改善RA患者临床症状和体征,降低血沉和RF。TGP治疗SLE和LN患者,能有效下调血清IL-6、IL-8、IL-18、TNF-α和INF- α水平。TGP 可减少每日激素和免疫抑制剂用量,降低复发及感染率。TGP治疗SS可改善口干、眼干症状,降低血沉,减少其饮水量等临床症状,并可长期应用。TGP联合硫酸羟氯喹治疗SS患者,其口干、眼干症状评分及饮水量均低于单独硫酸羟氯喹治疗的患者。TGP治疗银屑病可抑制细胞因子分泌,改善银屑病患者症状,也可降低阿维A在银屑病治疗中的不良反应。TGP不良反应少,发生率低且轻微,偶有软便和稀便,长期使用患者耐受性好。

Tab 4 Biological agents targeting molecules on cell surface and receptors
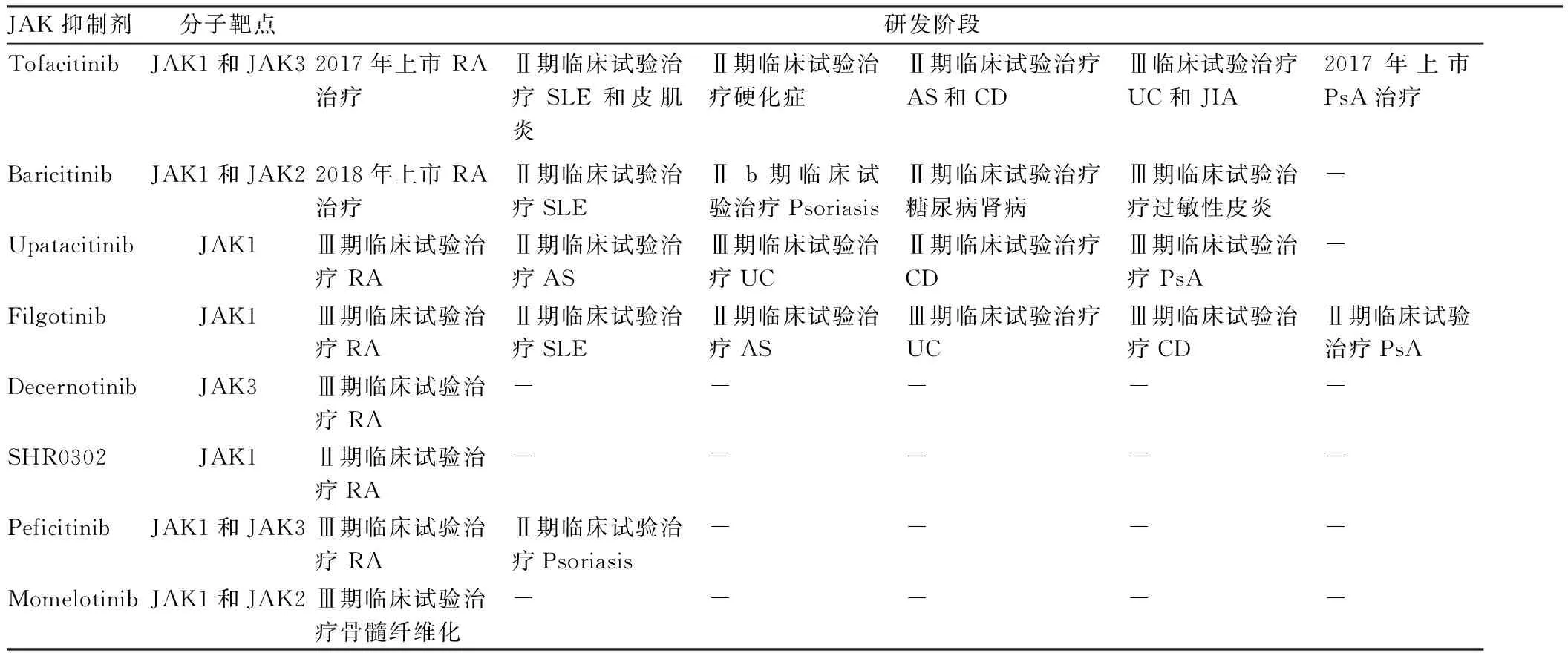
Tab 5 Development of JAK inhibitors
5.3青藤碱(sinomenine) 青藤碱是从青风藤中提取的生物碱,有较强的抗炎镇痛及免疫抑制作用,可抑制淋巴细胞增殖,降低培养细胞上清液中IL-1、IL-6、TNF等炎症细胞因子浓度。临床上,青藤碱可有效缓解RA疼痛和局部炎症。青藤碱不良反应显示,少数病人出现皮疹或白细胞减少,停药后即可消失。对本品过敏者禁用,孕妇及哺乳期妇女慎用[20]。
6 SAIDs
糖皮质激素(glucocorticoid)起效快,可用于控制急性期病变,可减少T淋巴细胞、嗜酸性粒细胞和单核细胞,抑制白介素合成和释放,降低补体和免疫球蛋白。常与传统DMARDs药物联合应用,延缓RA早期关节破坏,改善关节功能。糖皮质激素是治疗SLE最有效的药物之一,特别是治疗LN的首选基础药物。对控制IBD急性发作有较好疗效,有效率高达90%,主要用于中、重度或经氨基水杨酸类制剂治疗无效的UC、活动性及儿童和青春期生长发育迟缓的CD等。糖皮质激素不良反应多,停药后会复发,目前临床多主张与其他免疫抑制剂联合使用。近些年研究表明,低剂量糖皮质激素有疾病调修特性,特别对早期RA患者,可减慢RA病情进展,不良反应小。糖皮质激素不作为治疗RA首选药物,但在下述情况可选用:①伴随类风湿血管炎,包括多发性单神经炎、类风湿肺及浆膜炎、虹膜炎等;②在重症RA患者过渡治疗,可用小量糖皮质激素快速缓解病情,一旦病情控制,应首先减少或缓慢停用糖皮质激素;③经正规DMARDs治疗无效患者,可加用小剂量糖皮质激素;④对于关节肿胀明显、受累关节少、全身治疗有禁忌的患者,可行关节腔内注射,此疗法与口服相比全身不良反应小,可短期小剂量应用[3]。
7 SRIIR药物
上述NSAIDs、SAIDs、传统DMARDs、生物制剂、JAK抑制剂等治疗自身免疫病,疗效确切,但也存在胃肠道症状、免疫抑制、骨髓抑制、感染、新生肿瘤等不良反应。特别是靶向细胞因子、受体或信号分子的药物,通过阻断某一分子或受体,而完全阻断下游信号,导致细胞功能过度抑制,甚至凋亡,这可能是临床出现不良反应的重要机制之一。因此,研发具有抗炎免疫调节作用的SRIIR药物将是研究者关注的热点。SRIIR药物是一类选择性调控机体组织细胞功能、基因和蛋白异常变化所致的病理状态恢复至生理水平的药物,其作用机制可能是调控异常信号通路中某一个或几个关键信号分子的活性,来适度恢复机体稳态平衡,在发挥治疗作用时,尽量不损害生理功能,以减少不良反应。芍药苷-6-氧-苯磺酸酯(代号CP-25)来自于天然药物活性成分芍药苷的结构修饰[21]。CP-25能够通过下调炎症介质的产生和免疫应答而抑制大鼠佐剂性关节炎和小鼠胶原性关节炎的炎症,减轻骨损伤[22-23]。CP-25缓解SS模型小鼠症状,增加流涎率,减少腺体组织T细胞浸润,降低血清细胞因子IFN-γ、IL-4、 IL-6和IL-17A水平[24]。体外,CP-25通过下调CD40、CD80、CD83、CD86和MHC-Ⅱ的表达,来抑制PGE2或TNF-α刺激的树突状细胞成熟。CP-25下调BAFF刺激的B细胞增殖,下调CD19+B细胞、CD19+CD20+B细胞、CD19+CD27+B细胞和CD19+CD20+CD27+B细胞百分比,抑制BAFFR、TRAF2和p52的表达。CP-25与Etanercept、Rituximab疗效比较,CP-25是适度下调上述异常升高的指标,而Etanercept和Rituximab是过度抑制上述指标至正常水平以下[25]。进一步探讨CP-25的作用机制和调控靶点,发现CP-25对一些信号通路中关键调节蛋白的活性有调控作用,进一步调控异常信号通路。这些研究提示,CP-25可能是不良反应少、新的SRIIR药物。
8 总结与展望
总之,随着对自身免疫病病理机制的深入阐明和新药物靶点的发现,治疗炎症免疫病的药物除了NSAIDs、SAIDs、传统DMARDs外,靶向细胞因子和细胞表面分子的新型生物制剂获得较快发展。生物制剂通过阻断炎症细胞因子或细胞表面分子而发挥治疗作用,如靶向IL-1、IL-6、TNF-α和IL-17的单克隆抗体,抗CD20单抗、BAFF抑制剂、T细胞抑制剂、整合素单克隆抗体、选择性黏附分子抑制剂等。靶向JAK/STAT信号通路的多个小分子药物,如Tofacitinib、Baricitinib、Upatacitinib、Filgotinib等,近年来也被研发应用于临床。这些药物疗效确切,但也存在胃肠道症状、免疫抑制、骨髓抑制、感染新生肿瘤等不良反应。研发具有抗炎免疫调节作用的SRIIR药物,将是研究者追求的目标。CP-25可能是新的SRIIR药物,治疗自身免疫病将具有潜在前景。控制炎症免疫反应相关细胞过度活化,且不损害其生理功能的SRIIR药物,是治疗自身免疫病药物研发的新策略和主要方向之一。
