RA患者骨密度的特点及影响骨折风险的因素
2018-12-19康丽荣滑雅娜陈娜王永福刘媛
康丽荣 滑雅娜 陈娜 王永福 刘媛
内蒙古科技大学包头医学院第一附属医院,内蒙古 包头014010
RA是一种以关节侵蚀破坏为主要表现的系统性自身免疫性疾病,最终导致关节软骨、骨组织结构的广泛破坏和功能障碍,致残率高。患者早期即可出现全身性骨质疏松,这是继发性骨质疏松的重要原因之一[1]。RA 继发骨质疏松的发病机制尚不明确,但涉及多种因素。目前有研究显示Th17与Treg的失衡、炎性细胞因子的浸润、RANKL信号通路的活化等[2-3]在RA 继发骨质疏松过程中发挥重要作用。本研究旨在观察RA患者3D骨密度和二维骨密度的变化及骨折的发生率,并分析RA患者骨量流失的影响因素,为RA患者的早期骨质疏松的防治提供理论依据。
1 材料和方法
1.1 研究对象及评估指标
本研究纳入了2016年1月至2017年12月就住我院(包头医学院第一附属医院)及门诊检查的受试者149例。男性40例,女性109例。其中正常对照组的平均年龄为(59.2±8.7)岁,RA病例组平均年龄(61.1±8.8)岁,RA患者的诊断依据2009年ACR/ EULAR提出的RA分类标准。两组人群在年龄、性别、既往骨折史、一级亲属骨折史、吸烟饮酒史、有无糖尿病史、有无肾病史、有无甲状腺病史之间的比较差异无统计学意义 (P>0.05),但RA患者激素的使用与正常对照组存在差别(χ2=38.651,P<0.05),两组受试者的一般资料见表1。收集RA患者的临床资料并进行疾病活动度的评分(DAS28), DAS28=[0.56×(压痛关节数)1/2+0.28×(肿胀关节数)1/2+0.70×In(血沉)]+0.014×健康状况评分,DAS28>5.1为疾病高度活动;DSA28>3.2为疾病活动;DAS28<2.6为疾病缓解。两组人群进行跌倒评分及FRAX骨折风险的评估。
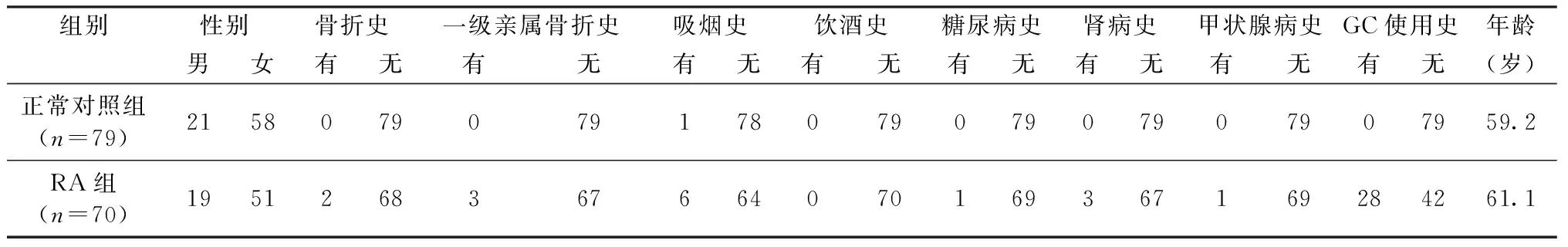
表1 正常对照组人群与RA患者一般资料的比较Table 1 Comparison of general data between normal controls and RA patients
1.2 骨密度测定
采用法国引进的型号为OSTEOCORE的双能X线骨密度测定仪,对每个研究对象进行股骨的骨密度测定。骨质疏松诊断参照2011年WHO推荐的骨质疏松的诊断标准,骨密度低于同性别、同种族健康成人的骨峰值不足1个标准差为骨量正常;骨密度降低1~2.5个标准差之间为骨量减少,降低≥2.5个标准差则为骨质疏松,符合骨质疏松诊断标准同时伴有一处或多处骨折时为严重骨质疏松。测定股骨BMD、T值及常用的3D骨密度评价指标(骨皮质厚度、体积骨密度)。
1.3 统计学处理
采用SPSS 13. 0统计软件, 两组之间定量资料的比较符合正态分布采用独立样本t检验,非正态分布采用U检验;计数资料比较采用卡方检验, 理论值<5时采用Fisher’s确切概率法;分析连续变量之间的相关性采用Pearson相关,P<0.05为差异具有统计学意义。
2 结果
2.1 RA患者股骨3D体积骨密度的变化
比较RA组患者与对照组健康人群股骨颈、大转子、转子间隙、全股骨的3D体积骨密度值,结果表明RA组上述部位的体积骨密度较正常对照组人群明显降低,无论是皮质骨还是骨小梁的体积骨密度都明显低于正常对照组(P<0.05),表2。
2.2 RA患者3D股骨平均骨皮质厚度的改变
分析正常对照组及RA组的股骨颈、股骨转子、股骨干3个部位的前、中、后节段,以及侧面和总体的平均骨皮质厚度,结果表明RA组患者股骨颈、股骨转子及股骨干各节段(除外股骨干中节段)的平均骨皮质厚度明显低于正常对照组,差异有统计学意义(P均<0.05),见表3。
2.3 RA患者股骨、髋部二维骨矿密度(BMD)的变化
对两组人群股骨颈、股骨转子、转子间隙、Ward三角区、整髋等部位的平均骨矿密度进行比较,结果表明RA组的骨矿密度明显低于正常对照组,差异有统计学意义(P均<0.01),表4。
2.4 RA患者的跌倒评分和骨折风险性评估
两组人群的跌倒评分及骨折风险度比较,无论有没有BMD,RA组患者的跌倒评分,以及腰椎和髋部的骨折风险均明显高于正常对照组,差异具有统计学意义(P<0.05),见表5。
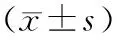
表2 RA患者与正常人3D体积骨密度变化的比较Table 2 Comparison of 3D volume bone density between RA patients and normal people
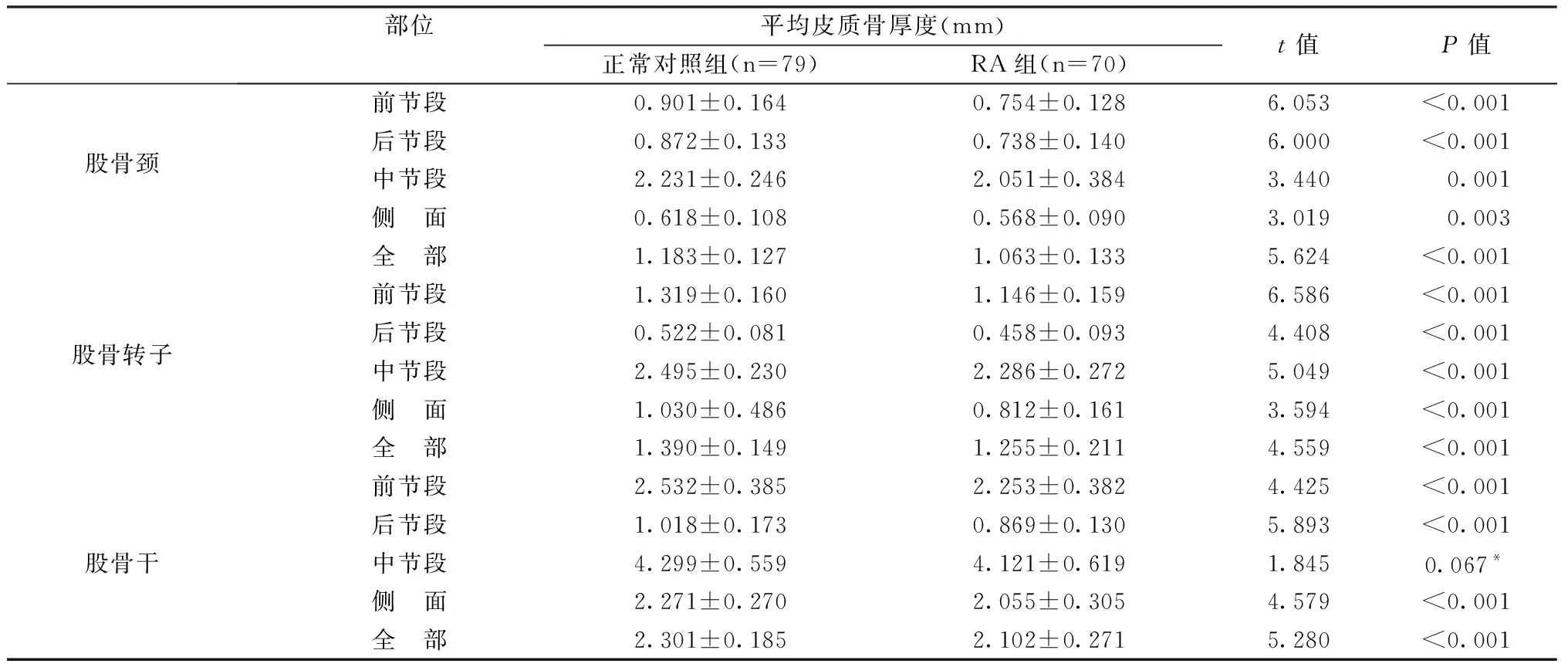
表3 RA患者与正常人平均骨皮质厚度的比较(mm)Table 3 Comparison of mean bone cortical thickness between RA patients and normal people (mm)

表4 RA患者与正常人二维BMD的比较Table 4 Comparison of 2-D BMD between RA patients and normal people
2.5 RA患者疾病活动度、激素的使用与骨量之间的关系
分析RA患者疾病活动度DAS28与骨密度的相关性,结果表明:DAS28评分与患者骨密度无明显相关性(r=-0.085,P>0.05),图1;同时,对RA患者使用激素和骨量之间的关系进行分析,结果提示:激素的使用与RA患者骨量流失相关(χ2=12.366,P<0.05), 表6。
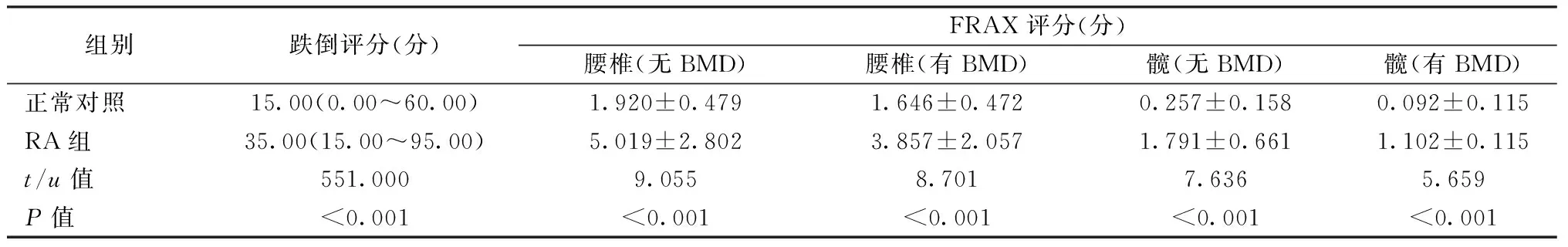
表5 RA患者与正常人跌倒评分和骨折风险性的比较Table 5 Comparison of fall score and fracture risk between RA patients and normal people
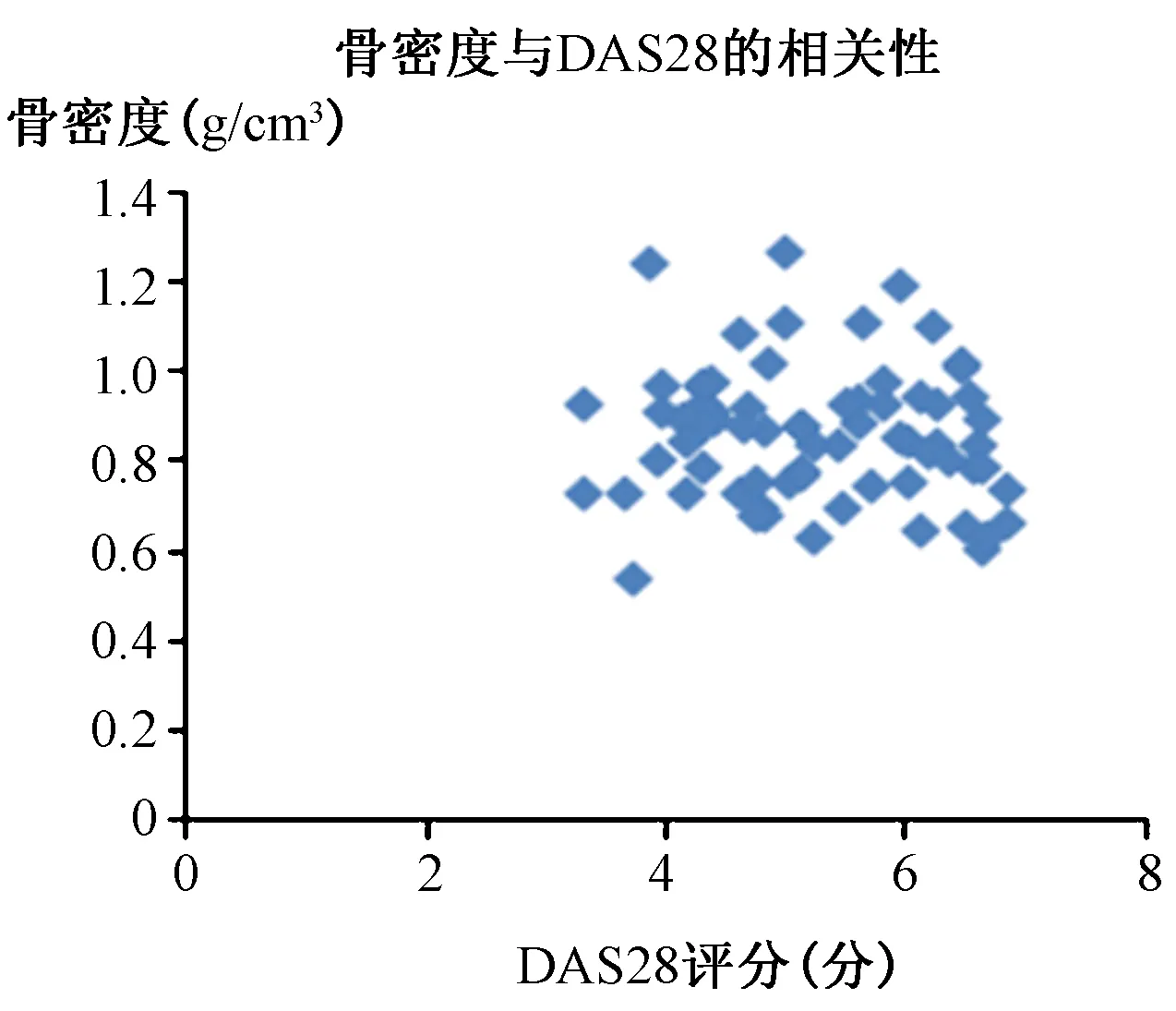
图1 RA患者疾病活动度与骨密度的关系Fig.1 Relationship between disease activity and BMD in RA patients

RA患者分组使用激素未使用激素骨量流失组(n=28)244骨量正常组(n=42)1725χ2值12.366P值<0.001
3 讨论
骨质疏松是RA骨侵蚀的一种表现,随着RA患者病程的延长,其骨密度明显低于健康人群,研究报道RA并发骨质疏松的发病率显著高于健康人群,在RA继发骨质疏松的患者早期X线上即可观察到软骨及其下面出现骨的部分吸收及关节周围的骨质疏松,其破坏度大小与骨矿丢失量相平行[4]。随着骨质疏松症状不断加重,骨折的风险相应增加,严重影响患者生活及生存质量。与之前的研究结果相符,本研究结果同样表明RA患者骨密度明显减低,骨折风险性明显高于健康人群。近年来,有学者认为炎性介质的大量产生在RA患者继发骨质疏松发病过程中发挥重要的作用[5],其中IL-17 是近些年来新发现的一种主要由Th17 细胞分泌的促炎因子,通过诱导炎性细胞(巨噬细胞、中性粒细胞等) 分泌IL-6、IL-8、TNF-α等炎性因子,后者进一步放大炎症级联反应,从而在RA 发生发展中发挥关键作用[6]。Taneja等[7]的研究中发现IL-17 主要是借助诱导软骨产生一氧化氮合酶(NOS)来刺激滑膜组织高表达MMP-1、2、9、13,同时减弱蛋白聚糖和胶原对基质的修复作用,从而起到破坏细胞外基质和软骨合成的作用。也有学者认为RA并发骨质疏松的机制可能是与机械因素、骨代谢失衡、长期应用生物制剂等相关,但尚无确切定论[8-9]。也有部分文献报道认为EBV 感染也是诱发RA继发骨质疏松的一种重要的环境因素,并且EBV有可能通过多种途径参与RA患者骨量流失的发生发展[10]。本研究结果发现与正常对照组人群相比,RA患者股骨的3D体积骨密度及平均骨皮质厚度都明显减低,股骨、髋部的二维BMD也明显减低,表明RA患者存在明显的骨量流失,同时,本研究还发现RA患者的骨量流失表现在皮质和小梁的体积骨密度均降低,不是单一的皮质改变或者小梁的改变,具体的影响因素还需要进一步探讨。
RA引起骨密度减少的本质为骨转换异常,已知骨转换指标分骨形成和骨吸收两项指标,前一项是指成骨细胞活动及骨形成时的代谢产物,后者则代表破骨细胞的活动及骨吸收时的代谢产物[11]。本研究通过测定3D体积骨密度值、平均骨皮质厚度及二维BMD值并与健康人群相比,发现RA 合并骨质疏松患者股骨颈、Ward三角区BMD、体积骨密度、平均骨皮质厚度明显降低,且具有统计学意义(P<0,05),与Roux等[12]的研究结果一致;且本研究结果表明股骨体积骨密度的改变及各节段平均骨皮质厚度的改变趋势与二维BMD的改变趋势一致,可能与RA患者的骨修复功能下降,骨吸收多于骨形成,导致骨体积密度降低和骨小梁的变细、数量减少及平均骨皮质厚度的变薄有关。同时,本研究对正常对照组人群和RA患者的跌倒评分和FRAX评分进行分析,结果发现与正常对照组人群相比,RA患者的跌倒风险及骨折风险性明显高于对照组。因此,基于RA患者出现骨密度减低以及发生骨量流失的风险较正常人明显升高,易导致骨质疏松,骨折风险亦增加,故及时测定RA患者的BMD及骨代谢相关指标以便较早发现骨量流失及骨质疏松、减少骨折危险性,并进行早期合理的干预,尤其是对早期RA患者,应积极控制疾病进展及骨破坏。
在生理情况下皮质醇及其类似物为成骨细胞和破骨细胞功能调节和分化的必需激素,可以增加成骨细胞的凋亡,延长破骨细胞的寿命,抑制骨形成,促进骨吸收[13],对骨组织的生长、发育与代谢产生不利影响,导致BMD和骨强度下降,从而出现继发骨质疏松[14-15]。因而激素的使用一方面可以缓解RA骨质破坏,改善临床症状,另一方面也可显著影响骨的微结构,降低骨强度,增加骨质疏松的风险。骨质疏松症作为RA的常见并发症, 尤其在长期糖皮质激素治疗者中骨量丢失表现的更为明显,骨折的风险增加,与既往研究中认为的GC的累积量是骨密度(BMD)减少的独立相关因素一致,骨密度的下降与激素累积剂呈显著正相关[16],且骨侵蚀性病变与低BMD 之间呈高度相关[17]。本研究同样表明,与正常对照组相比,RA患者激素的使用与RA骨量流失有一定的相关性,这与文献[18]报道结果一致,因此RA患者的激素使用应该遵循小剂量、短疗程的原则,合理的使用糖皮质激素对于预防RA患者的骨质疏松具有重要的意义。
综上所述,重视RA患者的骨量流失,加强对RA并发骨质疏松的早期预防和诊疗,积极控制RA病情活动,合理使用糖皮质激素,对RA患者的骨健康至关重要。定期对RA患者进行BMD监测,对骨质疏松的潜在危险因素进行评价,客观评价及预测骨质疏松性骨折发生的风险,以期尽可能降低RA患者骨质疏松及骨折风险的发生。
