重组普鲁兰酶在枯草芽孢杆菌中的高效表达
2018-11-06王海叶燕锐刘欣王斌潘力
王海,叶燕锐,刘欣,王斌,潘力
(华南理工大学生物科学与工程学院,广东广州 510006)
普鲁兰酶(Pullulanase,EC3.2.1.41)是α-淀粉酶家族 GH13中的一种脱支酶,最早由 Bender和Wallenfels发现并命名[1,2]。它能够以内切方式专一性地水解普鲁兰多糖、淀粉和糖原等多糖中的α-1,6糖苷键并形成直链淀粉[3]。在食品加工行业的大部分淀粉质原料中,支链淀粉占总淀粉质量约为70%~95%[4]。在支链淀粉中出现约每20~25个葡萄糖残基中存在一个 α-1,6糖苷键,所以支链淀粉中约含有4%~5%的α-1,6-糖苷键[5]。支链的存在阻碍淀粉的分解,影响了淀粉的利用和产品的质量,造成资源浪费。普鲁兰酶能专一性地切断支链淀粉中的 α-1,6-糖苷键,其转化率可达100%[6],因此普鲁兰酶在提高淀粉利用率、降低原料消耗及提高产品质量方面有着相当巨大的价值,在淀粉加工业中有良好的市场前景。
自从1966年Bender和Wallenfels通过产气杆菌(Aeorbaetere aerogenes)发酵获得普鲁兰酶以来[1,2],各国的科研人员经过广泛深入研究,获得了不同来源微生物的普鲁兰酶。迄今,已报道的有来自 Bacillus acidopullulyticus[7]、 Bacillus naganoensis[8,9]、Anoxybacillus sp. SK3-4[10]、Bacillus megaterium[11]、Thermus thermophilus HB27[12]以及 Bacillus subtilis 168[13]等微生物的普鲁兰酶基因,这些普鲁兰酶基因被克隆、测序并在大肠杆菌[7,9]、酵母[14]和枯草芽孢杆菌[8]中实现了异源表达。但是来源于这些微生物的普鲁兰酶大部分是没有商业价值的,不具有很好的耐酸性和高温耐受性,满足工业需要条件的仅有 Bacillus acidopullulyticus和 Bacillus naganoensis等极少数菌株,而且目前普鲁兰酶的表达水平不高,表达量较高的是Wan Song等[8]报道的普鲁兰酶活性(24.5 U/mL),这远远不足以工业化生产。在食品加工工业中,普鲁兰酶通常应用于糖化发酵中,与糖化酶协同使用,所以只有具有与糖化酶相似的作用温度和作用pH的普鲁兰酶,才能最大程度地实现淀粉质原料的分解,大大开拓其市场。由于长野芽孢杆菌(Bacillus naganoensis)的普鲁兰酶具有很好的酸性pH和高温耐受性,适宜于工业应用条件,是目前所筛选到的最好的普鲁兰酶基因之一。近年来,通过基因工程手段表达并提高普鲁兰酶产量已经成为普鲁兰酶基础研究和应用研究的主要发展方向。
本研究从长野芽孢杆菌基因组中克隆普鲁兰酶基因,构建重组质粒 pBE-pul。同时从枯草芽孢杆菌、地衣芽孢杆菌和解淀粉芽孢杆菌的转录组中选取高表达基因的启动子,克隆到重组质粒中,转化到枯草芽孢杆菌B.subtilis ATCC6051∆10中进行分泌表达。进一步尝试删除普鲁兰酶N-末端的108个氨基酸,得到普鲁兰酶突变体基因pul324,实现其在枯草芽孢杆菌中的高效表达。
1 材料与方法
1.1 材料
1.1.1 菌株与载体
本研究使用的菌株和质粒如表1所示。

表1 菌株和载体Table 1 Strains and vectors
1.1.2 试剂和仪器
PrimeSTAR® HS DNA Polymerase(premix)、DNA Ladder Marker和T4 DNA连接酶等购于宝生物工程(大连)有限公司;限制性内切酶以及Taq PCR Mix master购于Thermo Fisher Scientific;质粒小提试剂盒、凝胶回收试剂盒和 PCR产物回收试剂盒均购于广州美基(欣研)生物科技公司;普鲁兰酶标准品Pullulanase microbial和普鲁兰多糖均购于sigma公司;红普鲁兰多糖购于上海甄准生物科技有限公司;实验中所用其他试剂均为国产或进口分析纯。梯度PCR仪Veriti® 96-Well Thermal Cycler, 美 国 Applied Biosystems公司;全自动凝胶成像仪 Gel Logic 212 PRO,美国Carestream Health公司;紫外可见分光光度计NanoDrop1000,美国Thermo Fisher公司;电转化仪Eporator,德国Eppendorf公司;M200多功能酶标仪,德国TECAN。
1.1.3 引物设计
本研究使用的引物如表2所示。

表2 引物序列表Table 2 List of primers
1.1.4 培养基
LB 培养基(W/V):1% Tryptone,0.5% Yeast Extract,1% NaCl,121 ℃高压灭菌 20 min;SOC 培养基(W/V):2% Tryptone,0.5% Yeast Extract,0.05%NaCl,2.5 mM KCl,121 ℃高压灭菌20 min,加入10 mM MgCl2和20 mM葡萄糖溶液;LBS培养基(W/V):1% Tryptone,0.5% Yeast Extract,1% NaCl,0.5 M D-Sorbitol,121 ℃高压灭菌 20 min;种子培养基(W/V):1% Tryptone,0.5% Yeast Extract,1% NaCl,2% Glucose,115 ℃高压灭菌 20 min;发酵培养基(W/V):1% Tryptone,0.5% Yeast Extract,1% NaCl,2% Glucose,2% Starch soluble,115 ℃高压灭菌20 min。
1.2 方法
1.2.1 普鲁兰酶重组质粒的构建
根据来源于Bacillus naganoensis ATCC 53909的普鲁兰酶基因pul,设计引物F-pul(Xho I)、R-pul-His(XbaI)和 F-Pul324(Xho I)(表 2),以 B. naganoensis ATCC 53909基因组为模板扩增得到普鲁兰酶基因片段。用XhoI和XbaI双酶切pBE表达载体和普鲁兰酶基因 pul,分别进行琼脂糖凝胶电泳及胶回收。使用DNA Ligation Kit的T4 DNA Ligase将普鲁兰酶基因片段连接到载体pBE上,连接液转化至E.coli stellar感受态细胞中,加入SOC培养基复苏1 h后将复苏液涂布在含100 µg/mL氨苄青霉素的LB平板上培养,挑取转化子单菌落进行验证筛选,即可得到含有普鲁兰酶重组质粒的大肠杆菌菌株。普鲁兰酶重组质粒经过测序验证。
以B. subtilis 168基因组为模板进行PCR扩增得到启动子P43、PspovG、Phag、PywzA、Pveg、PaprE、PamyE、PfusA、PgapA、Ppgk、Ptsf、PnprB、PnprE、PyqfD片段,以Bacillus licheniformis基因组为模板进行 PCR扩增得到启动子 PamyL和 PglvA片段,以Bacillus amyloliquefaciens基因组为模板进行PCR扩增得到启动子PsigW片段,然后再分别对启动子片段和普鲁兰酶重组质粒进行EcoRI和SpeI双酶切,将酶切产物进行琼脂糖凝胶电泳并胶回收。使用 DNA Ligation Kit的T4 DNA Ligase将各个启动子片段分别连接到普鲁兰酶重组质粒上,连接液转化至 E.coli stellar感受态细胞中,加入SOC培养基复苏1 h后将复苏液涂布在含100 µg/mL氨苄青霉素的LB平板上培养,挑取转化子单菌落进行验证筛选,即可得到含有各个启动子的普鲁兰酶表达质粒。以上构建的质粒均经过测序验证。
1.2.2 重组普鲁兰酶在 Bacillus subtilis ATCC6051∆10中的表达
将上述测序正确的重组表达质粒电转化于 B.subtilis ATCC6051∆10感受态细胞,加入890 μL的LBS培养基复苏5~6 h后将复苏液涂布在含20 µg/mL硫酸卡那霉素的LB平板上,37 ℃培养过夜,挑取单菌落转化子进行验证筛选,即可得到普鲁兰酶重组表达菌株 pBE101(P43),pBE102(PamyL),pBE103(PglvA),pBE104(PsigW),pBE105(PspovG),pBE106(Phag),pBE107(PywzA),pBE108(Pveg),pBE109(PfusA),pBE110(PgapA),pBE111(Ppgk),pBE112(Ptsf),pBE113(PaprE),pBE114(PamyE),pBE115(PnprB),pBE116(PnprE),pBE117(PyqfD)。
长程脑电图和Glasgow昏迷量表评分对重症脑功能损伤患者预后的预测价值 ……………………………………………………………… 蒋颖,毛可适,岳春贤,等 257
取 20 μL活化的重组菌株接种于 1 mL含 20 μg/mL硫酸卡那霉素的种子培养基中,置于37 ℃摇床以200 r/min的转速培养24 h。然后将种子液以1%的接种量(V/V)转接至2 mL含20 μg/mL硫酸卡那霉素的发酵培养基中,每个菌株重复发酵三次。置于37 ℃摇床以200 r/min的转速培养48 h后取样,在4 ℃冷冻离心机中以转速10000 r/min离心4 min获取发酵上清液,发酵上清液用于进一步的实验研究。
1.2.3 重组普鲁兰酶的酶活性检测
根据降解Red-Pullulan的能力来确定普鲁兰酶的活性。普鲁兰酶酶活的测定参考Jinho Kang[15]的DNS方法和Megazyme公司Red-Pullulan使用说明书,并以诺维信公司市售普鲁兰酶作为标准品,测定方法如下:取适当稀释的标准普鲁兰酶酶液100 μL,加入300 μL以pH 4.75的Na2HPO4-柠檬酸缓冲液配制的1.0%的Red-Pullulane为底物,充分混匀后置于60 ℃水浴锅中孵育30 min。立即加入1 mL无水乙醇,振荡混匀后静置5 min,以5000 r/min的转速离心5 min,在M200多功能酶标仪中以波长510 nm测定出反应液的吸光度值。普鲁兰酶酶活测定时,以Bacillus subtilis ATCC6051∆10野生菌发酵上清液作为空白对照。每管样品重复检测三次。根据所检测OD510nm值和与酶活力之间的线性关系即可计算得到发酵液酶活。普鲁兰酶酶活单位定义:在相应条件下,每分钟分解普鲁兰所释放的还原糖,其还原力相当于1 μmol葡萄糖所需的酶量,以1 U表示。
1.2.4 普鲁兰酶突变体重组表达菌株的构建
在利用PCR方法缺失普鲁兰酶前面108个氨基酸得到普鲁兰酶突变体pul324,克隆到上一步研究中筛选到的强启动子 PspovG载体上,构建菌株 pBE202(PspovG-pul324),进行分泌表达。
1.2.5 摇瓶发酵
选取野生菌B.subtilis ATCC6051∆10,普鲁兰酶重组高表达菌株 pBE105(PspovG)和 pBE202(PspovG-pul324)进行摇瓶发酵。分别接种20 μL保种菌液于24孔板中,每个孔加入3 mL含有20 μg/mL硫酸卡那霉素的种子培养基,置于37 ℃摇床200 r/min培养至24 h;检测各个菌株的生物量OD600nm,并以等生物量(约为1%的接种量)接种适量菌液至50 mL发酵培养基中发酵;每隔12 h取样500 μL检测其生物量和上清液酶活,直至72 h。每个菌株重复发酵三瓶。
在4 ℃低温离心机中离心收集发酵上清液,然后通过0.45 μm超滤膜抽滤获取发酵蛋白样品液。随后利用AKTA蛋白纯化系统和5 mL HisTrapTM FF crude预装柱纯化处理后的蛋白样品液,结果表明在 20%Buffer B条件下洗脱时出现目的蛋白峰,收集此时的洗脱液。然后,分别取40 μL发酵蛋白样品液和纯化洗脱液,向其中加入 10 μL 5×SDS-PAGE Loading Buffer,涡旋振荡混匀,沸水浴中加热处理5 min使蛋白变性。使用5%的浓缩胶,12%的分离胶进行发酵液蛋白分离,然后在考马斯亮蓝R-250染液中染色,再经过脱色处理后显示蛋白条带。
1.2.7 数据统计分析
所有数据检测均重复三次或以上,结果以平均值±标准偏差表示。
2 结果与讨论
2.1 普鲁兰酶重组质粒的构建

图1 B.subtilis ATCC6051∆10中含不同启动子的表达质粒的构建Fig.1 Construction of expression plasmids for B. subtilis ATCC6051∆10 with different promoters

图2 普鲁兰酶基因PCR扩增电泳图Fig.2 Electrophoresis image of pullulanase gene PCR
从长野芽孢杆菌基因组中扩增出来的普鲁兰酶基因片段电泳图如图2所示。通过PCR方法,成功扩增得到普鲁兰酶基因片段pul,大小为2799 bp,大小与预期的相一致(图2)。再以限制性内切酶XhoI和XbaI对载体pBE-SPamyQ和片段pul分别进行双酶切,连接后转化至大肠杆菌stellar感受细胞中。挑取单菌落鉴定后送至公司测序,测序结果显示普鲁兰酶基因片段成功连接到表达载体上,成功构建质粒pBE-SPamyQ-Pul。

图3 不同启动子的PCR扩增产物Fig.3 PCR products of different promoters
分别从枯草芽孢杆菌、地衣芽孢杆菌和解淀粉芽孢杆菌基因组中扩增出来的启动子片段电泳图如图 3所示。通过PCR方法,成功扩增得到17种启动子片段,大小与预期的相一致(图3)。再以限制性内切酶EcoRI和SpeI对载体pBE-SPamyQ-pul和启动子片段分别进行双酶切,连接后转化至大肠杆菌stellar感受细胞中。挑取单菌落鉴定后送至公司测序,测序结果显示启动子片段成功连接到表达载体上,成功构建质粒pBE-Promoter-SPamyQ-pul。
2.2 不同启动子对普鲁兰酶重组菌株表达水平的影响
通过检测含不同启动子的普鲁兰酶重组表达菌株发酵液中的普鲁兰酶酶活发现,不同的启动子介导的普鲁兰酶的表达水平差异较大,其中启动子 P43和PspovG介导的普鲁兰酶的表达水平远远高于其他启动子(图4),在24孔板中培养发酵48 h后普鲁兰酶酶活分别为81.29 U/mL和86.67 U/mL,含有启动子PspovG的重组普鲁兰酶表达菌株所显示的普鲁兰酶酶活比含有传统强启动子P43的重组菌株更高。所以,选用启动子PspovG进行下一步实验。

图4 重组菌株的普鲁兰酶酶活性分析Fig.4 Pullulanase activity analysis of recombinant strains
2.3 普鲁兰酶高表达菌株摇瓶发酵

图5 重组菌株表达产物的普鲁兰酶酶活性分析及菌株生长曲线Fig.5 Pullulanase activity analysis and growth curve of recombinant strains
对于上述筛选出来普鲁兰酶活性最高的启动子PspovG,成功构建质粒pBE105(PspovG)和pBE202(PspovG-pul324)。对这两个质粒所在菌株进行发酵表达,测定不同时间点的各菌株普鲁兰酶活性变化情况(图5a)及菌株的生长情况(图5b)。普鲁兰酶酶活曲线表明,菌株 B.subtilis ATCC6051∆10/pBE105(PspovG)的发酵上清液中普鲁兰酶活性随着发酵时间的延长,酶活性持续升高,并在48 h达到相对稳定期,发酵72 h时酶活达到389.85 U/mL;而B.subtilis ATCC6051∆10/pBE202(PspovG-pul324)菌株发酵36 h达到相对稳定期,随着时间的增长,酶活力增长平缓,发酵72 h时酶活达到260.38 U/mL。同时重组菌株生长曲线表明,发酵菌株 B.subtilis ATCC6051∆10/pBE105(PspovG ) 和 B.subtilis ATCC6051∆10/pBE202(PspovG-pul324)均在36 h时生物量达到最高值,随着时间的延长,菌株B.subtilis ATCC6051∆10/pBE202(PspovG-pul324)生物量趋于平 缓 , 而 菌 株 B.subtilis ATCC6051∆10/pBE202(PspovG-pul324)生物量迅速下降,说明不同是重组质粒对宿主菌的生长影响差异较大。由图5展示的两株普鲁兰酶重组菌株的产酶曲线和生长曲线,可以明显发现菌株 pBE105(PspovG)更适用于工业生产。首先,在相同的表达宿主菌中,由相同的启动子介导表达,菌株pBE105(PspovG)发酵72 h后表达量比菌株 pBE202(PspovG-pul324)更高。其次,在菌体达到最高浓度时,菌株 pBE105(PspovG)的生长状态更佳,随着时间的延长,生物量可以保持相对稳定,这为持续表达普鲁兰酶提供了保障,这在工业化发酵中具有巨大优势。
2.4 发酵液SDS-PAGE分析
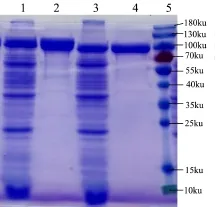
图6 重组菌表达产物的SDS-PAGE分析Fig.6 SDS-PAGE analysis of expression products of recombinant strains
SDS-PAGE鉴定结果表明,重组菌株 pBE105(PspovG)的发酵上清液及其纯化液在100 ku附近有一条表达条带,与普鲁兰酶理论大小一致,为普鲁兰酶蛋白,约为 100 ku;而重组菌株 pBE202(PspovG-pul324)的发酵上清液及其纯化液在70~100 ku之间有一条表达条带,与普鲁兰酶突变体理论大小一致,为普鲁兰酶突变体,约为90 ku。其中,重组菌株 pBE105(PspovG)的普鲁兰酶表达量比 pBE202(PspovG-pul324)的更高,条带更粗,该结果与普鲁兰酶酶活性检测结果一致。同时发酵液经过纯化后,效果显著,说明重组菌株的普鲁兰酶表达为胞外分泌表达,纯化步骤简单快捷,效果好,非常适用于工业生产,为下游生产工艺提供了研究基础。
3 结论
本研究成功构建了 17种含有不同启动子的普鲁兰酶重组质粒,并对其重组菌株的表达产物分别进行普鲁兰酶酶活性检测,其中重组菌株 B.subtilis ATCC6051∆10/pBE105(PspovG)的普鲁兰酶酶活性最高。接着,本研究又通过突变普鲁兰酶来进行一步摸索提高普鲁兰酶表达量的方法,成功构建了重组质粒pBE202(PspovG-pul324)。但是实验结果表明,在相同的载体和宿主菌中表达,普鲁兰酶突变体的表达量并没有普鲁兰酶原基因的表达量高,重组菌株B.subtilis ATCC6051∆10/pBE105(PspovG)发酵72 h后,最高普鲁兰酶酶活为389.85 U/mL。该酶活远远高于Wan Song等[8]报道的普鲁兰酶活性(24.5 U/mL),实现了普鲁兰酶在枯草芽孢杆菌中的高水平表达。本研究成功实现了普鲁兰酶在枯草芽孢杆菌中的高效分泌表达,为普鲁兰酶基因工程改造奠定了一定的基础,同时推动普鲁兰酶的工业化生产。
