肉桂酸蔗糖酯的酶法制备及其抗菌活性
2018-10-13何世军赵光磊何北海
何世军,赵光磊,何北海
(华南理工大学轻工科学与工程学院,广东广州 510640)
蔗糖成本低廉,来源广泛,容易获得,是重要的基础化工原料之一。蔗糖分子具有高亲水性,其结构中含有8个羟基,其中3个为伯羟基,因而具有醇的典型性质,可与有机酸发生典型的酯化反应,生成作为重要精细化工产品的蔗糖酯[1]。而蔗糖酯具有无毒无臭、无刺激及易生物降解等理化性质;在人体内可分解而被机体利用,安全性高[2]。同时大量研究成果表明,特定的蔗糖酯对微生物具有较广泛的抑制作用,对革兰氏阳性芽孢杆菌的抑菌作用尤为显著。如蔗糖癸酸酯对枯草芽孢杆菌、金黄色葡萄球菌、大肠杆菌和沙门氏菌具有较强的抗菌作用,抗菌效果与脂肪酸碳链长度成反比,且脂肪酸蔗糖双酯的抗菌作用要优于脂肪酸蔗糖单酯;蔗糖八硫酸酯对金黄色葡萄球菌、肺炎克雷伯氏菌、大肠杆菌、铜绿假单胞菌及变形杆菌具有良好的抑制作用;反丁烯二酸蔗糖甲酯对大肠杆菌、苏云金杆菌、酵母、黑曲霉具有较强的抑制能力,抗菌谱系包括细菌、酵母和霉菌[3~5]。蔗糖酯因在抗菌方面的独特理化性质而被广泛应用于食品、制药、化妆品和洗涤剂等生产行业中。
目前糖酯多采用化学法合成,往往反应选择性差,副产物含量高,且反应体系的局部高温会引起糖焦化,加大糖酯分离提纯的难度[6]。而非水相中酶法合成糖酯因其反应条件温和、选择性高、反应产物易分离和溶剂可循环多次利用,在糖酯合成领域引起了广泛关注[7]。目前已报道了大量利用酶法催化糖酯合成方法,如在离子液体中利用脂肪酶催化制备棕榈酸壳寡糖酯,在无水异丙醇中脂肪酶催化合成月桂酸木糖酯,在混合溶剂中利用脂肪酶催化甲基丙烯酸乙烯酯和木糖酯交换反应合成木糖酯[8~10]。
研究表明,α,β-不饱和羰基结构是体现抗菌活性的有效功能结构[11]。食品工业中常用的广谱防腐剂富马酸和山梨酸具有典型的α,β-不饱和羰基结构。但富马酸和山梨酸在有机溶剂中可游离出质子,刺激人体表皮引起过敏。保留α,β-不饱和羰基功能结构的衍生物具有一定程度的抑菌活性,而富马酸二甲酯和山梨酸甲酯是其代表性的衍生物[12]。但富马酸甲酯刺激性气味太重,山梨酸甲酯则易氧化和升华,因而限制了它们在食品、化妆品中的应用。为了消除富马酸、山梨酸及其酯类衍生物的不足,本文研究在蔗糖分子上引入肉桂酸,首次制备了一种保留α,β-不饱和羰基功能结构和同时具有两亲性基团的肉桂酸蔗糖酯。并探讨了混合有机溶剂中酶法制备肉桂酸蔗糖酯的方法和产物肉桂酸蔗糖酯的化学结构;此外,还进一步研究了产物的抗菌特性、热稳定性和保水性能等。
1 材料与方法
1.1 主要仪器与试剂
集热式恒温加热磁力搅拌器,DF-101S,广州市星烁仪器有限公司;离心机,TW-3021HR,安徽嘉文仪器装备有限公司;傅里叶变换红外光谱仪,TENSOR27,德国 Bruker公司;核磁共振波谱仪,AVANCE III HD 400,德国Bruker公司;UV-Vis光度计,Agilent cary 60,美国Agilent公司;热重分析仪,STA 449 F3 Jupiter,德国耐驰公司。
肉桂酸,纯度>97%,上海阿拉丁试剂有限公司;固定化的脂肪酶(Candida Rugosa Lipase,CRL),700 U/mg,西格玛奥德里奇贸易有限公司;蔗糖、氢氧化钠、4A分子筛,分析纯,上海润捷化学试剂有限公司;叔戊醇、二甲基乙酰胺(DMAc),分析纯,广州化学试剂厂;马铃薯葡萄糖琼脂(PDA)、营养琼脂,广东环凯微生物科技有限公司;白地霉GIM 2.12,广东微生物菌种保藏中心;大肠杆菌ATCC25922,广东环凯微生物科技有限公司。
1.2 方法
1.2.1 肉桂酸蔗糖酯的制备
将 DMAc与叔戊醇以一定的体积比配制混合有机溶剂并以此作为反应溶剂体系。蔗糖与肉桂酸按1:4的摩尔比溶解在DMAc/叔戊醇的混合溶剂中;同时加入脂肪酶和 4A分子筛,脂肪酶用量为蔗糖质量的15%;在通入氮气的恒温加热搅拌器中反应。反应结束后,将得到的溶液冷却,过滤脂肪酶;在5000 r/min、-4 ℃的条件下冷冻离心取出未反应的结晶蔗糖和肉桂酸,并将滤液在60 ℃、20 mBar、60 r/min条件下旋蒸去除溶剂。
1.2.2 取代度测定
皂化滴定法是测定甘油酯皂化值的方法,也是目前测定糖酯取代度(Degree of Substitution,DS)的方法之一。称取0.2 g肉桂酸蔗糖酯置于锥形瓶中,在20 mL的0.2 mol/L的NaOH和80 mL蒸馏水中溶解,再在75 ℃搅拌2 h进行充分皂化。皂化结束后加入三滴酚酞,用0.05 mol/L HCl的标准液滴定,以溶液红色消失为终点。重复滴定三次,取所消耗的HCl标准溶液体积平均值V。同时采用蔗糖原样做空白对照,记录滴定消耗HCl标准溶液体积V0。肉桂酸蔗糖酯的取代度计算公式如下:
n=C(V0-V)/1000
DS=342 n/(m-M'*n)
注:342为蔗糖是相对分子质量;n为羧基的量(mol);C为所用HCl标准溶液的浓度(mol/L);m为蔗糖酯样品的质量(g);M'为蔗糖被肉桂酸基团取代的增加量(g/mol)。
1.2.3 红外光谱分析
称取2 mg肉桂酸蔗糖酯样品,样品与溴化钾按照1/20的质量比混合研磨,在80 ℃的烘箱干燥4 h。将研磨均匀的粉末压片,进行红外光谱测试。扫描样品前测量背景通道的背底,排除水和二氧化碳的干扰。每个样品扫描32次,分辨率为4 cm-1,扫描范围为4000~400 cm-1。
1.2.4 热重分析
称取10 mg肉桂酸蔗糖酯样品放入坩埚中,升温程序设置中温度范围从20 ℃到700 ℃,升温速率为10 ℃/min,保护气体为氮气,氮气流量为25 mL/min。
1.2.5 核磁共振碳谱分析
将旋蒸产物样品在硅胶板点样、展开、刮板取样。取40 mg干燥的刮板样品溶解在1 mL DMSO-d6中;为了获得较好的信噪比,设置如下参数:扫描数,10000;扫描时间,1 h;弛豫时间,2.0 s;接收器增益,187;脉冲宽度,12.0 s;谱宽,36057.7 Hz。
1.2.6 抗菌测试
利用GB/T 20944.3-2008的振荡法进行肉桂酸蔗糖酯的抗菌性能评价。以肉桂酸蔗糖酯作为抗菌试样,分别称取0.25 g,0.50 g,0.75 g;以蔗糖作为对照样,称取0.75 g。从3代的保存菌种制成了接种菌悬液。菌悬液经过4次稀释程序后,用来对试样接种。准备15个250 mL三角烧瓶。在其中3个烧瓶中加入0.75 g蔗糖,3个烧瓶中加0.25 g肉桂酸蔗糖酯,3个烧瓶0.50 g肉桂酸蔗糖酯,3个烧瓶加0.75 g肉桂酸蔗糖酯,另3个烧瓶不加任何试样,然后在每个烧瓶中各加入70 mL 0.03 mol/L PBS缓冲液。12个烧瓶中各加入1 mL菌悬液,另外不加试样的3个烧瓶中不加入菌悬液。PBS和菌悬液混匀后,分别吸取1 mL试液移入装有9 mL、0.03 mol/L PBS缓冲液的试管中,充分混匀,在24 ℃,150 r/min,振荡18 h。到时间后,用10倍稀释法进行稀释。从每个烧瓶中吸取1 mL试液,移入装有9 mL 0.03 mol/L PBS级冲液的试管中,充分混匀。每个稀释倍数的试样分别吸取1 mL移人无菌的平皿,倾注培养基约15 mL。室温凝固,倒置平板,37 ℃培养24 h。通过稀释的方法测定振荡前及振荡24 h后的活菌浓度,计算抑菌率,以此评价试样的抗菌效果。
1.2.7 保水性能分析
参考GB 5009.3-2010食品中水分测定的第二法,测定肉桂酸蔗糖酯和蔗糖的含水量,以此评价其保水性能。将样品研磨成粒径小于2 mm的粉末,称取0.5 g样品置于80 ℃干燥箱中,恒温加热4.0 h。取出样品,置干燥器内冷却至室温称量,并重复干燥至前后两次质量差不超过2 mg。
2 结果与讨论
2.1 酶催化肉桂酸蔗糖酯合成反应体系的研究
2.1.1 混合溶剂的体积比对肉桂酸蔗糖酯合成反应的影响研究

图1 不同体积比的混合溶剂对肉桂酸蔗糖酯取代度的影响Fig.1 Effect on mixed solvents with different volume ratio to DS
溶剂的极性对酶法制备蔗糖酯的反应转化率具有重要影响[13]。DMAc毒性较小和对蔗糖溶解度较大,因而工业上一般使用亲水性的 DMAc作为生产蔗糖酯的溶剂,但是DMAc的极性较大而易使酶活降低。通过在溶剂 DMAc中混和适当比例的弱极性溶剂叔戊醇,可使酶保持较高活性,从而提升蔗糖酯的转化率。此外,叔戊醇是常用的常压下沸点为103 ℃的弱极性溶剂,通过旋蒸的方法可轻易去除,对蔗糖酯的分离提纯有利。通过研究混合溶剂比例对反应转化率的影响,可提高蔗糖酯的合成效率。图1展示了DMAc与叔戊醇在不同体积比时,对蔗糖取代度的影响。当叔戊醇的体积比从0增加到25%时,肉桂酸蔗糖酯的取代度从 0.38±0.02不断增加 0.71±0.02,增幅为86.84%,并达到最大;主要因为叔戊醇平衡了强极性溶剂 DMAc对酶分子活性的影响从而维持酶相对完整的空间构象[14]。当叔戊醇体积比由25%提升至45%时,肉桂酸蔗糖酯的取代度出现下降,取代度从0.71±0.02不断降低0.41±0.02,降幅为42.25%;主要是因为疏水性溶剂的增加降低了反应底物的溶解度,同时酶活性中心部位会形成水分子团簇而包围酶分子,增加传质阻力,引起酶分子的结构变形,使得酶活降低[13]。综合研究结果表明,混合溶剂的极性对蔗糖酯合成具有显著影响;同时说明溶剂体系中引入弱极性溶剂之后,可较好地溶解极性底物蔗糖,同时保持脂肪酶的良好活性。
2.1.2 温度对肉桂酸蔗糖酯合成反应的影响研究
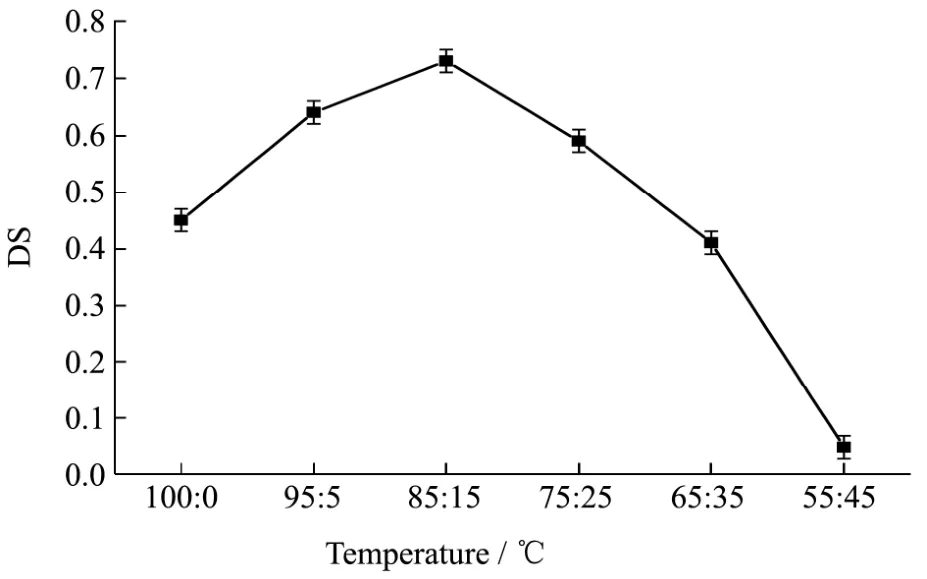
图2 温度对肉桂酸蔗糖酯取代度的影响Fig.2 Effect of temperature on the DS of enzymatic reaction
反应温度是影响酶催化反应最显著的因素之一,直接关系着催化反应速率和转化率。如图2所示,反应温度从40 ℃逐步升高到50 ℃时,反应产物的取代度从0.45±0.02增加到0.73±0.02,并达到最大值,增幅62.22%。主要是因为反应温度升高可以使底物分子的运动加快,提高有效碰撞几率,从而提高酶与底物的催化效率。但是随着反应温度从50 ℃升高到60 ℃时,反应产物的取代度开始出现下降,从 0.73±0.02降低到0.06±0.02。反应产物的取代度开始降低,主要是因为温度过高使酶蛋白中心构象转变而降低酶活。在60 ℃的反应温度时,脂肪酶仍具有一定的酶活,反应产物的取代度为0.39±0.02,说明说明固定化的脂肪酶能够耐受较高的反应温度,提升了脂肪酶在反应体系的热稳定性,表现出一定的催化活性。综合研究结果表明,反应体系的温度主要受到脂肪酶的耐受温度限制,反应温度偏高或偏低,对反应产物的取代度都不利;同时脂肪酶法合成肉桂酸蔗糖酯的最适温度为50 ℃,与化学法相比反应条件非常温和。
2.2 反应产物的红外光谱分析
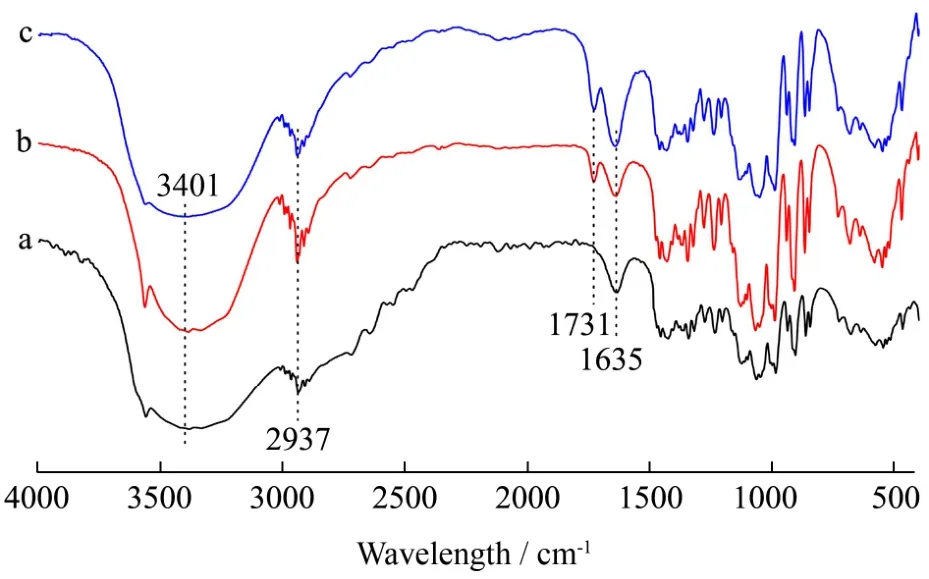
图3 反应产物红外光谱图Fig.3 FT-IR spectrum of the reaction product
红外谱图的吸收峰强度与峰形是由化合物不同基团互相作用的结果,不同基团的特征吸收峰,其峰位置、峰形和峰强也不同。蔗糖的主要特征吸收峰来自5个仲醇羟基和3个伯醇羟基,而蔗糖被酯化后利用红外光谱可快速分析糖酯产物的酯基特征结构。如图3所示,样品a作为空白对照,反应过程中没有使用脂肪酶,其它试验条件与样品b、样品c完全相同。样品a、b、c的红外谱图在3401 cm-1处有个宽而强的吸收峰,归属于产物中的羟基(-OH)伸缩振动峰。由于蔗糖是具有8个羟基,分子间可形成缔合氢键,该吸收峰的波数向低频移动,从而在此处形成宽大波形峰。2937 cm-1及1635 cm-1分别为产物中亚甲基的C-H伸缩振动峰和H-O-H弯曲振动峰。一般而言,羧基的伸缩振动峰出现在1770~1750 cm-1,酯基的伸缩振动峰出现在1750~1725 cm-1;从图3中观察可知,1731 cm-1处的吸收峰是酯基υ(C=O)特征峰[15]。综合研究表明,酯化产物b、c在1731 cm-1都出现新特征吸收峰,而样品a未出现该特征吸收峰,说明在脂肪酶的作用下肉桂酸与蔗糖发生了酯化反应;并且随着取代度的增大,1731 cm-1处的吸收峰增强。
2.3 反应产物的核磁共振碳谱分析(13C-NMR)
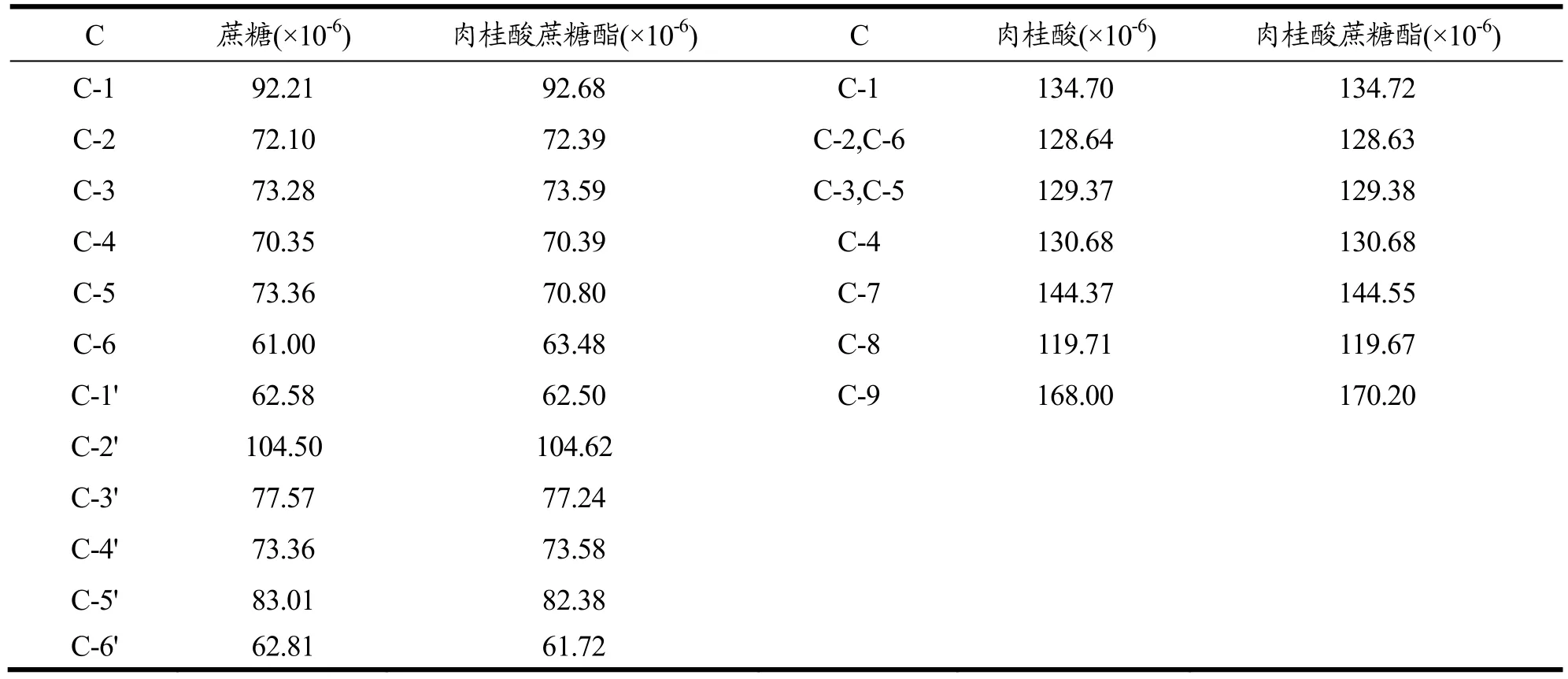
表1 蔗糖、肉桂酸及肉桂酸蔗糖酯的13C-NMR化学位移Table 1 13C-NMR chemical shifts of sucrose, cinnamic acid and cinnamate sucrose ester
为了进一步明确肉桂酸蔗糖酯的化学结构及酰化位点,利用13C-NMR对其进行结构鉴定。核磁共振技术可提供分子中碳原子的类型、周围化学环境的结构信息,该方法可分析肉桂酸蔗糖酯的化学结构。Michel[16,17]等利用13C-NMR技术对糖类化合物及其酰化产物进行了结构分析并总结了可用于鉴定糖类酰化产物结构的解析方法。该方法认为当糖类化合物的某一羟基发生酰化反应后,与该羟基直接相连碳原子信号峰的化学位移会向低场移动,而相邻碳原子信号峰的化学位移则会向高场移动。由表1的13C NMR谱数据所示,肉桂酸基团的 C-9由 168.00×10-6偏移至170.20×10-6,向低场偏移了2.20×10-6,说明肉桂酸与蔗糖发生了酯化反应。蔗糖基团 C-5信号峰由73.36×10-6偏移至70.80×10-6,向高场偏移了2.56×10-6;蔗糖基团C-6信号峰由61.00×10-6偏移至63.48×10-6,向低场偏移了2.48×10-6。综合分析,可以判断脂肪酶促酯化反应发生在蔗糖的C-6位点,同时说明脂肪酶对肉桂酸蔗糖酯的合成催化具有区域选择性。根据产物结构,确定脂肪酶催化肉桂酸蔗糖酯的合成反应式如图4所示:

图4 肉桂酸蔗糖酯合成反应式Fig.4 Reaction scheme of cinnamate sucrose estersynthesis
2.4 肉桂酸蔗糖酯的热稳定性研究
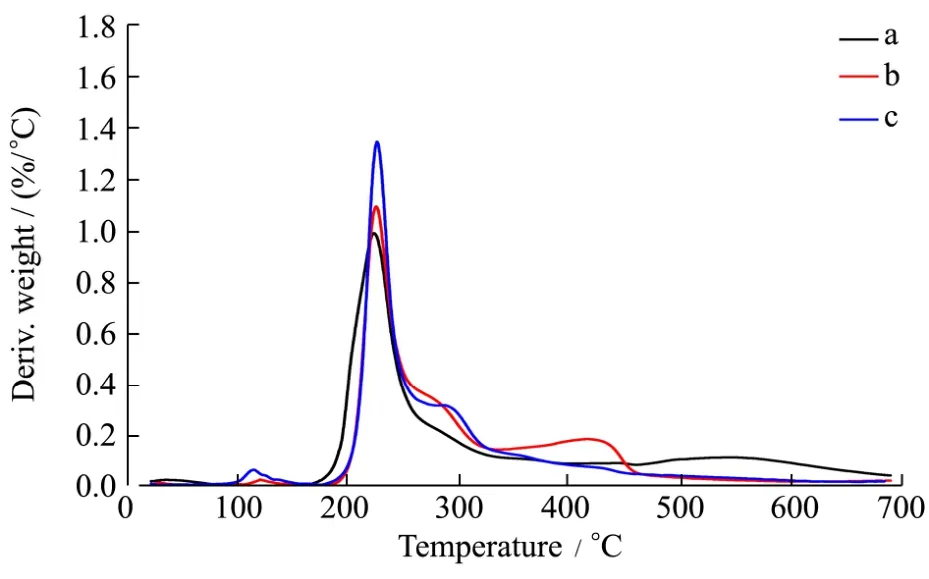
图5 肉桂酸蔗糖酯的DTG曲线Fig.5 DTG curves of cinnamate sucrose ester
食品工业中为了降低加工黏度或提升灭菌效率,常需要高温处理,从而提升生产效率。然而为了防止爆炸保证安全生产,或为了防止物料分解产生副反应,在食品的加工和灭菌过程要求物料性质保持稳定[18]。研究肉桂酸蔗糖酯的热稳定性非常必要。在氮气环境下进行热重分析,在升温程序中只有挥发、解聚、分解,可以反映肉桂酸蔗糖酯的热稳定性。由图5可知,曲线 a表明蔗糖样品的初始降解温度为 196 ℃,在224 ℃达到最大失重速率,说明蔗糖只对应着一个分解温度,主要过程是糖苷键的断裂。曲线b和曲线c表明肉桂酸蔗糖酯的初始降解温度为215 ℃,同时具有两个分解温度;在228 ℃的失重峰代表蔗糖糖苷键断裂的温度,在274 ℃的失重峰代表肉桂酸蔗糖酯的酯键断裂温度。曲线b和曲线c在115 ℃出现失重峰,主要由于肉桂酸蔗糖酯通过氢键吸附的水分挥发引起。研究发现,蔗糖酯化后,酯化产物肉桂酸蔗糖酯的热稳定性提升,其初始降解温度提高了19 ℃,可能与产物的平均分子相对质量提高有关。肉桂酸蔗糖酯可以承受高于220 ℃的高温而不分解,远高于食品中许多物料的加工温度,可在食品工业的热加工中保持稳定。
2.5 肉桂酸蔗糖酯的抗菌性能研究
肉桂酸蔗糖酯与食品工业中常用的防腐剂山梨酸都具有α、β不饱和羰基功能结构,具有较好的抗菌活性。而大肠杆菌是日常生活中常见细菌类病原菌,白地霉是食品中常见的真菌类腐败菌,研究肉桂酸蔗糖酯对大肠杆菌和白地霉的抗菌性能具有重要意义。从图6~8的观察可知,肉桂酸蔗糖酯的抗菌性能随着肉桂酸蔗糖酯量的增加,抑菌率不断增加。而肉桂酸蔗糖酯对大肠杆菌的最大抑菌率为97.83%,对白地霉的最大抑菌率为96.04%。这是由于微生物吸收肉桂酸蔗糖酯的同时,具有共轭基团连接的羧基碳正离子易与胞膜上带负电的蛋白质、类脂化合物相互吸附,导致细胞变形[19,20];同时被吸收的肉桂酸基团会阻碍菌体生物催化酶和蛋白质的合成;当肉桂酸蔗糖酯被微生物吸收时,羧基会与氨基酸分子中的琉基、羟基、亚氨基等基团作用发生缩合反应,这些具有供体性质的氨基酸残基常位于酶的催化域和结构域中,对维持酶类的活性及稳定性具有十分重要的作用[21]。研究结果表明,肉桂酸蔗糖酯对大肠杆菌和白地霉具有明显的抑制作用。肉桂酸蔗糖酯与其它保留α,β-不饱和羰基功能基团化合物的防腐抑菌机理一致[11,12]。
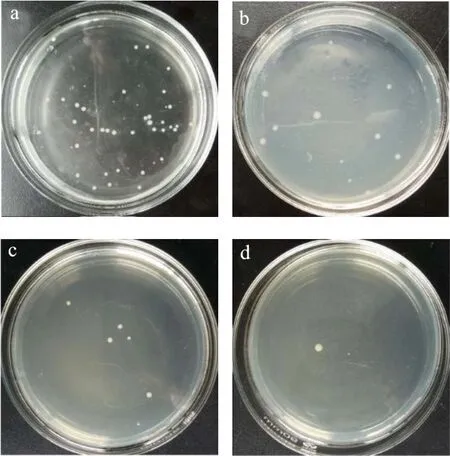
图6 肉桂酸蔗糖酯对大肠杆菌的抗菌测试Fig.6 Antimicrobial test of cinnamate sucrose ester againstEscherichia coli
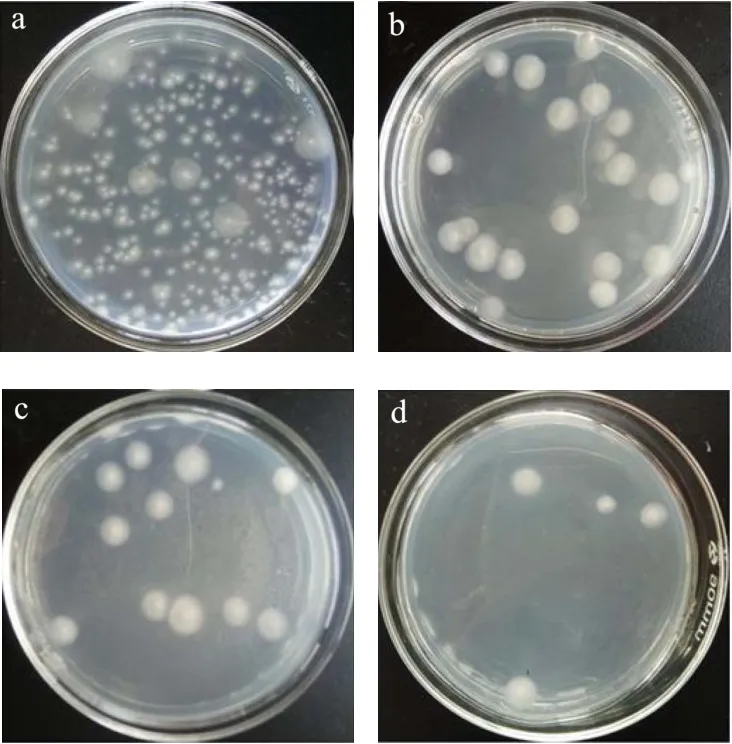
图7 肉桂酸蔗糖酯对白地霉的抗菌测试Fig.7 Antimicrobial test of cinnamate sucrose ester againstGeotrichum candidum

图8 肉桂酸蔗糖酯对大肠杆菌和白地霉的抑菌率Fig.8 Inhibition rates of cinnamate sucrose ester to Escherichia coli and Geotrichum candidum
2.6 肉桂酸蔗糖酯的保水性能研究
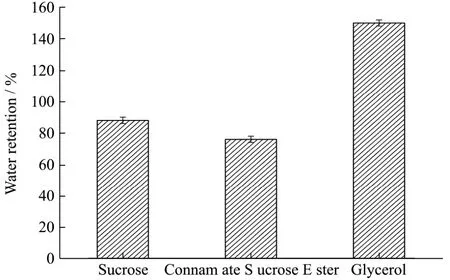
图9 蔗糖、肉桂酸蔗糖酯和丙三醇的保水率Fig.9 Comparison of water retention rates of sucrose,cinnamate sucrose ester and glycerol
水分是食品加工及贮藏过程中一项关键的质构参数,也是影响淀粉类食品老化因素之一;水分降低会使得食品变得坚韧并出现皱褶,丧失其柔软性,同时保持适量的水分可阻止某些组分结晶而变硬。图9显示,蔗糖、肉桂酸蔗糖酯和丙三醇的保水率分别为88%,76%和148%。与蔗糖相比,肉桂酸蔗糖酯的保水率下降了 8%,但仍具有良好的保水性能,肉桂酸蔗糖酯的保水性能来源于蔗糖分子中为被取代的羟基。此外,虽然肉桂酸蔗糖酯的保水率不及丙三醇,但肉桂酸蔗糖酯分子内具有裂褶结构有利于长时间保持水分,而丙三醇相对分子质量较小,吸附的水分易流失,持久性不良。研究结果表明,肉桂酸蔗糖酯在持久长效保水方面具有明显的优势,其良好的保水性能使其功能不限于食品的保水和抗菌,在保水补水的化妆品领域也具有广阔应用前景,发挥防腐和长效保湿的作用。
3 结论
3.1 酯化产物的红外光谱结果表明,在 DMAc/叔戊醇溶剂体系中脂肪酶催化下,蔗糖与肉桂酸发生了酯化反应,酯化产物在 1731 cm-1出现了酯基伸缩振动峰。
3.2 酯化产物的核磁共振碳谱结果表明,酯化反应发生在蔗糖的C6位点上。
3.3 酯化产物的热重分析结果表明,肉桂酸蔗糖酯的热稳定性提升,初始降解温度提高了19 ℃。
3.4 肉桂酸蔗糖酯对大肠杆菌的最大抑菌率为97.83%,对白地霉的最大抑菌率达到为96.04%。说明蔗糖与肉桂酸酯化后,赋予了肉桂酸蔗糖酯良好的抗菌性能。
3.5 肉桂酸蔗糖酯的保水保湿效果良好,保水率达到76%。说明肉桂酸蔗糖酯未被酯化的羟基保留了蔗糖良好的亲水性。
