GPS导航超声系统引导下超细经皮肾镜取石术治疗无积水肾下盏结石的临床应用
2018-08-31周酉枫齐勇陈伟樊晓栋周永汤春波
周酉枫,齐勇,陈伟,樊晓栋,周永,汤春波
(浙江省宁波市泌尿肾病医院 泌尿外科,浙江 宁波 315100)
肾下盏结石的微创治疗方法有体外冲击波碎石、输尿管软镜碎石术和经皮肾镜取石术(percutaneous nephroscope lithoipsy,PCNL)等,但各有不足之处。2017年1月-2017年9月,本研究采用GPS导航超声系统(Sonix GPS)引导超细经皮肾镜取石术(ultramini-percutaneous nephrolithotomy,UMP)治疗无积水肾下盏结石患者23例,疗效满意。现报道如下:
1 资料与方法
1.1 一般资料
本组共23例。其中,男13例,女10例。年龄24~76岁,平均(42.5±12.8)岁。其中,单发结石17例,多发结石6例,左侧15例,右侧8例;均为无积水肾下盏结石。结石大小以腹平片(kidney ureter bladder,KUB)结石最长径定义,多发性结石则以结石最长径总和计算,本组结石大小14.0~25.0 mm,平均(18.3±3.6)mm,结石CT值880~1 610 Hu,平均(1 253.6±182.8)Hu。无重复肾、马蹄肾和异位肾等解剖异常。
患者术前均常规行中段尿培养、CT等检查。尿白细胞异常患者均给予抗生素治疗,尿常规正常后手术。
1.2 器材与设备
德国LUT GmBH公司的F13超细经皮肾镜套件,由F3超细肾镜、F7.5内鞘、F13外鞘和闭孔器组成。加拿大Ultrasonix公司的GPS导航超声系统(Sonix GPS)。
1.3 手术方法
患者在全麻下取截石位,经尿道在膀胱镜下逆行留置F6输尿管导管,以便建立人工肾积水。然后改俯卧位,在Sonix GPS超声引导下,应用带有GPS位置接收器的超声探头和固定有接收器的16G穿刺针进行目标肾盏穿刺,退出针芯,见灌注液流出后,将F3超细肾镜直接沿穿刺针鞘进入肾集合系统,进一步确认穿刺针鞘头端在目标肾盏位置,并找到肾盏颈口,调整穿刺针鞘方向及深度使其头端靠近盏颈口或进入肾盂内,见附图。退出超细肾镜,镜体套上F7.5 UMP内鞘。往穿刺针内置入斑马导丝,沿导丝使用F14筋膜扩张器扩张通道至F14,置入F13 UMP外鞘,采用Lumenis钬激光用200μm光纤以16 W(0.8 J×20 Hz)将结石击碎至3.0 mm以下,通过逆行输尿管导管人工冲水联合外鞘内壁的冲水管在镜体前端形成的涡流,将结石碎片直接经镜鞘冲出。碎石结束后,常规留置F6 DJ管,若因角度问题无法留置DJ管,则保留输尿管导管,于术后第1天拔除,不留置肾造瘘管。术后第1或2天行KUB或CT检查评估术后即刻结石清除情况,结石清除定义为影像学检查显示无结石残留或残留结石直径<2.0 mm。
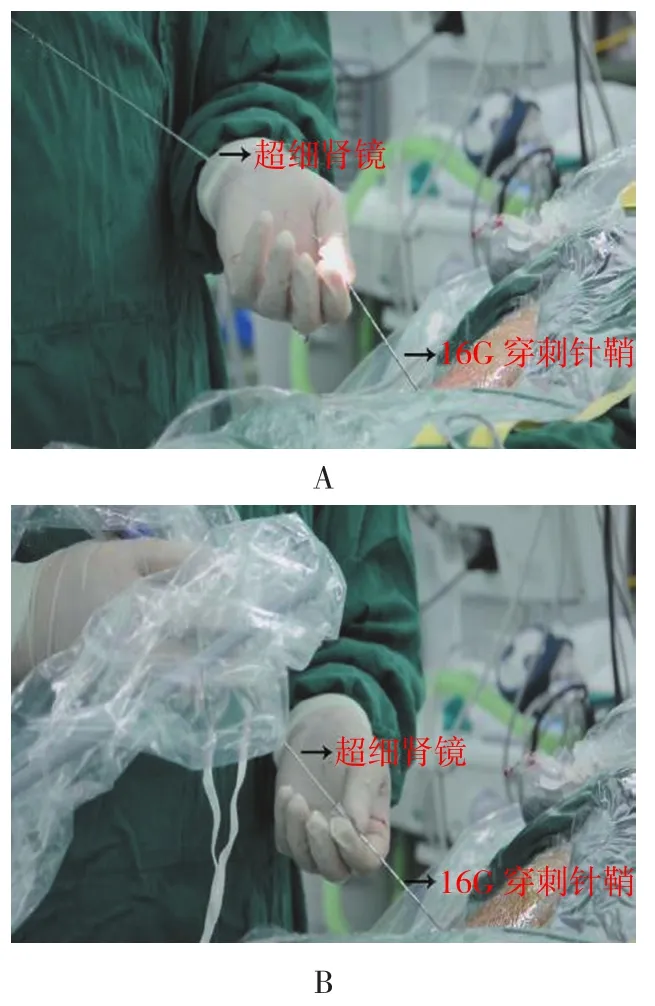
附图 UMP联合16G穿刺针确认穿刺位置Attached fig. Confirm the puncture position using UMP combined with 16 G puncture needle
2 结果
本组23例均单通道经下盏穿刺行UMP。定位穿刺时间2~8 min,平均(4.2±1.6)min,一次穿刺成功率为100.00%。手术时间30~65 min,平均(42.3±7.6)min;术后住院天数2~5 d,平均(2.6±0.5)d;血红蛋白下降 0 ~ 27 g/L,平均(11.2±5.1)g/L。术后止痛药的使用率为0。围手术期无发热、严重出血、集合系统穿孔、通道丢失和胸膜损伤等并发症发生。术后第1或2天复查KUB评估结石清除率为95.65%(22/23)。所有病例术后均未留置肾造瘘管,2周后拔除DJ管,1例术后完全无管化。
3 讨论
与其他部位的结石相比,肾下盏结石在解剖结构上具有一定特殊性,其主要因素包括肾盂肾下盏漏斗夹角(infundibulopelvic angle,IPA)、漏斗长度(infundibular length,IL)及漏斗宽度(infundibular width,IW)[1]。研究发现,对于2.0 cm以下的肾结石,体外冲击波碎石术(extracorporeal shock wave lithotripsy,ESWL)的总体结石清除率约为70.00%,而对于肾下盏结石却仅为41.00%[2]。ALBALA等[3]报道肾下盏结石ESWL后3个月的结石清除率为37.00%,且与结石负荷呈负相关。ELBAHNASY等[1]研究显示当同时包含IPA<70°、IL>3.0 cm、及IW≤5.0 mm这些不利因素时,肾下盏结石ESWL后的结石清除率仅为16.00%。
软性输尿管镜侵入性较小,灵活性优于ESWL,2015年欧洲泌尿外科指南已将其作为肾下盏结石的一线治疗方式[4]。随着新型软镜的应用,IL和IW对软镜的疗效已无明显影响,但很多国内外报道均显示IPA对软镜的结石清除率仍有着显著影响[5-9]。JESSEN等[7]发现当IPA>30°时,软镜钬激光碎石术结石清除率为92.50%,而当IPA≤30°时,结石清除率下降为38.50%。
PCNL受下盏解剖结构影响小,可直达目标肾盏,治疗肾下盏结石清除率可达85.00%~95.00%[3,10]。但PCNL手术难度及风险相对较大,如何在保证有效性的同时提高其安全性是许多泌尿外科医生追求的目标。对于无积水的肾下盏结石,如何精准地穿刺入目标肾盏是手术成功的前提。传统的B超往往很难观察到穿刺针道的全程,与积水肾或铸型肾结石相比,无积水肾下盏结石由于目标较小,穿刺难度进一步增加。而应用Sonix GPS可以实时观察到穿刺针的位置和方向,根据屏幕提供直观的穿刺针轨迹与超声切面及超声探头的位置关系,及时调整穿刺针的方向和角度,与传统B超引导相比,平均穿刺时间明显缩短,而且目标肾盏一次穿刺成功率明显提高[11]。本研究采用Sonix GPS引导进行穿刺,均顺利穿刺入目标肾盏,定位穿刺时间2~8 min,平均(4.2±1.6)min,一次穿刺成功率为100.00%,效果令人满意。
安全建立工作通道是保证PCNL手术顺利进行的关键。MICHEL等[12]对发表在PubMed上1 000例以上的PCNL文献进行统计分析,发现大出血、邻近脏器损伤等严重并发症的发生很大程度与工作通道建立不顺利相关。对于无积水肾下盏结石,肾盏内空间狭小,斑马导丝不易进入输尿管,仅盘曲于下盏,且斑马导丝尖端柔性大,同时肾下极具有一定的活动度,在扩张过程中,导丝容易弯曲及脱出,最终导致通道丢失。在本组研究中,GPS导航所用的16G穿刺针鞘内径为1.6 mm,穿刺成功后,直径为1.0 mm的F3超细肾镜刚好可以经穿刺针鞘进入集合系统直接观察穿刺深度、结石位置,并可在直视下将穿刺针方向调整至合适位置,甚至朝向肾盏出口,使斑马导丝头端柔性部分可以直接进入肾盂甚至输尿管,从而大大增强了导丝的引导作用,有效避免了通道扩张过程中导丝脱出集合系统、扩张过深等风险。本研究中的所有病例采用此“二步法”均顺利建立工作通道,无1例出现扩张过深、导丝脱出集合系统或置入静脉系统等现象,安全性可靠。但由于超细肾镜非常纤细,在调整穿刺针时需注意始终将肾镜与穿刺针保持同向性操作,否则易损坏肾镜。
出血是PCNL的常见并发症,而通道大小是影响出血的风险因素之一[13]。2013年DESAI等[14]首先报道采用F13通道的UMP处理2.0 cm以下的肾结石,认为其安全有效,尤其适合肾下盏结石。与传统PCNL或微通道PCNL相比,UMP通道直径更小,手术出血风险进一步降低。国内学者报道UMP的结石清除率为96.88%,而平均血红蛋白下降仅(14.6±8.4)g/L[15]。UMP将结石击碎至3.0 mm以下即可从外鞘中冲出,无需粉末化碎石,而且无积水的肾下盏更有利于术中涡流形成,清石效率较高。此外,UMP术后无需留置肾造瘘管,患者术后腰痛明显减轻,生活质量提高,恢复更快,住院时间缩短。
从研究结果来看,本研究充分发挥了GPS导航与UMP的优点,并使两者完美结合,治疗无积水肾下盏结石安全、有效,尤其适合IPA较小的肾下盏结石。但本研究样本量较小,尚需扩大样本,并设计随机对照研究来进一步确定其有效性及安全性。
