非小细胞肺癌患者经皮微波消融术后肿瘤相关性死亡危险因素
2018-07-26庞敏盛立军宿超宋鹏远安玉姬何伟娜张卫华张亚非
庞敏 盛立军 宿超 宋鹏远 安玉姬 何伟娜 张卫华 张亚非
1山东省医学科学院附属医院内五科(济南 250000);2山东省荣军总医院(济南 250013)
众所周知,原发性肺癌的发病率逐年增高的趋势,且死亡率相当高。目前来说,外科手术切除是治疗早期非小细胞肺癌(NSCLC)的重要手段,它不但能减低病死率,并在很大程度上改善患者的预后。但是部分早期肺癌患者因心肺功能较差、或者患有严重的肝肾病变,而导致失去外科手术的机会,使得经皮微波消融(MWA)备受国内外临床医师的推崇。MWA是肿瘤局部热消融治疗的一项分支,其原理就是使组织内的极性分子在磁场的作用下高速运动产热,从而造成肿瘤细胞的蛋白质凝固变性,从而使其不可逆性破坏。MWA的主要优势在于定位准确、患者痛苦小、术后易恢复,尤其适用于不能耐受外科手术的NSCLC患者,且疗效显著[1]。但是我国对MWA后患者的预后、生存质量以及术后相关性死亡的影响因素等研究甚少。故充分了解影响术后患者的相关因素,尤其是死亡影响因素就显得迫在眉睫了。笔者对行MWA的NSCLC患者的临床资料进行回顾分析,以期寻找到术后相关性死亡影响因素。现报告如下。
1 资料与方法
1.1 一般资料 2015年2-9月进行MWA治疗患者70例,其中,男42例,女28例;平均年龄(70±10)岁;≥65岁45例,<65岁25例;进行术后辅助治疗(包括术后辅助化疗、放疗、靶向治疗)者36例,未行辅助治疗者34例;术前癌胚抗原(CEA)升高39例,正常31例;肿瘤分期:0~ⅢA期24例,ⅢB~Ⅳ期46例;术前肿瘤平均直径(4.1±1.6)cm;术前肿瘤直径≥ 3 cm 59例,<3 cm 11例。对患者进行电话随访2年。
1.2 MWA操作方法 依照肿瘤的位置挑选更为舒适的体位,首先,给予胸部CT平扫后三维重建,并标记体表位置处放置定位器,并进行定位扫描。其次,通过胸部CT确定病灶的最大层面,并用光标大体测定所需的进针方向、深度等。患者定位后常规皮肤消毒,给予2%的利多卡因麻醉,并将注射器置于胸壁上,再次给予胸部CT扫描确定进针的方向角度,让患者保持平静呼吸微波消融针在体表标记处进针,达到病灶位置处时再次给予CT扫描,以明确针尖是否到达令人满意的肿瘤内部位置,然后依照肿瘤的大小决定针伞的长度,以保证消融灶边缘超过病灶边缘0.5~1.0 cm为标准,从而最大程度地杀死肿瘤生长最活跃的部分。重复CT扫描,再次明确消融范围后开始消融,温度为90℃,消融时间则需要根据肿瘤的直径确定。消融完成后观察患者的一般状态。
1.3 统计学方法 对临床资料中收集到的数据采用SPSS 17.0进行统计分析。用±s描述计量资料,百分比(%)表示计数资料,计量数据进行t检验,计数数据进行χ2检验、秩和检验、Logistic回归分析。P<0.05为差异有统计学意义。
2 结果
2.1 非小细胞肺癌患者微波消融术后肿瘤相关性死亡影响因素的单因素分析 表1可见,生存率为51.4%(36/70),死亡率为48.6%(34/70)。瘤直径<3 cm与≥3 cm患者的生存率分别为81.8%(9/11)、40.7%(24/59),接受辅助治疗与非接受辅助治疗患者的生存率分别为58.3%(21/36)、29.4%(10/34),两组比较差异有统计学意义(P<0.05)。
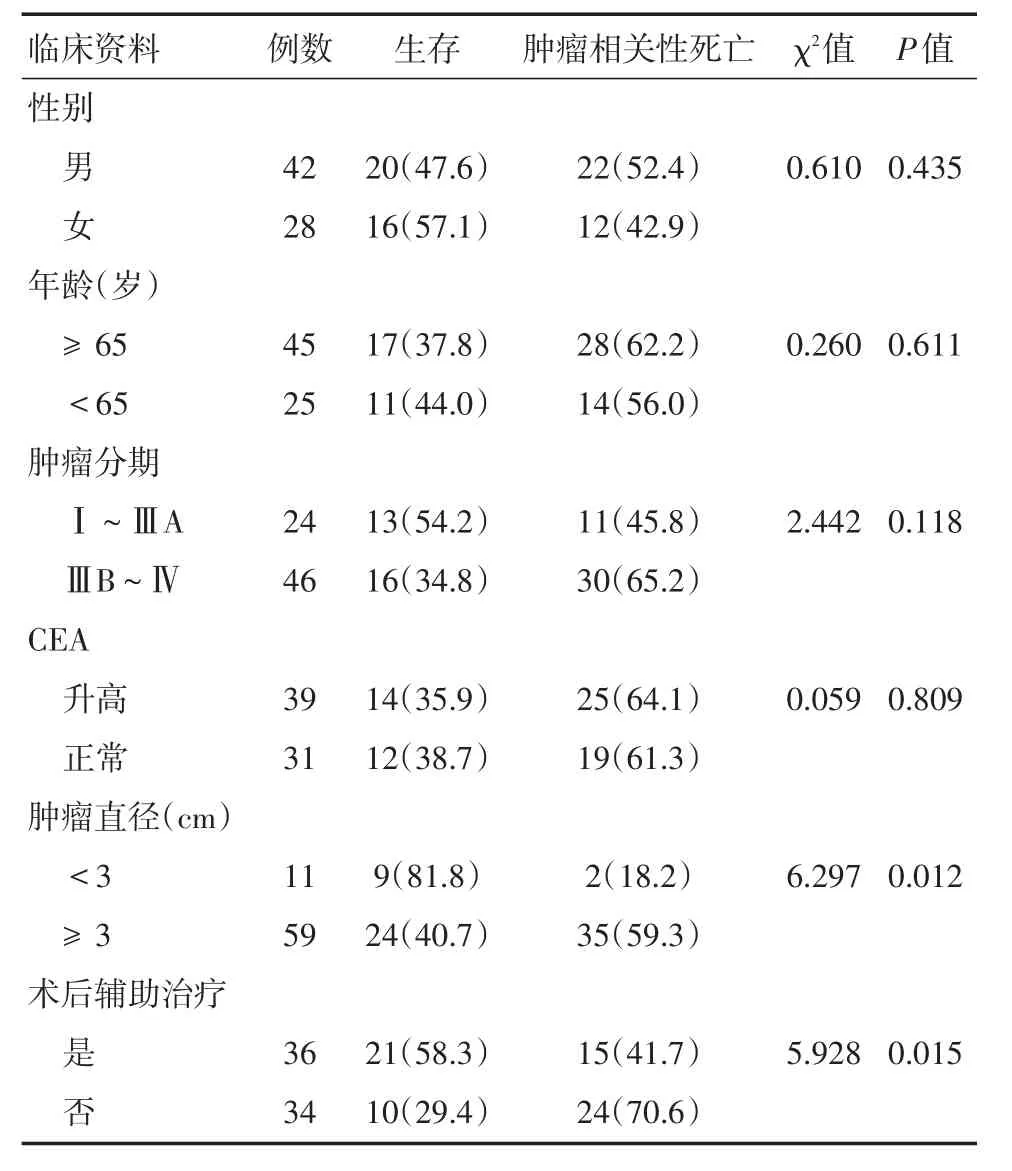
表1 非小细胞肺癌患者微波消融术后肿瘤相关性死亡影响因素的单因素分析Tab.1 A single factor analysis of the influencing factors of tumor related death after microwave ablation in patients with non⁃small cell lung cancer例(%)
2.2 非小细胞肺癌患者微波消融术后肿瘤相关性死亡影响因素的Logistic多因素分析 将影响微波消融患者病死的因素为自变量,病死率作为因变量进行逻辑回归分析,结果见表2,非小细胞肺癌患者经皮微波消融术后肿瘤相关性死亡的重要危险因素为肿瘤分期、肿瘤直径与术后辅助治疗(均P<0.05)。

表2 非小细胞肺癌患者微波消融术后肿瘤相关性死亡影响因素的Logistic多因素分析Tab.2 Multiple factors analysis of the factors affecting tumor related death after microwave ablation in patients with non⁃small cell lung cancer(Logistic)
3 讨论
本研究显示,MWA后影响非小细胞肺癌患者生存的主要因素为宿主因素、肿瘤因素以及治疗因素。
3.1 宿主因素 本研究发现,年龄、性别两因素不是影响NSCLC患者微波消融术后的危险因素,这与任守雷等[2]及李慎江等[3]报道的老年人 MWA的安全性分析相符。而本研究目的并不是只关注老年人的MWA的安全性,所以没有对气胸、胸腔积液等并发症进行探讨。本研究发现的年龄不是肿瘤相关性死亡的危险因素,显然不能说明对老年患者MWA安全性得到肯定,但也仅仅从侧面反映了年龄不会影响患者的长期生存。
CEA的本质是一种蛋白,且为酸性糖蛋白,最常用于胃肠道恶性肿瘤的标志物之一。有文献指出,胃肠道恶性肿瘤并肺转移时,CEA的水平对肺癌MWA患者的生存有一定的影响[4],但也有文章[5]持反对意见。本研究发现,术前不同的CEA对NSCLC患者的生存率无明显影响。还有文献指出,CEA在各种肺癌组织分型中的敏感度各不相同,且假阴性率较高,故不适合作为独立筛选手段存在[6]。故CEA的水平是否对肺癌的生存率有一定的影响,需要寻找更为高级的医学证据。
3.2 肿瘤因素 本研究发现,肿瘤分期是MWA后NSCLC患者生存率的危险因素,这提示ⅢB~Ⅳ期的MWA患者的生存率明显低于早期患者,其原因可能与患者的个人体质、肿瘤的进展情况以及是否有转移有关。众所周知,肺癌早期患者首选的治疗方法为外科手术切除,能够最大程度地降低患者的病死率,并提高生存质量,故较少有患者选择MWA进行治疗。有文献指出,手术切除、MWA后的患者相比较,其生存率无差异,但MWA能否代替外科手术,仍需要大样本的数据支持。目前,ⅢB期以上的肺癌患者,MWA常常作为放化疗后的一种治疗手段,其优点在于微创、疗效确切,尤其适用没有肺叶切除术的患者。
有研究发现,MWA对肿瘤直径<3 cm的肺癌患者疗效最佳[7-8],本研究发现,肿瘤的直径也是对MWA后NSCLC患者的生存率的危险因素,这提示肿瘤直径3 cm是肺癌患者生存情况的分水岭。其原因可能是微波消融的直径比CT观察的肿瘤直径大0.5~1.0 cm,而较大的肿瘤病灶由于微波针功率的问题使消融区域无法大于肿瘤直径0.5~1.0 cm的区域,故可能没有完全将周边的肿瘤细胞杀死,而且不能形成有效的凝固带阻止肿瘤的增生发展。
3.3 辅助治疗 辅助治疗就是通过放化疗、靶向药物等方法将残余的肿瘤细胞、血液中的转移灶统统杀死,进而改善患者的预后。本研究发现,MWA后给予辅助治疗可能明显改善患者的生存预后。放疗、化疗、靶向药物和MWA治疗肺癌的优缺点不尽相同。肿瘤细胞对放疗不敏感,就会造成不能完全将机体内的肿瘤病灶清除,尤其是存在远处转移的患者,放疗被认为最后的救命稻草被使用。化疗因其对肿瘤细胞的敏感度不同、较严重的不良反应,使很多患者不能达到满意的局部控制率,而对于控制远处转移的方面,化疗有着较强的优势。MWA主要作为局部治疗,虽然有着较高的局部控制率,而不能控制远处转移病灶。
国外一项多中心研究分析了将肺叶切除术的NSCLC患者根据是否术后给予化疗分为两组,中位随访7.5年,最后发现术后化疗能大大减少术后复发率和脑转移的可能[9-10],而在肺癌MWA后辅助化疗的研究几乎没有。本研究发现,术后辅助治疗能改善肺癌患者MWA后生存情况,这也提示我们,肺癌的辅助治疗是十分关键的,其原因可能是辅助治疗在一定程度上杀灭了残余肿瘤细胞、血液中的微转移灶及转移的病灶,进而减少了肿瘤复发的可能。
本研究比较创新地探讨了微波消融术后影响患者死亡的相关危险因素,给了临床医师及患者一定的指导作用,让临床医师更好地掌握微波消融这把利剑,最大程度地改善患者的预后,减轻患者的痛苦。由于本研究为回顾性研究,无法做到随机化,所以会存在偏倚,并且因为平时工作比较紧凑,随访存在不够规范,且随访时间比较短,加之本研究局限性大,样本采集数量仅仅70例,只能作为临床上的一种参考。
综上所述,本研究结果表明肿瘤的分期和直径影响NSCLC患者MWA后生存,术后辅助治疗对减少患者肿瘤相关性死亡具有积极作用。
