功能复位椎体强化治疗骨质疏松性椎体压缩骨折的有限元分析*
2018-06-21赵文韬秦大平张晓刚王志鹏
赵文韬,秦大平,张晓刚**,王志鹏,仝 尊
(1.甘肃中医药大学中医临床学院 兰州 730000;2.甘肃中医药大学附属医院脊柱外科 兰州 730020;3.云南中医学院临床医学院 昆明 650500)
中医在针对骨折治疗后骨折移位不能满足解剖复位的实际情况提出了骨折功能复位标准,并在长期中医骨伤科临床过程中加以实践。《中国骨伤科学辞典》把其定义为:功能性对位是指经过努力而不能达到解剖学或者接近解剖学对位时,为了不影响肢体功能,而要求达到的对位称功能性对位,又称功能复位[1]。骨质疏松性椎体压缩骨折(Osteoporotic vertebral compression fracture,OVCF)继发于骨质疏松症,可因轻微暴力沿着脊柱纵轴传导,产生脊柱轴向压缩力而导致,伴随人口老龄化出现骨质疏松症人群增加,OVCF患者逐渐增多的现象,而OVCF发病率中骨折部位以胸腰椎骨折最多(28.24%)[2]。椎体强化技术治疗OVCF的方法是通过将骨水泥经皮注射到骨折椎体中,以达到快速稳定骨折、缓解疼痛的治疗目的[3,4]。临床运用发现患者椎体强化治疗前骨折椎体前缘高度丢失与术后高度丢失均较正常有显著性差异,虽然治疗未能恢复到解剖复位,但是临床疗效满意[5]。这种现象是否存在着生物力学因素的影响,传统的生物力学研究方法由于难以还原实际临床治疗患者的真实情况,研究具有一定的难度。而运用有限元分析(Finite element analysis,FEA)的方法则可以通过计算机模拟还原较为真实的OVCF椎体强化治疗状态,还可以将实际临床病例的影像资料还原为接近真实情况的三维数字模型,通过对三维模型进行有限元生物力学分析则可以进一步了解骨折椎体局部的生物力学变化情况。
因此本文就OVCF椎体强化治疗过程中骨折椎体高度不能达到解剖复位但疗效满意的临床问题,结合中医骨伤功能复位理论,利用计算机有限元分析的方法寻找具体的生物力学依据。
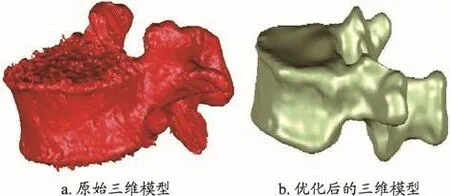
图1 原始三维模型和优化后的三维模型

图2 三维模型结构分解图
1 方法
1.1 纳入患者
本研究经甘肃中医药大学附属医院伦理委员会批准。研究纳入4名女性T12 OVCF志愿者。OVCF的纳入标准为(参考《2017原发性骨质疏松诊疗指南》):1.急性、轻度或中度暴力造成的骨折;2.腰背部疼痛视觉模量(VAS)评分≥评分;3.受伤椎体MRI检查T1加权像呈高信号,T2加权像呈低信号;4.通过双能X射线(Dual-energy X-ray,DXA)测定骨密度T密度2.5[6]。排除标准:其他病理性骨折。四名患者的年龄分别为63、71、77和84岁。行充分告知后,患者签署知情同意书。
1.2 CT扫描
患者进行脊柱CT扫描,扫描节段从T11水平到L1水平,扫描层厚为0.625 mm。患者椎体强化后CT影像通过Genant半定量方法进行分级,分别被分为0-3级各1例:椎体骨折畸形的程度分为正常(0度)、轻度(1度)、中度(2度)和重度(3度)骨折,其中轻度(1度)椎体骨折是指椎体前后的高度差小于20-25%;中度(2度)椎体骨折是指上述椎体高度差在25-40%之间;重度(3度)椎体骨折是指上述椎体高度差超过40%[7],不同椎体高度差通过CT三维重建影像进行椎体前后缘高度测量后计算得到。所有CT影像都通过医学数字成像与通讯(Digital Imaging and Communications in Medicine,DICOM)格式保存,用于三维FEA模型的生成。
1.3 T11-L1和T12骨折三维模型的构建
将DICOM影像导入交互式医学影像控制系统Mimics10.01软件(Materialize,Inc.,比利时)。首先使用阈值分割命令将骨骼和软组织分离;然后使用编辑蒙版工具编辑图像形状,选择所需区域;接下来使用区域增长命令逐层分割出所需的骨骼结构;最后,通过蒙板重建T11、T12、L1三个椎体,生成T11、T12、L1椎体(其中骨皮质厚1 mm)的三维模型。重建的三维模型以STL格式保存。
将STL格式的模型导入到自动逆向工程软件Geomagic 2012(Geomagic,Raindrop Geomagic,美国)后得到原始三维模型(图1a),通过软件对骨骼模型分别进行优化,优化过程中根据需要进行特征去除,重划网格,快速光顺,降噪,删除钉状物、填充空缺部分等操作,待模型呈现表面光滑、轮廓清晰,外观与真实状态完全一致以后进行编辑轮廓线,构造曲面片,拟合曲面等命令生成曲面模型(图1b)。Geomagic生成的模型以STP格式分别保存。将STP格式的模型导入到Solidworks 2012软 件(Dassault Systems,SolidWorks Corp.美国),利用装配体命令将T11、T12、L1椎体三维模型装配后转为零件,使用曲面和特征命令:等距曲面、分割、组合等来生成终板、关节突关节软骨和椎间盘(包括髓核和纤维环)(图2),再通过装配命令将这些结构装配获得所需的三维模型。最后参考先前文献报道的模拟方法,使用曲面命令切割椎体产生0.5 mm骨折线,T12椎体OVCF骨折的模型[8]。
1.4 T12椎体强化术后模型的构建
通过Solidworks软件生成一个体积为4 mL的圆柱模型,用于模拟注入后的骨水泥。将之前生成的T12模型导入Solidworks软件,运用装配体命令将骨水泥模型组装在椎体中央位置,然后通过布尔运算功能去除多余的骨骼,最后再将骨水泥模型组装至椎体空腔处。由此获得单侧骨水泥注射椎体强化术后的T12椎体三维模型。最后,通过Solidworks软件将T12-L1椎体、骨水泥、椎间盘、终板和软骨等各种模型进行装配即可生成整体的三维模型。最终得到四个强化术后不同T12椎体高度的三维模型(图3)。

图3 四个不同T12高度的三维模型
1.5 有限元分析前处理
对三维模型进行FEA前处理,将包括T12-L1椎体、骨水泥、椎间盘、终板和关节突关节软骨等部分的三维模型导入ANSYS 17.0软件(ANSYS,Canonsburg,PA,美国),补充相关结构,包括前纵韧带、后纵韧带、棘间韧带、棘上韧带、黄韧带和关节囊。参考近期关于OVCF研究中所使用的材料属性对之前构建的三维模型各个部分进行材料属性赋值(表1)[9-12]。所有模型均定义为各向同性材料,其中皮质骨、松质骨、终板、关节软骨和髓核定义为线性各向同性弹性材料的固体单元,前纵韧带、后纵韧带、棘间韧带、棘上韧带、黄韧带和关节囊的单元类型定义为张力变形无压缩。网格、节点和单元由软件生成,终板、关节软骨、骨折线和椎间盘划分为2 mm的网格,皮质骨、松质骨和骨水泥划分为5 mm的网格。终板与椎体、终板与椎间盘、关节软骨与骨骼之间的连接定义为绑定,关节软骨与关节软骨之间的连接定义为无摩擦(图4)。
1.6 有限元分析
本研究模型在分析前通过验证,证实结果与在不同载荷下与文献研究结果基本一致[13-15]。固定L1椎体下终板,自T11椎体上缘分别施加垂直压缩、屈曲、右侧屈、左侧屈四种不同的载荷,使用四个不同椎体高度T12椎体强化术后模型进行静态有限元分析。所有模型施加500 N的垂直压缩载荷,7.5 N.m的屈曲、左侧屈、右侧屈扭矩。参考脊柱三柱理论,载荷前中柱分配85%,后柱分配15%载荷[16]。
1.7 统计分析
提取T12椎体强化术后T12椎体在不同状态下的von Mises应力,采用t检验进行统计学处理,统计分析使用 SPSS 14.0软件(BM Corp.,Armonk,NY,美国),以P<0.05为差异具有统计学意义。

表1 有限元分析模型材料属性

图4 网格化后有限元模型
2 结果
椎体强化术后T12椎体压力具体结果(图5,表2)表现可以通过受力云图显示(图6)。T12不同椎体高度之间应力差异P>0.05。

图5 椎体强化术后T12椎体载荷
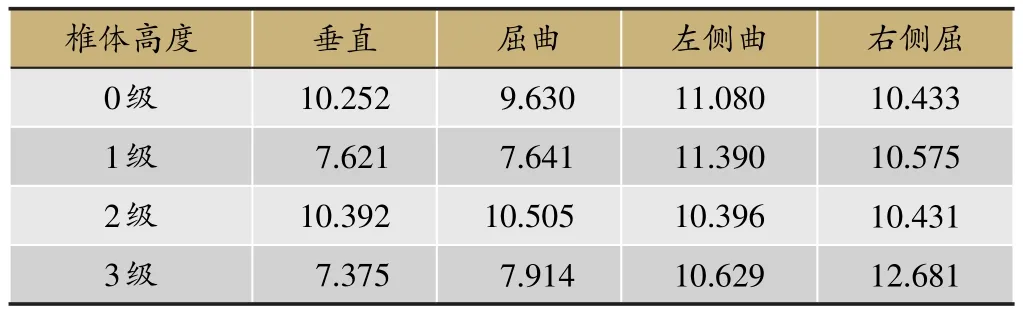
表2 椎体强化术后T12椎体载荷(MPa)
3 讨论
骨质疏松症是一种以骨量减少和骨组织结构性破坏为特点的全身性的骨病,其特点是骨量减少,骨组织显微结构破坏,骨脆性增加,易于产生骨折[17]。OVCF则是伴随人口老龄化后骨质疏松症高发出现的一个重要健康问题[18],由于骨质疏松症患病率和人类预期寿命的增加,OVCF的发生率也在上升[19]。目前OVCF的治疗已成为日益普遍而且治疗费用昂贵的公众健康问题[20],经过保守治疗后多数病例的疼痛会逐渐缓解,但不少患者的躯体疼痛仍会持续存在,同时还可以出现严重的脊柱畸形,并最终导致相关远期并发症,例如肺功能下降、消化功能紊乱、步态异常、及邻近椎体骨折产生[21],OVCF还存在潜在的不稳定性,容易发生骨折不愈合导致节段失稳,形成假关节或者后凸畸形愈合等[22],因此治疗存在一定的难度和风险。OVCF的非手术治疗适用于症状及体征较轻,影像学检查为轻度压缩骨折、无法耐受手术者。椎体强化手术治疗适用于非手术治疗无效、疼痛明显,不宜长时间卧床者;不稳定压缩骨折、骨折块不愈合或内部囊性变、椎体坏死,能耐受手术者,治疗方法可选经皮椎体成形术(Percutaneous vertebroplasty,PVP)和经皮椎体后凸成形术(Percutaneous kyphoplasty,PKP)两种椎体强化手术,因为PVP手术潜在较大的骨水泥渗漏风险而目前更多的倾向于PKP治疗[23]。因为OVCF患者非手术治疗由于长期卧床可能造成诸多的并发症[24],而椎体强化手术的出现,因其创伤小、能有效缓解疼痛,可早期下床活动以及减少老年人长期卧床的并发症而被广泛使用,如今这项技术已经成为治疗疼痛性椎体压缩骨折的金标准[25]。
中医功能复位理论已经在国内中医骨伤科及中西医结合骨科得到广泛的认可,功能复位是指骨折复位虽尽了最大的努力,某种移位仍未完全纠正,但骨折在此位置愈合后,对肢体功能无明显妨碍者[26,27]。该理论的运用还得益于中国中西医结合治疗骨折的经验总结,尚天裕教授等前辈提出了“动静结合,筋骨并重,内外兼治,医患合作”的原则,认为功能是骨折治疗的生命,在实践中系统地总结出一套骨折复位的标准并称之为“功能复位”,针对胸腰椎压缩骨折,即不主张对胸腰椎压缩骨折用机械外力强行复位,也不同意对其畸形置之不理[28]。OVCF发生后伤椎的前柱高度一般会存在不同程度的丢失,局部在矢状位上呈现后凸,严重时甚至引起脊柱失衡[29],椎体强化治疗后,压缩椎体高度的恢复在椎体前、中部可以恢复到原椎体高度的81%和78%[30],而且使用中医复位手法结合手术的结果也是一样的[31],尽管没有达到解剖复位,但是临床疗效是肯定的。这说明在脊柱椎体压缩骨折的治疗过程中功能复位现象是客观存在的,但如何满足功能复位的要求,复位多少才能够称为功能复位,这个问题不论是中医还是现代医学均没有一个确切的答案。本实验当中发现尽管术后椎体高度恢复不一致,但术后伤椎椎体所承受的载荷并无统计学差异,为OCVF椎体强化治疗后功能复位的可行性提供了生物力学依据。

图6 椎体强化术后T12椎体载荷云图
FEA又称有限元法,通过计算机模拟的方法研究力学问题,成为了现代生物力学发展的一个巨大成就[32]。FEA方法能够用来检测人体模型当中每个部分内在的相互作用[33],可以用来分析骨质疏松椎体压缩骨折的生物力学变化[34]。FEA证实椎体强化术可以恢复骨折椎体的机械稳定性,预测到骨水泥增强术后骨折椎体可以具有长期的稳定性[7]。FEA还证实椎体强化术中骨水泥量增加以后可以导致相邻椎体骨折风险增加[35],使用大体积的骨水泥对增加继发椎体骨折具有显著影响[36]。然而这些研究并没有具体研究椎体强化后骨折椎体功能复位椎体的生物力学变化。
综上,文章通过将功能复位的理论问题与OVCF椎体强化治疗的临床问题利用FEA方法进行研究,是对中医骨伤功能复位理论进行科学研究的一种尝试。通过研究发现,经椎体强化治疗后,尽管骨折椎体高度只能达到功能复位的水平,但是不同高度之间的力学载荷差异并没有统计学意义,与临床研究成果当中发现功能复位后临床效果的结果是一致的,进一步证实了中医功能复位的可靠性和科学性。
但是本研究仍然存在不足,最主要问题为三维模型和实际人体结构还有一定差距,只能够有限地模拟人体状况;此外对邻近椎体及肌肉、韧带、软组织的研究不理想,因此在今后的研究当中还有进一步提高的空间。
4 结论
本研究的目的在于通过有限元分析的方法寻找中医功能复位理论指导椎体强化术治疗OVCF的生物力学依据。研究结果证实尽管椎体强化术后伤椎椎体高度恢复不同,但椎体应力变化无显著差异,结合中医功能复位的相关理论,可以认为椎体强化术后椎体的复位达到了功能复位标准,而且在椎体强化术后伤椎达到功能复位即可满足临床治疗需要,说明中医功能复位适用于指导椎体强化术的临床治疗。在不考虑其他周围结构的应力改变的前提下,为了满足环节临床治疗的需要,达到尽快缓解患者症状的目的,OVCF椎体强化治疗只要达到功能复位即可,并不要求绝对追求伤椎椎体高度的恢复。
该研究从有限元分析生物力学研究的角度,论证了中医功能复位理论的科学性和可行性,也进一步证实了中医功能复位理论指导OVCF椎体强化治疗的临床实用性。
1 韦以宗.中国骨伤科学辞典.北京:中国中医药出版社,2001:89.
2 于沂阳,刘勃,陈伟,等.2008-2012年河北医科大学第三医院老年骨折流行病学特征分析.中华老年骨科与康复电子杂志,2016,2(3):172-176.
3 岑泽波.中医伤科学.上海:上海科技出版社,1985:70.
4 王和鸣,黄桂成.中医骨伤科学.北京:中国中医药出版社,2012:143.
5 李大鹏,黄永辉,左华,等.OVCFs患者经皮后凸成形术后椎体高度恢复的影响因素分析.中国矫形外科杂志,2017,25(14):1249-1253.
6 杜桂迎,余卫,林强,等.WHO双能X线吸收仪骨质疏松症诊断标准及其相关问题.中华骨质疏松和骨矿盐疾病杂志,2016,9(3):330-338.
7 Genant H K,Wu C Y,Van Kuijk C,et al.Vertebral fracture assessment using a semiquantitative technique.J Bone Miner Res,1993,8(9):1137-1148.
8 Liang D,Ye L Q,Jiang X B,et al.Biomechanical effects of cement distribution in the fractured area on osteoporotic vertebral compression fractures:a three-dimensional finite element analysis.J Surg Res,2015,195(1):246-256.
9 Polikeit A,Nolte L P,Ferguson S J.The effect of cement augmentation on the load transfer in an osteoporotic functional spinal unit:finite-element analysis.Spine(PhilaPa1976),2003,28(10):991.
10 Baroud G,Nemes J,Heini P,et al.Load shift of the intervertebral disc after a vertebroplasty:a finite-element study.Eur Spine J,2003,12(4):421-426.
11 Goel V K,Kong W,Han J S,et al.A combined finite element and optimization investigation of lumbar spine mechanics with and without muscles.Spine(Phila Pa1976),1993,18(11):1531-1541.
12 Zhang L,Yang G,Wu L,et al.The biomechanical effects of osteoporosis vertebral augmentation with cancellous bone granules or bone cement on treated and adjacent non-treated vertebral bodies:a finite element evaluation.Clin Biomech(Bristol,Avon),2010,25(2):166-172.
13 Xu G,Fu X,Du C,et al.Biomechanical effects of vertebroplasty on thoracolumbar burst fracture with transpedicular fixation:a finite element model analysis.Orthop Traumatol Surg Res,2014,100(4):379-383.
14 Qiu T X,Teo E C,Zhang Q H.Effect of bilateral facetectomy of thoracolumbar spine T11-L1 on spinal stability.Med Biol Eng Comput,2006,44(5):363-370.
15 Liao J C,Fan K F,Keorochana G,et al.Transpedicular grafting after short-segment pedicle instrumentation for thoracolumbar burst fracture:calcium sulfate cement versus autogenous iliac bone graft.Spine(Phila Pa1976),2010,35(15):1482-1488.
16 Denis F.The three-column spine and its significance in the classification of acute thoracolumbar spinal injuries.Spine(Phila Pa1976),1983,8(8):817-831.
17中华医学会骨质疏松和骨矿盐疾病分会.原发性骨质疏松症诊疗指南(2017).中华骨质疏松和骨矿盐疾病杂志,2017,10(5):413-443.
18 Svensson H K,Olsson L,Hansson T,et al.The effects of person-centered or other supportive interventions in older women with osteoporotic vertebral compression fractures-a systematic review of the literature.Osteoporos Int,2017,28(9):1-20.
19 Hemama M,Fatemi N E,Gana R.Percutaneous vertebroplasty in Moroccan patients with vertebral compression fractures.Pan Afr Med J,2017,26.
20 Svensson H K,Olofsson E H,Karlsson J,et al.A painful,never ending story:older women's experiences of living with an osteoporotic vertebral compression fracture.Osteoporos Int,2016,27(5):1729-1736.
21 Pongchaiyakul C,Nguyen N D,Jones G,et al.Asymptomatic vertebral deformity as a major risk factor for subsequent fractures and mortality:a long-term prospective study.J Bone Miner Res,2005,20(8):1349-1355.
22 Mc Kiernan F,Faciszewski T,Jensen R.Latent mobility of osteoporotic vertebral compression fractures.J Vasc Interv Radiol,2006,17(9):1479-1487.
23 邱贵兴,裴福兴,胡侦明,等.中国骨质疏松性骨折诊疗指南(全文).中华关节外科杂志(电子版),2015,9(6):795-798.
24 金才益,曾忠友,徐阿炳,等.胸腰椎骨折单纯椎弓根螺钉系统治疗的远期结果.中国脊柱脊髓杂志,2002,12(5):398-399.
25 周跃.微创脊柱外科:技术、循证与争论.济南:山东科学技术出版社,2015:218.
26 王和鸣,黄桂成.中医骨伤科学.北京:中国中医药出版社,2012:143.
27 施杞,王和鸣.骨伤科学.北京:人民卫生出版社,2001:732.
28 尚天裕,顾云五.中西医结合治疗骨折.天津:天津大学出版社,1990:253-255.
29 张义龙,任磊,孙志杰,等.椎体成形后新发椎体压缩骨折:与骨质疏松及脊柱矢状位序列失衡有关.中国组织工程研究,2016,20(35):5263-5269.
30 牛广续,刘振峰,王振斌,等.经皮椎体成形高黏度骨水泥注入修复老年椎体压缩骨折:椎体高度恢复评价.中国组织工程研究,2015,19(38):6126-6132.
31 冯献礼,赵景才,高彤.手法复位联合PKP治疗老年骨质疏松性椎体骨折效果分析.山东医药,2016,56(14):93-94.
32 汤亭亭,裴国献,李旭.骨科生物力学暨力学生物学.济南:山东科技出版社,2009:16-21.
33 马信龙,马剑雄,徐卫国,等.骨科生物力学研究的测量方法学专家共识.中国骨质疏松杂志,2014,20(9):1039-1054.
34 郝定均,谢恩,张子如,等.数字化建模在老年骨质疏松椎体压缩性骨折椎体成形术的应用研究.中国骨质疏松杂志,2013,19(4):319-323.
35 Cho A R,Cho S B,Lee J H.Effect of Augmentation Material Stiffness on Adjacent Vertebrae after Osteoporotic Vertebroplasty Using Finite Element Analysis with Different Loading Methods.Pain Physician,2015,18(6):E1101-1110.
36 Kim J M,Shin D A,Byun D H,et al.Effect of bone cement volume and stiffnesson occurrences of adjacent vertebral fractures after vertebroplasty.J Korean Neurosurg Soc,2012,52(5):435-440.
