三七二醇皂苷含量测定方法建立及其固有稳定性研究
2018-06-13余佳丽唐晓章周菲林美斯林大胜曹科
余佳丽,唐晓章,周菲,林美斯,林大胜,曹科
三七二醇皂苷 (Panaxadiolsaponins,PDS)是三七药材经乙醇提取、大孔吸附树脂分离纯化后得到的一类结构类似的原人参二醇型皂苷,具有较强的药理活性,其中人参皂苷Rb1和人参皂苷Rd为其主要活性成分[1],占PDS总组分的50% 以上。基于PDS在心脑血管系统、中枢神经系统、免疫系统及抗肿瘤等方面体现出的良好的药用价值[2-5],课题组拟将其作为候选药物,开发PDS新制剂。本实验选取人参皂苷Rb1和Rd作为代表性成分,建立同时测定PDS中两种主要药效成分的含量测定方法,并进行方法学考察,为PDS含量测定和过程质量控制提供方法。在此基础上,对PDS在多种条件下的固有稳定性进行初步研究,可为其进一步的制剂开发提供科学依据。
1 材料
1.1 仪器
Agilent 1260高效液相色谱仪(配有vwd检测器、自动进样器、四元梯度泵、在线脱气装置,美国Agilent公司),Agilent Chem Station色谱工作站(美国Agilent公司);BT 125D型十万分之一电子天平(德国Sartorius公司);SB25-12 DTD型超声波清洗机(宁波新芝生物科技股份有限公司);PCDXJB-10型实验室专用超纯水机(成都品成科技有限公司);SHH-SDT综合药品稳定性试验箱(重庆市永生实验仪器厂)。
1.2 试药
人参皂苷Rb1,人参皂苷Rd对照品(批号分别为110704-201625,111818-201603;纯度分别为93.7%,92.1%)均由中国食品药品检定研究院提供;乙腈为色谱纯(美国Fisher公司),水为超纯水,其它试剂均为分析纯。PDS原料药由成都泰合健康科技集团股份有限公司华神制药厂生产。
2 方法与结果
2.1 分析方法的建立
色谱柱:Waters Symetry Shield C18柱(4.6 mm×250 mm,5 μm);流动相:乙腈(A)-水(B),梯度洗脱(0~15min,31%A;15~16min,31%→36%A;16~25min,36%A);流速:1mL﹒min-1;检测波长:203 nm;柱温30℃;进样量:10 μL。
2.2 溶液的制备
2.2.1 空白溶液 31%的乙腈水溶液(初始流动相)。
2.2.2 混合对照品溶液 取人参皂苷Rb1对照品约15 mg,人参皂苷Rd对照品约2 mg,精密称定,置于20 mL容量瓶中,用31%乙腈水溶液溶解并定容至刻度,摇匀,即得。
2.2.3 供试品溶液 取PDS原料粉末约0.15 g,精密称定,置于具塞量瓶中,精密加入100 mL 31%乙腈水溶液后称重,超声(功率150w,频率40kHz)处理15min,冷却后补足损失的重量,摇匀,滤过,取续滤液,临用前用0.45 μm微孔滤膜滤过,即得。
2.3 方法学考察
2.3.1 系统适用性及专属性 按照“2.2”方法分别制备得到空白溶液、混合对照品溶液和供试品溶液,按“2.1”项下色谱条件进行测定,记录色谱图,见图1 。结果显示,对照品连续进样5针,人参皂苷Rb1的峰面积的 RSD 为 0.51%,人参皂苷Rd的峰面积的RSD 为0.86%,对照品和供试品溶液中人参皂苷Rb1和Rd色谱峰的对称因子在0.95~1.05之间,色谱峰与前后杂质峰的分离度均大于1.5,理论塔板数均不小于6000,且空白溶液对主色谱峰无干扰,该色谱条件的系统适用性及专属性良好。

图1 三七二醇皂苷及其对照品HPLC图
2.3.2 线性范围 取人参皂苷Rb1和Rd对照品适量,精密称定,置于10 mL容量瓶中,加入31% 乙腈水溶液溶解并定容,作为母液。分别精密量取适量上述母液,稀释配制成人参皂苷Rb1浓度分别为0.1502、0.6008、0.7510、0.9012、1.5020 mg﹒mL-1的系列对照品溶液,人参皂苷Rd浓度分别为0.0202、0.0809、0.1011、0.1213、0.2022 mg﹒mL-1的系列对照品溶液。按“2.1”项下色谱条件进行测定,记录色谱。以质量浓度(X,mg﹒mL-1)为横坐标、峰面积(Y)为纵坐标进行线性拟合,结果表明,人参皂苷Rb1的标准曲线线性方程为:Y=2295.3X+8.0707,r=0.9993,线性范围为0.1502~1.5020 mg﹒mL-1;人参皂苷Rd的标准曲线线性方程为:Y=2636.5X+11.733,r=0.9995,线性范围为0.0202~0.2022 mg﹒mL-1。
2.3.3 精密度 取“2.2.2”项下制备的混合对照品溶液,连续进样6次,记录峰面积,计算RSD,考察方法的精密度。结果见表1。
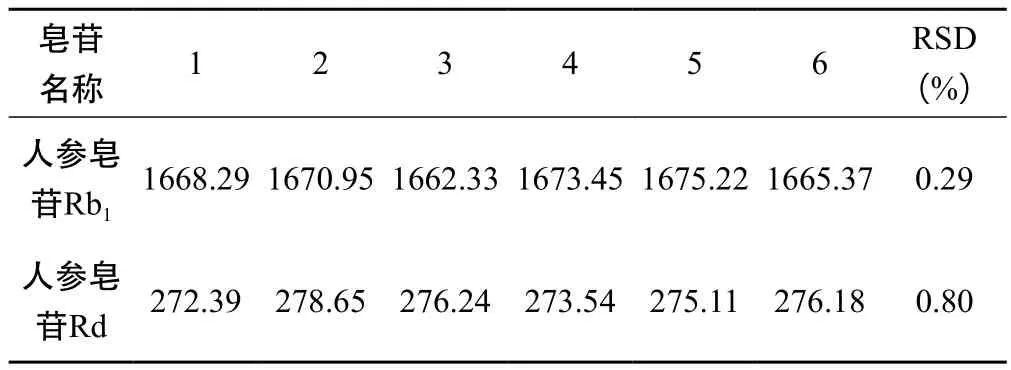
表1 精密度试验结果(n=6)
2.3.4 重复性 取PDS原料粉末约0.15 g,共6份,精密称定,按照“2.2.3”项下方法制备得到6份供试品溶液。按“2.1”项下色谱条件进行测定,记录色谱,分别计算人参皂苷Rb1和人参皂苷Rd的含量(%)。结果见表2。

表2 重复性试验结果(n=6)
2.3.5 加样回收率 精密量取已知浓度的混合对照品溶液0.5、1、1.5 mL,分别置EP管中,氮气吹干溶剂,每浓度下平行操作3份。精密量取已知浓度三七二醇皂苷供试品溶液1 mL,分别加入上述9个EP管中,涡旋、超声使完全溶解后。按“2.1”项下色谱条件进行测定,记录色谱,并计算加样回收率。结果见表3、表4。

表3 人参皂苷Rb1加样回收率试验结果

表4 人参皂苷Rd加样回收率试验结果

5 0.0492 0.0558 0.1039 98.10%6 0.049 0.0558 0.1047 99.74%7 0.049 0.0837 0.1326 99.85%8 0.049 0.0837 0.1317 98.82%9 0.0492 0.0837 0.1332 100.39%
2.3.6 溶液稳定性 取“2.2.2”和“2.2.3”项下混合对照品和供试品溶液各适量,分别于室温下放置0、2、4、6、8、12、24 h,按“2.1”项下色谱条件进行测定,记录色谱。结果对照品溶液中人参皂苷Rb1和Rd峰面积的RSD值分别为0.32%和0.62%,供试品溶液中人参皂苷Rb1和Rd峰面积的RSD值分别为0.41%和1.22%,提示对照品和供试品在溶剂中24h内均具有良好的稳定性。
2.3.7 耐用性 通过单变量分析法微调测试条件中的单个变量观察结果的不同影响程度,改变的测试变量为色谱条件变量(流速、柱温和色谱柱)[6],记录色谱,分别计算人参皂苷Rb1和人参皂苷Rd的含量。结果见表5。

表5 耐用性试验结果
2.4 固有稳定性研究
2.4.1 不同pH值溶液对PDS主要药效成分的影响 取PDS 原料药约0.15 g,共5份,精密称定,置于100 mL容量瓶中,分别加入蒸馏水、pH 7.4、pH 6.8、pH 4.5及pH 1.2的缓冲溶液使溶解,并定容至刻度,于室温下放置,分别于第0、2、4、8、12、24 h取样,按“2.1”项下色谱条件进行测定,记录色谱,并以0 h时各皂苷的含量为100%,分别计算不同时间点各皂苷的含量变化情况。结果见表6。
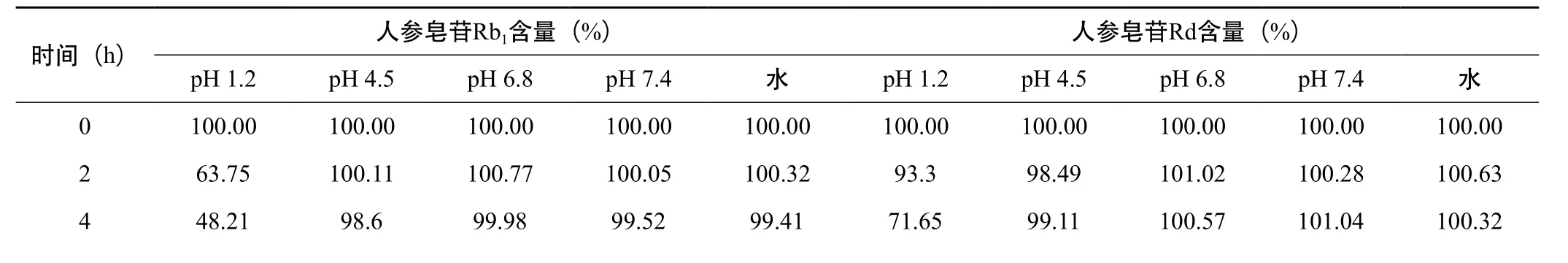
表6 不同pH值溶液中PDS主要成分稳定性实验结果

8 22.32 101.23 99.65 100.14 100.78 31.96 100.24 99.73 99.41 101.0912 10.18 100.47 101.21 100.34 99.65 17.53 98.82 100.44 100.69 100.7824 4.29 99.34 100.72 101.25 99.3 6.98 100.71 99.65 100.7 99.24
2.4.2 高温试验 取适量PDS原料药置称量瓶中,摊成厚度≤5 mm的薄层,在60℃ 综合药品稳定性试验箱中放置10d,于5,10d取样,考察样品含量的变化。结果见表7。

表7 高温试验结果
2.4.3 高湿试验 取适量PDS原料药置称量瓶中,摊成≤5 mm厚的薄层,在25℃ 相对湿度(75±5)%的综合药品稳定性试验箱中放置10 d,于5,10 d取样,考察样品的重量和含量的变化。结果见表8。

表8 高湿试验结果
2.4.4 强光试验 取适量PDS原料药置称量瓶中,摊成≤5 mm 厚的薄层,置于综合药品稳定性试验箱内,在照度为(4500±500)lx的条件下放置10 d,于5,10 d取样,考察样品的外观和含量的变化。结果见表9。

表9 强光试验结果
3 讨论
3.1 PDS主要药效成分含量测定方法的建立
本实验选取人参皂苷Rb1和Rd作为代表性成分,通过调整流动相比例,在保证目标成分分离完全的情况下,建立同时测定PDS中两种主要药效成分的含量测定方法,与三七药材含量测定方法比较,显著缩短了检测时间。该方法操作简单,重复性、准确度及耐用性等均良好,为PDS主要药效成分的含量测定和过程质量控制提供了科学合理的方法。
3.2 PDS固有稳定性的研究
药物固有稳定性研究作为处方前研究的重点内容[7],可以有效指导制剂开发过程中辅料与剂型的选择、处方设计及工艺优化等。但在传统中药制剂的研究中,鲜有针对制剂流程中某成分的含量变化或稳定性的关注。本实验通过对不同pH值溶液对PDS主要药效成分影响的考察,发现PDS在强酸溶液中极不稳定。因此,在制剂制备过程中应该避免使用强酸性溶媒,而在给药途径选择时,应考虑胃酸环境对PDS的影响。影响因素试验结果表明,高温、高湿和强光对PDS稳定性均有一定程度的影响,提示PDS应在常温、干燥、避光条件下制备与保存,作为口服剂型的原料药或应慎重选择辅料以保证其稳定性。
[1]王莹,褚扬,李伟,等.三七中皂苷成分及其药理作用的研究进展[J].中草药,2015,46(9):1381.
[2]姚宇涵.三七二醇皂苷对MCAO模型大鼠脂联素、sCD40L和GOX-2的影响[D].成都中医药大学,2015.
[3]惠永正,王玉芹,葛强.三七二醇组皂苷及其在制备治疗记忆力减退、预防和治疗老年痴呆药物中的应用, [P]CN101007035.2007.
[4]Zhang Y X, Wang L, Xiao E L, et al.Ginsenoside-Rd exhibits anti-inflammatory activities through elevation of antioxidant enzyme activities and inhibition of JNK and ERK activation in vivo[J].International Immunopharmacology, 2013,17(4):1094.
[5]刘晓慧.三七二醇组皂苷抑制Hela细胞生长的研究[D].昆明理工大学, 2009.
[6]相婷, 吴丽真, 王绍青,等.泽兰中迷迭香酸含量测定方法学研究[J].中国现代中药, 2017, 19(2):205.
[7]陆燕, 潘旭.三七总皂苷中代表性皂苷含量测定方法学的建立及稳定性研究[J].中国药物应用与监测, 2014(2):88.
