微波辅助三乙醇胺还原法制备高SERS活性AuNF
2018-06-05黎小椿庞永丰张志苏林静唐小闲罗杨合黄双全
黎小椿,庞永丰,2,张志,苏林静,唐小闲,罗杨合,2,*,黄双全,2
(1.贺州学院食品科学与工程技术研究院,广西贺州542899;2.大连工业大学食品学院,辽宁大连116034)
随着科学技术的发展与进步,胶体纳米材料的应用不断推广,应用领域也在不断扩大。金属纳米胶体的应用由化学催化、摄影、着色技术已发展到分子生物学、医学等多个领域。金属胶体纳米材料由于具有催化活性、生物相容性等倍受人们的追捧。Wiesner等最初将金属纳米胶体应用于表面增强拉曼散射(surface-enhanced Raman scattering,SERS)研究,其目的是获得胶体稳定机理的详细信息[1]。近几十年来,人们经过大量研究证明,金属胶体可作为高效SERS活性基底,它们可使吸附分子的拉曼信号强度增强105~107个数量级,尤其是银溶胶和金溶胶,以它们来做SERS活性基底已经获得了多种分子高质量的表面增强拉曼散射(SERS)光谱,并广泛用于探讨SERS增强机制的研究中[2-3]。由于金属溶胶是一种方便、有效、灵敏度很高的吸附衬底,同时在激光照射下金属溶胶中不存在像其它衬底那样的光损伤,因而它一直深受理论和实验工作者的重视,而且金纳米具有特殊的光学特性、生物相容性及催化特性,被作为检测H2O2、Hg2+、白蛋白最普遍的纳米标志物之一[4]。目前,金属胶体纳米材料的合成方法主要是还原法,而金纳米花的合成方法主要有种子生长法[5]、无核原位生长法[6]和仿生合成法[7]。最常用的合成方法是种子生长法,用于有核金纳米花的合成,而且通过对还原剂及反应条件的调节和控制可合成具有不同形态、尺寸和尖端的金纳米花[8-9]。采用胺还原法合成的金纳米花表面干净,尖端长而宽,具有较高表面增强拉曼活性,适用于发展为SERS标记和用于SERS成像[9],但耗时长。微波辅助合成表面增强拉曼活性基底的方法已有研究[10-12],它大大缩短了纳米材料合成的时间,且合成基底较为稳定。本文采用氧化还原微波制备方法,用三乙醇胺和氯金酸制备表面高度分支化的金纳米花。并通过反复试验摸索制备出稳定的、具有较高表面增强效果的蓝青色金纳米花(gold nano-flower,AuNF)溶胶,利用荧光分光光度计、紫外可见分光光度计测试了金纳米花(AuNF)溶胶的共振光谱和吸收光谱,结合AuNF测维多利亚蓝B(Victoria blue B,VBB)的SERS光谱筛选出最佳制备条件,并用VBB初步判断所制备银溶胶的增强效果。
1 材料与方法
1.1 仪器与试剂
633nm DXR smart拉曼光谱仪:美国Thermo公司,激光功率为8.0 mW,激光到样品表面的功率为3 mW,光阑为50,使用智能背景,采集时间为1.0 s,样品曝光时间为30 s;F-4600荧光分光光度计:日立高新技术公司,激发波长为200 nm,发射波长为200 nm~700 nm,狭缝为5.0,电压为380 V;Evolution300型紫外可见分光光度计:广西金鑫进出口有限公司,步长范围为200 nm~1 000 nm,频宽(Bandwidth)为0.5 nm,扫描速度(Scan Speed)为240 nm/min,间隔数据(Data Interval)为1.0 nm,灯变(Lamp Change)为Xenon,图高为2.000 A,图低为0.000 A;MR Hei-Tec加热型磁力搅拌器:德祥科技有限公司;JEM-2010高分辨透射电子显微镜:电子束加速电压200 kV。
氯金酸(AR):国药集团化学试剂有限公司;三乙醇胺(AR)、乙二醇(AR)、硝酸银(AR):广东光华科技股份有限公司;氯化钠(AR):成都科龙化工试剂厂;维多利亚蓝B(AR):汇普化工有限公司;超纯水(18.25 MΩ·cm)。
1.2 方法
金纳米花(AuNF)溶胶的制备:把装有20 mL乙二醇的锥形瓶放入磁力搅拌器上的烧杯中40℃水浴加热,在搅拌的条件下(700 r/min)先后加入 200 μL、1%的 HAuCl4和 405 μL、2.5 mol/L 新制备的三乙醇胺,充分混合后,颜色由淡黄色→无色→淡蓝色,当颜色为浅蓝色时立即移入700 W微波炉加热20 s,得到蓝青色金纳米花,其浓度为2.23×10-4mol/L。冷却后置于 4℃冰箱中密封保存。
准确配置 5.76 × 10-3mol/L 的硝酸银溶液、1 ×10-3mol/L的氯化钠溶液和1×10-4mol/L维多利亚蓝B(victoria blue B,VBB)溶液。试验时取 10 μL配置好的 1×10-4mol/L 维多利亚蓝 B 溶液与 90 μL、2.23×10-4mol/L蓝青色金纳米花溶胶混合,然后依次加入80 μL、5.76×10-3mol/L的硝酸银溶液和 90 μL、1×10-3mol/L的氯化钠溶液,最后定容2 mL,倒入比色皿直接进行常规拉曼光谱测试。
2 结果与分析
2.1 方法原理
在金属胶体溶液中,纳米粒子的聚集可使检测物的SERS信号得到增强。高氯酸盐、硝酸盐、氯化物及一些有机聚合物常被用来作为聚集剂。试验加入的Ag+通过分子间的作用力吸附在纳米表面使AuNF形成不稳定的聚集体,SERS信号得到增强。同样无机盐NaCl可使SERS信号增强。当同时加入AgNO3和NaCl时,AgNO3和NaCl形成溶解度较低的AgCl胶体,Au原子与AgCl分子表面通过强疏水作用力形成大而稳定的AuNF/AgCl聚集体,从而使SERS信号大幅度增强。
2.2 高SERS活性AuNF的TEM图
AuNF的TEM图见图1。

图1 AuNF的TEM图Fig.1 Figure TEM of AuNF
从AuNF的TEM图(图1)中可知,采用微波辅助三乙醇胺还原氯金酸可快速合成金纳米花(AuNF)溶胶,合成的AuNF粒径在50 nm~100 nm之间,尖端较多,且表面比较粗糙,有效增加基底与底物的接触,还有利于不同粒子间形成针尖效应,提高基底的增强效果。因此,可预测合成的AuNF溶胶适用于做表面增强拉曼的基底。
2.3 高SERS活性AuNF的紫外一可见吸收光谱
球状金纳米粒子只有一个位于500 nm~550 nm的吸收峰,伴随着粒径的增大或聚集吸收峰会发生红移或展宽,溶胶的颜色会由红色变为蓝色或紫色。棒状金纳米粒子产生2个吸收峰,垂直于棒轴向的横向吸收峰位于510 nm~530 nm,沿着棒轴向的众向吸收峰位于更长波长范围。试验制备的金纳米溶胶最大吸收峰在601 nm处见图2,且其吸收峰的半峰宽大于100 nm,说明制备的金纳米花状尖端较长,具有较好的尖端效应,适用于表面增强拉曼基底。在不同微波时间条件下其最大吸收峰的位置发生变化(见图3)。由此可知,微波时间在5 s~25 s之间,最大吸收峰会发生红移,表明金纳米花不断长大;微波时间超过25 s时,最大吸收峰发生蓝移,可能温度过高导致尖端纳米花被钝化,导致粒径变小。微波20 s制得的金纳米花溶胶吸收峰较高,说明该反应时间制得的金纳米花在溶液中的浓度最大,当微波时间超过20 s,会使生成的AuNF产生沉淀,导致吸收峰强度降低。故实验选择微波20 s的条件来制备金纳米花。
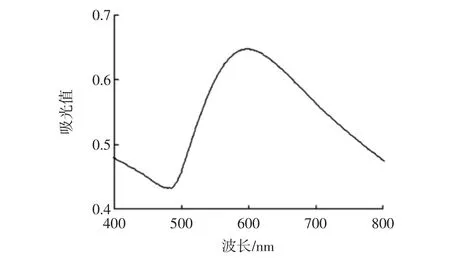
图2 AuNF的吸收光谱Fig.2 Absorption spectra of AuNF
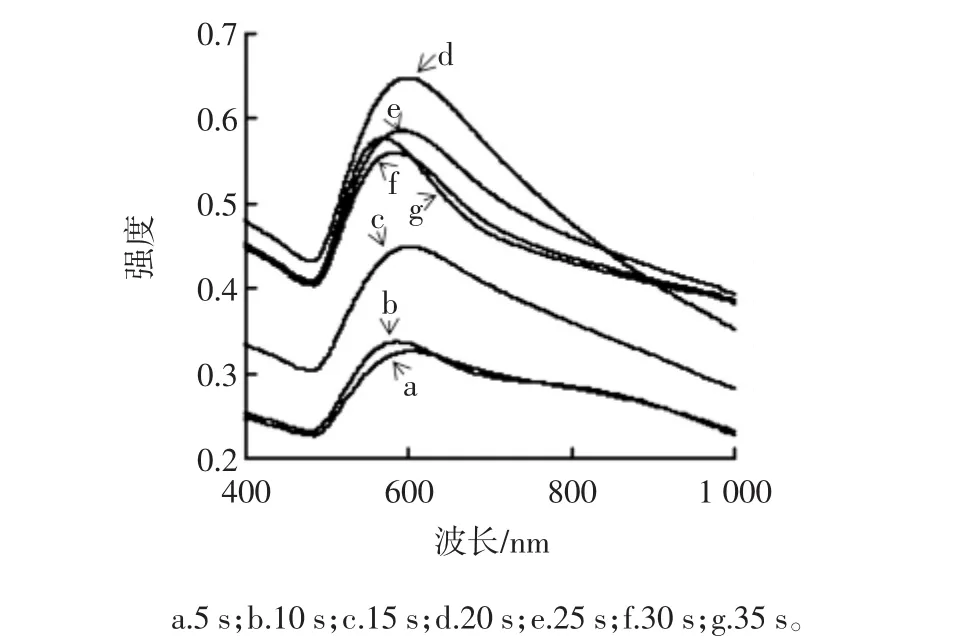
图3 不同微波时间AuNF的吸收光谱Fig.3 Absorption spectra of AuNF at different microwave time
2.4 高SERS活性AuNF的共振瑞利散射(resonance rayeigh scattering,RRS)光谱
AuNF有着特殊的表面粗糙度及尖端效应使其有4 个 RRS 峰,他们的位置分别为282、365、437、495 nm见图4。随着微波时间的增加,RRS峰先增强后减弱见图5。
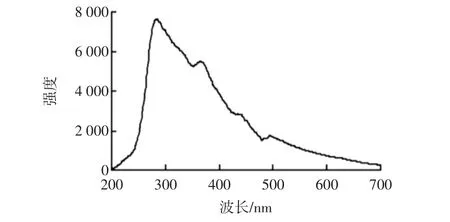
图4 AuNF的RRS光谱Fig.4 RRS spectra of AuNF

图5 不同微波时间AuNF的RRS光谱Fig.5 RRS spectra of AuNF at different microwave time
当微波时间为20 s时,RRS最强,故选择微波20 s来制备金纳米花。
2.5 高SERS活性AuNF的表面增强拉曼散射能力
以维多利亚蓝B为分子探针,检验试验制备的AuNF的SERS活性见图6。由图6分析可知,在1 618 cm-1处,出现了VBB的SERS光谱特征峰,随着AuNF浓度的增大,SERS光谱峰逐渐增强,由此可知,所制得的AuNF具有较强的表面增强效应。AuNF在不同无机盐的作用下SERS效应增强(见图7)。从图可知,在基底AuNF中分别加入无机盐AgNO3和NaCl后,1 618 cm-1处SERS峰增强,说明无机盐的加入使AuNF聚集,SERS效应增强。同时加入AgNO3和NaCl,两者反应生成AgCl胶体,在胶体的存在下,1 618 cm-1处SERS峰显著性增强,表明胶体AgCl使AuNF形成更稳定的聚集体,从而使SERS活性增强。

图6 不同浓度AuNF的SERS光谱Fig.6 SERS spectra of AuNF at different concentrations
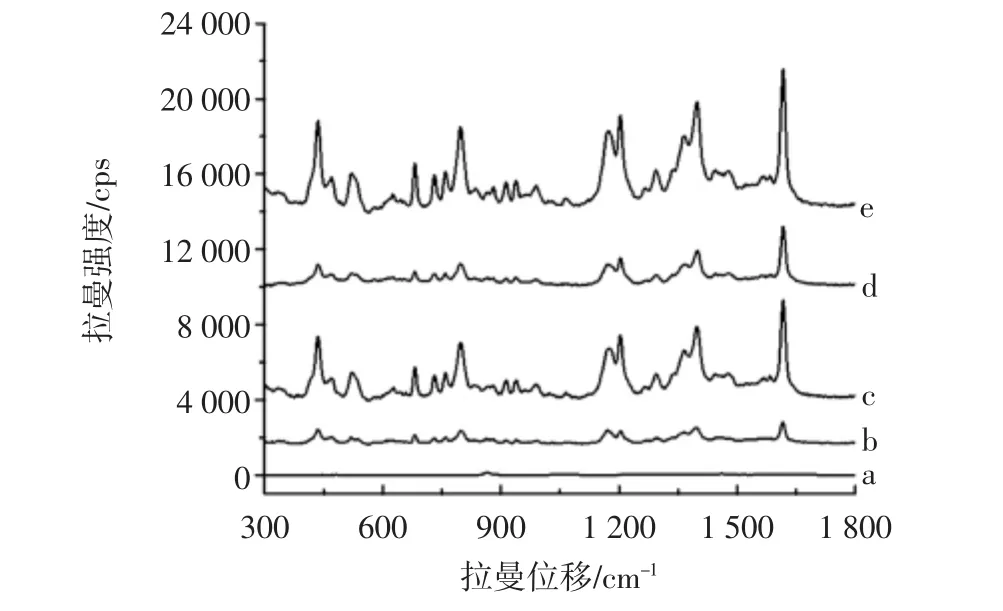
图7 不同聚集体下VBB的SERS光谱Fig.7 SERS spectra of VBB under different aggregates
3 结论
采用微波辅助氧化还原法,通过反复试验摸索制备得到了具有较好增强效果的金纳米花溶胶。测试并分析了所制备银溶胶的紫外一可见吸收光谱图,结果表明所制备金纳米花溶胶的粒径基本上分布在一个相当窄的范围内。以VBB为例检验了其SERS活性。综上所述,微波20 s条件下所制备的金纳米花溶胶适合用作SERS活性基底,同时胶体AgCl的存在,使SERS效应显著性增强。这为该基底用于食品分析研究工作奠定了好的基础。
[1]Wiesner J,Wokaun A,Hoffmann H.Surface enhanced Raman spectroscopy (SERS)of surfactants adsorbed to colloidal particles[J].Progress in Colloid and Polymer Science,1988,117:271-277
[2]Fornasiero D,Grieser F.Analysis of the visible absorption and SERS excitation spectra of silver sols[J].The Journal of Chemical Physics,1987,87(5):3213-3217
[3]Ji Y W,Ren M L,Li Y P,et al.Detection of aflatoxin B 1 with immunochromatographic test strips:Enhanced signal sensitivity using gold nanoflowers[J].Talanta,2015,142:206-212
[4]Jiang Z L,Qin H M,Liang A H.A New Nanocatalytic Spectrophotometric Assay for Cationic Surfactant Using Phosphomolybdic Acid-Formic Acid-Nanogold as Indicator Reaction[J].Chinese journal of structural chemistry,2012,30(1):59-64
[5]Zou X Q,Ying E B,Dong S J.Seed-mediated synthesis of branched gold nanoparticles with the assistance of citrate and their surfaceenhance Raman scattering properties[J].Nanotechnology,2006,17(18):4758-4764
[6]Han J,Li J,Jia W,et al.Photothermal therapy of cancer cells using novel hollow gold nanoflowers[J].International Journal of Nanomedicine,2014,16(9):517
[7]Huang P,Pandoli O,Wang X S,et al.Chiral Guanosine 5'-Monophosphate-Capped Gold Nanoflowers:Controllable synthesis,Characterization,Surface-Enhanced Raman Scattering Activity,Cellular Imaging and Photothermal Therapy[J].Nano Research,2012,5(9):630-639
[8]Zhang Q L,Zhou D L,Li Y F,et al.Cytosine-assisted synthesis of gold nanochains and gold nanoflowers for the construction of a microperoxidase-11 based amperometric biosensor for hydrogen peroxide[J].Microchimica Acta,2014,181(11/12):1239-1247
[9]Jiang Y Y,Wu X J,Li Q,et al.Facile synthesis of gold nanoflowers with high surface-enhanced Raman scattering activity[J].Nanotechnology,2011,22(38):385601
[10]Wang Y H,Zhang X H,Wen G Q,et al.Facile synthesis of a highly SERS active nanosilver sol using microwaves and its application in the detection of E.coli using Victoria blue B as a molecular probe[J].Analytical Methods,2016,8(24):4881-4887
[11]范培迪,汪孝亮,梁爱惠,等.微波辐照乙醇还原法绿色合成纳米金溶胶[J].光谱学与光谱分析,2016,36(10):317-318
[12]彭宇涛,梁爱惠,蒋治良.微波绿色合成金纳米溶胶及其光谱特性研究[J].光谱学与光谱分析,2016,36(10):407-408
