过渡金属氧化物空心球的制备及催化性能研究进展
2018-05-11汪长安
汪长安,张 健,龚 铭,李 洒,2
1清华大学 材料学院,新型陶瓷与精细工艺国家重点实验室,北京100084 2同济大学 材料科学与工程学院,上海201804
过渡金属氧化物空心球由于具有高比表面积、高孔隙率、良好的渗透性和特殊的多级孔结构,在催化、药物缓释、能源环境、化妆品、颜料和传感器等领域有着广泛的应用前景[1-4]。近10年来,微纳米氧化物中空结构的合成得到了飞速发展,研究者设计出了形式多样的中空结构制备技术,并能够稳定合成出各种形貌可控、多壳层、多组分的复合金属氧化物中空结构,为将来实际应用打下了坚实的基础,也进一步拓宽了其应用范围。
过渡金属氧化物是一类重要的催化材料,具有抗中毒、热稳定性好、使用寿命长、对氧化反应的选择性高、非化学计量的Men+/O2-比值、且Me离子在反应气氛作用下价态可变等特点。过渡金属氧化物中空结构吸引了催化领域研究者的浓厚兴趣。对于中空结构的制备,早在2002年,韩国研究者Kim等人[5]就将单分散SiO2纳米球为模板制备得到的金属钯纳米空心球应用到Suzuki偶联反应中,并显现出了良好的催化活性和循环稳定性,经过7次循环后催化活性仍然达到了95%以上。
近10年来,过渡金属氧化物中空结构在催化中的应用更是取得了突飞猛进的发展,究其缘由大概可从以下几个方面来分析:其一,与其它组分相同但结构不同的材料相比,金属氧化物中空结构通常具有更大的比表面积,对于催化剂而言,比表面积越大催化活性点就越多,故提高比表面积是提高催化剂催化活性最好的方法之一[6]。其二,金属氧化物空心球是由介孔的壳层和内部的大孔所组成的多级孔结构材料,可作为催化的微型反应器将催化活性物种束缚在中空结构内部,这样不仅可以有效解决贵金属等活性物种在催化过程中的烧结团聚问题,也能够将相互不兼容的催化功能组元统一到同一个结构中[7]。其三,空心球的壳层是由纳米颗粒组装而成,因而可通过控制纳米颗粒大小和壳层厚度来控制壳层的孔径,空心球的多级孔结构可大幅度提高反应物的传输速率,使反应物与催化活性中心充分接触,进而提高其催化活性[8]。其四,组成壳层的纳米颗粒尺寸通常只有几个纳米,而尺寸越小,纳米颗粒的表面缺陷越多,活性物种的配位数也就越低,这一点也是空心球具有良好催化活性的一大原因[9]。除以上四个优点外,对于特殊的反应,过渡金属氧化物空心球在催化反应中也有其独特的优势,比如在光催化中,空心球可以有效地增强光的散射与吸收,从而提高光的利用率;再比如可通过控制空心球的亲水/憎水特性,将反应溶剂填充到空心球内部,从而提高催化剂催化活性[10]。总而言之,过渡金属氧化物空心球在催化反应中有其它材料不可比拟的优点,有许多特性尚待进一步发掘。
本文总结了作者所在课题组在近年来开展的过渡金属氧化物空心球制备及催化性能的一些研究进展,并对未来发展作了简单的展望。
1 Co3O4空心球的制备及其在甲烷燃烧中的催化作用[11]
我们制备了具有多级孔结构和高比表面积的Co3O4空心球,并通过对碳球模板酸处理或碱处理,实现了空心球球壳厚度和孔结构的调节,获得了优异催化CH4燃烧活性和催化稳定性。
选择葡萄糖水热法制备的胶体碳球 (Colloidal Carbon Spheres, CCS) 作为硬模板,通过静电吸附和原位氧化还原反应来制备 Co3O4纳米空心球。采用葡萄糖水热法制备的碳球具有以下三个特点:其一,制备过程简单,通过控制水热条件可得到不同尺寸、单分散良好、粒径分布均匀的亚微米碳球;其二,由于表面富含 -OH、-CHO、C-O等活性基团,胶体碳球表面带负电且具有还原性;其三,在较低温度下能够分解,因此成为研究者制备空心球最常用的模板之一[12]。

图1 水热法制备胶体碳球的SEM和TEM照片Figure1 (a) SEM and (b) TEM images of as-synthesized carbon spheres by hydrothermal process
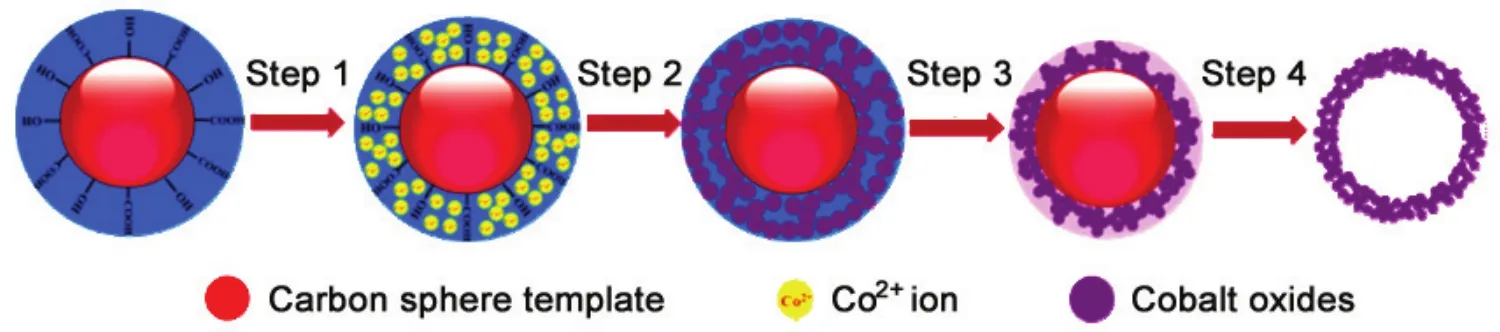
图2 Co3O4纳米空心球的制备原理图Figure2 Schematic illustration of formation process of the hollow Co3O4 sphere
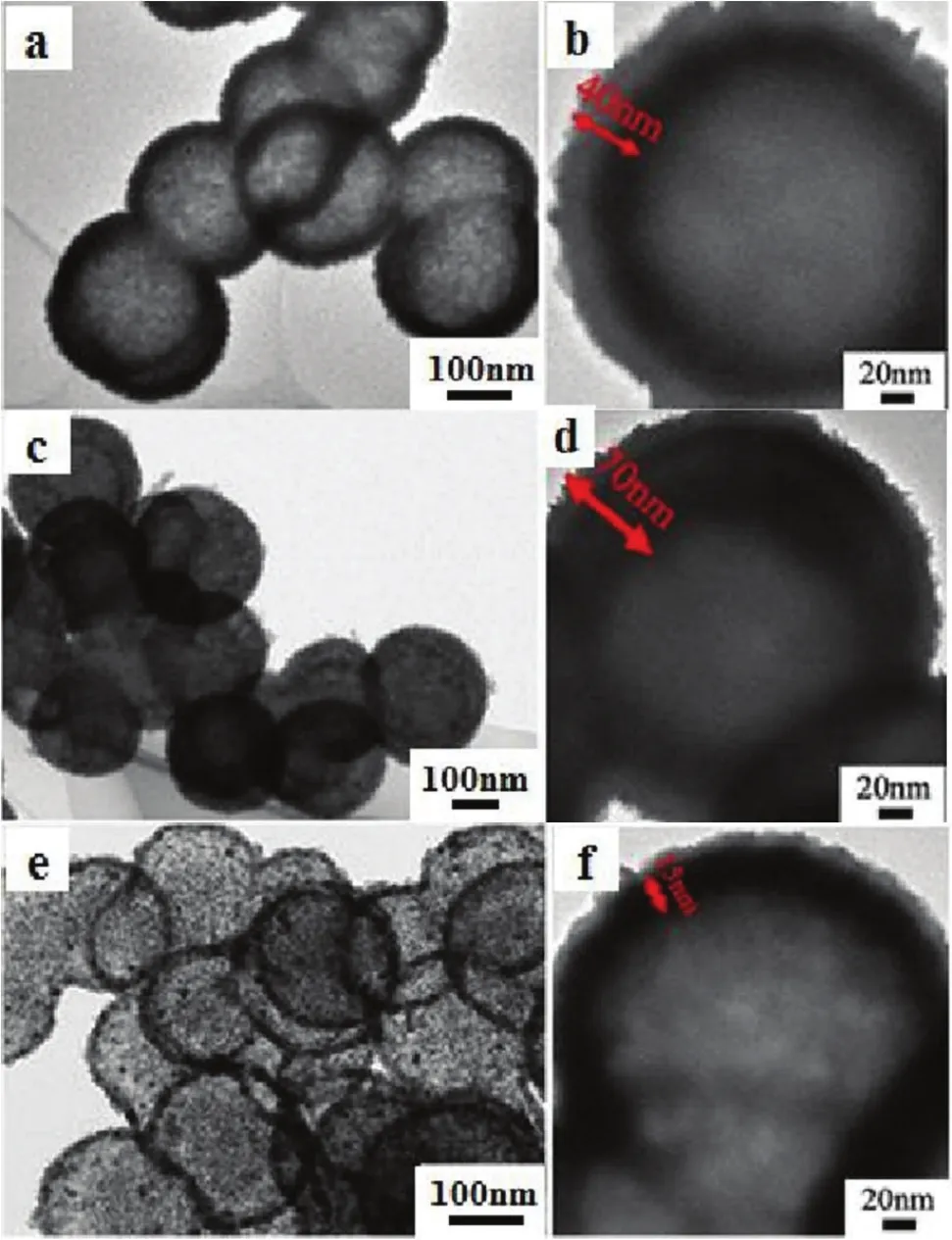
图3 经不同方式处理的碳球模板所合成的Co3O4空心球TEM 照片:(a, b) 碳球模板未处理;(c, d) 用碱处理碳球模板;(e, f) 碳球模板酸处理Figure3 TEM images of hollow spheres synthesized by using (a, b) un-treated, (c, d) alkali-treated and(e, f) acid-treated carbon spheres as the template
图1所示为胶体碳球的扫描电镜 (SEM) 和透射电镜 (TEM) 照片,可以看出胶体碳球的直径约为200 nm ~ 300 nm。图2所示为Co3O4空心球的制备流程图。我们利用碳球表面带负电的特点,通过静电吸附方法来得到CCSs@Co3O4核壳结构。但通过静电吸附方法得到的空心球壳层厚度是不可控的。基于这一点,我们创造性地利用HCl和NaOH对碳球表面进行改性。通过HCl改性后碳球表面的官能团会减少,ξ-电位增加;而通过NaOH改性则会使碳球表面的有机官能团增加,ξ-电位进一步降低,这样就能得到壳层厚度可控的Co3O4空心球。
图3所示为分别使用未处理、碱处理和酸处理碳球制备得到的Co3O4空心球,其壳层厚度分别为40 nm、70 nm和15 nm。
模板法合成空心球的一个难点就是当模板去除后,中空结构容易坍塌。我们设计了一个特殊的两步煅烧法热处理制度来避免这一问题:首先在氩气环境下煅烧包覆Co3O4前驱体的复合球体,将氧化钴纳米晶壳层部分烧结在一起形成坚硬的外壳,增加了包覆层的机械强度,从而阻止了去除碳球核芯时发生塌陷;然后再将球体在空气中450°C下高温处理去除芯部的碳核。如图3 (e) ~ (f) 所示,壳层厚度为15 nm时中空结构仍然能够保持完整。
将制备得到的空心球应用于甲烷燃烧实验,结果如图4所示,三种空心球均具有良好的催化活性,远高于共沉淀法得到的实心纳米粉,其中酸处理得到的空心球具有最高的催化活性,在 325°C时对甲烷燃烧的催化率达到了100%,经过48 h的定温测试后催化活性仍然没有衰减迹象,说明Co3O4空心球具有良好的催化稳定性。催化活性的差异来源于比表面积及孔隙率的不同。壳层厚度越薄,比表面积越大,孔隙率也越高,催化活性越大。
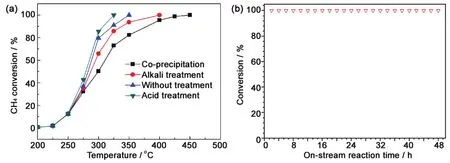
图4 不同制备条件下得到的Co3O4空心球在催化甲烷转化时的催化活性与稳定性曲线(a) 温度与转化率的关系曲线;(b) 325°C下催化CH4燃烧时的转化率与催化时间的关系Figure4 (a) Methane conversion curves versus temperature over porous Co3O4 catalysts under different preparation conditions, and (b) time dependent CH4 conversion at 325°C
2 Ag负载TiO2空心球的合成与光催化性能[13]
TiO2的光催化活性已经得到广泛的研究。研究表明,TiO2光催化活性很大程度上取决于它的形貌与结构,而特别值得注意的是,TiO2空心球由于具有低密度、高比表面积和较好的表面渗透率等特性而呈现出优异的光催化性能,但光生电子与空穴的快速复合则严重影响了TiO2的光催化活性。Ag纳米颗粒作为电荷俘获剂添加到TiO2结构中能够有效地分离电子和空穴,从而显著提高材料的催化性能。因此,我们制备了由Ag和TiO2纳米颗粒所组成的复合结构空心球Ag/TiO2,并研究了其光催化活性。
图5所示为Ag负载TiO2空心球的制备流程示意图。我们首先在碳球模板上负载纳米Ag颗粒,然后再包裹TiO2,这样就可以有效避免因为在去除模板和催化过程中纳米Ag颗粒的长大和团聚而影响材料的催化性能。在如图5所示的制备过程中发生了以下反应:
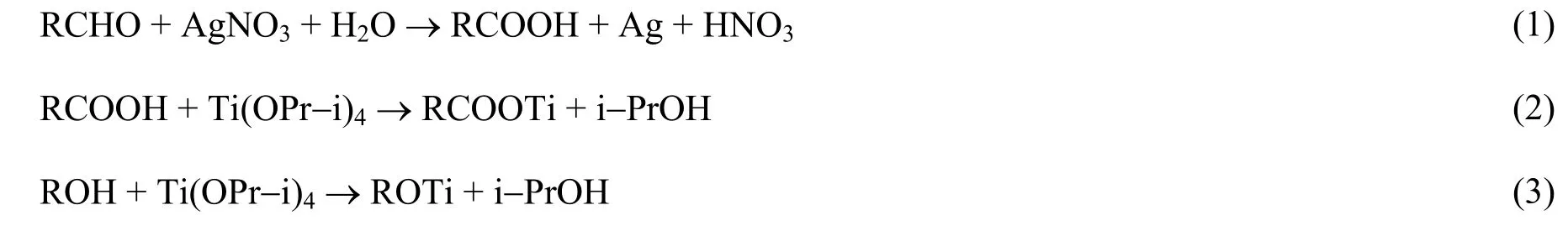
图6所示为Ag负载TiO2空心球的SEM和TEM照片,可以看到:碳球模板单分散性好,平均直径约为280 nm;Ag/TiO2空心球平均直径约260 nm,Ag颗粒尺寸约为9 nm,而且分布均匀,无明显团聚存在。
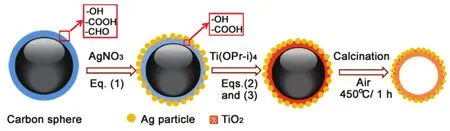
图5 Ag负载TiO2空心球的制备流程图Figure5 Schematic illustration of the formation process of silver/titania hollow spheres

图6 (a) 碳球模板的SEM照片;Ag/TiO2空心球的 (b) SEM照片、(c) TEM照片和 (d) HRTEM照片Figure6 (a) SEM image of carbon sphere templates and (b) SEM image, (c) TEM image and (d) HRTEM image of Ag/TiO2 hollow spheres
图7所示为不同Ag:TiO2摩尔比的 Ag/TiO2空心球和商业催化剂 P25对甲基橙溶液吸收谱的比较,从图中可看出,Ag/TiO2空心球的光催化活性明显好于商用光催化剂 P25,其中0.18Ag:TiO2为最佳配比,其光降解速率常数是纯 TiO2空心球的两倍以上,是商业催化剂P25的三倍以上。
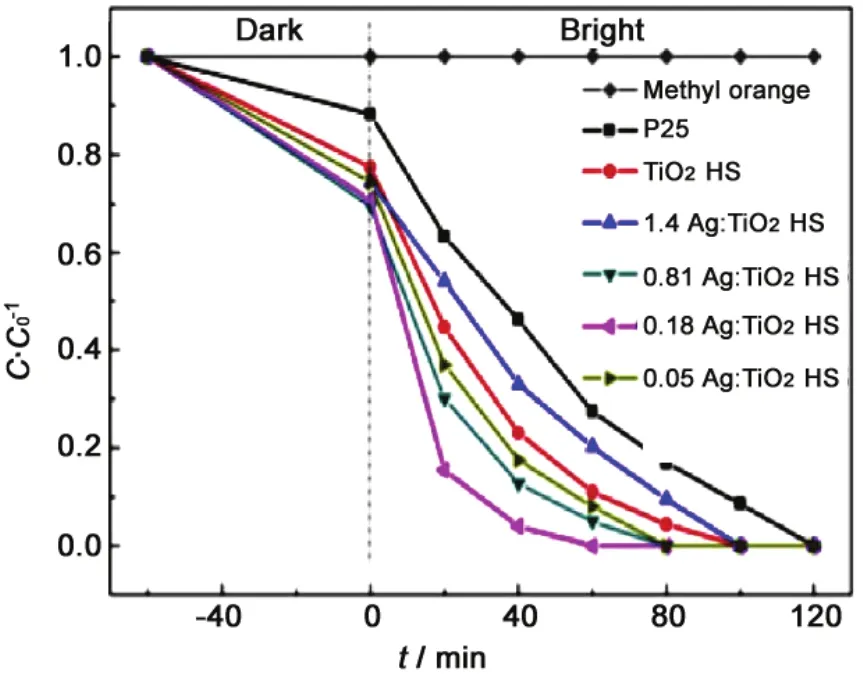
图7 不同Ag:TiO2摩尔比的 Ag/TiO2空心球和P25对光催化甲基橙分解性能的比较Figure7 Photocatalytic decomposition of methyl orange using P25 and various Ag/TiO2 hollow spheres with different Ag:TiO2 mole ratio

图8 CeO2-CuOx复合氧化物空心球的(a) SEM和 (b) TEM照片Figure8 Morphology of CeO2-CuOx composite hollow spheres: (a) SEM and (b) TEM
3 CeO2-CuOx复合氧化物空心球的制备及其CO氧化性能[14]
先前的研究表明,在Ce-Cu复合氧化物体系中,Cu物种是催化活性中心,而且有三种存在形式,分别为:高分散的CuO/CuOx、大颗粒的 CuO/CuOx及进入晶格取代 Ce离子的 Cu。以上三者对催化的贡献依次降低[15]。因而,要得到高催化活性的Ce-Cu复合氧化物,就必须让Cu物种以高分散的状态存在于材料的表面。而在之前的研究中,制备相类似的纳米结构材料时多以水热法和自模板法为主。使用这些方法得到的复合氧化物中,Cu物种多以上述后面两种形式存在。有报道发现Cu离子的表面能低于Ce离子,当它们在温和条件下沉淀时,Cu物种会自动富集于CeO2表面以降低体系的表面能,我们即以此为切入点设计实验。
本研究仍以胶体碳球为模板,通过层层自组装法在其表面沉积CeO2-CuOx复合氧化物,然后在550°C空气气氛下煅烧2 h去除模板后得到空心球。图8所示为CeO2-CuOx复合氧化物空心球的SEM和TEM照片,从照片中可看出空心球单分散良好,粒径分布均匀,其中厚度约40 nm的壳层由尺寸为15 nm ~ 20 nm的纳米颗粒组装而成,从电镜照片可以明显看出壳层有着丰富的孔结构。
图9所示为不同CuOx含量CeO2-CuOx复合氧化物空心球的CO氧化曲线,结果表明该材料具有优异的CO催化活性,当CuOx摩尔含量为10% 时材料具有最高的活性,在116°C能获得100% 的CO转化率,经过5次催化循环和10 h的定温测试后仍然能够在130°C下保持100%的转化率 (如图10所示),表现出良好的热稳定性。这一性能优于当前报道的大部分研究结果。
CeO2-CuOx复合氧化物空心球良好的催化性能主要归因于以下三个方面:(1) 由于铜物种高分散于CeO2表面使相互之间有广泛的接触界面,CuOx与CeO2之间存在强有力的协同效应;(2) CeO2-CuOx复合氧化物空心球具有较高的比表面积,实验结果表明10% CuOx-CeO2的比表面积高达123.67 m2/g,比表面积越高说明催化活性中心也越多;(3) 特殊的多孔结构有利于反应气体的扩散,使空心球壳层内外表面的活性中心都能与CO充分接触,从而更有效的利用催化活性点。
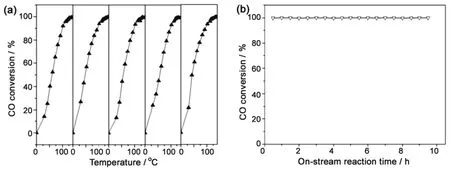
图10 10% CuOx-CeO2复合氧化物空心球的 (a) 催化循环曲线及 (b) 在130°C下定温测试曲线Figure10 (a) Cycle test curve and (b) constant temperature test curve at 130°C of 10% CuOx–CeO2 composite hollow spheres
4 MnO2/CeO2-MnO2双层壳结构复合氧化物空心球的制备及其在CO氧化中的应用[16]
在复合金属氧化物催化剂中,两相接触界面无疑是其催化活性中心。研究表明,要获得有效的高活性界面需满足以下四个条件:(1) 不同组分间需充分接触;(2) 两组分间需有很强的协同效应;(3) 界面接触区域的面积需要足够大;(4) 两组分间需有丰富的氧化还原关系。
基于以上四点考虑,再结合先前的研究结果,我们设计了如图11所示的实验方案:首先通过层层自组装法在碳球模板 (CSs) 上包裹厚度约20 nm的CeO2壳层,而后将CSs@CeO2核壳结构与强氧化性的高锰酸钾溶液反应得到蛋黄-蛋壳结构的 CSs@MnO2/CeO2-MnO2(这一步是基于碳模板表面官能团的还原特性),最后在空气中煅烧就得到了MnO2/CeO2-MnO2双壳结构空心球。
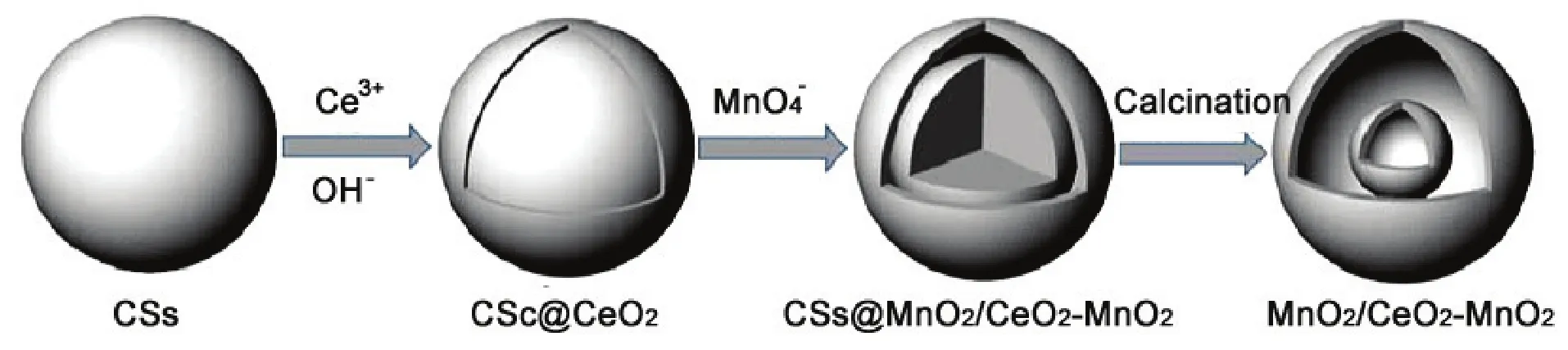
图11 MnO2/CeO2-MnO2复合氧化物空心球的制备流程图Figure11 Schematic illustration of the synthesis process of MnO2/CeO2-MnO2 composite hollow spheres

图12 MnO2/CeO2-MnO2复合氧化物空心球的 (a) 扫描电镜和 (b) 透射电镜照片Figure 12 Morphology of MnO2/CeO2-MnO2 composite hollow spheres: (a) SEM; (b) TEM

图13 MnO2/CeO2-MnO2复合氧化物空心球的 (a) EDS能谱分析曲线、(b) HAADF-STEM照片以及相应的O、Mn、Ce元素面扫描照片Figure 13 (a) EDS spectra, (b) HAADF-STEM images of an individual hollow MnO2/CeO2−MnO2 sphere and its element mappings of O, Mn, and Ce
图12所示为煅烧后得到的MnO2/CeO2-MnO2双壳结构空心球的SEM和TEM照片。从照片中可以看出空心球分散良好,没有发现团聚现象存在,粒径分布均匀,颗粒尺寸约800 nm,壳层厚度约40 nm。
图13所示为MnO2/CeO2-MnO2双壳结构空心球的EDS能谱分析和元素的面扫描照片,确定了空心球中Ce、Mn、O三种元素的分布情况。从照片中可以看到Ce与Mn均匀分布在外面的壳层上,这种均匀分布说明铈物种与锰物种之间有广泛的接触界面,有助于提高这两种组分间的协同效应。实验同时也发现,内部壳层中只有Mn与O两种元素存在,并没有铈元素的信号,说明内部小球为纯MnO2。
为了研究制备出的双层壳结构MnO2/CeO2-MnO2空心球的潜在应用,我们以CO催化氧化作为模型实验来测试材料的催化性能。图14所示为CO转化率随温度的变化关系曲线,从图中可以看出材料的催化活性依次如下:Ce/Mn =3/8 > Ce/Mn =4/6 > Ce/Mn = 6/4 > 纯 MnO2空心球 > CeO2与MnO2的机械混合物 > CeO2空心球,其 T50 值分别为 116°C、158°C、165°C、175°C、213°C 和 253°C。很明显,双壳结构MnO2/CeO2-MnO2空心球具有比纯纯二氧化铈空心球、二氧化锰空心球及二者的机械混合物更优越的催化活性。样品C (Ce/Mn = 3/8) 在206°C能使CO完全转化为CO2,与CeO2和MnO2相比分别低了104°C与56°C。
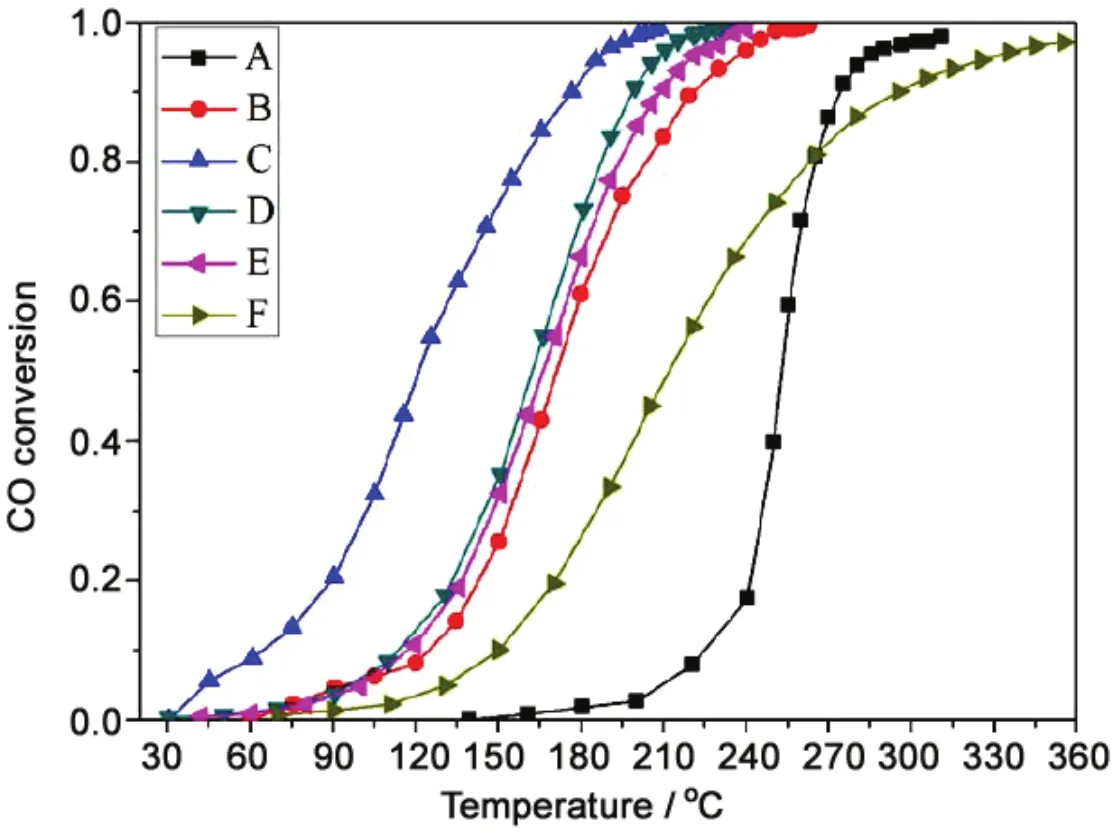
图14 不同样品对CO的催化转化曲线:(A) CeO2空心球、(B) MnO2空心球、Ce/Mn摩尔比分别为(C) 3/8、(D) 4/6 和 (E) 6/4 的 MnO2/CeO2−MnO2空心球、 (F) 机械混合 MnO2和 CeO2空心球(Ce/Mn = 3/8)Figure 14 CO conversion curves of (A) CeO2 hollow spheres; (B) MnO2 hollow spheres; MnO2/CeO2−MnO2 composite hollow spheres with (C) Ce/Mn = 3/8, (D) Ce/Mn = 4/6, (E) Ce/Mn = 6/4; (F) physical mixture of CeO2 and MnO2 hollow spheres with Ce/Mn = 3/8.
MnO2/CeO2-MnO2空心球卓越的催化性能可归因于以下几个方面。其一,CeO2与MnO2之间广泛的接触界面及较强的协同效应;其二, MnO2丰富的氧化还原价态及 CeO2较强的储氧性能;其三,MnO2/CeO2-MnO2的高比表面积和孔隙率。
5 总结及展望
我们采用水热法制备的胶体碳球为模板,通过静电吸附和原位氧化还原反应工艺,制备出了多种中空纳米结构的过渡金属氧化物催化材料,如单一氧化物空心球、复合氧化物空心球、双壳层复合氧化物空心球、高度分散的贵金属纳米颗粒负载的氧化物空心球结构等,因其具有多级气孔结构、高比表面积等特性,在有害气体的催化氧化方面具有重要的应用前景。这种中空核壳纳米结构复合氧化物的制备思路和工艺具有一定的普适性,可以适用于不同材料体系、不同核壳异质结构的复合氧化物中空纳米结构的制备和催化应用。
近20年来,过渡金属氧化物空心球的应用几乎已经涵盖了催化的各个领域,已经从最初设计材料再寻找催化反应,发展到当前的根据催化反应来选择设计合理的材料体系和中空结构,其中的进步是不言而喻的。但过渡金属氧化物空心球的制备和应用研究方面仍然存在着诸多问题,其中最主要的是制备工艺大多不具有普适性,而且重复率低,绝大部分制备方法都只适用于实验室小规模的生产,这严重限制了其在催化及相关领域的应用和发展。金属氧化物中空结构催化剂的发展与中空结构制备技术的发展是息息相关的,只有中空结构的制备技术克服上述不足,金属氧化物中空结构催化剂才能够真正从基础研究阶段走向实际的应用。
[1] ZHU Y, SHI J, SHEN W, et al. Stimuli-responsive controlled drug release from a hollow mesoporous silica sphere/polyelectrolyte multilayer core-shell structure [J]. Angewandte Chemie, 2005, 117 (32):5213-5217.
[2] YUAN J, LAUBERNDS K, ZHANG Q, et al. Self-assembly of microporous manganese oxide octahedral molecular sieve hexagonal flakes into mesoporous hollow nanospheres [J]. Journal of the American Chemical Society, 2003, 125 (17): 4966-4967.
[3] HU J, CHEN M, FANG X, et al. Fabrication and application of inorganic hollow spheres [J]. Chemical Society Reviews, 2011, 40 (11): 5472-5491.
[4] LOU XWD, ARCHER LA, YANG, Z. Hollow micro-/nanostructures: synthesis and applications [J].Advanced Materials. 2008, 20 (21):3987-4019.
[5] KIM SW, KIM M, LEE WY, et al. Fabrication of hollow palladium spheres and their successful application to the recyclable heterogeneous catalyst for Suzuki coupling reactions [J]. Journal of the American Chemical Society, 2002, 124 (26): 7642-7643.
[6] CHENG F, MA H, LI Y, et al. Ni1-xPtx(x = 0 ~ 0.12) hollow spheres as catalysts for hydrogen generation from ammonia borane [J]. Inorganic chemistry, 2007, 46 (3): 788-794.
[7] ARMAL PM, COMOTTI M, SCHUTH F. High-temperature-stable catalysts by hollow sphere encapsulation [J]. Angewandte Chemie, 2006, 118 (48): 8404-8407.
[8] LI J, LIANG X, JOO JB, et al. Mass transport across the porous oxide shells of core-shell and yolk-shell nanostructures in liquid phase [J]. The Journal of Physical Chemistry C, 2013, 117 (39): 20043-20053.
[9] MUNNIK P, DE JONGH PE, DE JONG KP. Recent developments in the synthesis of supported catalysts[J]. Chemical Reviews, 2015, 115 (14): 6687-6718.
[10] PRIETO G, TUYSUZ H, DUYCKAERTS N, et al. Hollow nano-and microstructures as catalysts [J].Chemical Reviews, 2016, 116 (22): 14056-14119.
[11] WANG CA, LI S, AN L. Hierarchically porous Co3O4hollow spheres with tunable pore structure and enhanced catalytic activity [J]. Chemical Communications, 2013, 49 (67): 7427-7429.
[12] SUN X, LI Y. Colloidal carbon spheres and their core/shell structures with noble metal nanoparticles [J].Angewandte Chemie International Edition. 2004, 43 (5): 597-601.
[13] LI S, SHAKKED SH, WANG CA. Fabrication of porous silver/titania composite hollow spheres with enhanced photocatalytic performance [J]. Materials Chemistry and Physics, 2015, 149-150: 1-6.
[14] ZHANG J, GONG M, CAO Y, et al. Facile synthesis of well-dispersed CeO2-CuOxcomposite hollow spheres with superior catalytic activity for CO oxidation [J]. RSC Advances, 2015, 5 (115): 95133-95139.
[15] LUO MF, SONG YP, LU JQ. Identification of CuO species in high surface area CuO-CeO2catalysts and their catalytic activities for CO oxidation [J]. The Journal of Physical Chemistry C. 2007, 111 (34):12686-12692.
[16] ZHANG J, CAO Y, WANG CA, et al. Design and preparation of MnO2/CeO2-MnO2double-shelled binary oxide hollow spheres and their application in CO oxidation [J]. ACS Applied Materials & Interfaces, 2016,8 (13): 8670-8677.
