硫脲功能化的螯合纤维在测定水溶液中痕量Hg(II)的应用
2018-05-09孙玉利孔志云吴晓青魏俊富
孙玉利 ,孔志云 ,康 恺 ,陈 远 ,吴晓青 ,魏俊富
(1.天津市城市排水监测站,天津 300011;2.天津工业大学 省部共建分离膜与膜过程国家重点实验室,天津300387;3.天津工业大学环境与化学工程学院,天津 300387;4.天津工业大学 天津市水质安全评价与保障技术工程中心,天津 300387;5.天津工业大学纺织学院,天津 300387)
随着现代产业的发展进步,冶金业、采矿业、制造业等活动日益增加,重金属污染日益严重.汞是一种毒性很强的重金属元素,广泛存在于天然水体中[1].汞在环境中不能分解,在环境与生物体内累积,并通过食物链转移到人体[2].人体内存在的微量汞可造成人体中枢神经系统、肾脏和其他器官的不可逆伤害,甚至引发恶性肿瘤的形成[3-4].我国饮用水标准中规定汞的含量(质量浓度)不得超过1 μg/L[5],据美国环保署估计,人体内的部分重金属是由于饮用被污染的水引起的,因此准确测定并监测饮用水中汞离子含量对人类健康和安全至关重要[6].
常见的金属汞测定方法主要有光谱法[7]、冷原子吸收光谱法(CVAAS)[8]、原子荧光光谱法(AFS)[9]、电感耦合等离子体发射光谱法(ICP-OES)[10]、电感耦合等离子体质谱法(ICP-MS)[11]等.但是对于痕量的重金属汞来说,光谱法测定不准确,CVAAS需要的样品量较大,电感耦合等离子体方法对仪器和精度要求较高,而且仪器价格昂贵.原子荧光法是近年来发展的较为经济的测定汞的方法,具有较高灵敏度、检测限较低,但是对于复杂样品的分析,样品中存在的杂质经常会影响测定的准确性和稳定性,因此需要将样品进行前处理[12].
固相萃取是一种常用的样品前处理方法,其分离富集的灵敏性和选择性取决于吸附剂和分析物之间的相互作用.常见的固相萃取剂有多孔介质[1]、二氧化硅[13]、活性炭[14]、纤维[15-16]、树脂[17]、石墨烯[18]、磁性纳米粒子[19]、矿石[20]等,其中离子交换纤维具有有效比表面积大、吸附和解吸速度快、解析效率高、流体阻力小以及容易再生等优点[21],纤维管内固相微萃取方法已用来分析有机物,但对金属的测定较少.本文制备了聚丙烯基功能化螯合纤维用于管内纤维内固相微萃取方法中的吸附剂,和原子荧光光谱法结合,检测样品中痕量的 Hg(II).
1 实验部分
1.1 材料与仪器
所用材料包括:聚丙烯非织造布,石家庄烟草技术中心产品;丙烯酸、硫酸亚铁铵、乙醇、硫酸、氢氧化钠、盐酸、磷酸,均为分析纯,天津市科密欧化学试剂有限公司产品;1-(3-二甲基氨基丙基)-3-乙基碳化二亚胺盐酸盐、N-羟基琥珀酰亚胺、2-N-吗啡啉乙磺酸、硫脲,均为分析纯,阿拉丁生化科技股份有限公司产品.
所用仪器包括:GJ-15型高能电子束辐射装置,无锡爱邦辐射技术有限公司产品;VECTOR22红外光谱仪,德国Bruker公司产品;QUANTA-200型扫描电子显微镜,荷兰FEI公司产品;PHS-25C酸度计,上海雷磁实业有限公司产品;AFS-9700原子荧光光度计,北京海光仪器有限公司产品.
1.2 吸附纤维的制备
将聚丙烯纤维在使用前用乙醇清洗以去除杂质.取干燥的聚丙烯纤维(约1.0 g)放入密封袋中,加入一定浓度的AA溶液、硫酸亚铁铵和硫酸,保持纤维蓬松,平整.浸泡24 h,使纤维充分溶胀.通氮气20 min,充分除去袋中的氧气.用高能电子束辐射装置进行小车模式辐照,能量为3~5 MeV,平均束流为30 mA,辐照剂量为20~80 kGy.反应结束后,把纤维取出,用蒸馏水和乙醇反复冲洗,除去均聚物后,60℃减压干燥,得弱酸性PP-g-AA纤维.
将 1.0 g PP-g-AA 纤维、0.006 mol EDC·HCl和0.006 mol NHS加入到250 mL的烧杯中,量取100 mL pH 5~6的MES缓冲溶液,加入烧杯中混合均匀,磁力搅拌,室温下活化反应60 min,使纤维样品得到充分活化;将活化后的纤维置于 100 mL(0.2 mol/L,pH 7.2)的磷酸缓冲溶液中,并加入0.006 mol硫脲,混合均匀后在室温下磁力搅拌2 h,待反应结束,用超纯水和无水乙醇洗涤多次,真空干燥,得到硫脲功能化的螯合纤维PP-g-AA-TU.反应产率用下式计算:

式中:W0和W1分别为反应前后纤维的质量.
反应过程如图1所示.
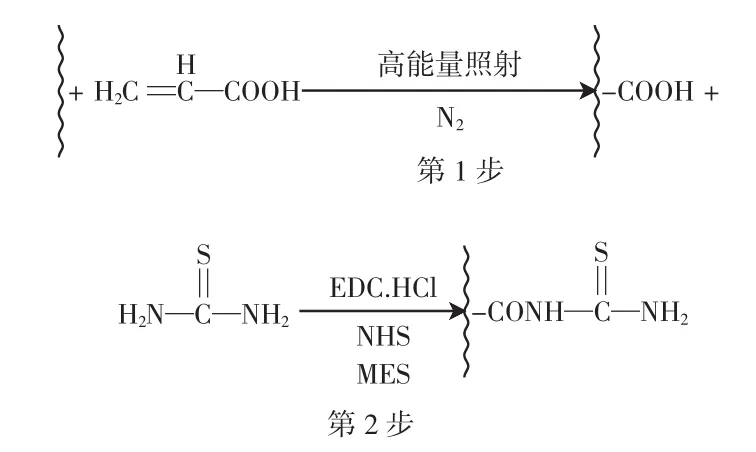
图1 纤维制备过程示意Fig.1 Procedure for preparation of PP-g-AA-TU fibers
1.3 纤维管内固相微萃取法测定溶液中痕量Hg(II)
将约10 mg的PP-g-AA-TU交换纤维纵向填充进PE塑料管(3 mm×25 mm)作为管内固相微萃取柱.在使用前需使用1.0 mol/L的HNO3及1.0 mol/L的NaOH清洗微柱,然后用去离子水洗至中性.
将 100 mL 含有 100 μg/L Hg(II)的溶液以一定的流速通过微柱,Hg(II)保留在纤维表面,吸附后的溶液流进废液里.然后用一定体积的洗脱剂以一定的流速通过吸附后的微柱,将保留在纤维表面的离子洗脱,洗脱液用原子荧光光度计检测.
2 结果与讨论
2.1 结构表征
2.1.1 FTIR红外光谱表征
图2为PP-g-AA-TU纤维反应前后的红外光谱图.
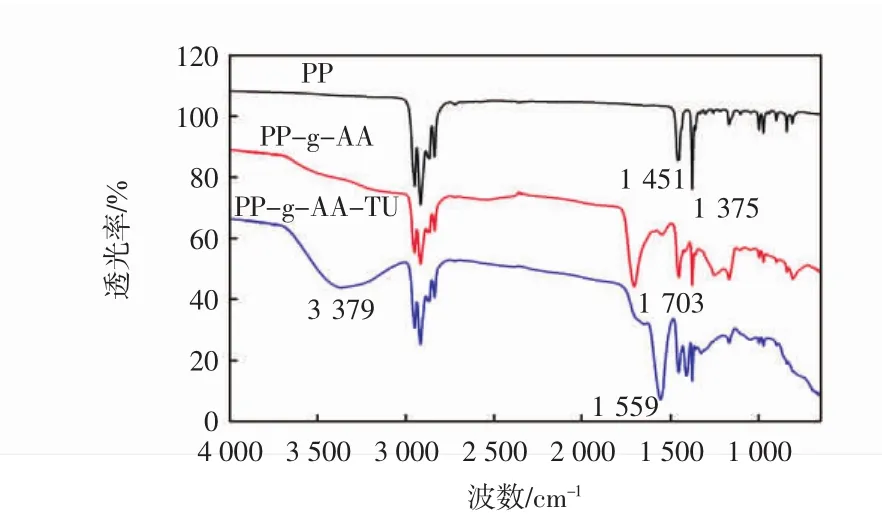
图2 PP-g-AA-TU纤维反应前后的红外光谱比较Fig.2 IR spectra of PP fiber,grafted PP fiber and PP-g-AA-TU fiber
图2中,原始PP纤维谱图中2 960~2 915 cm-1为CH2、CH3的不对称伸缩振动峰;2 870~2 840 cm-1为CH2、CH3的对称伸缩振动峰;1 460 cm-1附近为CH3的不对称弯曲振动峰;1 380 cm-1附近为CH2的对称弯曲振动峰.同原纤维谱图相比,PP-g-AA纤维的谱图中在1 740 cm-1左右出现了C—O较强的伸缩振动峰,此为羧酸的羰基基团特征峰.同PP-g-AA纤维相比,PP-g-AA-TU纤维在1 559 cm-1左右出现了C—O—N的酰胺振动特征峰,在3 379 cm-1处出现了NH2特征振动吸收峰,1 400 cm-1处出现了N—C—S的特征吸收峰,这证明硫脲通过反应已经成功地修饰到丙烯酸改性的聚丙烯纤维上.
2.1.2 FESEM扫描电镜表征
图3所示为反应前后的纤维的扫描电镜照片.由图3可以看出,原纤维表面光滑平整,接枝后后纤维(PP-g-AA)的表面变粗糙,有明显的一层颗粒形状的表层,而硫脲功能化的螯合纤维PP-g-AA-TU的表面形成一层粗糙表层,说明通过反应已经成功把功能基团引入到纤维表面.

图3 PP纤维、接枝纤维和功能化纤维的扫描电镜比较Fig.3 FESEM images of original PP fiber,grafted fiber and PP-g-AA-TU fiber
2.2 溶液pH值的影响
溶液pH值影响金属离子的存在状态和吸附剂的表面性能,因此直接影响金属离子的吸附.图4为不同pH值下,原液质量浓度为0.1 mg/L、原液体积为50 mL、吸附流速为2 mL/min时,PP-g-AA和PP-g-AATU纤维对Hg(II)的吸附影响图.
由图4可以看出,在较低pH值下,接枝纤维的表面带正电荷,同电相斥原理有较少的金属离子向纤维表面迁移,而且由于大量氢离子的存在,使得氢离子和金属离子形成竞争吸附,氢离子占据更多的吸附位点,因此金属的吸附量很小.随着pH值的增加,氢离子减少,Hg(II)和氢离子的竞争减少,因此吸附量增加,PP-g-AA-TU 纤维(pKa=3.1)在 pH值为 4~6达到最大吸附(98%以上).而PP-g-AA纤维(pKa=4.25)在pH值为5达到最大吸附(68%).随着pH值的继续增大,Hg(II)沉淀占据了纤维表面的吸附位点,阻止了金属离子的进一步吸附.而且水解后的金属离子的溶解度较低也是吸附降低的一个原因[22].因此选择的吸附溶液pH值为4~6.
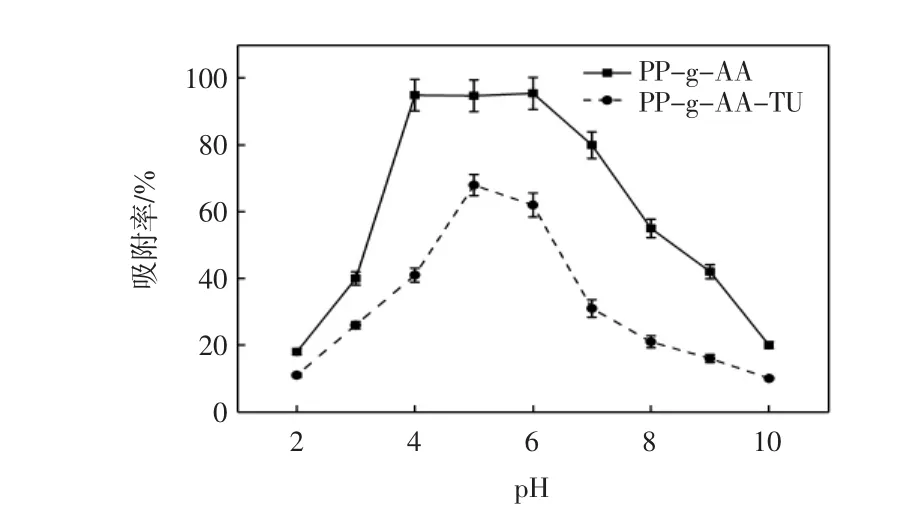
图4 溶液pH值对Hg(II)吸附的影响Fig.4 Effect of solution pH on adsorption percentage of Hg(II)
2.3 溶液流速的影响
由于PP-g-AA-TU上存在硫脲基团,硫脲基团和Hg(II)相结合形成络合物[23].因此吸附能力和接触时间将影响Hg(II)在管内纤维固相微萃取柱内的吸附.图5为溶液质量浓度0.1 mg/L、原液体积为50 mL、吸附pH值为4~6时溶液流速对Hg(II)吸附影响曲线.
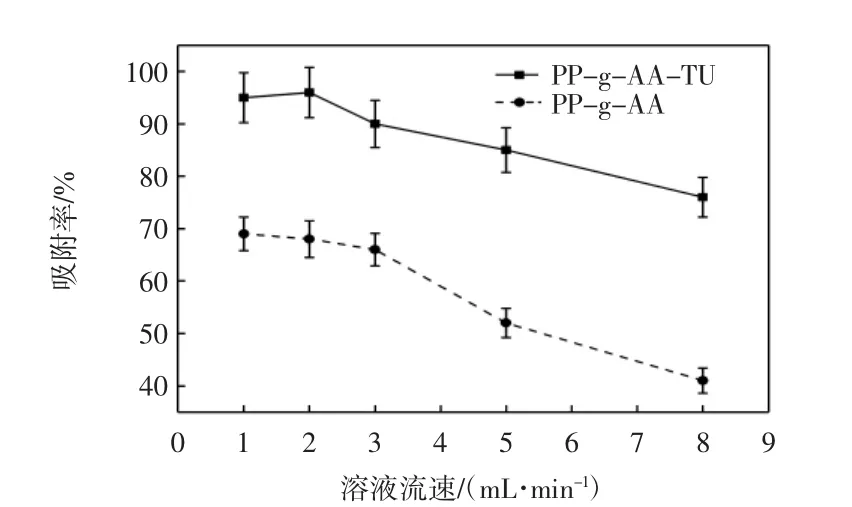
图5 溶液流速对Hg(II)吸附的影响Fig.5 Effect of sample flow rate on adsorption percentage of Hg(II)
由图5可见,当流速小于2 mL/min时,PP-g-AATU纤维Hg(II)的吸附率接近100%,当大于2 mL/min时,吸附率急剧下降.而PP-g-AA纤维流速小于2 mL/min时,吸附率也达到最大值,随着流速的增加,吸附率下降.这表明流速高于2 mL/min时管内纤维固相微萃取柱吸附Hg(II)不完全或者两相间的接触时间不够.因此次试验中选择溶液流速为2 mL/min.
2.4 溶液初始浓度的影响
表1所示为初始溶液浓度对2种纤维Hg(II)吸附的影响.由表1可见,当溶液质量浓度从0.001 μg/L增加至 100 μg/L 时,对 Hg(II)的吸附效率无影响,这可能是由于填充的PP-g-AA-TU纤维的吸附量为0.5 mg Hg(II),远大于质量浓度为 100 μg/L 的 Hg(II)量(10 μg),为金属的吸附提供了足够的吸附位点,因此在此范围内对吸附效率无影响.
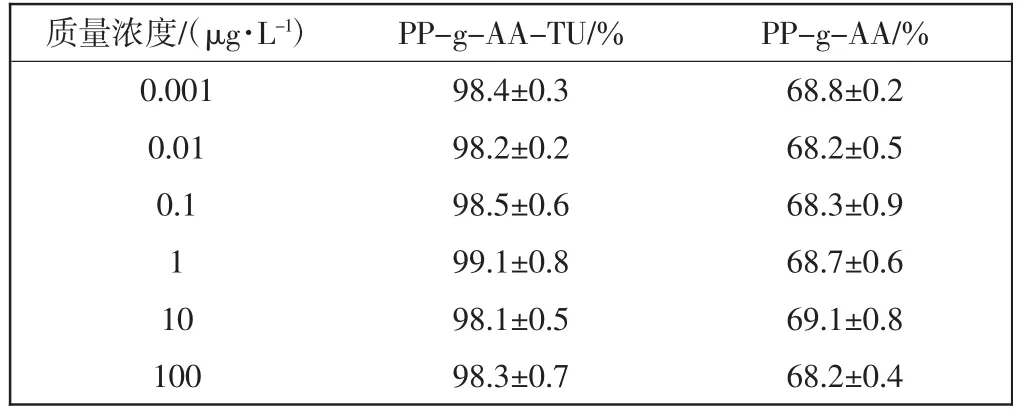
表1 初始溶液浓度对吸附的影响Tab.1 Effect of initial concentration on adsorption percentage of Hg(II)
2.5 洗脱液浓度的选择
合适的洗脱剂对样品富集是很重要的[24],在低pH值下Hg(II)的吸附量较小,因此通过调节溶液的pH能达到洗脱的效果,本文选择不同浓度的盐酸作为洗脱剂.图6为溶液质量浓度为0.1 mg/L、体积为50 mL、吸附pH值为4~6、吸附流速为2 mL/min、洗脱体积为1 mL时,洗脱液浓度对洗脱效果的影响曲线.由图6可见,当盐酸浓度较低时,洗脱效率不高,当盐酸浓度为5 mol/L解吸效率达到最大值,因此选择洗脱液浓度为5 mol/L HCl.
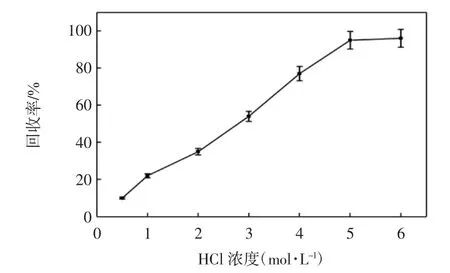
图6 洗脱液浓度对Hg(II)洗脱效果的影响Fig.6 Effect of eluent on recovery of Hg(II)
2.6 洗脱液流速的影响
图7所示为洗脱流速对洗脱效果的影响曲线.
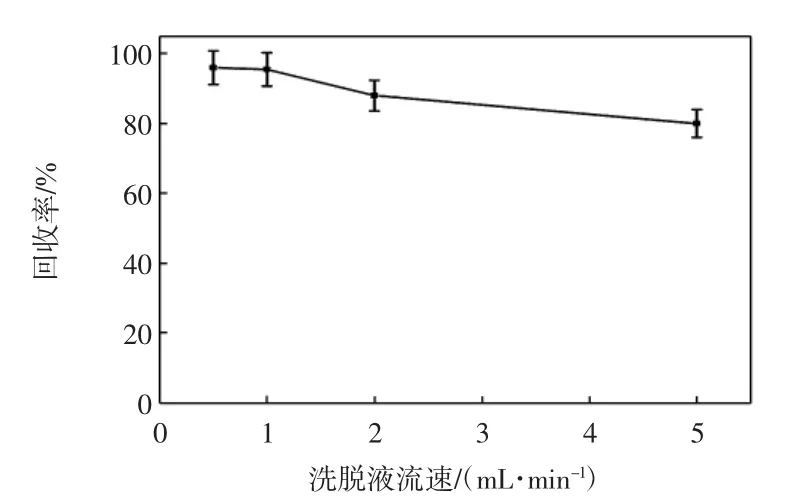
图7 洗脱液流速对Hg(II)洗脱效果的影响Fig.7 Effect of eluent flow rate on recovery of Hg(II)
由图7可见,原液质量浓度为0.1 mg/L、吸附液pH值为4~6、吸附流速为2 mL/min、1 mL盐酸作为洗脱剂时,洗脱效率随着洗脱流速的增加而降低,当洗脱流速为0.5 mL/min时解吸效率最高.这是由于洗脱液流速太快时,洗脱液和Hg(II)的接触时间较短,不能充分的发生螯合反应,因此选择洗脱流速为0.5 mL/min.
2.7 洗脱液体积的选择
图8为洗脱液体积对Hg(II)洗脱效果的影响.
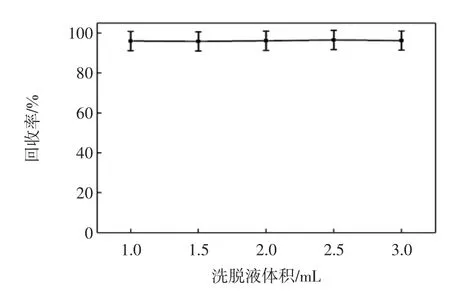
图8 洗脱液体积对Hg(II)洗脱效果的影响Fig.8 Effect of eluent volume on recovery of Hg(II)
由图8可见,原液质量浓度为1 μg/L、原液体积为50 mL、吸附pH在4~6范围内、吸附流速为1 mL/min、洗脱液为5 mol/L盐酸、洗脱流速为0.5 mL/min时,洗脱体积为1 mL时洗脱效率最佳.这是由于富集微柱的死体积为0.628 mL,因此洗脱液体积需要大于微柱的死体积,在流速为1 mL/min时,Hg(II)能完全洗脱,洗脱液体积的增加不影响Hg(II)的回收率,因此选择最佳洗脱体积为1 mL.
2.8 干扰离子的影响
PP-g-AA-TU超细纤维的吸附机理为配位作用力,水中存在的阳离子会和Hg(II)发生竞争配位,因此阳离子的存在会影响Hg(II)的吸附.水中最常见的共存阳离子为 K+、Na+、Ca2+和 Mg2+,选择不同浓度的干扰离子浓度测定其对0.1 mg/L的Hg(II)吸附的影响,结果如表2所示.由表2可以看出,10 mg/L的K+、Na+对汞离子的吸附几乎无影响.而Ca2+和Mg2+离子会影响管内纤维固相微柱对Hg(II)的吸附,但是影响很小,这可能是因为 K+、Na+、Ca2+和 Mg2+为硬离子配位中心,而纤维上起主要作用的含氮和硫原子的配体为交界离子配体,二者配位不匹配.
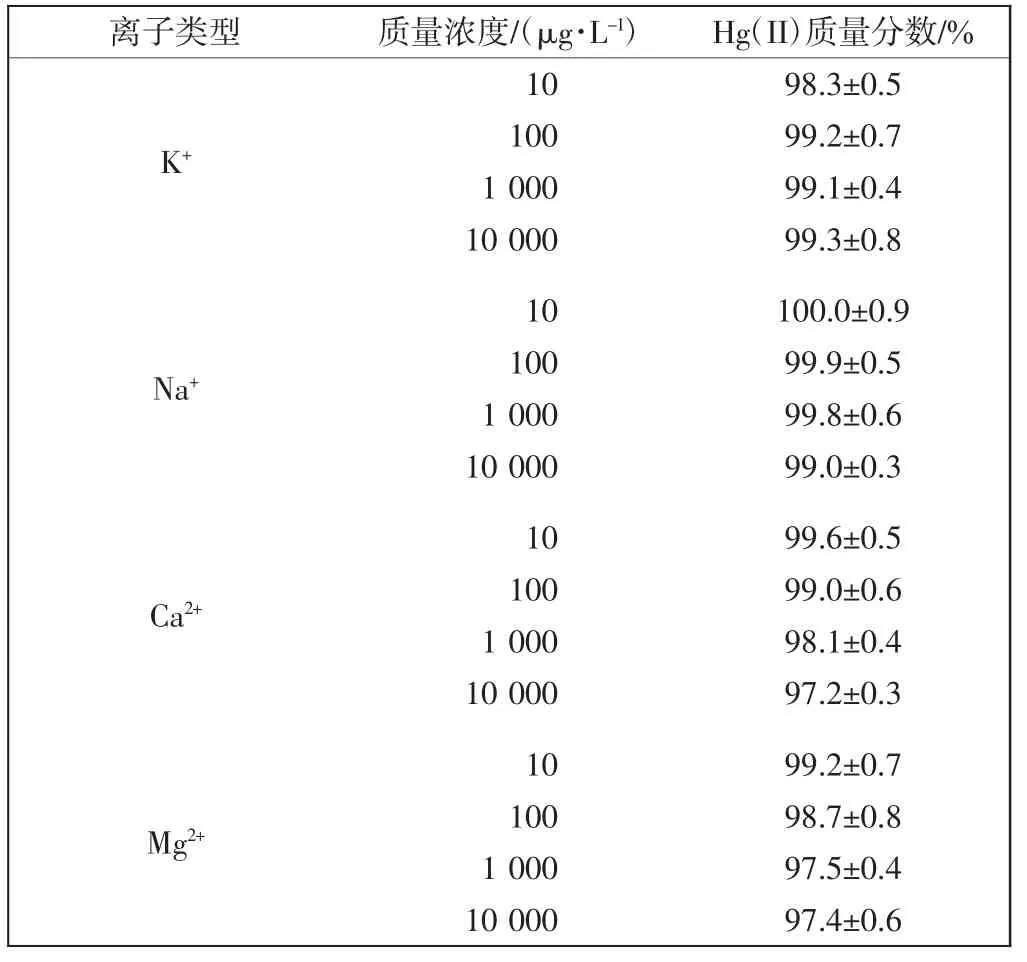
表2 干扰离子的浓度对吸附的影响Tab.2 Effect of coexist ion concentration on adsorption percentage of Hg(II)
2.9 方法的评价
本实验采用原子荧光光度计测量汞离子的浓度.根据IUPAC的定义,对该方法进行验证,实验结果如表3所示.
表3中数据表明,此法具有较好的富集精密度,可满足样品中痕量Hg(II)的分析测试要求.

表3 方法评价Tab.3 Evaluation of method performance
2.10 样品测定
使用此分析富集方法测定自来水Hg(II)的含量.采用标准加入法对所测结果进行验正,结果如表4所示.由表4可见,加样回收率在95%~110%之间,表明此方法可以用来测定水样中的Hg(II).
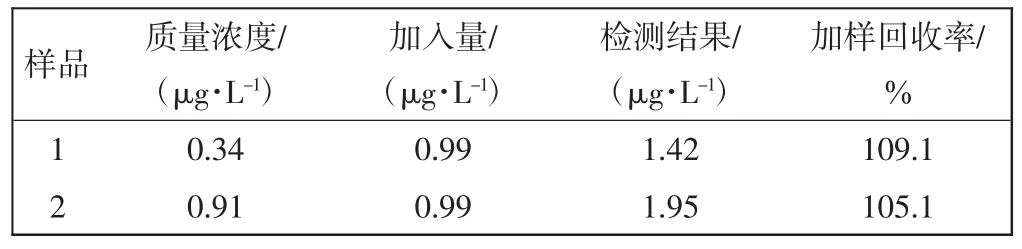
表4 样品分析结果Tab.4 Analytical results of Hg(II)in drinking water
3 结论
(1)本文制备了一种硫脲功能化的螯合纤维,将此纤维用于纤维管内固相微萃取方法中的吸附剂,建立了一种简单、快速的分析溶液中痕量Hg(II)的方法.
(2)此法在25 min内能将样品富集100倍,其最小检测限为0.001 μg/L,且在pH值为4~6时,得到最大吸附效率.10 000 μg/L 的 K+、Na+、Ca2+和 Mg2+干扰离子溶液中Hg(II)的测定影响不大.采用1 mL 5 mol/L的盐酸,以0.5 mL/min的速率可得到98%以上的回收率.
(3)此法简便、灵敏、准确,有望用于测定复杂基质如自来水、污水、废水和食品中Hg(II)的含量.
参考文献:
[1]ZHANG X,JIA X,ZHANG G,et al.Efficient removal and highlyselectiveadsorptionofHg2+bypolydopaminenanospheres with total recycle capacity[J].Applied Surface Science,2014,314:166-173.
[2]HUANG Y,HU D,WEN S,et al.Selective removal of mercury ions using thymine-grafted electrospun polymer nanofibers[J].New Journal of Chemistry,2014,38:1533-1539.
[3]莫洁芳,韩英.水环境中汞离子检测技术研究进展[J].现代仪器,2010(3):14-17.
MO J F,HAN Y.Research advances in determination of mercury ion in environmental water[J].Modern Instruments,2010(3):14-17(in Chinese).
[4]徐宁,樊静,贾录阳,等.一种高选择性汞(II)吸附剂的制备和应用[J].分析化学,2012,40:257-262.XU N,FAN J,JIA L Y,et al.Preparation,properties and application of a high selective solid phase adsorbent for mercury[J].Chinese Journal of Analytical Chemistry,2012,40:257-262(in Chinese).
[5]中华人民共和国卫生部.GB5749-2006生活饮用水卫生标准[S].北京:中国标准出版社,2006.Ministry of Health of the People′s Republic of China.GB5749-2006 Standards for drinking water quality[S].Beijing:China Standards Press,2006(in Chinese).
[6]MA R,VAN MOL W,ADAMS F.Determination of cadmium,copper and lead in environmental samples:An evaluation of flow injection on-line sorbent extraction for flame atomic absorption spectrometry[J].Analytica Chimica Acta,1994,285:33-43.
[7]YIN C,IQBAL J,HU H,et al.Sensitive determination of trace mercury by UV-visible diffuse reflectance spectroscopy after complexation and membrane filtration-enrichment[J].Journal of Hazardous Materials,2012,233/234:207-212.
[8]SOHRABI M R.Preconcentration of mercury(II)using a thiolfunctionalized metal-organic framework nanocomposite as a sorbent[J].Microchimica Acta,2013,181:435-444.
[9]ARANDA P R,GIL R A,MOYANO S,et al.Slurry sampling in serum blood for mercury determination by CV-AFS[J].Journal of Hazardous Materials,2009,161:1399-1403.
[10]GIERSZ J,BARTOSIAK M,JANKOWSKI K.Sensitive determination of Hg together with Mn,Fe,Cu by combined photochemical vapor generation and pneumatic nebulization in the programmable temperature spray chamber and inductively coupled plasma optical emission spectrometry[J].Talanta,2017,167:279-285.
[11]HE M,HUANG L,ZHAO B,et al.Advanced functional materials in solid phase extraction for ICP-MS determination of trace elements and their species:A review[J].Analytica Chimica Acta,2017,973:1-24.
[12]ENSAFI A A,ALLAFCHIAN A R,SARAJI M,et al.In-situ differential pulse anodic stripping voltammetry combined with hollow fiber-based liquid-three phase micro extraction for determination of mercury using Au-nanoparticles sol-gel modified Pt-wire[J].Talanta,2012,99:335-341.
[13]ROFOUEI M K,SABOURI A,AHMADALINEZHAD A,et al.Solid phase extraction of ultra traces mercury(II)using octadecyl silica membrane disks modified by 1,3-bis (2-ethoxyphenyl)triazene (EPT)ligand and determination by cold vapor atomic absorption spectrometry[J].Journal of Hazardous Materials,2011,192:1358-1363.
[14]AHN C K,PARK D,WOO S H,et al.Removal of cationic heavy metal from aqueous solution by activated carbon impregnated with anionic surfactants[J].Journal of Hazardous Materials,2009,164:1130-1136.
[15]MONIER M,ABDEL-LATIF D A.Synthesis and characterization of ion-imprinted chelating fibers based on PET for selective removal of Hg2+[J].Chemical Engineering Journal,2013,221:452-460.
[16]WANG Y,QU R,PAN F,et al.Preparation and characterization of thiol-and amino-functionalized polysilsesquioxane coated poly(p-phenylenetherephthal amide)fibers and their adsorption properties towards Hg(II)[J].Chemical Engineering Journal,2017,317:187-203.
[17]LEMOS V A,NOVAES C G,LIMA A D S,et al.Flow injection preconcentration system using a new functionalized resin for determination of cadmium and nickel in tobacco samples[J].Journal of Hazardous Materials,2008,155:128-134.
[18]CUI L,WANG Y,GAO L,et al.Removal of Hg (II)from aqueous solution by resin loaded magnetic β-cyclodextrin bead and graphene oxide sheet:Synthesis,adsorption mechanism and separation properties[J].Journal of Colloid and Interface Science,2015,456:42-49.
[19]FARAJI M,SHARIATI S,YAMINI Y,et al.Preconcentration of trace amounts of lead in water samples with cetyltrimethylammonium bromide coated magnetite nanoparticles and its determination by flame atomic absorption spectrometry[J].Arabian Journal of Chemistry,2016,9:S1540–S1546.
[20]LOPEZ-MUNOZ M-J,ARENCIBIA A,CERRO L,et al.Adsorption of Hg(II)from aqueous solutions using TiO2and titanate nanotube adsorbents[J].Applied Surface Science,2016,367:91-100.
[21]WEI J F,WANG Z P,ZHANG J,et al.The preparation and the application of grafted polytetrafluoroethylene fiber as a cation exchanger for adsorption of heavy metals[J].React Funct Polym,2005,65:127-134.
[22]KADIRVELU K,FAUR-BRASQUET C,CLOIREC P L.Removal of Cu(II),Pb(II),and Ni(II)by adsorption onto activated carbon cloths[J].Langmuir,2000,16:8404-8409.
[23]ZHOU L,WANG Y,LIU Z,et al.Characteristics of equilibrium,kinetics studies for adsorption of Hg(II),Cu(II),and Ni(II)ions by thiourea-modified magnetic chitosan microspheres[J].Journal of Hazardous Materials,2009,161:995-1002.
[24]GHAEDI M,AHMADI F,SOYLAK M.Preconcentration and separation of nickel,copper and cobalt using solid phase extraction and their determination in some real samples[J].Journal of Hazardous Materials,2007,147:226-231.
