MIL-53(Fe)@聚多巴胺@Fe3O4磁性复合材料的制备及其用于环境水样中磺酰脲类除草剂的磁固相萃取
2018-04-02邓玉兰李傲天王燕飞北京化工大学理学院北京0009中国检验检疫科学研究院北京003
邓玉兰, 李傲天, 王燕飞, 孙 鹏, 苏 萍*, 杨 屹*(. 北京化工大学理学院, 北京 0009; . 中国检验检疫科学研究院, 北京 003)
磺酰脲类除草剂(SUHs)在1982年由美国杜邦公司首次开发使用,包括甲嘧磺隆(SMM)、苄嘧磺隆(BSM)等,目前已成为世界上使用量最大的一类作用独特的除草剂[1]。然而,近年来随着该类除草剂使用量和使用范围的加大,其在环境与作物中因残留而产生的负面影响也越来越大[2]。为此,国内外先后制定了相应的残留限量标准,如欧盟规定苄嘧磺隆在谷物和稻草中的最大残留限量分别是0.01 mg/kg和0.05 mg/kg[3,4];我国农业部也陆续发布公告限制氯磺隆、甲磺隆等的销售和使用[5]。因此,建立一种准确、灵敏的检测磺酰脲类除草剂残留的方法十分必要。
样品前处理是农药残留检测过程中的一项重要环节。1999年Aguilar-Arteag等[6]根据固相萃取法建立了以吸附剂为磁性材料的磁固相萃取法(MSPE)。Fe3O4纳米粒子是广泛使用的磁性材料,为了防止团聚和表面氧化,通常对其表面进行修饰[7-9]。聚多巴胺(PDA)是一类由多巴胺在碱性条件下发生自聚生成的聚合物,包覆聚多巴胺的Fe3O4具有独特的黏附性和优良的生物相容性,并且由于含有丰富的羧基和氨基等官能团[10,11],可以对其表面进行进一步修饰。
金属-有机骨架材料(MOFs)是近年来快速发展的一种新型多孔材料,在气体储存分离、催化、药物输送以及分析化学领域均有广泛应用[12-15]。拉瓦锡系列材料(MILs)由Mellot-Draznieks等[16]首次设计合成,其由不同的过渡金属元素和二羧酸配体组装形成。其中最有代表意义的是由Cr3+与对苯二甲酸配位形成的MIL-101[17]和Cr3+、A13+、Fe3+与对苯二甲酸配位形成的MIL-53[18]。MIL-53(Fe)具有一维孔道结构,不仅具有良好的化学稳定性、热稳定性、高孔隙度和丰富的不饱和位点等特点,还具有因其骨架柔软性而形成的独一无二的呼吸效应[19-22],这些特点使其在萃取富集有机农药残留领域中具有很大的应用潜力。
基于PDA和MIL-53(Fe)两类物质独特的优势,本文采用封装法将MIL-53(Fe)进一步修饰在PDA包覆的Fe3O4表面,制备了MIL-53(Fe)@PDA@Fe3O4磁性复合材料,利用磁固相萃取技术,结合高效液相色谱法(HPLC)对3种环境水样中的磺酰脲类除草剂残留进行富集检测。研究发现,制备的MIL-53(Fe)@PDA@Fe3O4磁性复合材料能够通过MIL-53(Fe)中的羧酸配体、不饱和金属位点Fe3+与磺酰脲类除草剂分子产生π-π共轭作用、π电子间络合作用,从而实现吸附萃取。实验结果表明,该复合材料可以作为一种性能优异的磁性吸附剂,用于环境水样中磺酰脲类除草剂残留的萃取分析。
1 实验部分
1.1 仪器、试剂与材料
LC-20A液相色谱-二极管阵列检测器、 ODS-XR C18色谱柱(150 mm×4.6 mm, 5 μm)(日本岛津公司), DSY-Ⅱ自动快速浓缩仪(北京金科精华苑技术研究所), 0.45 μm、0.22 μm尼龙66针筒式滤膜过滤器(天津津腾实验设备公司), VORTEX-5旋涡混合器(海门市其林贝尔仪器制造有限公司), Nicolet傅里叶红外光谱仪(FT-IR,上海赛默飞世尔科技有限公司), Vario EL cube元素分析仪(德国Elementar公司), Rigaku Ultima3 X射线粉末衍射仪(XRD,日本Tokyo公司), ASAP 2010比表面及孔隙度分析仪(BET,美国麦克仪器公司), T20透射电子显微镜(TEM,日本Hitachi公司), SUPRA55扫描电子显微镜(SEM,德国蔡司公司)。
FeCl356H2O、无水乙酸钠(CH3COONa)、HCl(37.5%)均购自北京化工厂;对苯二甲酸购自上海阿拉丁生化科技股份有限公司;三羟甲基氨基甲烷(Tris)购自国药集团化学试剂有限公司;盐酸多巴胺购自上海阿达玛斯有限公司;甲醇和乙腈(均为色谱级)购自百灵威科技有限公司。4种农药标准物质:甲嘧磺隆、苄嘧磺隆、吡嘧磺隆(PSE)、氯嘧磺隆(CME),质量浓度均为100 mg/L,均购自农业部环境保护科研监测所。
3种环境水样分别采自北京陶然湖、护城河和昌平十三陵水库。
1.2 实验方法
1.2.1MIL-53(Fe)@PDA@Fe3O4磁性复合材料的制备
首先,采用溶剂热法合成Fe3O4纳米粒子[8]。然后,称取0.40 g Fe3O4纳米粒子于三口烧瓶中,加入溶解了0.40 g盐酸多巴胺的Tris缓冲溶液(10 mmol/L, pH 8.5),于25 ℃水浴反应10 h。产物用去离子水和无水乙醇分别洗涤3次,于60 ℃真空烘干,得到PDA@Fe3O4纳米粒子。最后,采用封装法制备MIL-53(Fe)@PDA@Fe3O4磁性复合材料。
称取4.10 g FeCl356H2O和2.49 g对苯二甲酸,分别置于含有40 mLN,N-二甲基甲酰胺(DMF)的烧杯中,超声溶解后将二者混合均匀,然后加入0.50 g PDA@Fe3O4纳米粒子,超声分散10 min,转移至反应釜内于150 ℃反应17 h,自然冷却至室温。产物用去离子水洗涤1次后,用热乙醇洗涤数次至上清液澄清,于80 ℃干燥12 h至恒重,得到棕褐色产物,即MIL-53(Fe)@PDA@Fe3O4磁性复合材料。
1.2.2样品前处理
去除实际水样中的不溶物和固体杂质,然后用0.45 μm尼龙滤膜过滤,置于棕色玻璃瓶中储存,于4 ℃冰箱中备用。
取25 mL实际水样,置于50 mL离心管中,加入0.5 g NaCl超声溶解,并用0.1 mol/L的HCl水溶液调节pH至3。然后加入60 mg MIL-53(Fe)@PDA@Fe3O4磁性复合材料作为吸附剂,涡旋4.5 min进行萃取。在外加磁场作用下使吸附剂和水溶液分离,弃去上清液,在离心管中加入5 mL丙酮进行超声洗脱。收集洗脱液后经0.22 μm尼龙滤膜过滤,于30 ℃氮气缓慢吹扫至干,复溶于400 μL乙腈,待高效液相色谱分析。
1.2.3分析条件
ODS-XR C18色谱柱(150 mm×4.6 mm, 5 μm);柱温为30 ℃;流动相A为乙腈,B为水(含0.01%(体积分数)三氟乙酸)。梯度洗脱程序:0~2.0 min, 30%A~45%A; 2.0~5.0 min, 45%A~55%A; 5.0~8.0 min, 55%A~60%A; 8.0~12.5 min, 60%A。流速为1 mL/min;进样体积为20 μL;检测波长为233 nm。
2 结果与讨论
2.1 MIL-53(Fe)@PDA@Fe3O4磁性复合材料的表征
2.1.1透射电镜和扫描电镜分析
本实验分别对Fe3O4纳米粒子、PDA@Fe3O4纳米粒子和MIL-53(Fe)@PDA@Fe3O4磁性复合材料进行透射电镜和扫描电镜分析(见图1)。由图1a~1c可见,与裸露的Fe3O4纳米粒子相比,PDA@Fe3O4纳米粒子表面明显包覆了一层薄膜,而MIL-53(Fe)@PDA@Fe3O4磁性复合材料中包覆层的厚度增加,形成了较为明显的核-壳结构。由扫描电镜图(见图1d)也可以看出,MIL-53(Fe)@PDA@Fe3O4磁性复合材料表面比较粗糙。说明MIL-53(Fe)已经成功修饰在PDA@Fe3O4纳米粒子表面。
2.1.2红外光谱分析
红外光谱分析可以测定样品表面的官能团或化学键,对物质表面结构进行定性分析。实验对制备的磁性材料进行了FT-IR分析,结果见图2。从图2可以看出,3 417 cm-1处的峰是产物中-OH和-NH的伸缩振动峰;1 593 cm-1处的强振动峰可归属为有机配体对苯二甲酸中苯环的骨架振动;750 cm-1处的峰对应于苯环的C-H面外变形振动峰;1 392 cm-1处的峰对应于 -COOH的伸缩振动峰;578 cm-1处的峰则是Fe-O键伸缩振动引起的特征吸收峰,说明了Fe3O4的存在。

图 2 Fe3O4纳米粒子、PDA@Fe3O4纳米粒子、MIL-53(Fe)和MIL-53(Fe)@PDA@Fe3O4磁性复合材料的FT-IR谱图 Fig. 2 FT-IR spectra of Fe3O4 nanoparticle, PDA@Fe3O4 nanoparticle, MIL-53(Fe) and MIL-53(Fe)@PDA@Fe3O4magnetic composites
2.1.3X射线晶体衍射分析
X射线晶体衍射分析可以进一步鉴别材料的晶体结构。由图3可以看出,PDA@Fe3O4中出现的衍射峰对应Fe3O4特征晶面,表明Fe3O4纳米粒子被PDA包覆后仍保持立方尖晶石结构。MIL-53(Fe)@PDA@Fe3O4磁性复合材料中Fe3O4的所有特征衍射峰均有出现,MIL-53(Fe)的部分特征衍射峰也较为明显,说明复合材料中Fe3O4和MIL-53(Fe)均存在。

图 3 PDA@Fe3O4纳米粒子、MIL-53(Fe)和MIL-53(Fe)@PDA@Fe3O4磁性复合材料的XRD谱图 Fig. 3 X-ray diffraction (XRD) patterns of PDA@Fe3O4 nanoparticle, MIL-53(Fe) and MIL-53(Fe)@PDA@Fe3O4 magnetic composites
2.1.4比表面积和孔径分布分析
图4a和图4b分别为实验合成的MIL-53(Fe)@PDA@Fe3O4磁性复合材料的N2吸脱附曲线图和孔径分布图。从图4a可以看出,MIL-53(Fe)@PDA@Fe3O4磁性复合材料的N2吸脱附曲线符合I型等温线,有较为明显的拐点和水平平台,说明以微孔吸附为主。通过计算可知,MIL-53(Fe)@PDA@Fe3O4磁性复合材料的BET比表面积为76.4 m2/g。由图4b可知,MIL-53(Fe)@PDA@Fe3O4磁性复合材料的孔径分布只有一个单峰,主要集中在1.1 nm左右,属于超微孔。

图 4 MIL-53(Fe)@PDA@Fe3O4磁性复合材料的(a)N2吸脱附曲线等温线和(b)孔径分布图Fig. 4 (a) Nitrogen adsorption-desorption isotherms and (b) pore diameter distribution curve of MIL-53(Fe)@PDA@Fe3O4 magnetic composites
2.1.5元素分析
通过元素分析仪可以检测物质中C、H、N和S元素的百分含量,如表1所示,PDA@Fe3O4磁性材料中存在C元素和N元素,说明PDA包覆成功。而进一步修饰MIL-53(Fe)后,C的百分含量进一步增加,这主要是因为对苯二甲酸有机配体的存在。该结果也证明成功制备了MIL-53(Fe)@PDA@Fe3O4磁性复合材料。

表 1 磁性复合材料的元素分析Table 1 Elemental analysis of magnetic composites
2.2 磁固相萃取条件的优化
2.2.1洗脱剂种类
洗脱剂种类的选择对萃取结果有非常重要的影响,一定极性的洗脱剂可以将目标物充分洗脱,而将杂质留在吸附剂表面。考察了甲醇、乙腈、丙酮和乙酸乙酯4种有机溶剂的洗脱效果。由图5a可知,对SMM、BSM、PSE和CME 4种磺酰脲类除草剂而言,丙酮的洗脱效果最好,因此选择丙酮作为洗脱剂。
2.2.2洗脱剂用量
洗脱剂用量的选取原则是在保证萃取效率的基础上,尽可能减少使用量。考察了丙酮用量在1~9 mL时的萃取效果,如图5b所示,随着洗脱剂用量的增加,洗脱效果逐渐增强,当洗脱剂用量超过5 mL,洗脱效果的增强不再明显。因此选择5 mL丙酮用于后续实验。
2.2.3萃取时间
吸附剂从样品中吸附目标物的过程需要一定的时间,萃取时间过短可能会导致萃取不完全。考察了0.5~5.5 min的涡旋萃取时间对萃取效率的影响。由图5c可以看出,萃取效率随着时间的延长而增强,当涡旋时间达到4.5 min之后,萃取效率基本稳定,说明在很短的时间里吸附剂就能够与目标物充分接触,传质速度加快,吸附可以很快达到平衡。因此选择萃取时间为4.5 min。
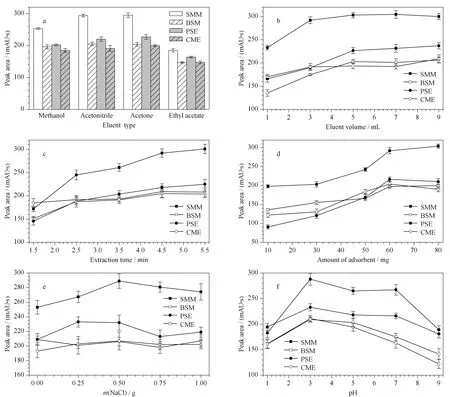
图 5 (a)洗脱剂种类、(b)洗脱剂用量、(c)萃取时间、(d)吸附剂用量、(e)离子强度和(f)溶液pH值对4种磺酰脲类除草剂(100 μg/L)萃取效率的影响(n=3)Fig. 5 Effects of (a) type of desorption solvent, (b) volume of desorption solvent, (c) extraction time, (d) adsorbent dosage, (e) ionic strength and (f) pH value of the solution on the extraction efficiencies of the four sulfonylurea herbicides (SUHs) (100 μg/L) (n=3) SMM: sulfometuron methyl; BSM: bensulfuron methyl; PSE: pyrazosulfuron ethyl; CME: chlorimuron ethyl.
2.2.4吸附剂用量
吸附剂的用量将直接影响萃取的效果。分别称取10、30、50、60和80 mg的吸附剂,考察吸附剂用量对萃取效率的影响。由图5d可知,萃取效率随着吸附剂用量的增加而增强,当用量达到60 mg时萃取效率基本保持恒定。因此选择60 mg吸附剂用于后续实验。
2.2.5离子强度
离子强度会对目标物的萃取效果产生不同的影响。一方面,离子强度的增大会降低目标物的溶解度(盐析效应),有利于萃取效率的提高;另一方面,离子强度的增大也会使得样品溶液的黏度上升,降低吸附剂与目标物间的相互作用,阻碍萃取的进行。此外,客体粒子种类的增加,也可能引起吸附剂表面MIL-53(Fe)呼吸效应的发生,使其从狭窄孔转换为大孔进而增强其吸附性能。实验考察了在25 mL样品溶液中加入0~1.0 g NaCl对萃取效果的影响。从图5e可以看出,目标物的萃取效率在加入0.5 g NaCl时达到最优,因此后续实验中在25 mL样品溶液中添加0.5 g NaCl进行萃取。
2.2.6溶液pH值
本实验所检测的4种磺酰脲类除草剂均呈弱酸性(pKa3.3~5.2),在碱性条件下会发生较大程度的水解[22]。同时,过酸或过碱的环境还可能破坏吸附剂的结构,造成萃取效率的降低。实验分别用0.1 mol/LHCl溶液和0.1 mol/LNaOH溶液调节样品溶液的pH值至1、3、5、7和9,考察pH值对萃取效果的影响。如图5f所示,pH为3时萃取效果最好。在pH为3的溶液中,4种磺酰脲类除草剂均呈电中性,该结果也说明MIL-53(Fe)@PDA@Fe3O4磁性复合材料主要通过π-π共轭作用、π电子络合作用对磺酰脲类除草剂分子实现吸附萃取。
2.3 方法学考察
准确量取4种磺酰脲类除草剂标准溶液,用水进行逐级稀释,配制系列不同质量浓度(1.0、2.5、5.0、10.0、100、200 μg/L)的加标水样,在1.2.2节和1.2.3节条件下进行磁固相萃取和高效液相色谱分析。以目标物的色谱峰面积(y)和对应的质量浓度(x, μg/L)绘制工作曲线。结果如表2所示,SMM和CME的线性范围为1.0~200 μg/L, BSM和PSE的线性范围为2.5~200 μg/L, 4种目标物的线性相关系数(r)均≥0.998 0。方法的检出限(LOD,S/N=3)为0.28~0.77 μg/L。选择质量浓度为100 μg/L的加标水样重复6次实验,目标物色谱峰面积的RSD值≤7.5%,说明方法重复性良好。
2.4 与文献方法比较
如表3所示,将本文建立的方法与传统的固相萃取(SPE)磺酰脲类除草剂的方法[3,4,24,25]进行对比。结果表明,本方法能得到较好的线性范围、回收率和较低的检出限,满足分析检测的要求。

表 2 4种磺酰脲类除草剂的线性范围、线性方程、相关系数、检出限和相对标准偏差Table 2 Linear ranges, linear equations, correlation coefficients (r), LODs and RSDs of the four SUHs.
y: peak area;x: mass concentration, μg/L.

表 3 与文献中固相萃取磺酰脲类除草剂方法的比较Table 3 Comparison of proposed method with SPE methods for the determination of the SUHs
CLC: capillary liquid chromatography; DAD: diode array detection; MSPE: magnetic solid-phase extraction.

表 4 3种环境水样中4种磺酰脲类除草剂的加标回收率和相对标准偏差Table 4 Spiked recoveries and RSDs of the four SUHs in the environmental water samples
N.D.: not detected; -: no data; N.Q.: found but can not be quantified.
2.5 实际样品测定
将制备的MIL-53(Fe)@PDA@Fe3O4磁性复合材料用于3种环境水样中目标物的萃取富集,未经萃取的原始水库水样(图6a)及萃取后3种原始水样中均未检测到目标物(见图6b~6d)。配制含质量浓度分别为5、50和100 μg/L的4种目标物混合标准溶液,进行加标回收试验(平行测定3次),结果见表4。可知该MIL-53(Fe)@PDA@Fe3O4磁性复合材料的萃取效果良好,加标回收率为78.8%~109.7%,相对标准偏差为2.2%~9.7%,说明该方法满足分析检测的要求,可以用于实际环境水样中磺酰脲类除草剂残留的富集和分析检测。
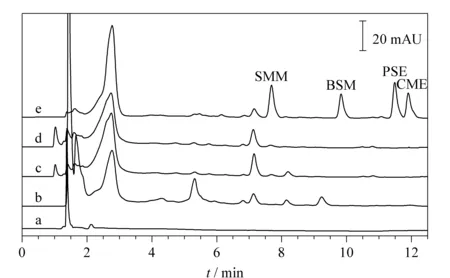
图 6 磁固相萃取前、后实际水样中4种磺酰脲类除草剂的色谱图Fig. 6 Chromatograms of the four SUHs in the real water samples after MSPE or not a. blank reservoir water without MSPE; b. lake water with MSPE; c. river water with MSPE; d. reservoir water with MSPE; e. reservoir water spiked at 100 μg/L standard solutions with MSPE.
3 结论
本文采用封装法成功制备了修饰MIL-53(Fe)和聚多巴胺(PDA)的磁性复合材料MIL-53(Fe)@PDA@Fe3O4,该复合材料结合了Fe3O4纳米粒子独特的磁性特征和表面修饰材料MIL-53(Fe)优良的吸附性能。建立了磁固相萃取-高效液相色谱检测环境水样中4种磺酰脲类除草剂的分析方法。建立的方法简单快速,而且具有更高的萃取效率。实验结果表明制备的MIL-53(Fe)@PDA@Fe3O4磁性复合材料在富集萃取磺酰脲类除草剂的应用中具有很大的发展潜力。
参考文献:
[1]Deng J B. World Pesticides, 2003, 25(3): 24
邓金保. 世界农药, 2003, 25(3): 24
[2]Ma J P, Jiang L H, Wu G G, et al. J Chromatogr A, 2016, 1466: 12
[3]Zhang L Y, Cao B C, Yao D, et al. J Sep Sci, 2015, 38(10): 1733
[4]Wang H X, Li Y Q, Yong L, et al. Chinese Journal of Chromatography, 2007, 25(4): 536
王和兴, 黎源倩, 雍莉, 等. 色谱, 2007, 25(4): 536
[5]Zhu J, Li M X, Wang Q, et al. Chinese Journal of Chromatography, 2016, 34(11): 1120
朱婧, 李明昕, 王倩, 等. 色谱, 2016, 34(11): 1120
[6]Aguilar-Arteaga K, Rodriguez J A, Barrado E. Anal Chim Acta, 2010, 674(2): 157
[7]Alizadeh A, Fakhari M, Khodeai M M, et al. RSC Adv, 2017, 7(56): 34972
[8]Zhou L, Su P, Deng Y L, et al. J Sep Sci, 2017, 40(4): 909
[9]Guo J, Song H X, Liu H, et al. J Mater Chem C, 2017, 5(22): 5334
[10]Fang Q L, Duan S X, Zhang J F, et al. J Mater Chem A, 2017, 5(6): 2947
[11]Wang Y, Ma X D, Ding C, et al. Anal Chim Acta, 2015, 862: 33
[12]Tian F M, Zhang X H, Chen Y L. RSC Adv, 2016, 6(37): 31214
[13]Qin L, Li Z W, Hu Q, et al. Chem Commun, 2016, 52(44): 7110
[14]Erucar I, Keskin S. J Mater Chem B, 2017, 5(35): 7342
[15]Ghani M, Font Picó M F, Salehinia S, et al. J Chromatogr A, 2017, 1488: 1
[16]Mellot-Draznieks C, Serre C, Surblé S, et al. J Am Chem Soc, 2005, 127(46): 16273
[17]Yue X X, Guo W L, Li X H, et al. Environ Sci Pollut Res, 2016, 23(15): 15218
[18]Bezverkhyy I, Popova E, Geoffroy N, et al. J Mater Chem A, 2016, 4(21): 8141
[19]Zhang C H, Ai L H, Jiang J. J Mater Chem A, 2015, 3(6): 3074
[20]Zhang X Q, Wang T, Wang P Y, et al. Chinese Journal of Chromatography, 2016, 34(12): 1176
张晓琼, 汪彤, 王培怡, 等. 色谱, 2016, 34(12): 1176
[21]Coudert F X. Phys Chem Chem Phys, 2010, 12(36): 10904
[22]Wang Y H, Rui M, Lu G H. J Sep Sci, 2018, 41(1): 180
[23]Ghobadi M, Yamini Y, Ebrahimpour B. Ecotoxicol Environ Saf, 2015, 112: 68
[24]Lerma-García M J, Simó-Alfonso E F, Zougagh M, et al. Talanta, 2013, 105(4): 372
[25]Sui K, Li J, Wei F, et al. Chinese Journal of Chromatography, 2006, 24(2): 152
隋凯, 李军, 卫锋, 等. 色谱, 2006, 24(2): 152
