共水蒸馏法提取金银花挥发油及其成分分析
2018-01-27李建军任美玲尚星晨连笑雅王红磊
李建军,任美玲,尚星晨,连笑雅,王红磊
(1.河南师范大学 生命科学学院,河南省高校道地中药材保育及利用工程技术研究中心,河南 新乡 453007;2.河南绿生堂金银花生物发展股份有限公司,河南 新乡 453007)
金银花为忍冬科植物忍冬(LonicerajaponicaThunb.)的干燥花蕾或带初开的花,是常用大宗中药材,具有很好的凉散风热、杀菌消炎等功效[1-2]。挥发油是一类植物源次生代谢物质,分子量小且可随水蒸气蒸出,为具有一定挥发性的油状液体物质,植物学上称为精油,商业上称芳香油,化学和医药学上称挥发油[3]。金银花挥发油不仅具有浓烈的芳香气味,还有清咽、解热、化痰、平喘等功效[4],常用于医药、化妆、香料、食品等工业[5]。
河南省作为金银花的道地主产区[6],具有丰富的金银花资源和种植炮制技术。河南道地产区封丘,具有独特的生态条件和地理条件[7],十分适宜金银花生长。可是因深加工环节薄弱,制约了金银花种植产业的可持续发展。因此,深入开展金银花深加工[8-10],延伸产业链条,不仅可以促进金银花产业的健康发展,产生显著的经济与社会效益,还能提升河南金银花产业的核心竞争力。
本研究采用共水蒸馏法提取金银花挥发油,通过单因素试验,考查了金银花粉碎度、料液比、浸泡时间和提取时间对金银花挥发油得率的影响,在此基础上进行正交试验,优化提取工艺,并对所得挥发油进行了气相色谱-质谱联用分析(GC-MS),优化了检测条件,为工业化提取金银花挥发油提供理论技术支撑。
1 材料和方法
1.1 材料
金银花花蕾(大毛花,购于河南封丘金银花种植专业合作社),无水硫酸钠、乙醚均为分析纯,去离子水(实验室自制)等。
1.2 仪器设备
ZNHW恒温电加热套(上海恬恒仪器有限公司);Agilent 6890/5973型气相色谱-质谱联用系统:Agilent 7683型自动进样器、Nist 98标准质谱谱库(美国Agilent 公司)。
1.3 试验方法
1.3.1 共水蒸馏法提取金银花挥发油单因素试验
1.3.1.1 金银花粉碎度对得率的影响 取250 g不同粉碎度的金银花样品,置于5 L圆底烧瓶中,加入2 500 mL 5%氯化钠[11],连接挥发油测定器,在测定器中加去离子水至溢流入烧瓶为止,加热溶液至沸腾,提取时间8 h,测定所得挥发油质量。比较不同金银花粉碎度下金银花挥发油的得率。
1.3.1.2 浸泡时间对得率的影响 取250 g粉碎度0.85 mm的金银花样品,置于5 L圆底烧瓶中,加入2 500 mL 5%氯化钠浸泡不同时间,其他步骤同1.3.1.1。比较不同浸泡时间下金银花挥发油的得率。
1.3.1.3 料液比对得率的影响 取250 g粉碎度0.85 mm的金银花样品,置于5 L圆底烧瓶中,以不同料液比加入5%氯化钠,其他步骤同1.3.1.1。比较不同料液比下金银花挥发油的得率。
1.3.1.4 提取时间对得率的影响 取250 g粉碎度0.85 mm的金银花样品,置于5 L圆底烧瓶中,加入2 500 mL 5%氯化钠,连接挥发油测定器,在测定器中加去离子水至溢流入烧瓶为止,加热溶液至沸腾,提取不同时间,测定所得挥发油质量。比较不同提取时间下金银花挥发油的得率。
1.3.2 正交试验 选择粉碎度、提取时间、浸泡时间和料液比作为正交试验的研究因素,在单因素最佳试验参数上下选取3个参数进行正交试验,因素水平表见表1。
1.3.3 金银花挥发油GC-MS分析 取挥发油产物适量,溶于乙醚溶液中,再加入适量无水硫酸钠进行脱水处理,过0.45 μm滤膜,样品质量浓度8 g/L。

表1 正交试验因素水平
色谱条件:色谱柱HP-5MS 5%Phenyl MethylSiloxane Capillary 30.0 m×250 μm×0.25 μm nominal;载气为高纯氦气(He);流速0.6 mL/min;不分流进样;进样量为1.0 μL;柱温:程序升温,初始温度 80 ℃,升温速率为8 ℃/min升至120 ℃,保留20 min,5 ℃/min升至250 ℃,保留25 min。
质谱条件:进样口温度200 ℃,辅助线温度280 ℃,离子源温度230 ℃。 四级杆160 ℃;电离方式EI;电子能量70 eV,电子倍增管电压1.89 kV;扫描质量范围15.00~550.00 amu;采用Nist 98标准谱库对采集到的各个成分质谱图进行检索。
2 结果与分析
2.1 金银花挥发油提取单因素试验结果
2.1.1 金银花粉碎度对得率的影响 由图1可知,挥发油得率随着金银花粉碎度的升高而增加。当金银花粉碎度大于0.25 mm时,在加热过程中溶液易出现糊底现象,不利于试验进行。前人研究表明,粉末太细时,提取挥发油得率很低甚至没有,切断处理后的金银花采用共水蒸馏法提取出的金银花挥发油质量更高[12]。本试验结果表明,粉碎0.85 mm处理比切断2~3 mm处理挥发油质量高很多。因此,在试验中或生产中不适宜使用太细的粉末,金银花最佳粉碎度为粗粉,直径0.85 mm。

图1 金银花不同粉碎度的挥发油得率
2.1.2 浸泡时间对得率的影响 由图2可知,浸泡时间较短时对得率影响不明显,可能因为加热时间较长,浸泡时间对提取率的影响可以忽略不计,在后期延长浸泡时间后,挥发油得率有明显提高,加水浸泡能使细胞间隙变大,细胞膨胀,加速细胞内外液动态交换,利于挥发油的浸出[13]。浸泡24 h与浸泡36 h挥发油得率相当,从节约时间成本考虑,在生产中可以采用浸泡24 h。

图2 金银花不同浸泡时间的挥发油得率
2.1.3 料液比对得率的影响 由图3可知,挥发油得率随着料液比的增加而增加,当料液比升至1∶12 (g∶mL,下同)时,得率反而下降,可能由于料液比的增加,挥发油在水中的溶解量增加[14],使得随水蒸气蒸出的挥发油量减少,挥发油得率降低。综合以上因素,确定料液比最佳为1∶10。
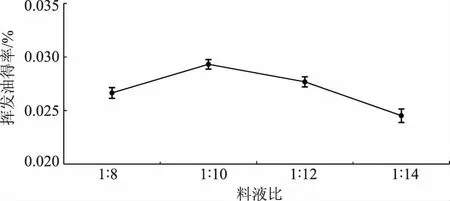
图3 金银花不同料液比的挥发油得率
2.1.4 提取时间对得率的影响 由图4可知,挥发油得率随着提取时间的增加而增加,提取40 h与46 h 差异不大,说明在本试验条件下,提取40 h时金银花挥发油大约能够提取完全,此时金银花挥发油得率约为0.170%。

图4 金银花不同提取时间的挥发油得率
2.2 金银花挥发油提取正交试验结果
按照表1进行挥发油共水蒸馏提取正交试验,结果见表2。由表2可知,共水蒸馏法提取金银花挥发油中4个因素的影响顺序为:粉碎度>提取时间>浸泡时间>料液比。由直观分析可知,最佳提取条件为A2B2C3D3,即粉碎度0.85 mm,料液比1∶10,浸泡时间28 h,提取时间42 h。

表2 共水蒸馏正交试验结果
以正交试验得到的最佳条件进行验证试验,取250 g 粉碎度0.85 mm的金银花置于5 L圆底烧瓶中,加入2 500 mL 5%氯化钠溶液,搅拌摇匀后,浸泡28 h,连续提取42 h,试验平行进行3次,得到金银花挥发油的平均得率为0.171%,高于正交试验结果中的最高值,证明通过正交试验得到的优化条件可信。确定最佳提取工艺为:粉碎度0.85 mm,料液比1∶10,浸泡时间28 h,提取时间42 h。
2.3 金银花挥发油GC-MS分析
产物挥发油经处理后进行GC-MS分析,得到挥发油总离子流色谱(图略);对每个成分进行Nist 98质谱库检索,共鉴定出79种成分,外标法计算各个物质的峰面积,并对色谱图中的各峰面积进行归一化,得到各组分的相对含量,结果见表3。
由表3可知,采用共水蒸馏提取的金银花挥发油成分种类繁多,鉴定成分79种,其含量占总成分的99.14%,其中脂肪酸类成分9种,占69.10%,酯类成分18种,占18.15%,烷烃类成分15种,占5.33%,酮类成分6种,占1.89%,烯烃类成分7种,占0.81%,醛类成分7种,占0.58%,炔烃类成分2种,占0.36%,醇类成分6种,占1.38%,其他成分9种,占1.54%。含量较高的单体成分及其含量为:棕榈酸占46.42%,亚油酸占14.32%,十六烷酸甲酯占6.02%,亚麻酸甲酯占4.45%,亚油酸甲酯占3.19%,十八烷酸占2.66%,二十七烷占1.87%,月桂酸占1.59%,邻苯二甲酸二丁酯占1.32%,二十五烷占1.08%,十九烷占1.03%等,含量较高的单体成分大部分为脂肪酸、脂类和烷烃类物质。
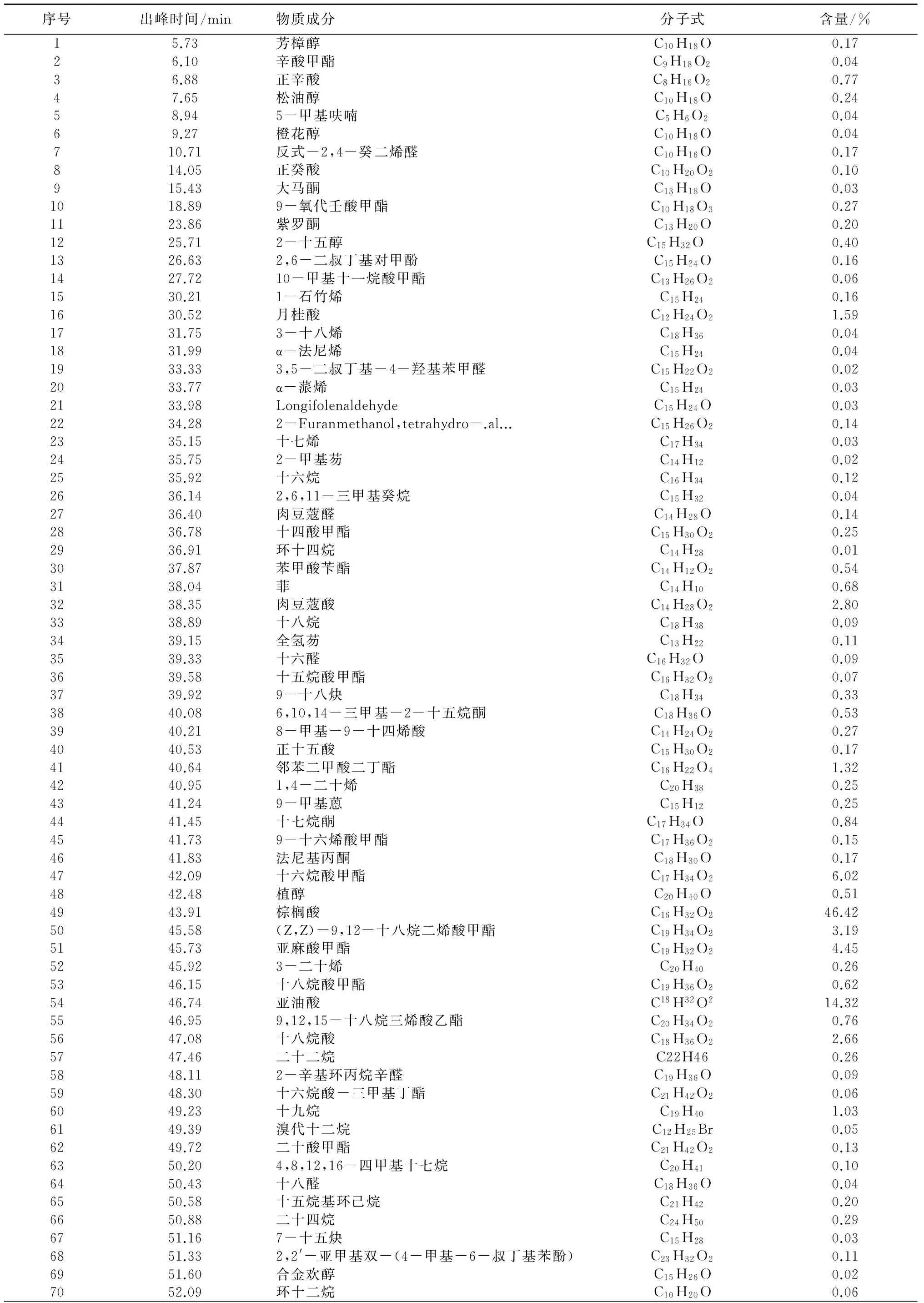
表3 金银花挥发油成分的GC-MS分析

续表3 金银花挥发油成分的GC-MS分析
注:21和22号物质,在CAS库中暂无相应的中文名,21号物质CAS号为019890-84-7,22号物质CAS号为026184-88-3。
3 结论与讨论
目前,生产上大多采用水蒸气蒸馏法来提取药材中的挥发油,该法可使挥发油的提取和药材煎煮同时进行,节约时间和能源[15]。水蒸气蒸馏法可分为2种:共水蒸馏法,即把植物浸在水中再进行加热来产生水蒸气;通水蒸气蒸馏法,即直接把水蒸气通入放有植物的容器中[11]。本研究采用共水蒸馏法提取金银花挥发油,以250 g金银花为原料,在单因素试验的基础上进行正交试验,得到最佳提取条件为金银花粉碎度0.85 mm,5%氯化钠溶液浸泡28 h,料液比1∶10,提取42 h,得率0.171%。
何文全等[16]以100 g粉碎金银花为原料,通过正交试验得到共水蒸馏提取金银花挥发油的最佳工艺为浸泡2 h,提取时间5 h,加水量8倍,得率0.056%。与何文全等[16]的结果相比,本研究提取时间较长,考虑与所用金银花的量较大有关,本研究挥发油提取率较高,说明对金银花粉碎度进行优化[11]和氯化钠浸泡处理能够提高挥发油得率。
在试验中发现,通过提高检测样品质量浓度(8 g/L),减慢气相色谱升温速率(初始温度 80 ℃,以8 ℃/min升至120 ℃,保留20 min,以5 ℃/min升至250 ℃,保留25 min),能够优化检测条件,使挥发油出峰情况良好,在该色谱条件下,检测到金银花挥发油成分79种。狄留庆等[17]通过水蒸气蒸馏提取的挥发油被鉴定出成分27种,主要成分为有机酸类和有机酸脂类;宋兴良等[18]通过共水蒸馏提取的挥发油鉴定物质38种,主要成分为有机酸类、有机酸脂类和饱和烷烃类。本研究与前人鉴定的挥发油主要成分种类相同,检出成分较多,在每个物质种类下检测得到的单体化合物种类丰富,并且检测到其他种类化合物较多。说明本研究优化的色谱条件良好,有利于分离挥发油中单体化合物。
本研究以封丘大毛花为试验材料,优化共水蒸馏法提取工艺和挥发油检测条件,提取率达0.171%,鉴定挥发油成分79种,可为工业化提取金银花挥发油及其质量控制提供技术理论支撑。
[1] 国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2015:221.
[2] 李建军,李军芳,李景原,等.金银花与山银花的性状差异及鉴别方法[J].河南农业科学,2011,40(4):134-137.
[3] 王巨媛,翟胜.植物精油应用进展及开发前景展望[J].江苏农业科学,2010(4):1-3.
[4] 苏香萍,龚大春,张亚雄,等.金银花CO2超临界萃取物的体外抑菌作用研究[J].时珍国医国药,2009,20(4):832-834.
[5] 马勤川,贾凯,卢杰,等.亚临界R134a萃取金银花挥发油[J].食品工业科技,2012,33(13):197-200.
[6] Shang X F,PAN H,LI M X,etal.LonicerajaponicaThunb.:Ethnopharmacology,phytochemistry and pharmacology of an important traditional Chinese medicine[J].Journal of Ethnopharmacology,2011,138(1):1-21.
[7] 李建军,王君,任美玲,等.金银花新品系与主栽品种的表皮毛、叶色素及光合速率的比较分析[J].河南师范大学学报(自然科学版),2016,44(1):137-141.
[8] 冷慕婵,董诚明,乔毅琳,等.金银花中产绿原酸内生真菌的分离与鉴定[J].河南农业科学,2014,43(7):107-111.
[9] 李建军,贾国伦,李静云,等.金银花不同花期花蕾质量及指标成分含量比较分析[J].河南农业科学,2013,42(10):110-114.
[10] 李宁,李楚.金银花中绿原酸提取工艺的正交优化法研究[J].山西农业科学,2010,38(3):14-15,22.
[11] 蒙永业,梁红,李修善.金银花挥发油提取工艺研究[J].企业科技与发展,2012,28(15):67-68.
[12] 童巧珍,周日宝,杜方麓,等.金银花中挥发油提取工艺探讨[J].湖南中医学院学报,2002,22(4):24-25.
[13] 郑勇,张志兰.正交实验法优选豆蔻挥发油提取工艺[J].时珍国医国药,2006,17(4):596.
[14] 肖敏,谭红军,李晓华,等.金银花茎叶挥发油提取工艺研究[J].重庆中草药研究,2012,33(2):6-10.
[15] 刘华钢,陆峥琳,赖茂祥,等.中药挥发油类成分提取分离研究概况[J].辽宁中医药大学学报,2009,11(11):5-8.
[16] 何文全,林江蔚,刘汉儒.金银花挥发油的提取及包合工艺研究[J].中国兽药杂志,2009,43(6):32-34.
[17] 狄留庆,蔡宝昌,李伟东,等.金银花挥发性成分的GC-MS分析[J].中药材,2003,26(7):491-492.
[18] 宋兴良,吕莉.金银花中挥发性成分的GC/MS分析及其指纹图谱的建立[J].临沂师范学院学报,2010,32(3):96-100.
