离子色谱法测定肉制品中5种食品添加剂
2018-01-23许晶冰蔡灵利
许晶冰,蔡灵利,毛 庆
亚硝酸盐、硝酸盐是肉制品加工中常用的发色剂和防腐剂[1]。硝酸盐与亚硝酸盐在一定条件下能够相互转化,食品中的亚硝酸盐在一定条件下会转化为亚硝胺,而亚硝胺是一种致癌物质[2]。在国家标准方法中,测定亚硝酸盐和硝酸盐第一法为离子色谱法[3]。
山梨酸和苯甲酸是食品加工中常用的防腐剂,国家标准规定:肉制品中允许添加一定量的山梨酸,苯甲酸不得添加[1]。目前常用的测定山梨酸和苯甲酸的方法有紫外分光光度法、气相色谱法、液相色谱法等[4]。
安赛蜜是食品加工中常用的甜味剂,在肉制品中不允许添加[1],但有不法商家为节约成本而违法使用。目前常用液相色谱法对其进行测定[5]。
对于肉制品的日常监管中,常需要对其中的亚硝酸盐、硝酸盐、山梨酸、苯甲酸、安赛蜜同时进行测定。由于这几种物质在碱性条件下均呈阴离子状态,故能够通过离子色谱仪的电导检测器测定,目前已有多篇文献进行了报道[6-10]。本工作以基质较为复杂的火腿肠和肉灌肠为研究对象,采用离子色谱法,探讨样品前处理方法以及样品基质对于目标物测定的影响,为肉制品中添加剂的测定提供一种新的可靠方法。
1 试验部分
1.1 仪器与试剂
ICS 5000型离子色谱仪,配EGC 500OH-型离子发生器、电导检测器;On Guar d II Ag固相萃取(SPE)小柱;0.22μm尼龙滤膜;Millipore纯水仪。
混合 标 准 溶 液:20 mg·L-1,分 别 移 取1.00 g·L-1的亚硝酸盐(以NO-2计)、硝酸盐(以NO-3计)、苯甲酸、山梨酸、安赛蜜标准储备溶液各1.00 mL混合于50 mL容量瓶中,用水定容。
亚硝酸根、硝酸根、苯甲酸、山梨酸、安赛蜜标准储备溶液:1.00 g·L-1。
试验用水为超纯水(电阻率为18.2 MΩ·c m)。
1.2 仪器工作条件
Ion Pac AS 19阴离子交换分析柱(250 mm×4 mm);Ion Pac AG 19 阴离子保护柱 (50 mm×4 mm);ASRS 400型抑制器,自循环模式,抑制电流174 mA。KOH 淋洗液梯度:0~11 min,5 mmol·L-1;11.1~15 min,18 mmol·L-1;15.1~23 min,25 mmol·L-1;23.1~28 min,70 mmol·L-1;28.1~32 min,5 mmol·L-1。流量1.0 mL·min-1;进样量25μL。
1.3 试验方法
称取样品1.000 0 g于10 mL比色管中,用20 mmol·L-1Na OH 溶液溶解并稀释至刻度,涡旋振荡4 min,超声提取10 min,置于-18℃冻藏静置40 min。移取水10 mL,以2 mL·min-1流量冲洗SPE小柱。移取样品管中层液体,过SPE小柱,弃去前3 mL流出液,收集后过0.22μm水性样品滤膜,在仪器工作条件下进行测定。
2 结果与讨论
2.1 样品前处理条件的选择
用离子色谱法测定肉制品中的阴离子,干扰物质为脂肪、蛋白质以及肉品调料所带入的阴离子。由于肉制品一般含有较多脂肪,部分文献使用有机溶剂去除脂肪。文献[11]使用加入三氯甲烷振摇离心的方法去除油脂,得到较好结果。对于蛋白质的去除,则大多使用SPE小柱净化样品。文献[12]使用C18小柱和0.145μm滤膜净化样品,有较好净化效果。但本试验使用该小柱后发现,肉制品中存在大量卤素离子,其出峰时间与山梨酸和亚硝酸盐的出峰时间接近,对样品的分析产生干扰,而C18柱无法去除卤素离子且会降低目标物回收率。因此,不使用C18小柱,用 On Guard II Ag柱结合0.22μm滤膜净化样品,有效去除了样品中的卤素离子和蛋白质,且目标物的回收率在80.0%~110%之间。对样品中油脂的去除,则采用低温处理的方法,使动物油脂凝固于上层,且低温也有助于样品中蛋白质的沉淀。本方法步骤简单且无需使用有机试剂,能够有效去除样品中的脂肪、蛋白质及卤素离子,对目标物质均有较高的回收率。
现有文献中,使用离子色谱法分析肉类样品,绝大部分使用去离子水提取样品。试验过程中发现,肉类样品本身可能呈酸性,而苯甲酸、山梨酸、安赛蜜在碱性条件下才电离,呈阴离子状态。因此,在使用低浓度洗脱液进行分析的时候,出现目标物的响应值不高,或是个别样品无法检测到某一目标物。试验最终选取20 mmol·L-1Na OH溶液为提取液,在不引入其他离子的同时,又能保证样品溶液呈碱性,提高了试验的稳定性。
2.2 色谱条件的选择
试验比较了3种阴离子分析柱的分离效果。Ion Pac AS 16阴离子交换分析柱是亲水性较强的高容量柱,对于苯甲酸、山梨酸、安赛蜜有良好的分离效果,但亚硝酸盐的保留时间较短,其被样品杂峰掩盖而无法分离。Ion Pac AS 11-HC阴离子交换分析柱对硝酸盐及亚硝酸盐有良好的分离效果,但对于安赛蜜和苯甲酸有很强的吸附能力,需要高浓度OH-进行洗脱,且分离效果不理想。因此,试验最终选用Ion Pac AS 19阴离子交换分析柱,能够用较低浓度OH-洗脱将目标物分离,使用70 mmol·L-1洗脱剂可将样品剩余残留物洗脱,可获得平稳基线和良好的峰形。在此条件下,混合标准溶液的离子色谱图见图1。
2.3 标准曲线和检出限
移取混合标准溶液并用水稀释,配制成质量浓度依次为0,0.2,0.4,0.8,1.6,2.4,3.2,4.0,8.0 mg·L-1的混合标准溶液系列,在仪器工作条件下进行测定,以各组分的质量浓度(mg·L-1)为横坐标,峰面积(μS·min)为纵坐标绘制标准曲线。结果表明:各组分的质量浓度在0.2~8.0 mg·L-1内与峰面积呈线性关系,线性回归方程及相关系数见表1。
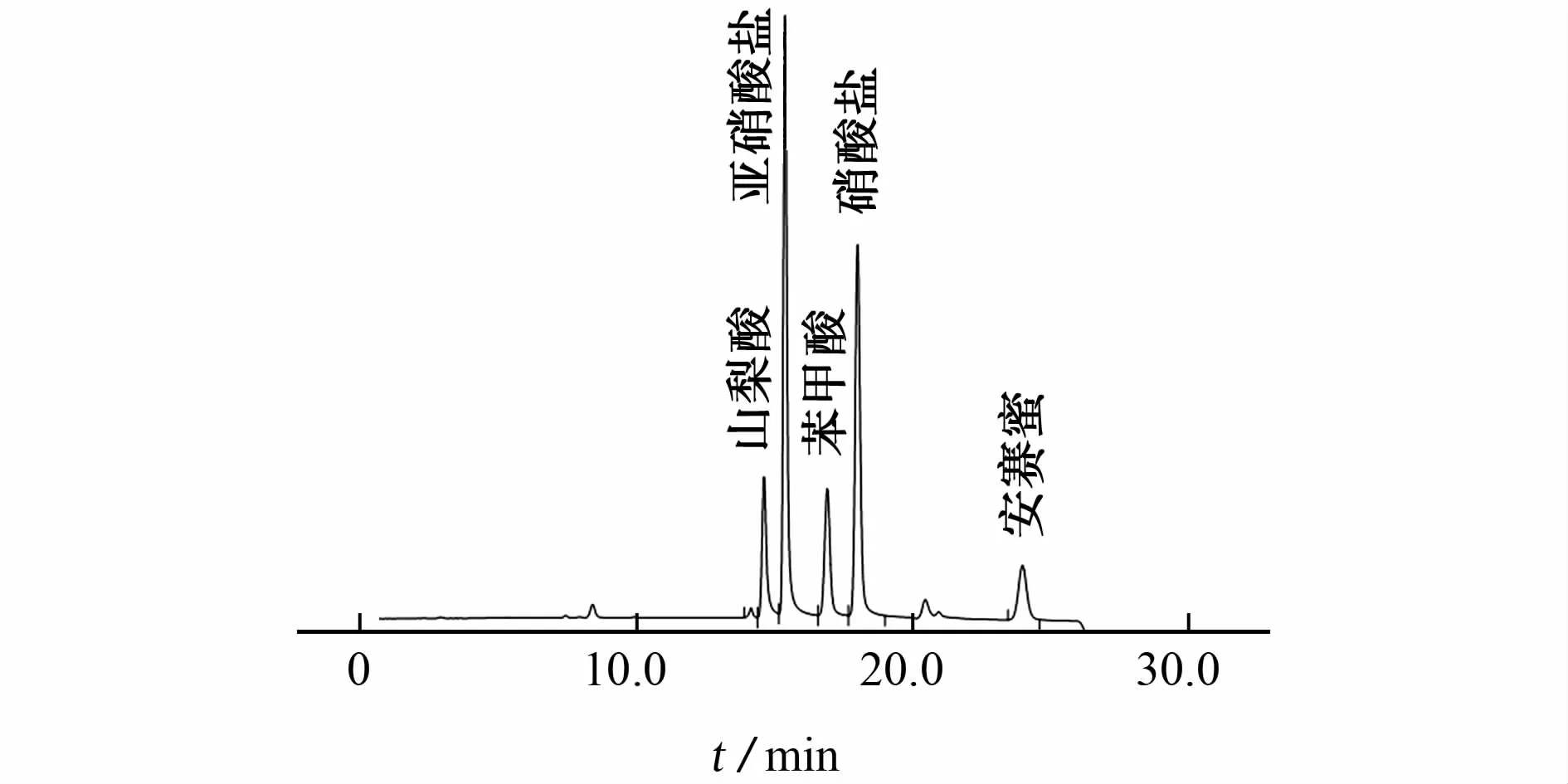
图1 混合标准溶液的离子色谱图Fig.1 IC chr o mat ogra m of mixed standard solution
按3倍信噪比计算检出限(3S/N),结果见表1。
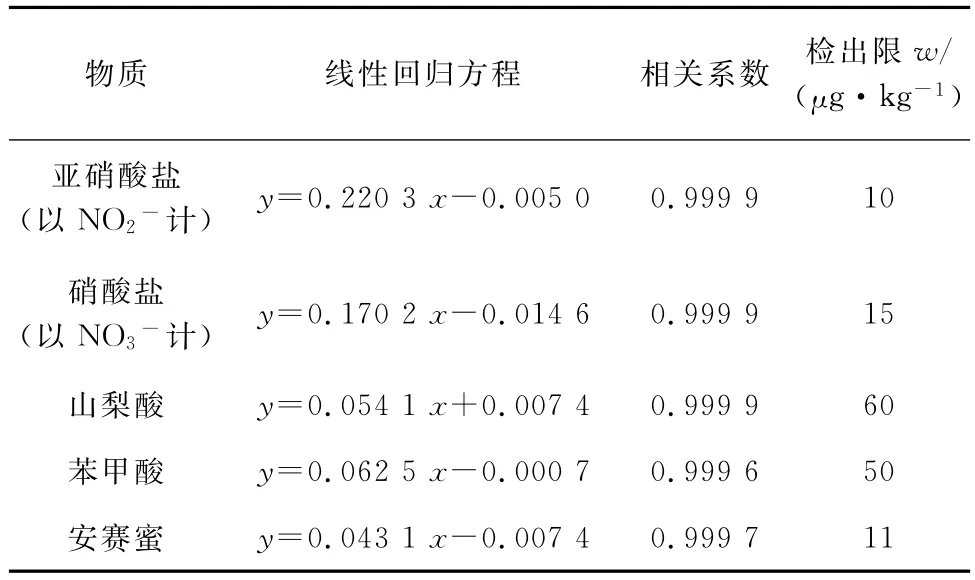
表1 线性参数与检出限Tab.1 Linearity para meters and detection li mits
2.4 样品分析及精密度与回收试验
选取具有代表性的市售河南猪肉火腿肠(S1)、成都猪肉火腿肠(S2)、重庆肉灌肠(S3)进行样品分析及加标回收试验,平行测定6次,结果见表2。
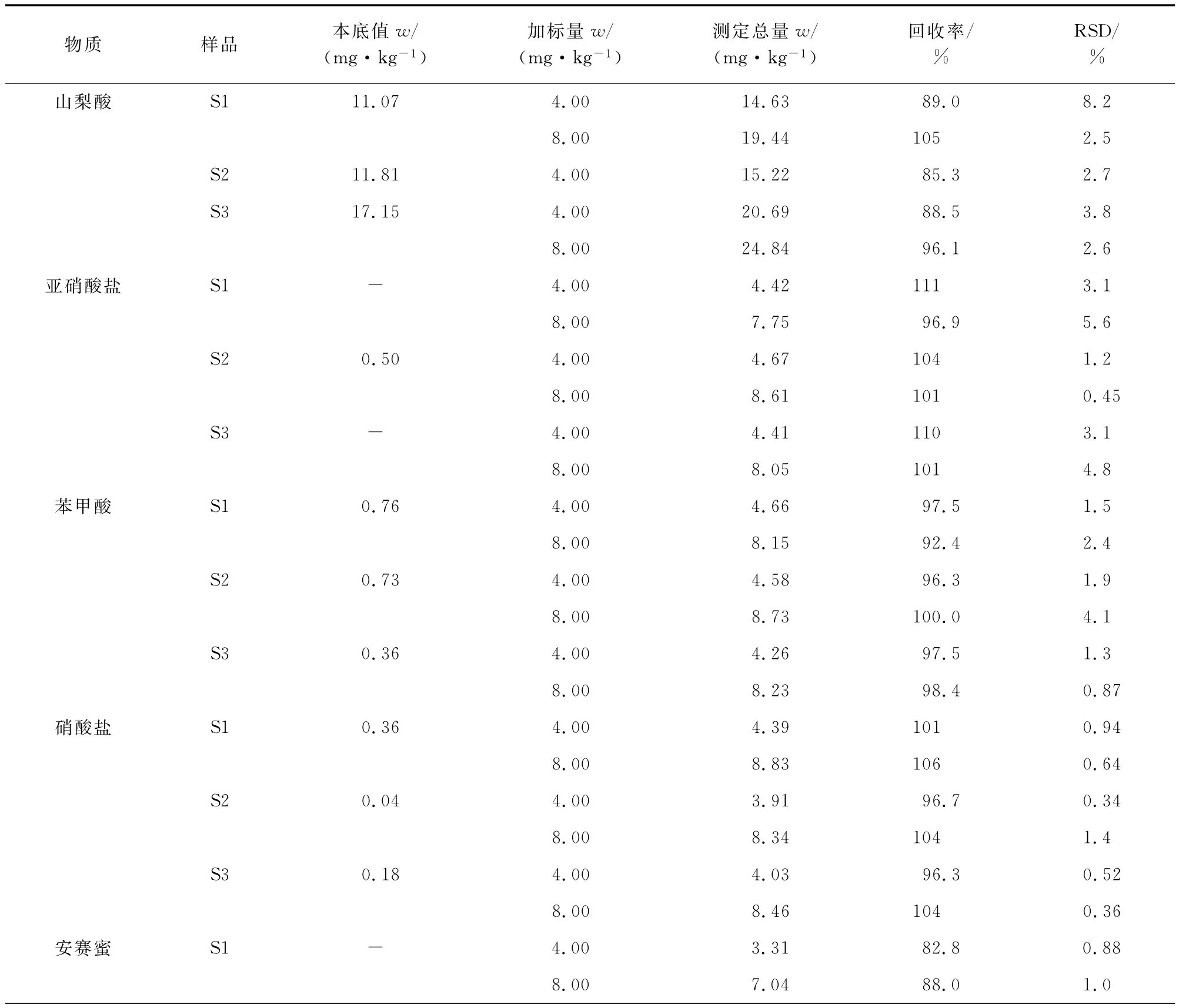
表2 样品分析及精密度与回收试验结果(n=6)Tab.2 Results of sa mple analysis and tests f or precision and recovery(n=6)

表2 (续)
由表2可知:3种样品中的5种食品添加剂含量符合国家标准要求[1],样品加标回收率在82.5%~111%之间,测定值的相对标准偏差(RSD)在0.26%~8.2%之间。
3种样品的色谱图见图2。
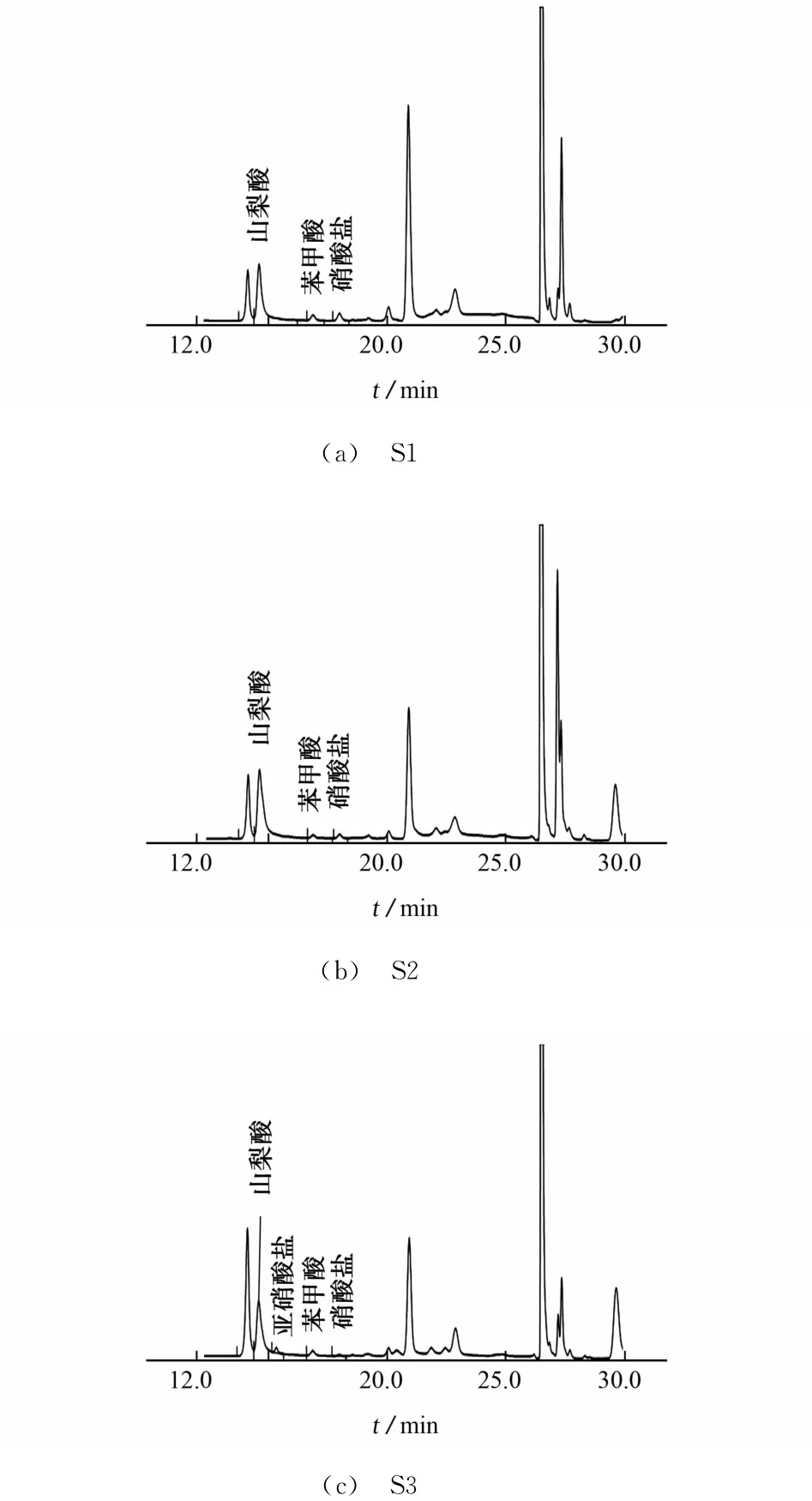
图2 样品的色谱图Fig.2 Chromatograms of samples
由图2可知:3种样品的基体峰均集中在19~22 min和26~29 min,避开了待测物质的出峰区域,达到了很好的分离效果,基本没有干扰峰存在。由此可见:本方法稳定可靠,准确性高。
本工作建立了能够同时测定肉制品中的山梨酸、苯甲酸、硝酸盐、亚硝酸盐、安赛蜜的离子色谱法,方法有效节约检测时间及检测成本,分析快速,结果稳定可靠,可适用于卤素离子含量较高的肉制品中食品添加剂的快速测定。
[1] GB 2760-2011 食品添加剂使用标准[S].
[2] 夏延斌.食品化学[M].北京:中国轻工业出版社,2001:358-360.
[3] GB 5009.33-2010 食品中亚硝酸盐与硝酸盐的测定[S].
[4] GB/T 23495-2009 食品中苯甲酸、山梨酸和糖精钠的测定 高效液相色谱法[S].
[5] GB/T 5009.140-2003 饮料中乙酰磺胺酸钾的测定[S].
[6] 林华影,张琼,盛丽娜,等.离子色谱法同时测定食品中五种添加剂[J].中国卫生检验杂志,2004,14(5):556-558.
[7] 郭坚,何光源,崔海容,等.抑制型离子色谱法检测蔬菜中的亚硝酸盐与硝酸盐[J].检验检疫学刊,2010(6):16-18.
[8] 钟志雄,梁春穗,姚敬,等.离子色谱法测定食品中的甜蜜素和苯甲酸[J].中国卫生检验杂志,2005,15(9):1062-1064.
[9] 曾爱民.淋洗液发生器离子色谱电导抑制法测定饮料中的添加剂[J].现代科学仪器,2005(5):64-65.
[10] 刘丽敏,彭敬东.5种甜味添加剂的反相高效液相色谱法同时测定[J].分析测试学报,2008,27(5):549-552.
[11] 刘岚松,康绍英,张丽,等.离子色谱法测定肉制品中亚硝酸盐与硝酸盐的改进研究[J].食品与机械,2015,31(2):83-86.
[12] 王新芳.离子色谱法测定火腿肠中的硝酸盐和亚硝酸盐[J].食品研究与开发,2015,29(9):104-106.
