高效液相色谱-串联质谱法测定猪肉中氯霉素和五种磺胺类药物的残留量
2018-01-22,,,,,,,,*
, ,,,,,, ,*
(1.贵州医科大学药学院,贵州贵阳 550004; 2.贵州医科大学贵州省药物制剂重点实验室,贵州贵阳 550004; 3.贵州医科大学民族药与中药开发应用教育部工程研究中心,贵州贵阳 550004)
随着人们生活日益富裕,对猪肉的需求量也越来越多。然而,动物源性食品兽药残留的安全问题也日益突显,严重危害着公共卫生安全及人体健康,引起了各方面的高度关注[1-2]。兽药作为预防、治疗、诊断畜禽等动物疾病药物,在养殖业中发挥着重要的作用,但是由于养殖者合理用药知识缺乏或经济利益的驱使,滥用兽药的现象在养殖业中时有发生[3-7]。
氯霉素和磺胺类药物由于具有抗菌谱广、价格低廉和性质稳定等特点,成为畜禽抗感染治疗中的重要药物[8-9]。但是,这些药物的不当使用会造成其在动物组织中富集,可直接或间接地通过环境和食物链的作用对人体产生一定的毒副作用,引起细菌耐药性的增加。目前,国内外报道的检测动物源性食品中氯霉素或磺胺类药物残留的检测方法主要有液相色谱法(HPLC)、高效毛细管电泳法(HPCE)、液相色谱-质谱法(LC-MS)、液相色谱-串联质谱联用法(LC-MS/MS)[10-13]等。由于LC-MS/MS联用技术具有灵敏度高、专属性强、准确、快速和高效的优点,在很大程度上提高了分析能力和分析效率,在残留分析技术上应用广泛。目前,氯霉素和磺胺类药物是常监控的兽药,但是它们的检测方法是两种独立的方法,若能合并检测,将提高分析效率。
因此,本实验建立超高效液相色谱-串联质谱(UPLC-MS/MS)方法同时检测猪肉中氯霉素和5种磺胺类药物(磺胺甲嘧啶、磺胺二甲嘧啶、磺胺噻唑、甲氧苄啶和磺胺嘧啶),该方法快速简便、定量准确、灵敏度高,缩短了样品前处理和进样时间,提高了分析能力和分析效率,以保障对该类药物的残留监控。
1 材料与方法
1.1 材料与仪器
甲氧苄啶(≥99.9%)、磺胺甲嘧啶(≥98%)、磺胺噻唑(≥98.0%) 大连美仑生物有限公司;磺胺二甲嘧啶(≥100.0%)、磺胺嘧啶(≥99.7%) 中国食品药品检定研究院;氯霉素(≥98.5%)、氯霉素-D5(≥99.0%,100 μg/mL) Dr.Ehrenstorfer;乙腈 色谱纯,德国Merck 公司;猪肉 北京华联超市(经测定不含甲氧苄啶、磺胺二甲嘧啶、磺胺甲嘧啶、磺胺噻唑、磺胺嘧啶、氯霉素)。
TQ Detector/ESI+型超高液相色谱仪三重四级杆质谱联用仪 美国Waters公司;Allegra 64R低温高速离心机 美国Beckman Coulter公司;AE240十万分之一电子天平 梅特勒-托利多仪器上海有限公司;KNSY0020超纯水机 四川沃特尔科技发展有限公司;KQ-300DE型数控超声波清洗器 昆山市超声仪器有限公司。
1.2 实验方法
1.2.1 内标溶液的配制 准确吸取100 μg/mL的氯霉素-D5溶液1 mL,氮气吹干后,加乙腈定容至25 mL棕色容量瓶中,得4 μg/mL的氯霉素-D5储备液,然后将储备液制备成8 ng/mL的工作液。
1.2.2 对照品溶液的配制 精密称取氯霉素9.6 mg、甲氧苄啶10.4 mg、磺胺二甲嘧啶10.4 mg、磺胺甲嘧啶10.2 mg和磺胺噻唑10.2 mg,加乙腈分别定容至10 mL,分别得到浓度为0.96、1.04、1.04、1.02、1.02 mg/mL的氯霉素、甲氧苄啶、磺胺二甲嘧啶、磺胺甲嘧啶、磺胺噻唑的标准储备液;精密称取磺胺嘧啶9.5 mg,加乙腈定容至100 mL,得到浓度为95 μg/mL磺胺嘧啶的标准储备液。将储备液制备成混合标准溶液(氯霉素、磺胺二甲嘧啶、甲氧苄啶、磺胺甲嘧啶、磺胺噻唑和磺胺嘧啶分别为0.192、10.4、10.4、10.2、10.2、9.5 μg/mL),再按倍数稀释至表1中系列浓度的标准溶液。
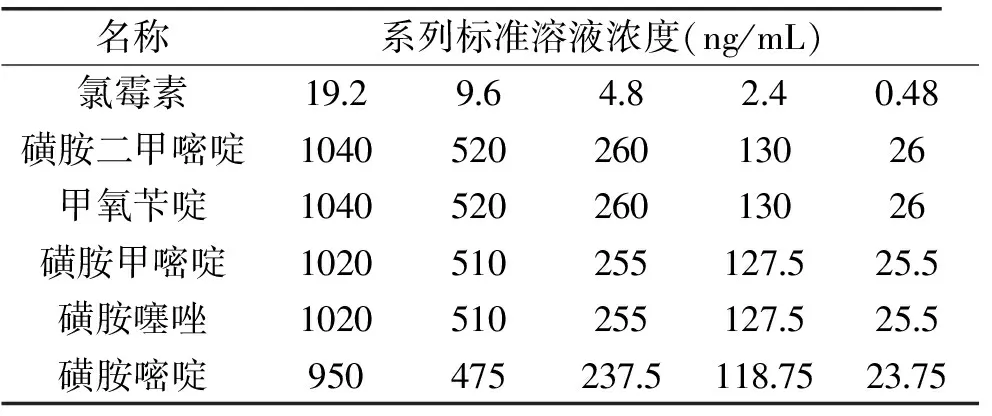
表1 6种兽药系列标准溶液浓度Table 1 The series concentration of six kinds of veterinary medicines
1.2.3 分析条件 色谱条件:色谱柱:Acquity UPLC BEH C18(2.1 mm×50 mm,1.7 μm);进样量:10 μL;柱温:45 ℃;流动相A:乙腈;流动相B:水;流速:0.35 mL/min;梯度洗脱程序:0~1.5 min用20%~38% A;1.5~2 min用38%~95% A;2~3 min用95% A;3~5 min用95%~20% A。质谱条件:电喷雾电离源(ESI);毛细管电离电压(3 kV);离子源温度(120 ℃),去溶剂气(氮气,650 L/h),去溶剂气温度(350 ℃),碰撞气(氩气,0.16 mL/min),扫描方式为多反应离子监测模式(MRM)。氯霉素和五种磺胺类药物用于定量分析的监测离子见表2。

表2 质谱分析条件Table 2 Mass spectrometric conditions of six kinds of veterinary medicines
1.2.4 猪肉前处理 称取5.00 g猪肉,置于50 mL离心管中,加入8 ng/mL氯霉素-D5100 μL后,加入10 mL乙酸乙酯后匀浆,涡混3 min,90 Hz超声5 min,6000 r/min离心5 min,转移上清液至另一试管中,下层重复以上操作,合并乙酸乙酯,有机层用氮吹仪在40 ℃下吹干,残渣用0.4 mL 10%乙腈水超声溶解,加0.5 mL正己烷除脂,6000 r/min离心5 min,弃上层,下层过0.22 μm微孔滤膜,UPLC-MS/MS进样分析。
1.2.5 方法的适用性 分别取6份空白猪肉5.00 g,除不加内标外,其余按“1.2.4”项操作,获得空白猪肉色谱图。将标准溶液(氯霉素、磺胺二甲嘧啶、甲氧苄啶、磺胺甲嘧啶、磺胺噻唑和磺胺嘧啶分别为4.8、260、260、255、255、237.5 ng/mL)和内标溶液加入空白猪肉,同上操作得加标猪肉色谱图。
1.2.6 标准曲线和线性范围 分别取6份空白猪肉5.00 g,除不加内标外,其余按“1.2.4”项操作,获得空白猪肉基质。分别将100 μL内标溶液和“1.2.2”中系列浓度的标准溶液分别加入至空白猪肉基质中。5种磺胺类药物采用外标法定量,氯霉素采用内标法定量。以5种磺胺类药物的峰面积为纵坐标Y,各物质浓度(C)为横坐标X进行直线回归;以氯霉素的峰面积与内标峰面积之比(A/Ai)为纵坐标Y,各物质浓度(C)为横坐标X进行直线回归,求得直线方程,即为标准曲线。氯霉素等6种成分的定量限(LOQ)定义为S/N≥10,检测限(LOD)定义为S/N≥3。
1.2.7 方法的准确度和精密度 取空白猪肉5.00 g,按“1.2.2”项分别配制6种成分低、中、高三个浓度的样品,按“1.2.4”项下操作,每一个浓度进行6样本分析,日内连续进样,并与标准曲线同时进行。每个系列浓度做6份,计算日内精密度;3种浓度连续测定3 d,计算日间精密度。
1.2.8 提取回收率和基质效应 取空白猪肉5.00 g,按“1.2.2”项下分别配制6种成分低、中、高三个浓度的样品,每个浓度平行测定5份,按“1.2.4”项下操作(A样品);另取空白猪肉5.00 g,除不加混合标准溶液外,其余按“1.2.4”项下操作,向获得的上清液中加入相应低、中、高浓度的混合标准溶液和内标,吹干,残留物以0.4 mL 10%乙腈水溶解(B样品);另取上述低、中、高浓度的混合标准溶液与内标,吹干,残留物以0.4 mL 10%乙腈水溶解(C样品)。A样品与B样品色谱峰面积之比为提取回收率,B样品与C样品的色谱峰面积之比为基质效应。
1.2.9 稳定性 取空白猪肉5.00 g,按“1.2.2”项下分别配制6种成分低、中、高三个浓度的样品,样品处理后置于自动进样器中,在0、6 h分别进样,以考察处理后样品在自动进样器条件下的稳定性,每一浓度分析5个样本。同法配制低、中、高三个浓度的样品,分别在室温(约20 ℃)下放置6 h,4 ℃下冷藏8 h,冻融循环3次,经处理后进样测定,以考察样品中各指标成分在室温,冷藏,反复冻融条件下的稳定性,每一浓度分析5样本。
2 结果与分析
2.1 方法的适用性
进样检测得到空白猪肉色谱图1(A)和加标猪肉色谱图1(B)。空白猪肉在6种药物及其对应内标的出峰位置均没有干扰峰,方法的专属性较高,加标样品中磺胺嘧啶、磺胺噻唑、磺胺甲氧嘧啶、磺胺甲嘧啶、甲氧嘧啶、氯霉素和氯霉素-D5的保留时间分别为1.55、1.93、2.24、2.78、2.93、3.14、3.14 min,出峰时间稳定,分离完全。

图1 空白猪肉样品(A)和加标猪肉样品(B)的多反应监测色谱图Fig.1 Multiple reaction monitoring chromatograms of the blank sample(A)and the sample added six kinds of veterinary medicines(B)注:1.磺胺嘧啶;2.磺胺噻唑;3.磺胺甲嘧啶;4.甲氧嘧啶; 5.磺胺二甲嘧啶;6.氯霉素-D5;7.氯霉素。
2.2 标准曲线和线性范围
在本方法所确定的条件下,5种磺胺类药物以峰面积为纵坐标,基质匹配标准溶液浓度为横坐标作图;氯霉素和内标的特征离子质量色谱峰面积比为纵坐标,基质匹配标准溶液浓度为横坐标作图,各药物均呈现良好的线性关系,见表3。
氯霉素和5种磺胺类药物分别在9.6~384 ng/kg和0.51~20.8 μg/kg浓度呈良好的线性关系,相关系数(R2)均在0.99以上(表3)。氯霉素的检测限为3.2 ng/kg,5种磺胺类药物检测限为0.158~0.173 μg/kg,氯霉素的定量限为9.6 ng/kg,5种磺胺类药物定量限0.475~0.52 μg/kg。
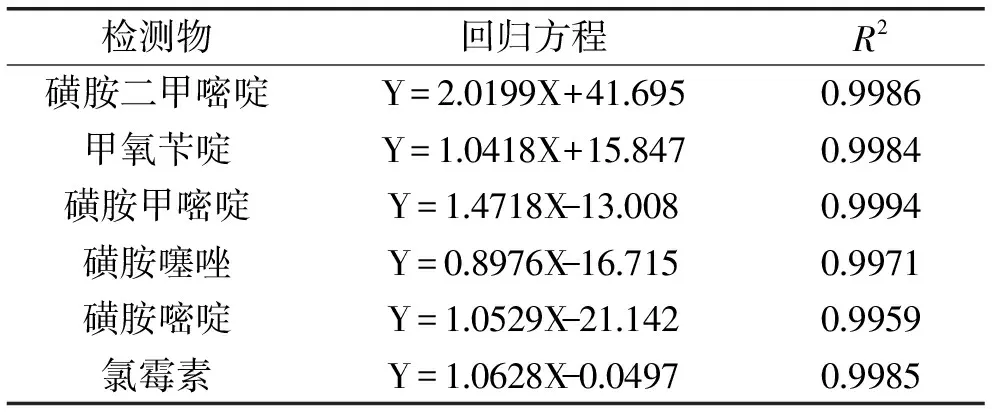
表3 6种药物的标准曲线Table 3 Linear equations and correlation coefficients of six kinds of veterinary medicines
2.3 方法的准确度和精密度

表4 6种药物在血浆中的准确度、日内和日间精密度(n=6,3 days)Table 4 Intra-and inter-day precision and accuracy of six kinds of veterinary medicines(n=6,3 days)
结果表明6种药物的准确度范围为85.21%~93.04%,日内和日间精密度RSD(%)均小于5%,提示该方法准确、可靠、重现性好。测定结果见表4。
2.4 提取回收率和基质效应
空白猪肉样品中分别加入高、中、低3个浓度水平的混合标准溶液进行回收率实验,方法平均回收率为70.84%~103.99%,相对标准偏差为1.98%~8.01%,实验结果表明各药物提取回收率良好,无明显的基质效应。结果见表5。
2.5 稳定性实验
各浓度下的样品在室温下放置6 h,4 ℃冷藏8 h,冻融3次以及自动进样器中放置6 h后稳定性考察结果见表6,结果表明含6种药物的样品在上述放置条件下稳定。
3 讨论
3.1 猪肉前处理条件的优化
提取残留药物时一般使用甲醇、乙腈溶液[14-18],本实验考察了甲醇、乙腈、乙酸乙酯等提取液,实验结果表明使用乙酸乙酯的回收率较高,且无杂质峰干扰。在溶解残渣时加入正己烷进一步除去猪肉样品中的杂质。
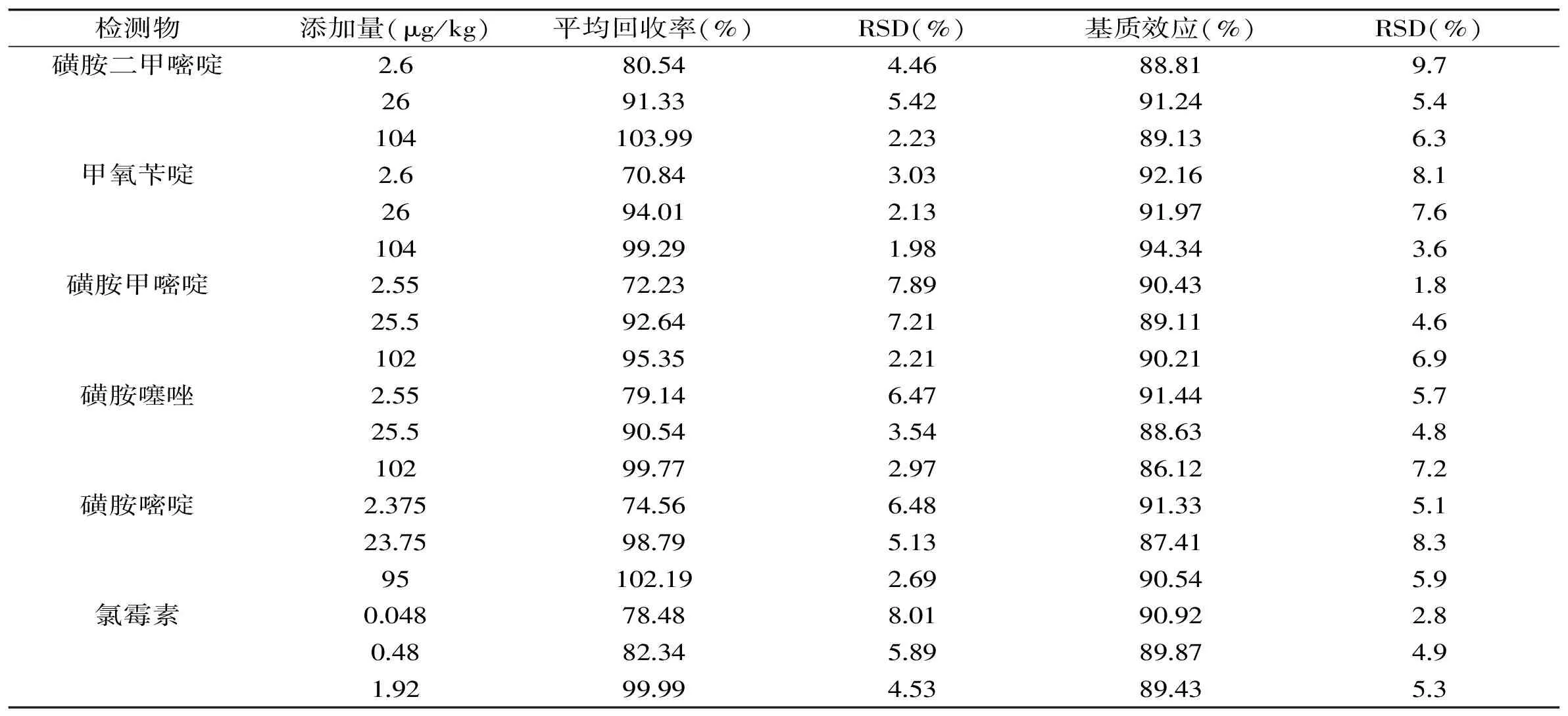
表5 6种药物的提取回收率和基质效应(n=5)Table 5 Added recovery and matrix effects of six kinds of veterinary medicines in pork(n=5)
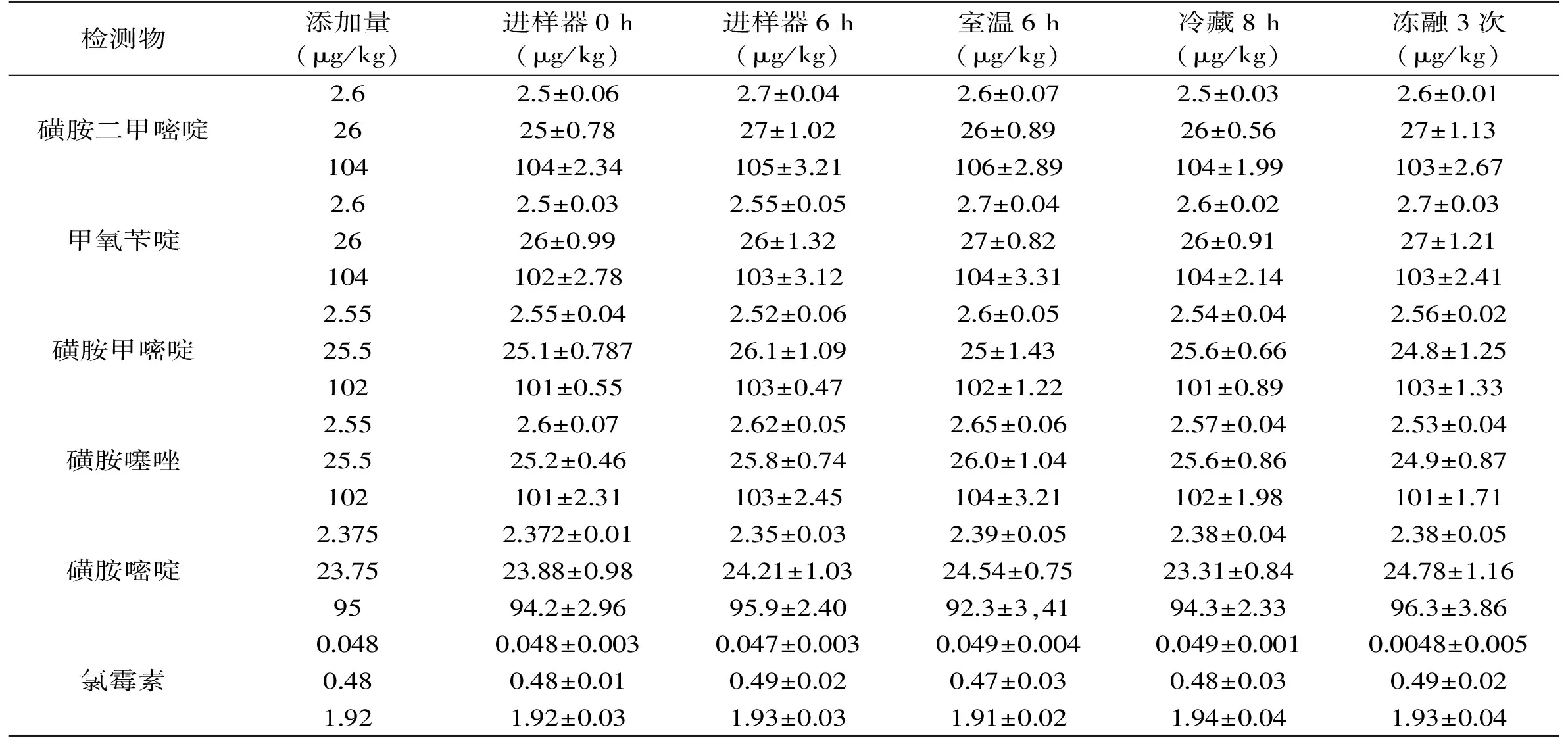
表6 6种药物的稳定性(n=5)Table 6 Stability of six kinds of veterinary medicines in pork(n=5)
3.2 液相条件优化
对于多组分分析,采用梯度洗脱易于药物的分离。本方法以Acquity UPLC BEH C18(2.1 mm×50 mm,1.7 μm)作为色谱柱。考察了0.1%甲酸乙腈-0.1%甲酸水溶液、0.1%甲酸甲醇-0.1%甲酸水溶液、甲醇-水、乙腈-水四种流动相体系,经过对比发现,乙腈-水能获得较好的峰型和较高的响应。
3.3 质谱条件优化
实验采用各个药物的标准溶液在电喷雾离子源下进行全扫描,确定准分子离子。以分子离子为母离子对子离子全扫描,在多反应检测模式下对其质谱条件进行优化。得到各药物灵敏度较高的质谱条件。
4 结论
本实验采用超高效液相色谱-串联四级质谱联用仪,建立了猪肉中6种兽药残留量测定方法。样品前处理采用液-液萃取的方法,与固相萃取法相比,能大大降低实验成本,并且缩短了样品前处理时间。样品分析时间仅为5 min,与传统液相色谱方法相比,分离效率高、极大地缩短了分析时间。并且,该方法线性、回收率均能满足检测要求,该法简便、快速、准确,可用于猪肉中氯霉素、磺胺甲嘧啶、磺胺二甲嘧啶、磺胺噻唑、甲氧苄啶和磺胺嘧啶药物残留的检测。
[1]文利侠,李舒强. 动物源性食品安全问题与对策[J]. 畜牧兽医杂志,2013,32(1):69-71.
[2]王娟. 控制兽药残留-保障食品安全[J]. 中国兽药杂志,2011,45(8):43-45.
[3]国家质量监督检验检疫总局. GB/T 21316-2007动物源性食品中磺胺类药物残留量的测定液相色谱一质谱/质谱法[S].北京:中国标准出版社,2007.
[4]国家质量监督检验检疫总局. SN 0208-1993出口肉中十种磺胺残留量检验方法[S].北京:中国标准出版社,1993.
[5]国家质量监督检验检疫总局. GB/T 20756-2006可食性动物肌肉、肝脏和水产品中氯霉素、甲砜霉素和氟苯尼考残留餐的测定液相色谱-串联质谱法[S]. 北京:中国标准出版社,2006.
[6]国家质量监督检验检疫总局. SN 0208-1993出口肉中十种磺胺残留量检验方法[S].北京:中国标准出版社,1993.
[7]国家质量监督检验检疫总局. SN 0341—1995 出口肉及肉制品中氯霉素残留量检验方法[S]. 北京:中国标准出版社,1995.
[8]孙雷,张骊,等. 超高效液相色谱-串联质谱法检测动物源
食品中氯霉素类药物及其代谢物残留[J]. 中国兽药杂志,2009,43(3):42-45.
[9]刘吉成. HPLC-MS/MS测定猪肉和猪肝中氯霉素残留量的研究[J]. 食品与机械,2012,28(4):93-95.
[10]黄华,陈君慧,冯楠,等. 动物源性食品中磺胺类药物残留前处理和检测方法研究进展[J]. 食品工业科技,2013(4):378-381.
[11]孙伟红,冷凯良,王志杰,等. HPLC-MS/MS内标法同时测定水产品中18种磺胺类药物残留量[J]. 食品科学,2009,30(24):294-298.
[12]张素霞,李俊锁,钱传范.猪肌肉组织中磺胺类药物的MSPD净化和HPLC测定[J].畜牧兽医学报,1999,30(6):531-535.
[13]奉夏平,张亮,张卓恒,等.MSPD/PVT-GC-MS 测定动物源食品中氯霉素[J].中山大学学报:自然科学版,2005,44(2):65-68.
[14]A Kaufmann,P Butcher,K Maden,et a1.Quantitative multiresidue method for about 100 veterinary drugs in different meat matrices by sub 2-microm particulate high-performance liquid chromatography coupled to time of flight mass spectrometry[J].J Chromatoqr A,2008,1194(1):66-79.
[15]D Ortelli,E Cognard,P Jan,et a1.Comprehensive fast multiresidue screening of 150 veterinary drugs in milk by ultra-performance liquid chromatography coupled to time of flight mass spectrometry.[J]. J Chromatogr B Analyt Technol Biomed Life Sci,2009,877:2363-2374.
[16]R J Pete,Y J Bolck,P Rutgers,et a1.Multi-residue screening of veterinary drugs in egg,fish and meat using high-resolution liquid chromatography accurate mass time of flight mass spectrometry[J].J Chromatogr A,2009,1216(46):8206-8216.
[17]Yamada R,Kozono M,Ohmori T,et a1.Simuhaneous determination of residual veterinary drugs in bovine,porcine,and chicken muscle using liquid chromatography coupled with electrospray ionization tandem mass spectrometry[J]. Biosci Biotechnol Biochem,2006,70(1):54-65.
[18]C Chiaochan,U Koesukwiwat,S Yudthavorasit,et a1.Efficient hydrophilic interaction liquid chromatography-tandem mass spectrometry for the multiclass analysis of veterinary drugs in chicken muscle[J].Anal Chimica Acta,2010,682(1-2):117-129.
