稀土Eu3+荧光探针法测定饮用水中那氟沙星的含量
2018-01-19,,,
, , ,
(内蒙古科技大学 化学与化工学院, 包头 014010)
水环境中的抗生素有两个主要的来源途径:医用和农用抗生素[1]。喹诺酮类抗生素主要用于医用,病人排泄物中的抗生素和医药企业制药过程中流失的抗生素会经过不同的途径对水体造成污染。目前测定水体中抗生素含量的方法有高效液相色谱法、高效液相色谱-质谱法[2]。这些方法虽然能够有效地测定水中抗生素的含量,但操作复杂,仪器昂贵。而荧光光谱法具有检出限低、灵敏度高等特点,建立抗生素的荧光光谱检测方法非常有意义。
那氟沙星属于喹诺酮类抗生素,目前那氟沙星的测定方法包括高效液相色谱法、非水和酸碱滴定法[3-4],未见荧光光谱法测定其含量的报道。有关喹诺酮类药物与稀土络合物的光谱性质研究已有较多报道[5-8],未见那氟沙星与稀土荧光性质的报道。本工作经过体系的筛选,发现在表面活性剂十二烷基苯磺酸钠存在下那氟沙星与稀土铕形成配合物后可以激发出Eu3+的荧光,对其荧光特性进行了研究,建立了那氟沙星定量分析的方法,并且用于饮用水体中的那氟沙星含量的测定。
1 试验部分
1.1 仪器与试剂
Waters e2695型高效液相色谱仪,F 4500型荧光光谱仪,RY-TQ-LC型超声提取罐。
Eu3+溶液:2.0×10-3mol·L-1,称取六水合硝酸铕0.089 2 g,用水溶解并定容至100 mL。
那氟沙星(NDFX)溶液:4.0×10-3mol·L-1。
十二烷基苯磺酸钠(SDBS)溶液:1.8×10-2mol·L-1。
三羟甲基氨基甲烷(Tris)-盐酸(HCl)缓冲溶液:pH 7.5,称取Tris 1.211 4 g,加水溶解至100 mL,用6 mol·L-1HCl调节pH至7.5。
那氟沙星对照品纯度大于97%,十二烷基苯磺酸钠、三羟甲基氨基甲烷为光谱纯,六水合硝酸铕、盐酸、邻苯二甲酸氢钾、冰乙酸、碳酸钠、碳酸氢钠、氯化铵、氯化钾、硝酸铝、磷酸二氢钠、氯化钠为分析纯,乙腈、磷酸二氢铵、四氢呋喃为色谱纯。
1.2 仪器工作条件
那氟沙星的荧光激发波长和发射波长分别为288,458 nm,Eu3+的荧光激发波长为335 nm,发射波长为594,618 nm。光谱通带宽度均为5 nm,扫描速率为1 500 nm·min-1。
1.3 试验方法
将饮用水用超声浓缩仪浓缩5 000倍后,取2 mL,依次加入4.0×10-3mol·L-1NDFX溶液、2.0×10-3mol·L-1Eu3+溶液、1.8×10-2mol·L-1SDBS溶液、Tris-HCl缓冲溶液各2 mL,放置20 min后,在25 ℃下进行测定。
2 结果与讨论
2.1 体系的光谱性质
2.1.1 Eu3+与NDFX的特征光谱
不同溶液的荧光激发光谱和发射光谱见图1。

1,1′-NDFX;2,2″-Eu3+;3,3″-Eu3+-SDBS; 4,4′,4″-NDFX-Eu3+;5,5′,5″-NDFX-Eu3+-SDBS 1~5-激发光谱;1′,4′,5′-NDFX的发射光谱; 2″~5″-Eu3+的发射光谱 cNDFX=5.0×10-5mol·L-1;cEu3+=4.0×10-4mol·L-1; cSDBS=3.6×10-3mol·L-1;cTris-HCl=5.0×10-3mol·L-1,pH 7.5图1 体系的荧光光谱图Fig. 1 Fluorescence sprectra of the system
由图1可知:Eu3+单独存在和在SDBS中均不发射荧光,其实在文献报道中,Eu3+是有荧光性质的,只是不具备发射荧光的条件。那氟沙星单独存在时有荧光[2],其荧光激发波长和发射波长分别为288,458 nm。当Eu3+和那氟沙星在体系中共存时,那氟沙星的荧光和Eu3+的荧光均存在,Eu3+在波长为594,618 nm处存在特征荧光峰,分别对应于铕的5D0-7F1和5D0-7F2跃迁,从荧光激发光谱来看,那氟沙星的一个特征峰变为两个峰。当加入表面活性剂SDBS后荧光激发强度和发射强度都明显增大。
2.1.2 Eu3+和那氟沙星配合物的形成
对比图1中曲线1和曲线4可知,那氟沙星与Eu3+共存时体系的荧光激发光谱由那氟沙星单独存在时的一个特征峰变为两个特征峰,288 nm处的最大激发波长发生了红移,335 nm处的荧光峰应为Eu3+的荧光激发峰,说明了那氟沙星与Eu3+发生了相互作用。那氟沙星有羧基,其中氧原子具有空轨道,容易与稀土形成配合物,在稀土离子与药物的相互作用中都见报道[9-10]。试验通过连续等摩尔法确定两者形成配合物的比例。Eu3+与那氟沙星的总浓度保持不变,两者的物质的量之比发生变化,以激发波长为288 nm和发射波长为618 nm进行荧光的测定,结果见图2。
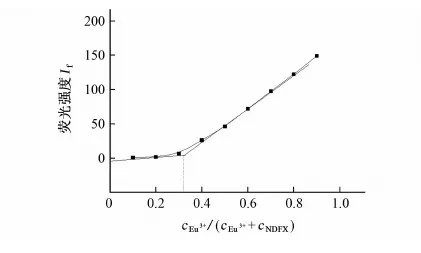
cEu3++cNDFX=1.0×10-3mol·L-1; cTris-HCI=5.0×10-3mol·L-1,pH 7.5图2 Eu3+-NDFX配合物的组成比对荧光强度的影响Fig. 2 Effect of the component ratio of Eu3+-NDFX coordination complex on the fluorescence intensity
由图2可知:随着cEu3+/(cEu3++cNDFX)增大,体系的荧光强度开始时变化不大,随后荧光强度急剧增大,在图中出现了一个转折点,该点所对应的cEu3+/(cEu3++cNDFX)为0.33。说明Eu3+和NDFX物质的量比为1∶2时,发生了配合作用导致荧光强度的增大,由此确定配合物中Eu3+与NDFX的物质的量之比为1∶2。
2.1.3 表面活性剂的选择
表面活性剂的浓度达到临界胶团浓度后,对配合物发射荧光的荧光强度有增敏作用,从而提高分析的灵敏度。那氟沙星有羧酸根离子与带正电的Eu3+以配位比2∶1形成配合物后带有一个正电荷。按照同种电荷相互排斥、异种电荷相互吸引的原理,该配合物应该增溶于带负电的表面活性剂形成的胶团中,所以选择两种常见的阴离子表面活性剂十二烷基硫酸钠(SDS)和SDBS作为增溶的表面活性剂。试验发现,由于SDS的临界胶团浓度(cmc)值较大,需要的添加量较大,可能会与没有参与形成配合物的Eu3+反应形成沉淀。而SDBS本身不易沉淀,表面活性剂的cmc值又小,在反应时没有沉淀的生成,在SDBS形成的胶团溶液中体系的荧光强度明显增强。如图1中曲线5所示,试验发现表面活性剂SDBS会使体系的荧光激发光谱和荧光发射光谱的荧光强度都有所增强,并且SDBS的浓度为3.6×10-3mol·L-1时体系的荧光强度最大。
2.2 那氟沙星的测定条件
2.2.1 浓度的影响
试验发现Eu3+浓度为4.0×10-4mol·L-1时,荧光强度最大,由于那氟沙星与Eu3+以2∶1比例存在,那氟沙星的浓度控制为8.0×10-4mol·L-1。
2.2.2 酸度的影响
固定Eu3+的浓度为4.0×10-4mol·L-1,那氟沙星的浓度为8.0×10-4mol·L-1,SDBS的浓度为3.6×10-3mol·L-1,用不同的缓冲溶液调节体系的酸度,使pH在2.2~10.2内变化,测定体系的荧光强度。结果发现:在pH为2.2~7.5时荧光强度逐渐增大;在pH=7.5时达到最大;当pH大于7.5时,荧光强度随pH的增大而减小。所以试验选择体系的最佳pH为7.5,所用缓冲溶液是Tris-HCl。Tris-HCl是一种有机的碱性缓冲溶液,其稳定性好,对体系干扰小,不与重金属离子发生沉淀反应,常用作化学及生物反应过程中的溶剂。
2.2.3 溶液加入顺序与反应时间的影响
固定Eu3+的浓度为4.0×10-4mol·L-1,那氟沙星的浓度为8.0×10-4mol·L-1,SDBS的浓度为3.6×10-3mol·L-1,pH为7.5,测定了NDFX、Eu3+、SDBS和Tris-HCl不同加入顺序对体系荧光强度的影响,当加入的4种物质的顺序为NDFX、Eu3+、SDBS和Tris-HCl时体系的荧光强度最大。
试验考察了体系的反应时间和温度的影响。25 ℃下,溶液配制好后即可产生荧光,但是当溶液放置20 min后反应完全,荧光强度会达到最大且稳定。试验分别测定了温度为20,25,30,35,40 ℃时体系的荧光强度,发现25 ℃和30 ℃时,荧光强度基本上保持最大且一致。所以试验中采用25 ℃作为反应温度。
2.3 干扰试验
在NDFX-Eu3+-SDBS体系处于最佳测定条件下,分别加入Na+、K+、NH4+、La3+、Ce3+、Cl-、SO42-、NO3-、葡萄糖和淀粉等干扰物质考察其对体系荧光强度的影响。结果发现:400倍的Na+、K+、NH4+、La3+、Ce3+、Cl-、SO42-、NO3-和100倍的葡萄糖和淀粉不干扰测定。添加1倍的喹诺酮药物巴洛沙星进行干扰试验,发现体系的荧光强度增大,造成测定结果13.3%的误差,说明其对那氟沙星的测定产生干扰,具体干扰程度需进一步研究证明。但作为饮用水中喹诺酮类药物的总量分析不产生影响。
2.4 标准曲线与检出限
以Eu3+的浓度为4.0×10-4mol·L-1、SDBS的浓度为3.6×10-3mol·L-1、pH 7.5的最佳测定条件下配制一系列那氟沙星呈浓度梯度变化的NDFX-Eu3+-SDBS溶液,静置20 min,测定溶液的荧光强度。以荧光强度(I)对那氟沙星的浓度(c)进行线性回归,得I=2.75c-3.89,相关系数为0.993 7,线性范围为2.0×10-5~1.0×10-4mol·L-1。以3s/k(s为空白溶液连续测定8次的相对标准偏差,k为标准曲线的斜率)计算得方法的检出限为4.0×10-6mol·L-1。
2.5 饮用水中那氟沙星的测定
将饮用水浓缩后,使用高效液相色谱仪进行那氟沙星的测定,对于质量浓度为1.0 mg·L-1那氟沙星对照品的保留时间为7.54 min,浓缩后的饮用水在7.54 min处不存在特征峰,说明此饮用水中不存在那氟沙星。
以浓缩后的饮用水为溶剂,向其中加入不同质量的那氟沙星对照品,配成一系列浓度的那氟沙星溶液,按试验方法进行分析检测,并进行精密度和回收试验,测定结果见表1。

表1 精密度和回收试验结果(n=5)Tab. 1 Results of tests for precision and recovery(n=5)
Eu3+-NDFX在SDBS溶液中能够形成配合物,可以将Eu3+在618 nm处的特征荧光峰激发出来,并且Eu3+的荧光强度与NDFX浓度间呈线性关系,由此可以对那氟沙星的含量进行测定,也可以用于饮用水中那氟沙星含量的测定。
[1] 闵敏,陆光华.水环境中的抗生素[J].化学与生物工程, 2013,30(11):19-22.
[2] 李艳艳,刘迎亚,范霄,等.引用水中抗生素残留检测方法的研究进展[J].化学通报, 2016,79(3):213-219.
[3] 张锦锋,马佳龙,吴沉.高效液相色谱法测定那氟沙星乳膏含量[J].中国药师, 2006,9(6):507-508.
[4] 王启帅,韩莹,程建新,等.那氟沙星含量测定方法研究[J].中国药业, 2007,16(23):29-30.
[5] 陈传燕.稀土-药物配合物荧光探针新体系的建立及其分析应用[D].济南:山东大学, 2009.
[6] 边江鱼,徐莉英.铕(Ⅲ)-培氟沙星-EDTA络合物的荧光特性及其应用[J].理化检验-化学分册, 2007,43(7):580-584.
[7] 王晓丽,孟双明,冯瑞琴,等.钇(Ⅲ)-莫西沙星配合物的荧光性质及分析应用[J].分析试验室, 2005,24(1):30-32.
[8] 童裳伦,项光宏,黄迪金,等.表面活性剂敏化的铽离子荧光探针对氧氟沙星的测定[J].分析化学, 2004,32(5):619-621.
[9] 褚志杰.巴洛沙星-稀土配合物荧光新体系的研究及应用[D].济南:山东大学, 2009.
[10] KUNKELY H, VOGLER A. Excited state behavior of tetrakis (2,2,6,6-tetramethyl-3,5-heptane-dionato) cerium (Ⅳ): Emission and photoredox reaction from ligand-to-metal charge transfer states[J]. J Photochemistry and Photobiology A: Chemistry, 2001,146(1/2):63-66.
