高效液相色谱法同时测定四季三黄丸中4种活性成分的含量
2018-01-19,,2,,,
, ,2, , ,
(1. 上海市计量测试技术研究院, 上海 201203; 2. 上海师范大学 生命与环境科学学院, 上海 200234)
四季三黄丸由大黄、黄柏、黄芩和栀子共4味药制成,临床上用于口鼻生疮、咽疼齿痛、口干舌燥、目眩头晕、大便秘结、小便赤黄等症状[1],其中大黄具有泻热毒、破积滞、行瘀血等功效,主要活性成分为大黄素、大黄酸、大黄酚等物质[2];黄柏具有清热、燥湿、泻火、解毒等功效,主要活性成分为小檗碱、巴马汀、黄柏碱等[3];黄芩具有清热泻火、燥湿解毒功效,主要活性成分为黄芩苷、黄芩素、汉黄芩素等[4];栀子清热、泻火、凉血,主要成分为栀子苷[5]。目前,四季三黄丸收载于为《卫生部药品标准》中药成方制剂第二册,该标准仅在检查项下规定了该药物应符合丸剂项下有关的各项规定,对其有效成分含量或质量控制方面并未做具体规定[1]。目前公开报道的四季三黄丸药物中有效成分的质量控制方法主要为薄层色谱法和液相色谱法[6-8],对其中一种成分(如大黄酚)或两种成分(如黄芩苷、盐酸小檗碱)进行定性或定量研究[9-16],但同时测定四季三黄丸中4种活性成分含量的方法尚未见报道。本工作以栀子苷、盐酸小檗碱、黄芩苷和大黄素等4种活性成分作为四季三黄片的质控指标,应用高效液相色谱法(HPLC)对这4种活性成分进行含量测定。
1 试验部分
1.1 仪器与试剂
Agilent 1100型高效液相色谱仪,配二极管阵列检测器(DAD);Mettler-Toledo MX 5型百万分之一电子分析天平;SK 8210LHC型超声波清洗器。
混合对照品储备溶液:称取栀子苷7.662 mg、盐酸小檗碱8.996 mg、黄芩苷3.871 mg、大黄素4.458 mg置于10 mL容量瓶中,用甲醇溶解并稀释至刻度,制成质量浓度分别为766.2,899.6,387.1,445.8 mg·L-1的栀子苷、盐酸小檗碱、黄芩苷和大黄素混合对照品溶液。
大黄素标准品(纯度不小于98%)、栀子苷标准品(纯度不小于98%)、黄芩苷标准品(纯度不小于98%),盐酸小檗碱纯度(按含C20H18ClNO4计) 86.7%;乙腈为色谱纯。
1.2 仪器工作条件
Phenomenex Luna C18色谱柱(250 mm×4.6 mm,5 μm);流动相A为乙腈,B为0.1%(体积分数,下同)甲酸溶液;流量为1.0 mL·min-1;进样量为5 μL。梯度洗脱程序:0~5 min时,A为15%;5~10 min时,A由15%升至21%;10~12 min时,A由21%升至30%;12~24 min时,A由30%升至32%;24~28 min时,A由32%升至55%;28~48 min时,A由55%升至80%。栀子苷、盐酸小檗碱、黄芩苷、大黄素的检测波长分别为240,345,278,287 nm。在此条件下栀子苷、小檗碱、黄芩苷、大黄素的保留时间分别为8.76,17.38,18.63,38.17 min。
1.3 试验方法
取四季三黄丸1袋,研磨至细粉,取细粉约0.1 g,精密称定后置具塞锥形瓶中,加入甲醇20 mL,称定质量,于40 ℃超声30 min取出,放冷,称质量,加甲醇补足减失质量,过滤,取续滤液作为样品溶液。根据四季三黄丸中药物处方比例及工艺,再按样品溶液的制备方法,分别配制栀子苷阴性对照溶液、盐酸小檗碱阴性对照溶液、黄芩苷阴性对照溶液和大黄素阴性对照溶液。
2 结果与讨论
2.1 色谱行为及专属性试验
取混合对照品溶液、样品溶液和4种阴性对照溶液,分别进样,记录色谱图(见图1~图4)。结果显示,样品中的辅料及其他成分均不干扰目标物的测定。
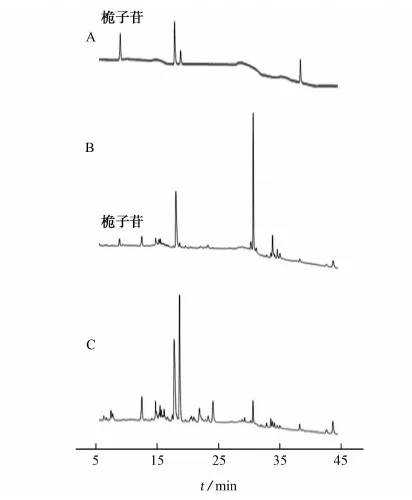
图1 混合对照品(A)、样品(B)和栀子苷阴性样品(C) 在240 nm处的色谱图Fig. 1 Chromatograms of the mixed reference substance (A), the sample (B) and the negative sample without geniposide (C) at 240 nm
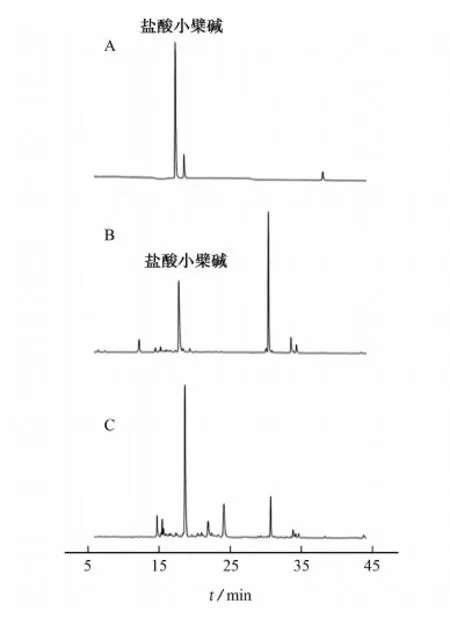
图2 混合对照品(A)、样品(B)和盐酸小檗碱阴性样品(C) 在345 nm处的色谱图Fig. 2 Chromatograms of the mixed reference substance (A), the sample (B) and the negative sample without berberine hydrochloride (C) at 345 nm

图3 混合对照品(A)、样品(B)和黄芩苷阴性样品(C) 在278 nm处的色谱图Fig. 3 Chromatograms of the mixed reference substance (A), the sample (B) and the negative sample without baicalin (C) at 278 nm
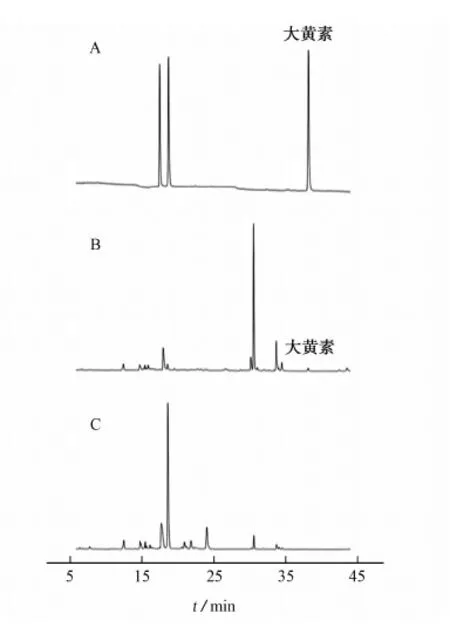
图4 混合对照品(A)、样品(B)和大黄素阴性样品(C) 在287 nm处的色谱图Fig. 4 Chromatograms of the mixed reference substance (A), the sample (B) and the negative sample without emodin (C) at 287 nm
2.2 色谱条件的选择
2.2.1 色谱柱
试验考察了Phenomenex Luna C18色谱柱(250 mm×4.6 mm,5 μm)和ZORBAX Rx-C18色谱柱(250 mm×4.6 mm,5 μm)的分离效果。结果发现,在相同的流动相条件下前者的分离效果较好。因此,试验选择Phenomenex Luna C18色谱柱作为分离色谱柱。
2.2.2 流动相
根据待测成分的理化特征和色谱行为,试验考察了甲醇-水、甲醇-0.1%甲酸溶液、乙腈-水、乙腈-0.1%甲酸溶液等流动相体系,结果发现乙腈-0.1%甲酸溶液梯度洗脱待测成分时,盐酸小檗碱和黄芩苷分离度较好,基线较低,因此试验选择乙腈-0.1%甲酸溶液作为流动相。
2.2.3 检测波长
采用DAD进行全波长扫描(190~400 nm),分析4种活性成分的紫外吸收光谱,得到这4种化合物的最大吸收波长,最终确定栀子苷、盐酸小檗碱、黄芩苷、大黄素的检测波长分别为240,345,278,287 nm。在样品检测过程中,同时记录4个波长的色谱图。
2.3 提取溶剂的选择
先后采用加热回流法、索氏提取法、超声提取法对四季三黄丸中栀子苷、盐酸小檗碱、黄芩苷和大黄素等4种化合物进行提取,结果发现超声提取效率高且操作简便;提取溶剂考察了甲醇(3+7)溶液、甲醇(1+1)溶液、甲醇、乙醇,结果表明甲醇的综合提取效率最高。
2.4 标准曲线与检出限
分别移取混合对照品储备溶液0.10,0.20,0.30,0.60,0.80,1.00 mL置于10 mL容量瓶中,用甲醇稀释至刻度,制成系列质量浓度的溶液,在仪器工作条件下进行测定,记录峰面积。以质量浓度为横坐标,峰面积为纵坐标进行线性回归,线性参数见表1。
以3倍信噪比计算检出限,结果见表1。
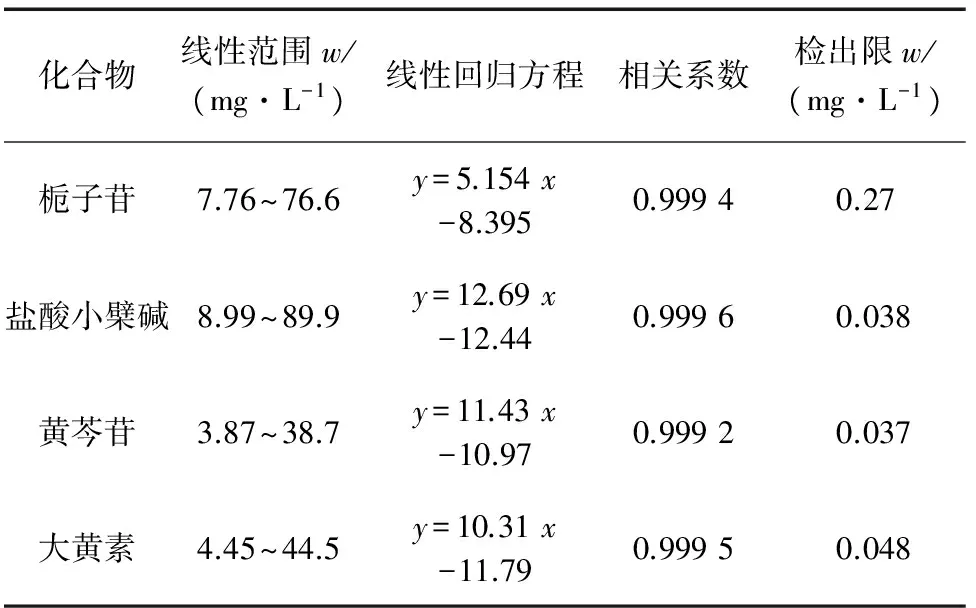
表1 线性参数与检出限Tab. 1 Linearity parameters and detection limits
2.5 重复性和稳定性试验
取同一批四季三黄丸6份,按试验方法制备进行平行测定,记录待测成分的峰面积,计算出栀子苷、盐酸小檗碱、黄芩苷、大黄素峰面积的相对标准偏差(RSD)分别为1.9%,2.6%,3.1%,1.4%,表明方法的重复性良好。
取同一样品溶液每隔2小时进样1次,连续进样6次,记录待测成分的峰面积,计算得栀子苷、盐酸小檗碱、黄芩苷、大黄素峰面积的RSD分别为3.3%,4.9%,4.6%,4.4%,表明样品溶液的稳定性良好。
2.6 精密度与回收试验
取已知含量的同一批样品,各加入栀子苷、盐酸小檗碱、黄芩苷、大黄素对照品适量,制备高、中、低等3种浓度水平的加标样品,按试验方法测定4种成分的含量,平行测定6次,计算回收率和RSD,结果见表2。
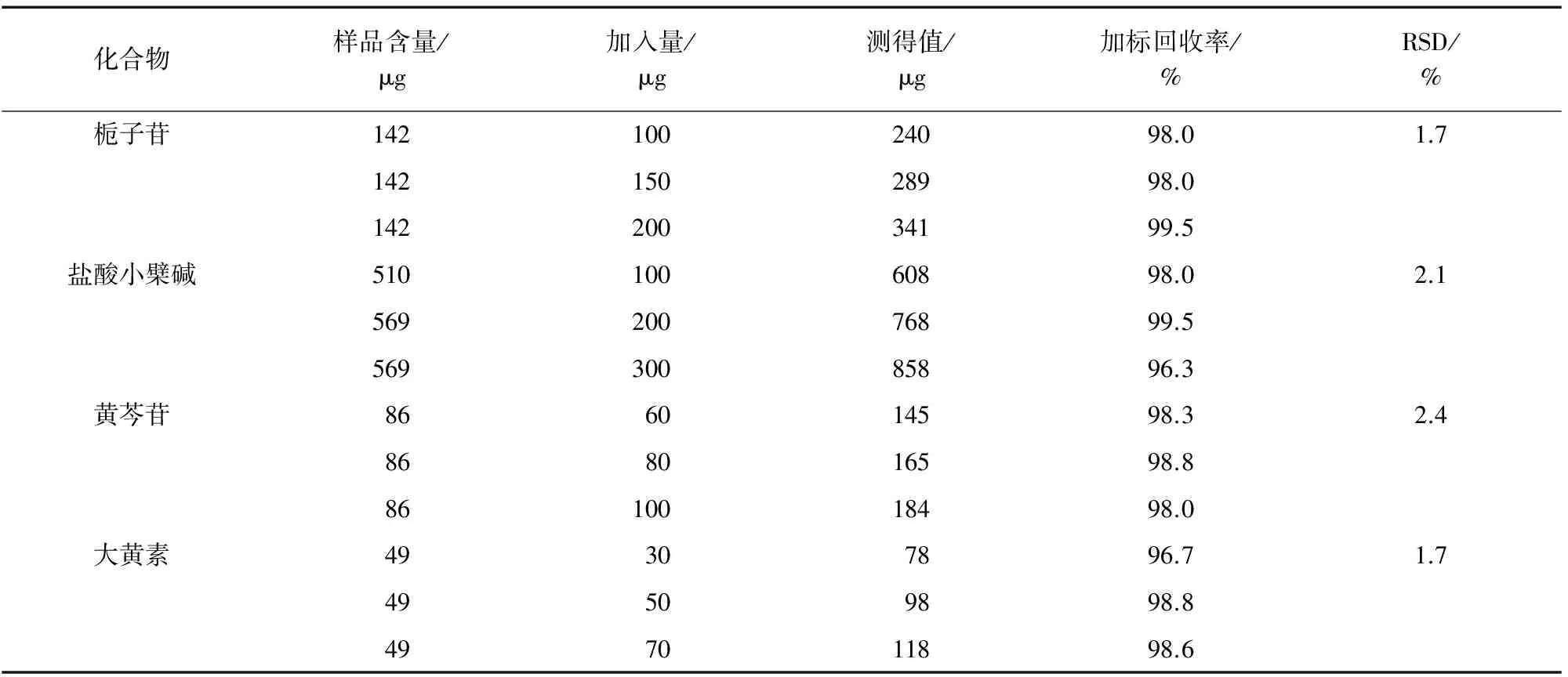
表2 精密度与回收试验结果(n=6)Tab. 2 Results of tests for precision and recovery(n=6)
2.7 样品分析
取3批四季三黄丸样品,按试验方法制备样品溶液,在仪器工作条件下进样测定,四季三黄丸中栀子苷、盐酸小檗碱、黄芩苷和大黄素含量的测定结果见表3。
本工作采用高效液相色谱法测定四季三黄丸中4种活性成分,在同一色谱条件下同时测定栀子苷、盐酸小檗碱、黄芩苷和大黄素的含量。该方法与传统方法相比,可以更加全面地评价四季三黄丸的质量。该方法简单、快速,并具有较高的准确度和精密度,可以满足检测工作的需要。
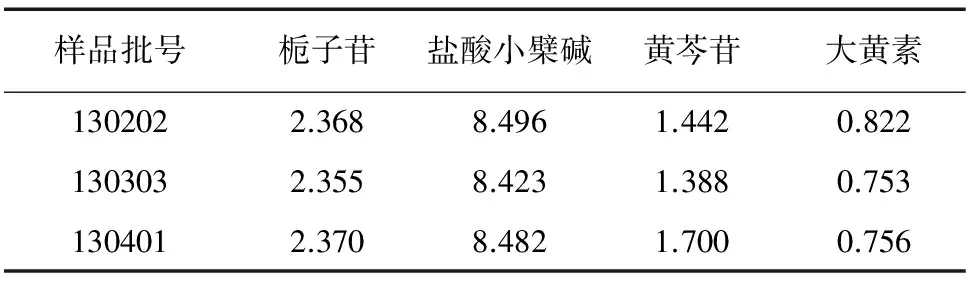
表3 样品中4种活性成分含量的测定结果Tab. 3 Determination results of the 4 effective components in samples mg·kg-1
[1] 中华人民共和国卫生部药典委员会.中华人民共和国卫生部药品标准.第二册,中药成方制剂[M].北京:中华人民共和国卫生部药典委员会, 1989:76.
[2] 黄娟,张庆莲,皮凤娟,等.大黄的药理作用研究进展[J].中国医院用药评价与分析, 2014,14(3):282-284.
[3] 张博,张婷,王树春.黄柏的化学成分、质量分析方法及药理作用研究[J].现代医药卫生, 2013,29(10):1505-1507.
[4] 王艳春,张忠艳,姜小卓.中药黄芩的药理及应用[J].中外医疗, 2009,28(13):158-158.
[5] 谢学建,张俊慧.中药栀子研究进展[J].时珍国医国药, 2000,11(10):943-945.
[6] 宋文焕.四季三黄片和四季三黄丸薄层色谱分析[J].中国中药杂志, 2002,76(9):713-713.
[7] 应文婷,许润娟,刘金友.四季三黄丸质量标准研究[J].中医药导报, 2005,11(7):81-83.
[8] 梁慧敏,陈贤天.HPLC法测定四季三黄丸中黄芩苷和盐酸小檗碱的含量[J].首都医药, 2009,15(2):54-54.
[9] 张玉祥,王希,袁旭江.高效液相色谱法测定四季三黄软胶囊中盐酸小檗碱的含量[J].中国药业, 2006,15(16):21-22.
[10] 吴继周,王燕,韩海霞.HPLC法测定四季三黄片中黄芩苷的含量[J].新疆医科大学学报, 2014,37(6):715-716.
[11] 吉曙光,闫花丽,黄安军.反相高效液相色谱法测定四季三黄软胶囊中栀子苷的含量[J].中国药事, 2004,18(9):561-562.
[12] 刘啸凡,黄诗远,黎强,等.RP-HPLC同时测定四季三黄软胶囊中黄芩苷和盐酸小檗碱的含量[J].中国药师, 2008,11(4):420-421.
[13] 王溶溶,陈丹菲,黄建瑜.四季三黄胶囊的剂型研究Ⅰ──与四季三黄丸溶出度的比较[J].中成药, 1995(4):1-3.
[14] 李轶.RP-HPLC法测定四季三黄软胶囊中黄芩苷的含量[J].西北药学杂志, 2005,20(4):152-153.
[15] 苏艳华,许萍.HPLC法测定四季三黄软胶囊中大黄素的含量[J].天津药学, 2000,12(3):62-63.
[16] 赵敏,冯鑫.薄层扫描法测定四季三黄胶囊中大黄素含量[J].安徽中医药大学学报, 2000,19(4):53-53.
