VerifyNow-P2Y12系统评价氯吡格雷抵抗性对急性心肌梗死患者主要心血管事件影响的初步探索△
2018-01-06吴樱冉鹏郭晓升谭虹张莹黎励文
吴樱,冉鹏,郭晓升,谭虹,张莹,黎励文
[广东省心血管病研究所心内科广东省人民医院(广东省医学科学院),广州510080]
VerifyNow-P2Y12系统评价氯吡格雷抵抗性对急性心肌梗死患者主要心血管事件影响的初步探索△
吴樱,冉鹏,郭晓升,谭虹,张莹,黎励文
[广东省心血管病研究所心内科广东省人民医院(广东省医学科学院),广州510080]
目的初步探索氯吡格雷抵抗性与急性心肌梗死(acute myocardial infarction,AMI)患者经皮冠状动脉介入(percutaneous coronary intervention,PCI)治疗或经皮腔内冠状动脉成形术(percutaneous transluminal coronary angioplasty,PTCA)后主要心血管事件(major adverse cardiovasular events,MACEs)发生率的关系。方法前瞻、连续入组2015年5月至2015年8月在广东省人民医院行PCI治疗或PTCA的AMI患者89例。MACEs定义为心源性死亡、非致死性心肌梗死、脑卒中、血运重建、急性心力衰竭。通过VerifyNow-P2Y12系统检测血小板功能,根据血小板反应单位(platelet reaction unit,PRU)(P2Y12反应单位,代表血小板残余活性)分为两组:氯吡格雷反应正常组(PRU<208)35例和氯吡格雷抵抗组(PRU≥208)54例。收集患者临床和6个月随访的资料,及部分患者CYP2C19基因型的资料,比较两组基线资料和半年MACEs发生率。结果CYP2C19基因型检测提示中、快代谢型高达56.2%。正常组慢代谢型、中代谢型、快代谢型、未检测比例分比为3(5.5%)、13(24.1%)、19(35.2%)、19(35.2%),抵抗组为4(11.4%)、11(31.4%)、7(20.0%)、13(37.2%),两组比较差异无统计学意义(P>0.05)。与正常组比较,抵抗组MACEs发生率有增高趋势,但两组比较差异无统计学意义(18.2%vs.7.5%,P=0.173);抵抗组急性心力衰竭的发生率比正常组高,差异有统计学意义(12.1%vs.0,P=0.019);两组心源性死亡、非致死性心肌梗死、卒中、血运重建发生率比较,差异无统计学意义(P>0.05)。结论PCI治疗或PTCA术后双联抗血小板治疗的AMI患者较高比例CYP2C19基因型为中、快代谢型;氯吡格雷抵抗患者的MACEs发生有增加趋势。
心肌梗死;VerifyNow-P2Y12系统;氯吡格雷;血管成形术,经腔,经皮冠状动脉
介入治疗是冠状动脉粥样硬化性心脏病(冠心病)的重要治疗方式,对于冠状动脉植入支架的患者,指南推荐双联抗血小板治疗,即阿司匹林联合P2Y12拮抗剂[1];即便如此,仍有6.8%~12.1%患者发生缺血事件甚至死亡[2-4]。不同个体均采用相同的抗血小板治疗策略值得商榷,VerifyNow是新近发展的评估血小板功能的技术,国外报道:根据VerifyNow评估的血小板功能可预测缺血、出血事件,甚至可能根据血小板功能调整抗血小板治疗策略[5-7]。目前,国内有关VerifyNow的报道较少,尤其对于急性心肌梗死(acute myocardial infarction,AMI)患者。因此,本研究初步探索使用VerifyNow-P2Y12系统检测血小板功能与临床预后的关系。
1 资料和方法
1.1 一般资料
本研究为前瞻性观察研究,入选2015年5月至2015年8月在广东省人民医院行经皮冠状动脉介入(percutaneous coronary intervention,PCI)治疗或经皮腔内冠状动脉成形术(percutaneous transluminal coronary angioplasty,PTCA)的AMI患者。患者均符合全球第3版AMI[8]的诊断标准。入选标准:(1)AMI患者;(2)年龄18~80岁;(3)必须签署经伦理委员会批准的知情同意书。排除标准:(1)估算肾小球滤过率<15 mL/min或终末期肾功能衰竭;(2)氯吡格雷禁忌证;(3)口服抗凝药物治疗;(4)血小板计数<70×109;(5)既往3个月内冠状动脉旁路移植手术;(6)心源性休克、心肺复苏术或心脏骤停;(7)预计生存寿命<1年;(8)多脏器功能衰竭的患者。
1.2 方法
在介入治疗后(包括PCI治疗及PTCA)使用VerifyNow-P2Y12检验二磷酸腺苷(ADP)受体拮抗剂对于血小板活性的抑制作用。标本的留取和检测时间:(1)PCI治疗中未使用糖蛋白IIb/IIIa受体拮抗剂,术后8~12 h留取血标本;(2)PCI治疗中使用糖蛋白Ⅱb/Ⅲa受体拮抗剂,术后48~72 h留取血标本。取得血标本4 h内行血小板反应性检测。血小板反应性通过VerifyNow抗血小板治疗检测系统(Accumetrics公司,美国)进行检测。本研究使用的试剂盒为P2Y12试剂盒,通过全血标本的透光聚集度检测。该原理为将纤维蛋白原包裹的聚苯乙烯微粒混入全血中,二磷酸腺苷激活血小板,通过检测全血标本的透光聚集度来反映血小板的功能,以血小板反应单位(platelet reaction unit,PRU)(血小板残余活性)表示血小板功能,反映氯吡格雷拮抗血小板的情况。根据血运重建指南[1]的要求:术前给予阿司匹林300 mg嚼服,氯吡格雷300 mg顿服;术中均应用普通肝素;根据患者临床及冠状动脉介入治疗的情况,由介入治疗医生及临床医生自由决定使用抗血小板药物、β受体阻断药、血管紧张素转移酶抑制剂(ACEIs)/血管紧张素Ⅱ受体拮抗剂(ARBs)、利尿剂、硝酸酯类、他汀类药物、糖蛋白Ⅱb/Ⅲa受体拮抗剂、血管活性药物及主动脉内球囊反搏(intra aortic balloon pump,IABP)等。
1.3 临床定义
(1)PRU<208定义为氯吡格雷反应正常组,PRU≥208定义为氯吡格雷反应抵抗组[7]。(2)根据简化肾脏病膳食改良试验(MDRD)公式估测肾小球滤过率(estimated glomerular filtration rate,eGFR)[mL/(min·1.73 m2)]=186×血肌酐(mg/dL)-1.154×年龄-0.203×(0.742女性)。(3)主要心血管事件(major adverse cardiovasular events,MACEs)定义为心源性死亡、非致死性心肌梗死、脑卒中、血运重建、急性心力衰竭。
1.4 随 访
通过电话或门诊完成随访,随访时间为术后6个月±1周。电话随访,询问患者健康情况,询问服用药物情况。如果患者已经死亡,若患者家属明确具体死亡原因,予记录;若患者家属不能明确死亡原因,详细询问死亡时症状体征,死亡原因由两位副高职称以上医师判定。
1.5 统计学分析
数据统计使用SPSS软件(19.0版)。计量资料用()表示,当变量满足正态分布时,采用独立样本t检验进行两组间的比较,否则使用t′检验。计数资料用[n(%)]表示,率的比较根据实际情况使用卡方检验或者精确概率法。以P<0.05为差异有统计学意义。
2 结果
2.1 患者总体基线临床资料
本研究共入选89例患者(其中12例女性,77例男性)。患者年龄(61±12)岁,eGFR为(80.99±23.66)mL(/min·1.73 m2)。76.4%(68例)为急性ST段抬高型心肌梗死,23.6%(21例)为急性非ST段抬高型心肌梗死。51.7%(46例)的患者存在活动吸烟史,48.3%(43例)并发原发性高血压(高血压),27.0%(24例)并发糖尿病,36.0%(32例)并发高脂血症。2.2%(2例)存在既往心肌梗死病史。CYP2C19基因型检测提示中、快代谢型高达56.2%。整体6个月病死率为2.2%(2例)。
2.2 两组基线资料比较
入选患者按PRU值分为两组:氯吡格雷反应正常组、抵抗组。与正常组比较,抵抗组的女性、Killip心功能≥Ⅱ级患者比例更高,年龄更大、病变的血管数更多、血红蛋白浓度更低,靶血管为前降支患者比例更低,危险因素如高血压、糖尿病、高脂血症、活动吸烟,既往病史如心肌梗死、PCI治疗、冠状动脉旁路移植病史,生化指标如肾功能(包括eGFR、血肌酐)、肌酸激酶同工酶峰值、基因检测,介入治疗方面如靶血管、植入支架数目比较,差异均无统计学意义(P>0.05),详见表1。其中,患者的CYP2C19基因型,将未检测部分统计在内,抵抗组、正常组快代谢型的比例分别达20%、35.2%,中代谢型达31.4%,24.1%。
2.3 两组半年的主要心血管事件发生率比较
两组间半年的MACEs发生率比较,差异无统计学意义(7.5%vs.18.2%,P=0.173);其中两组心源性死亡、再发非致死性心肌梗死、卒中、血运重建发生率比较,差异无统计学意义(P>0.05);抵抗组急性心力衰竭发生率显著高于正常组,差异有统计学意义(0vs.12.1%,P=0.019),详见表2。
3 讨论
本研究主要通过VerifyNow-P2Y12系统检测氯吡格雷抵抗性对临床预后的影响。近年来,VerifyNow检测血小板功能的临床价值逐步得到学界的认可。Malinin等[9]通过对VerifyNow-P2Y12检测方法的特异性、精密度、干扰因素等多方面进行验证,研究结果提示VerifyNow-P2Y12检测方法可靠、敏感。
Marcucci[6]、Price[7]及 Patti[10]分别进行的研究证实,PCI治疗后VerifyNow-P2Y12检测的PRU增高,即血小板抵抗性增高,MACEs风险增高。2011年GRAVITAS研究[7]提示:PRU<208与PCI治疗后60 d、6个月的研究主要终点(包括死亡、心肌梗死和脑卒中)低风险相关;校正其他危险因素,仍然是PCI治疗后60 d主要终点低风险的独立危险因素,与术后6个月低风险保持相关性倾向。但GRAVITAS研究未纳入急性ST段抬高型心肌梗死等人群。本项探索性研究主要针对AMI患者。抵抗组与正常组MACEs的发生率比较,差异无统计学意义(18.2%vs.7.5%,P=0.173),但有增加的趋势,可能与样本量小(n=89)、随访时间周期较短相关;同时,抵抗组急性心力衰竭的发生率比正常组显著增高,差异有统计学意义(12.1%vs.0,P=0.019),可能与氯吡格雷抵抗及其引起的心肌缺血相关。因此,推测VerifyNow提示的氯吡格雷抵抗与MACEs的发生有增加趋势,需延长随访时间和增加样本量进一步明确在AMI人群中的应用。
AMI及血运重建指南均推荐AMI或PCI治疗后患者需双联抗血小板治疗,即阿司匹林联合P2Y12拮抗剂,新型口服P2Y12拮抗剂如替格瑞洛、普拉格雷推荐等级高于氯吡格雷。目前,国内冠状动脉粥样硬化心脏病(冠心病)包括AMI的治疗趋于规范,双联抗血小板治疗已经普遍应用;但限于条件,P2Y12拮抗剂仍以氯吡格雷为主,与国外情况不一致。本研究提示39.3%的AMI患者合并氯吡格雷抵抗,与新近国内研究的数据大致相当[11-12],该数据对于个体化的抗血小板治疗策略有重要的提示意义,不同患者尤其是合并氯吡格雷抵抗者均采用相同的抗血小板治疗策略值得商榷,国外研究者已对氯吡格雷抵抗者采用个体化的抗血小板治疗进行尝试[7],但治疗效果仍无定论。对于氯吡格雷抵抗患者,常规剂量氯吡格雷可能效果不佳,增加氯吡格雷剂量、新型口服P2Y12拮抗剂成为可能选择[13]。然而,2011年GRAVITAS研究提示增加氯吡格雷的剂量并未减少氯吡格雷抵抗患者心血管事件的发生[7];PLATO研究显示替格瑞洛疗效优于氯吡格雷[3],可能与改善血小板抵抗有关;国内研究提示对于氯吡格雷抵抗者改用替格瑞洛或普拉格雷等新型口服P2Y12受体拮抗剂,在短期内即可有效抑制血小板聚集[14],两方面的研究资料提示,改用新型的P2Y12受体拮抗剂可能成为另一种潜在的选择[13]。
表1 两组基线资料比较 [±s,n(%),M(P25~P75)]
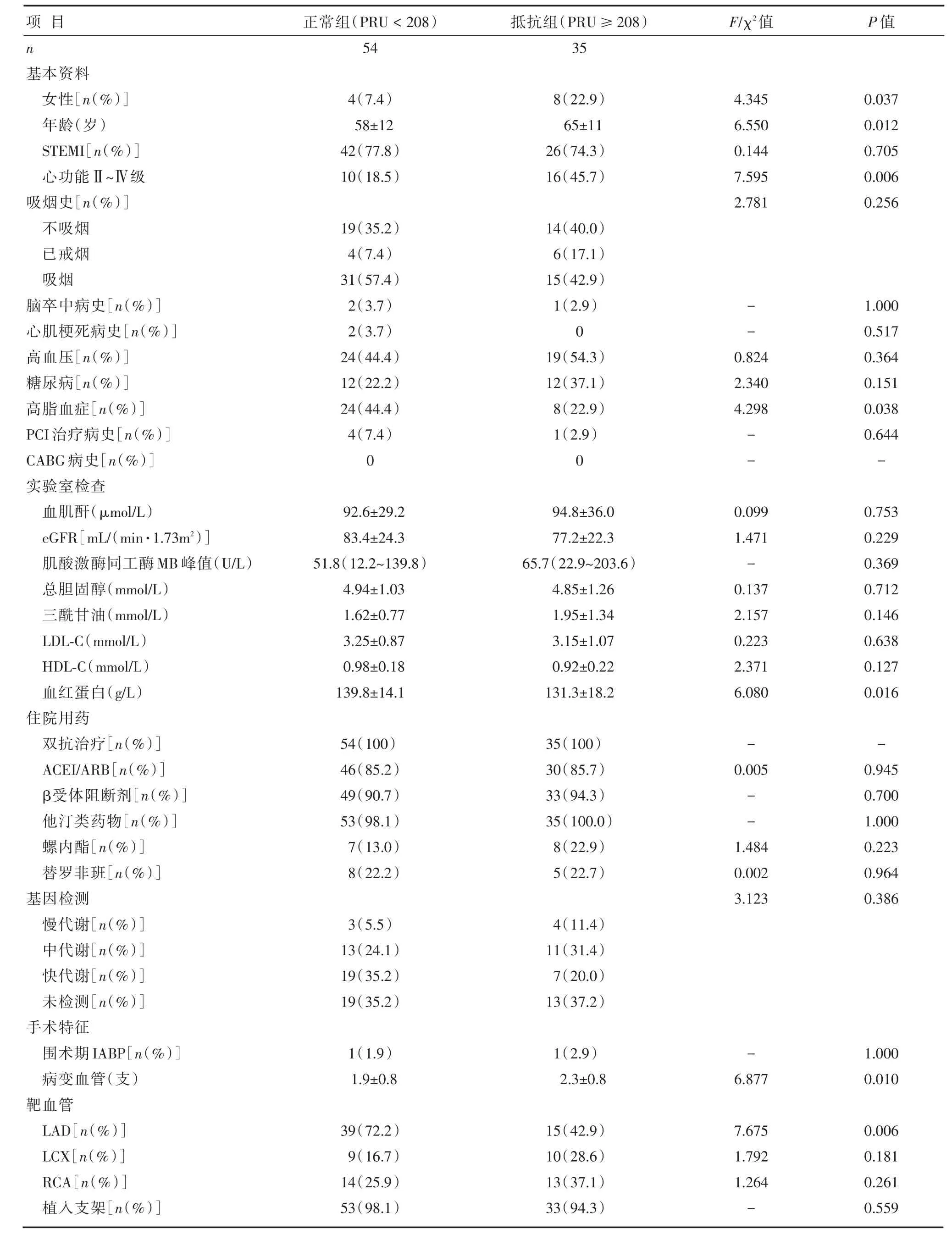
表1 两组基线资料比较 [±s,n(%),M(P25~P75)]
注:CABG为冠状动脉旁路移植术;LDL-C为低密度脂蛋白胆固醇;HDL-C为高密度脂蛋白胆固醇;ACEI为血管紧张素转化酶抑制剂;ARB为血管紧张素Ⅱ受体拮抗剂;LAD为冠状动脉左前降支;LCX为冠状动脉左回旋支;RCA为右冠状动脉
项 目 正常组(PRU<208) 抵抗组(PRU≥208)F/χ2值P值n基本资料女性[n(%)]年龄(岁)STEMI[n(%)]心功能Ⅱ~Ⅳ级吸烟史[n(%)]不吸烟已戒烟吸烟脑卒中病史[n(%)]心肌梗死病史[n(%)]高血压[n(%)]糖尿病[n(%)]高脂血症[n(%)]PCI治疗病史[n(%)]CABG病史[n(%)]实验室检查血肌酐(μmol/L)eGFR[mL/(min·1.73m2)]肌酸激酶同工酶MB峰值(U/L)总胆固醇(mmol/L)三酰甘油(mmol/L)LDL-C(mmol/L)HDL-C(mmol/L)血红蛋白(g/L)住院用药双抗治疗[n(%)]ACEI/ARB[n(%)]β受体阻断剂[n(%)]他汀类药物[n(%)]螺内酯[n(%)]替罗非班[n(%)]基因检测慢代谢[n(%)]中代谢[n(%)]快代谢[n(%)]未检测[n(%)]手术特征围术期IABP[n(%)]病变血管(支)靶血管LAD[n(%)]LCX[n(%)]RCA[n(%)]植入支架[n(%)]5435 4(7.4)58±12 42(77.8)10(18.5)8(22.9)65±11 26(74.3)16(45.7)4.345 6.550 0.144 7.595 2.781 0.037 0.012 0.705 0.006 0.256 19(35.2)4(7.4)31(57.4)2(3.7)2(3.7)24(44.4)12(22.2)24(44.4)4(7.4)0 14(40.0)6(17.1)15(42.9)1(2.9)0 19(54.3)12(37.1)8(22.9)1(2.9)0--0.824 2.340 4.298--1.000 0.517 0.364 0.151 0.038 0.644-92.6±29.2 83.4±24.3 51.8(12.2~139.8)4.94±1.03 1.62±0.77 3.25±0.87 0.98±0.18 139.8±14.1 94.8±36.0 77.2±22.3 65.7(22.9~203.6)4.85±1.26 1.95±1.34 3.15±1.07 0.92±0.22 131.3±18.2 0.099 1.471-0.137 2.157 0.223 2.371 6.080 0.753 0.229 0.369 0.712 0.146 0.638 0.127 0.016 54(100)46(85.2)49(90.7)53(98.1)7(13.0)8(22.2)35(100)30(85.7)33(94.3)35(100.0)8(22.9)5(22.7)--0.005--1.484 0.002 3.123 0.945 0.700 1.000 0.223 0.964 0.386 3(5.5)13(24.1)19(35.2)19(35.2)4(11.4)11(31.4)7(20.0)13(37.2)1(1.9)1.9±0.8 1(2.9)2.3±0.8-6.877 1.000 0.010 39(72.2)9(16.7)14(25.9)53(98.1)15(42.9)10(28.6)13(37.1)33(94.3)7.675 1.792 1.264-0.006 0.181 0.261 0.559
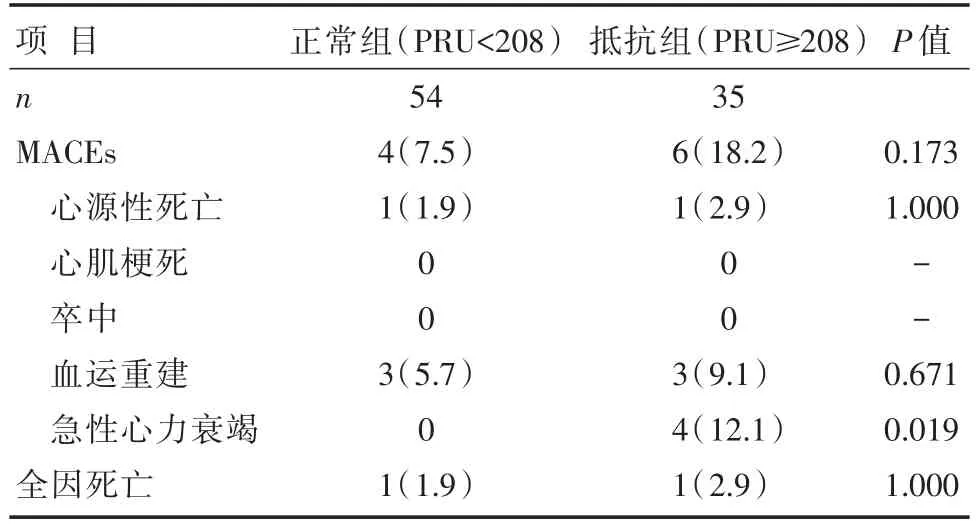
表2 两组间半年的MACEs发生率比较 [n(%)]
本研究同时检测了部分患者的CYP2C19基因型,将未检测患者统计在内,抵抗组、正常组患者的快代谢型比例分别达20%、35.2%,中代谢型达31.4%,24.1%,与国内中小样本量的临床研究结果相近[15-17];上述数据提示至少高达半数的AMI患者存在氯吡格雷抵抗的基础。通过Verify-P2Y12系统对于血小板功能学的检测可进一步筛选出氯吡格雷抵抗患者。新近,国内付东亮等[17]研究报告CYP2C19基因型与血栓弹力图检测的氯吡格雷血小板抑制率之间无明显相关性。目前,欧美和我国的指南均未推荐常规检测血小板功能及CYP2C19基因型,但对于高血栓风险患者例外,为不同患者是否需要检测血小板功能及CYP2C19基因型提供了方向,仍需要进一步研究。本研究中,无论基因型还是血小板功能均提示AMI患者合并氯吡格雷抵抗性的比例较高;此外,AMI是冠心病最严重的一种表现形式,可反复发作心血管缺血事件,临床预后不佳。因此,对于AMI人群,常规检测CYP2C19基因型和血小板功能可能对于氯吡格雷抵抗的早期识别有帮助,能否增加临床获益需进一步临床研究予以明确。
本研究存在的不足之处:(1)本研究为单中心、小样本、观察性研究,需要大样本、多中心的临床研究进一步明确Verify-P2Y12系统检测的氯吡格雷抵抗的发生率及对临床预后的影响;(2)只有部分研究人群检测了CYP2C19基因,同时样本量小,不能明确等位基因的比例,只能提供一定的参考。
[1]WINDECKER S,KOLH P,ALFONSO F,et al.2014 ESC/EACTS Guidelines on myocardial revascularization:The Task Force on Myocardial Revascularization of the European Society of Cardiology(ESC)and the European Association for Cardio-Thoracic Surgery(EACTS)Developed with the special contribution of the European Association of Percutaneous Cardiovascular Interventions(EAPCI)[J].Eur Heart J,2014,35(37):2541-2619.
[2]BHATT D L,FOX K A,HACKE W,et al.Clopidogrel and aspirin versus aspirin alone for the prevention of atherothrombotic events[J].N Engl J Med,2006,354(16):1706-1717.
[3]WALLENTIN L,BECKER R C,BUDAJ A,et al.Ticagrelor versus clopidogrel in patients with acute coronary syndromes[J].N Engl J Med,2009,361(11):1045-1057.
[4]WIVIOTT S D,BRAUNWALD E,MCCABE C H,et al.Prasugrel versus clopidogrel in patients with acute coronary syndromes[J].N Engl J Med,2007,357(20):2001-2015.
[5]MANGIACAPRA F,RICOTTINI E,BARBATO E,et al.Incremental value of platelet reactivity over a risk score of clinical and procedural variables in predicting bleeding after percutaneous coronary intervention via the femoral approach:development and validation of a new bleeding risk score[J].Circ Cardiovasc Interv,2015,8(5):e002106-e002106.
[6]MARCUCCI R,GORI A M,PANICCIA R,et al.Cardiovascular death and nonfatal myocardial infarction in acute coronary syndrome patients receiving coronary stenting are predicted by residual platelet reactivity to ADP detected by a point-of-care assay:a 12-month follow-up[J].Circulation,2009,119(2):237-242.
[7]PRICE M J,ANGIOLILLO D J,TEIRSTEIN P S,et al.Platelet reactivity and cardiovascular outcomes after percutaneous coronary intervention:a time-dependent analysis of the Gauging Responsiveness with a VerifyNow P2Y12 assay:Impact on Thrombosis and Safety(GRAVITAS) trial[J].Circulation,2011,124(10):1132-1137.
[8]TAYLOR J.Third universal definition of myocardial infarction[J].Eur Heart J,2012,33(20):2506-2507.
[9]MALININ A,POKOV A,SWAIM L,et al.Validation of a VerifyNow-P2Y12 cartridge for monitoring platelet inhibition with clopidogrel[J].MethodsFind Exp Clin Pharmacol,2006,28(5):315-322
[10] PATTI G,NUSCA A,MANGIACAPRA F,et al.Point-ofcare measurement of clopidogrel responsiveness predicts clinical outcome in patients undergoing percutaneous coronary intervention results of the ARMYDA-PRO(Antiplatelet therapy for Reduction of MYocardial Damage during Angioplasty-PlateletReactivity Predicts Outcome) study[J].J Am Coll Cardiol,2008,52(14):1128-1133.
[11]钟桃娟,柯于梵,萧湛潮,等.冠脉支架术后口服多种P2Y12受体拮抗剂发生抵抗的影响因素分析[J].中山大学学报(医学科学版),2015,36(5):704-709.
[12] 朱俊,梁岩,杨艳敏,等.应用VerifyNow-P2Y12系统评估氯吡格雷抗血小板效应及其影响因素分析[J].中国循环杂志,2014,29(z1):60-60.
[13]中华医学会心血管病学分会与中华心血管病杂志编辑委员会.抗血小板治疗中国专家共识[J].中华心血管病杂志,2013,41(3):183-194.
[14] 钟桃娟,刘品明,王景峰,等.新型P2Y12受体抑制剂对急性冠状动脉综合征介入治疗后患者血小板反应性的影响[J].中华心血管病杂志,2016,44(2):138-143.
[15] 吴龙梅,田新利,李俊峡,等.CYP2C19基因多态性与氯吡格雷低反应发生率的研究[J].中国循证心血管医学杂志,2015,7(4):458-460.
[16] 吴丹,杨胜利,路靖,等.冠心病患者支架术后根据检测药物代谢酶CYP2C19基因调整抗血小板治疗的价值[J].中国循环杂志,2015,30(3):216-219.
[17] 付东亮,刘晓飞,彭文华,等.冠心病介入治疗术后服用氯吡格雷患者的CYP2C19基因型与血小板抑制率的关系研究[J].中国心血管杂志,2015,20(6):434-437.
A pilot for effect of clopidogrel resistance detected by VerifyNow-P2Y12 on major adverse cardiovascular events in patients with acute myocardial infarction
WU Ying,RAN Peng,GUO Xiao-sheng,TAN Hong,ZHANG Ying,LI Li-wen
(Department of Cardiology,Guangdong Cardiovascular Institute,Guangdong General Hospital,Guangdong Academy of Medical Sciences,Guangzhou 510080,China)
Absctract:ObjectivesTo explore the relationship between major adverse cardiovasular events(MACEs)and clopidogrel resistance detected by VerifyNow-P2Y12 in patients with acute myocardial infarction(AMI).MethodsThe 89 patients with AMI and undergoing percutaneous coronary intervention(PCI)or percutaneous transluminal coronary angioplasty(PTCA)were continuously enrolled from May to August 2015 in Guangdong General Hospital,prospectively.MACEs was defined as cardiovascular death,non-fatal myocardial infarction,stroke,revascularization and acute heart failure.Platelet reaction unit(PRU)was detected by VerifyNow-P2Y12.Then patients were divided into normal group(PRU<208)[35(39.3%)patients]and resistant group(PRU≥208)[54(61.7%)patients].Baseline clinical and 6-month follow-up data were obtained,while the data of CYP2C19 gene was obtained in part of patients.Baseline,genetic data and 6-month MACEs were compared between the two groups.ResultsIncluding those not detected,it was detected that intermediate metabolizer and extensive metabolizer of CYP2C19 gene was 56.2%in study population.The proportion of extensive,intermediate,slow metabolizer and un-detected was 3(5.5%),13(24.1%),19(35.2%),19(35.2%)in normal group,while 4(11.4%),11(31.4%),7(20.0%),13(37.2%)in resistant group(P=0.386).Compared to normal group,there was a increasing trend in resistance group in incidence of MACEs(18.2%vs.7.5%,P=0.173).Besides,acute heart failure occurred in 4(4.5%)patients,including 4(12.1%)in resistance group,and 0 in normal group(P=0.019),respectively.There were no significant differences of incidences of cardiac death,nonfatal myocardial infarction,stroke,revascularization between the two groups(P>0.05).ConclusionsThe high proportion of AMI patients following PCI and dual-antiplatelet therapy carry extensive and intermediate metabolizer of CYP2C19 gene.Comparing to normal group,there is a increasing trend of incidence of MACEs in resistance group.
myocardial infarction;VerifyNow-P2Y12;clopidogrel;percutaneous coronary intervention
R542.2+2
A
1007-9688(2017)06-0653-05
10.3969/j.issn.1007-9688.2017.06.02
2015年广州市科技计划《急性冠脉综合征优化抗栓治疗策略》(项目编号:201510010256);广东省科技计划《老年急性冠脉综合征患者优化抗血小板策略研究》(项目编号:2014A020212552)。
吴樱(1978-),女,主治医师,研究方向为冠心病的诊治。
黎励文,E-mail:gdghllw@163.com
2017-09-22)
