手性金属-有机骨架[Cu3(HL)2(L)2(bpy)3]·4H2O用于高效液相色谱拆分手性化合物
2017-12-27付仕国袁宝燕谢生明袁黎明
李 丽,付仕国,袁宝燕,谢生明,袁黎明
(云南师范大学 化学化工学院,云南 昆明 650500)
手性金属-有机骨架[Cu3(HL)2(L)2(bpy)3]·4H2O用于高效液相色谱拆分手性化合物
李 丽,付仕国,袁宝燕,谢生明*,袁黎明*
(云南师范大学 化学化工学院,云南 昆明 650500)
手性金属-有机骨架材料(MOFs)作为一种新型多孔材料,由于具有比表面积大、结构多样、孔尺寸可调和化学稳定性良好等特点,而备受色谱分离领域的关注。该文以(1R,2R)-1,2-环己烷二甲酸(H2L)和4,4′-联吡啶(bpy)为配体与铜离子反应,通过溶剂热法合成了一种具有二维手性网状结构的手性MOF [Cu3(HL)2(L)2(bpy)3]·4H2O。将该手性MOF作为手性固定相制备了高效液相色谱柱。为了考察MOF [Cu3(HL)2(L)2(bpy)3]·4H2O的手性识别能力,在正相色谱(流动相:正己烷-异丙醇)条件下,对一系列外消旋化合物在手性MOF柱上进行了拆分。该手性MOF柱对醇类、酮类、酸类、环氧化合物和醚类等10种手性化合物表现出较好的拆分效果。对该手性MOF柱的重现性、稳定性作了评价,考察了进样量对分离效果的影响,结果表明该手性MOF柱具有较好的重现性和稳定性。
金属-有机骨架;高效液相色谱;手性固定相;手性分离
金属-有机骨架材料(Metal-organic frameworks,MOFs)是由过渡金属离子或金属簇与有机多齿配体通过分子自组装和晶体工程的方法得到的一维或多维周期性网状结构的多孔配位聚合物[1-5]。手性MOFs因具有大的比表面积,稳定的手性孔结构,易于功能化,组装过程可调控和敞开的手性孔穴等特点,而在不对称催化和手性识别等方面有着广阔的应用前景[6-12]。
色谱法是目前手性化合物拆分最为常用的方法[13-14]。其中,高效液相色谱法因分析速度快、操作简便、灵敏度高、重现性好和适用范围广等优点[15-17],已成为手性化合物最常用的拆分方法。1999年,Aoyama等[18]成功合成了一种光学纯的手性MOF Cd(apd)(NO3)2(H2O)(EtOH),手性MOFs逐渐引起了人们的广泛关注。2000年,Kim课题组[9]将一种具有均一手性结构的MOF材料POST-1成功用于手性拆分和异相不对称催化。2007年,Brliakov课题组[19]首次将纯手性的[Zn(bdc)(L-lac)(dmf)]·DMF(bdc)晶体用作液相色谱固定相分离了手性亚砜类化合物质。2011年,Padmanaban等[20]合成了一种单一手性MOF材料Bn-Chir UMCM-1,并将其用作液相色谱固定相拆分了外消旋化合物1-苯基乙醇。近年来,本课题组[21-23]将多种手性MOFs材料用作液相色谱固定相制备了手性柱,成功拆分了多种不同类型的手性化合物,如醇类、酮类、黄酮、酚类和胺类等。
(1R,2R)-1,2-环己烷二羧酸是一种手性柔性配体,含有两个相邻的羧基,能提供多种配位模式(如螯合、桥接和螯合/桥接等)构筑出不同构型的手性配位聚合物[17]。目前,尚未见将以(1R,2R)-1,2-环己烷二羧酸分子为手性配体合成的手性MOF作为液相色谱固定相拆分手性化合物的研究报道。本文以(1R,2R)-1,2-环己烷二甲酸(H2L)和4,4′-联吡啶(bpy)为配体与铜离子通过溶剂热反应合成了一种具有二维手性网状结构的手性MOF材料[Cu3(HL)2(L)2(bpy)3]·4H2O,并将其用作固定相制备了高效液相色谱手性柱。考察了该手性柱对外消旋化合物的拆分能力,有多种不同类型的外消旋化合物得到了较好拆分,表明该固定相对外消旋化合物具有良好的手性识别能力。
1 实验部分
1.1 仪器与试剂
230Ⅱ型高效液相色谱仪(大连伊利特分析仪器有限公司),仪器控制和数据采集在EC-2006高效液相色谱工作站上进行;液相色谱匀浆法装柱机(美国Alltech公司);不锈钢液相色谱空柱(美国Alltech公司);粉末X射线衍射仪(Rigaku公司);XL30ESEM-TMP型扫描电子显微镜(荷兰飞利浦公司);SMZ-B4连续变倍体视显微镜(重庆奥特光学仪器有限公司)。
(1R,2R)-1,2-环己烷二甲酸(H2L)、4,4′-联吡啶(bpy)和高氯酸铜(Ⅱ)六水合物(分析纯,上海Adamas试剂有限公司);正己烷、异丙醇和无水乙醇(分析纯,天津风船化学试剂科技有限公司);实验中所用到的10种手性化合物购自日本TCI公司和美国Fluka公司;去离子水由ELGA LabWater纯水机提供。
1.2 手性[Cu3(HL)2(L)2(bpy)3]·4H2O晶体的合成
参照文献[17]合成了[Cu3(HL)2(L)2(bpy)3]·4H2O晶体:将(1R,2R)-1,2-环己烷二甲酸(0.172 g,1 mmol)、Cu(ClO4)2·6H2O(0.37 g,1 mmol)和4,4′-联吡啶(0.156 g,1 mmol)混合置于100 mL聚四氟乙烯衬套中,加入60 mL去离子水,在室温下搅拌30 min,随后将衬套密封在不锈钢反应釜中于110 ℃下反应3 d,待冷却至室温,得到蓝绿色晶体,将其收集后用去离子水清洗3次,干燥备用。
1.3 手性固定相的制备
由于合成的[Cu3(HL)2(L)2(bpy)3]·4H2O晶体颗粒较大且不均匀,为减小涡流扩散的影响,保证合成的手性MOF晶体材料在高效液相色谱柱上的柱效,对合成的MOF晶体进行了手工研磨,再用无水乙醇悬浮收集粒径在5~10 μm范围的晶体,干燥备用。
1.4 手性[Cu3(HL)2(L)2(bpy)3]·4H2O柱的填装
采用高压匀浆法进行液相色谱柱的填装,称取1.2 g制备好的[Cu3(HL)2(L)2(bpy)3]·4H2O晶体于50 mL小烧杯中,加入23 mL的正己烷-异丙醇(9∶1,体积比)配成悬浮液,然后迅速将其倒入匀浆罐中,以正己烷-异丙醇(9∶1)为顶替液在40~50 MPa下高压5~10 min,将顶替液缓慢降压到20~30 MPa再压30~40 min。制备好的[Cu3(HL)2(L)2(bpy)3]·4H2O手性柱先用正己烷-异丙醇(9∶1)流动相冲洗1~2 h,待基线平稳后即可进行色谱分离试验。
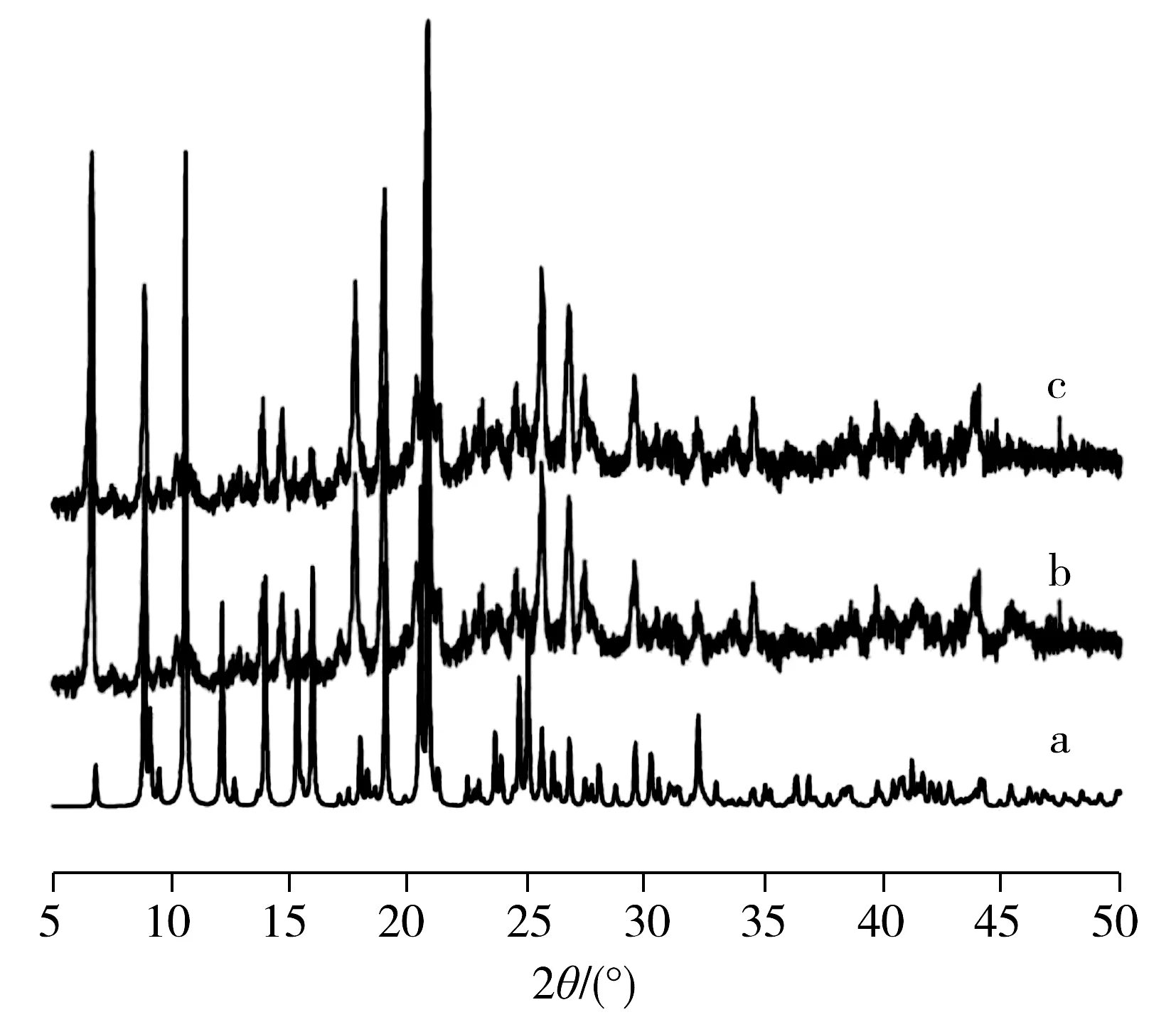
图1 [Cu3(HL)2(L)2(bpy)3]·4H2O晶体的XRD谱图Fig.1 XRD patterns of [Cu3(HL)2(L)2(bpy)3]·4H2Oa:simulated;b:as-synthesized;c:after HPLC measurement for more than two months

图2 制备的[Cu3(HL)2(L)2(bpy)3]·4H2O晶体扫描电镜图Fig.2 SEM image of the prepared [Cu3(HL)2(L)2(bpy)3]·4H2O
2 结果与讨论
2.1 [Cu3(HL)2(L)2(bpy)3]·4H2O晶体的表征
将合成的[Cu3(HL)2(L)2(bpy)3]·4H2O晶体进行粉末XRD表征,并与文献中报道的单晶模拟XRD图进行对比。由图1可知,实验所得XRD图衍射峰与模拟图基本一致,表明成功合成了手性MOF材料[Cu3(HL)2(L)2(bpy)3]·4H2O。此外,将测样两个月后的手性柱中的MOF进行了粉末XRD测定,其XRD图与装柱前的晶体XRD图基本一致,表明该手性MOF具有良好的稳定性。图2为经手工研磨和溶剂悬浮后得到的晶体颗粒SEM图,显示晶体颗粒平均粒径约5~10 μm。
2.2 [Cu3(HL)2(L)2(bpy)3]·4H2O柱的手性分离性能
为了考察[Cu3(HL)2(L)2(bpy)3]·4H2O柱(柱A)对手性化合物的拆分能力,采用不同体积比的正己烷-异丙醇体系作为流动相,对一系列手性化合物进行了拆分。结果表明,该手性MOF具有良好的手性识别能力,有10种手性化合物得到了不同程度的拆分,分别为2-苯基-1-丙醇、反-1,2-二苯基环氧乙烷、酮洛芬、1-苯基-1,2-乙二醇、3-苄氧基-1,2-丙二醇、奥美拉唑、扁桃酸、1,2-二苯基乙醇酮、吡喹酮和马来酸氯苯那敏,10种手性化合物在[Cu3(HL)2(L)2(bpy)3]·4H2O柱上的拆分结果见表1。为了比较该手性MOF与其它手性MOFs的手性识别能力,表1还列出了本课题组已报道的3种不同类型的手性MOFs柱:[(CH3)2NH2][Cd(bpdc)1.5]柱(柱B)[21]、[Cu(D-Cam)2-(4,4′-bpy)]n柱(柱C)[22]和[Co2(D-cam)2(TMDPy)]柱(柱D)[23]对手性化合物的拆分结果。
从表1和图3可知,2-苯基-1-丙醇、反-1,2-二苯基环氧乙烷、酮洛芬、1-苯基-1,2-乙二醇、3-苄氧基-1,2-丙二醇、奥美拉唑和马来酸氯苯那敏在[Cu3(HL)2(L)2(bpy)3]·4H2O柱上得到了较好的拆分,分离度为0.90~1.75,其中2-苯基-1-丙醇和马来酸氯苯那敏达到基线分离,分离度高达1.75;扁桃酸、1,2-二苯基乙醇酮和吡喹酮3种手性化合物得到了一定程度的拆分,分离度在0.54~0.60之间。此外,酮洛芬、奥美拉唑、扁桃酸和马来酸氯苯那敏在[Cu3(HL)2(L)2(bpy)3]·4H2O柱上得到了拆分,而在其它3根手性柱上未实现拆分。对于这10种手性化合物,柱B和柱D分别对3种手性化合物有拆分效果,而柱C仅对2-苯基-1-丙醇实现了拆分。因此,[Cu3(HL)2(L)2(bpy)3]·4H2O柱相对本课题组之前报道的3种手性MOFs柱具有明显的手性拆分互补作用。
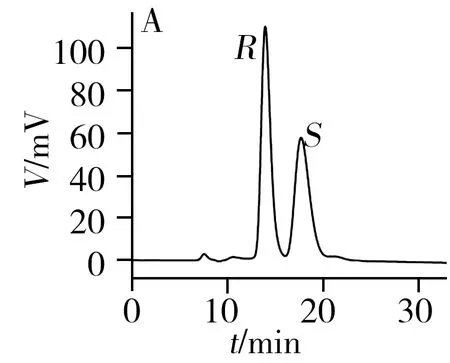
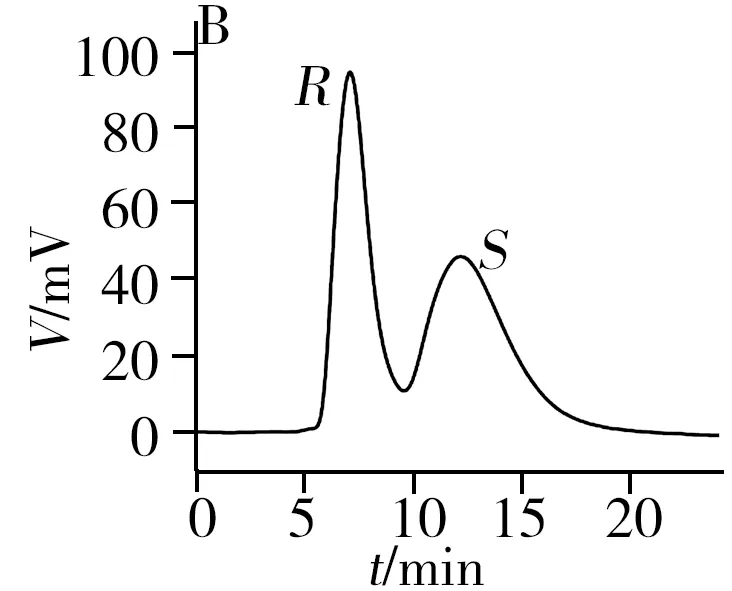
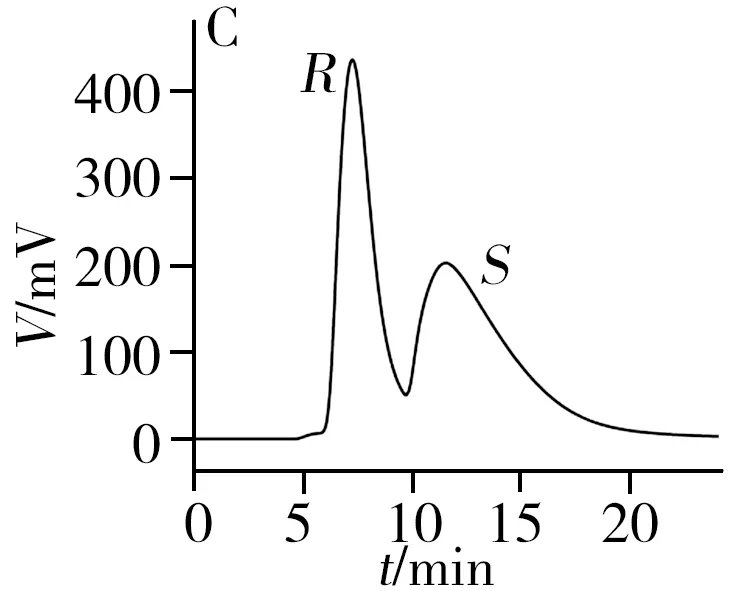
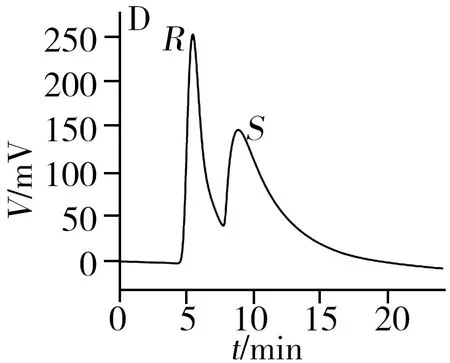
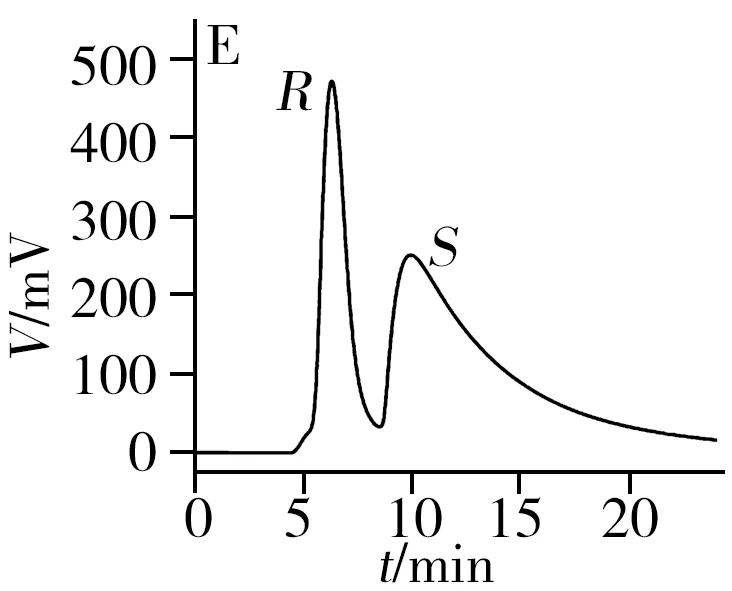
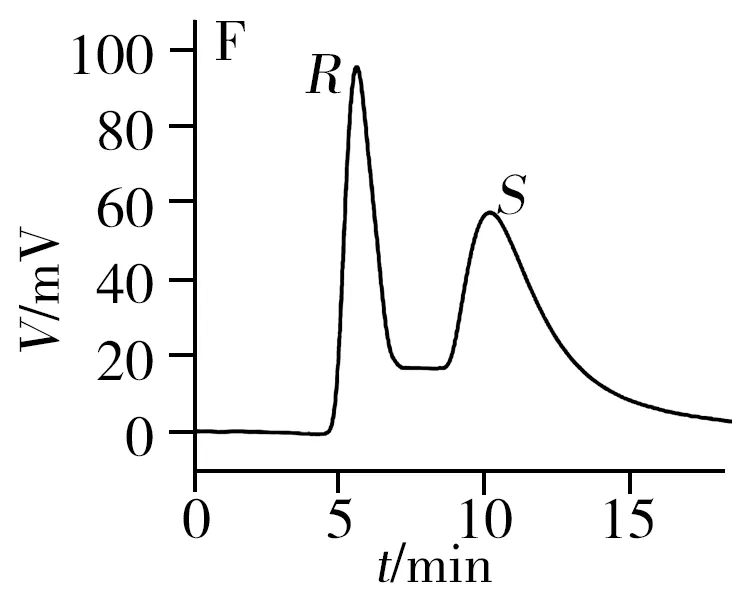
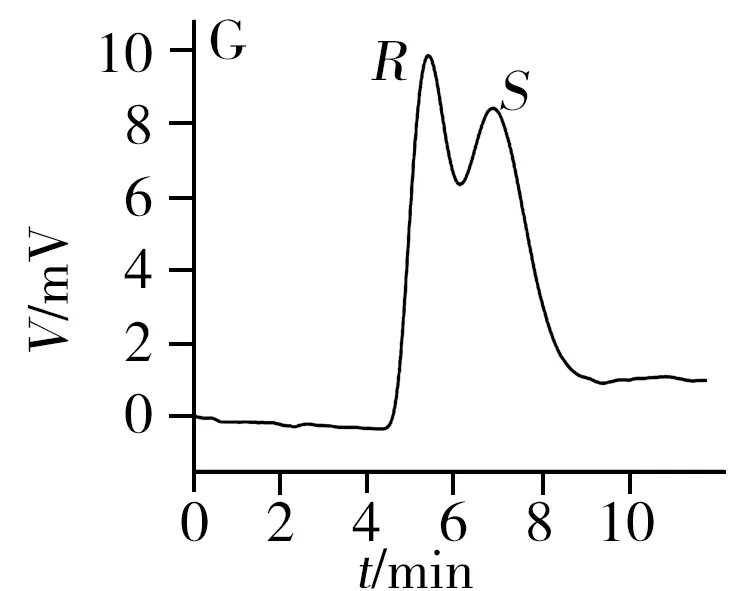
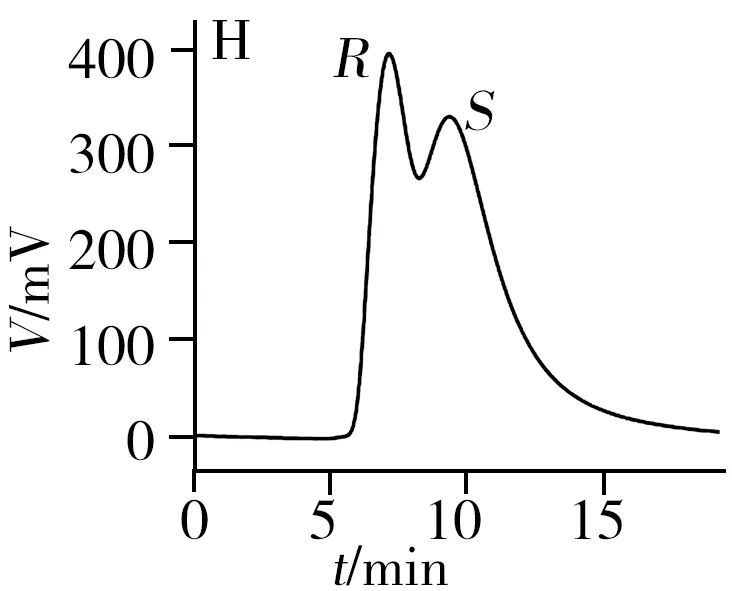
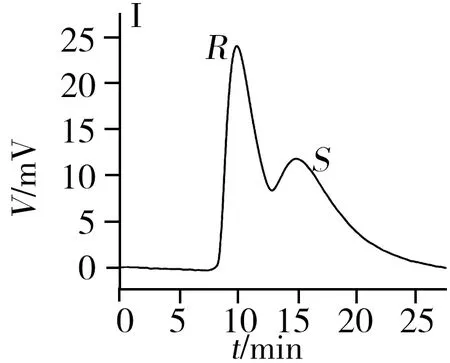
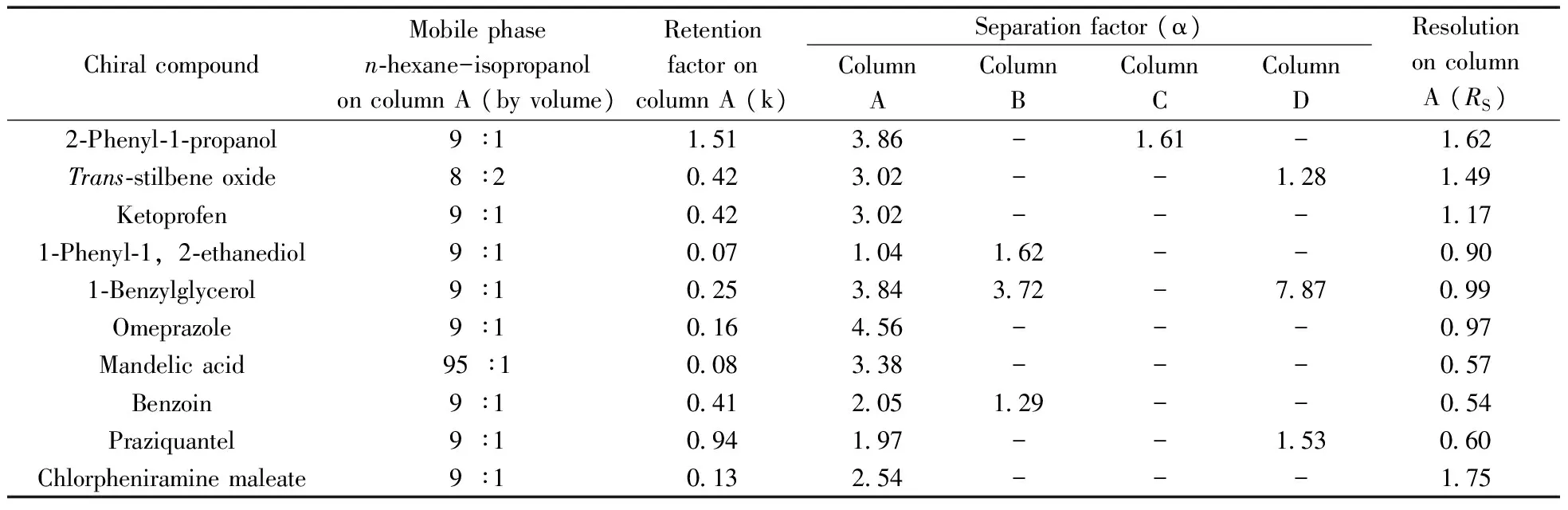
表1 手性化合物在柱A、柱B、柱C和柱D上的拆分Table 1 Separation of the chiral compounds on columns A,B,C and D
a:paked with MOF [Cu3(HL)2(L)2(bpy)3]·4H2O;b :packed with MOF [(CH3)2NH2][Cd(bpdc)1.5];c: packed with MOF [Cu(D-Cam)2-(4,4′-bpy)]n;d :packed with MOF [Co2(D-cam)2(TMDPy)]
2.3 手性化合物进样量对手性分离的影响
为了考察手性化合物进样量对手性分离的影响,探讨了在同一色谱条件下2-苯基-1-丙醇不同进样量对分离效果的影响。结果显示,2-苯基-1-丙醇的进样量从2 μL增加至20 μL时,仍可达到基线分离。随着2-苯基-1-丙醇进样量的增加,两个对映异构体的峰高和峰面积也相应增加,其中第一个峰的保留时间几乎不变,第二个峰的保留时间逐渐减小,对样品的手性选择性略有降低。因此,在拆分手性化合物过程中应选择适宜的进样量。
2.4 [Cu3(HL)2(L)2(bpy)3]·4H2O手性柱的重现性与稳定性
为了考察[Cu3(HL)2(L)2(bpy)3]·4H2O柱的重现性和稳定性,以正己烷-异丙醇(9∶1)作为流动相,对反-1,2-二苯基环氧乙烷和2-苯基-1-丙醇连续进样5次。由图4可知,该手性MOF柱对两者的拆分效果基本保持不变,其保留时间(n=5)与峰面积的相对标准偏差(RSD)分别为0.98%和0.86%,表明手性MOF柱具有良好的稳定性和重现性。

2.5 [Cu3(HL)2(L)2(bpy)3]·4H2O晶体对手性化合物的拆分机理
[Cu3(HL)2(L)2(bpy)3]·4H2O固定相对多种手性化合物表现出良好的分离能力,主要归因于MOF晶体的拓扑片层网状结构提供的手性微环境。[Cu3(HL)2(L)2(bpy)3]·4H2O手性晶体的拓扑结构是铜离子先与柔性配体(1R,2R)-1,2-环己烷二甲酸(H2L)进行螯合反应形成三角双锥体的手性链状结构,手性链状结构又通过与bpy配体相互连接扩展形成1个二维手性层面网状结构(图5),且层与层之间存在氢键作用力。手性MOF [Cu3(HL)2(L)2(bpy)3]·4H2O材料的晶体结构在很大程度上决定了其对一些手性化合物具有一定的识别能力:其手性识别能力主要来源于手性化合物的构型与晶体二维手性层面网状结构功能位点间的立体匹配作用。此外,溶质分子在固定相和流动相之间的相互作用力(氢键、色散、偶极-偶极和π-π等相互作用)也参与了手性MOF对手性化合物的选择性识别。
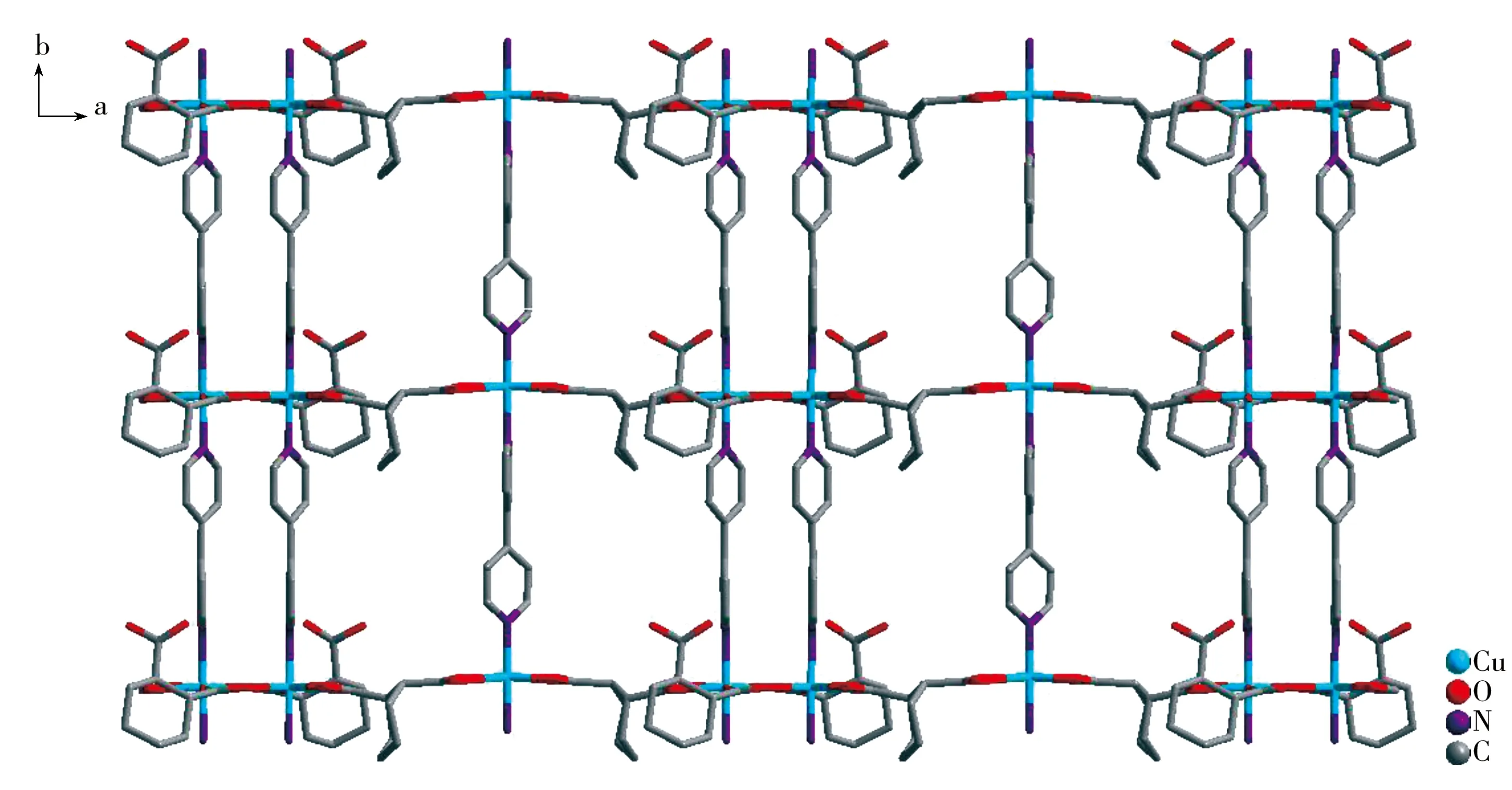
图5 [Cu3(HL)2(L)2(bpy)3]·4H2O的结构图Fig.5 Structure of [Cu3(HL)2(L)2(bpy)3]·4H2O
3 结 论
本文将一种手性二维多孔网状结构的手性MOF [Cu3(HL)2(L)2(bpy)3]·4H2O晶体用作固定相制备了高效液相色谱手性柱,并对一系列手性化合物进行了拆分。实验结果表明,多种不同类型的手性化合物在该色谱柱上得到了较好的拆分,且对本课题组报道的3种手性MOFs柱表现出明显的互补性。因此,手性MOF [Cu3(HL)2(L)2(bpy)3]·4H2O作为一种新型的高效液相色谱手性固定相用于手性分离具有一定的研究意义。
[1] Wei W Y,Fang J,Kong H N,Han J Y,Chang H Y.Prog.Chem.(魏文英,方键,孔海宁,韩金玉,常贺英.化学进展),2007,17(6):1110-1115.
[2] Mu C Z,Xu F,Lei W.Prog.Chem.(穆翠枝,徐峰,雷威.化学进展),2007,19(9):1345-1356.
[3] Mueller U,Schubert M,Teich F,Puetter H,Schierle-Arndt K,Pastre J.Cheminform,2006,37(23):626-636.
[4] Liu Z H,Ji Y S,Zhang J,Huang H Y,Liang B.J.Instrum.Anal.(刘志华,纪永升,张静,黄华宇,梁蓓.分析测试学报),2015,34(8):939-943.
[5] Xie S M,Yuan L M.Prog.Chem.(谢生明,袁黎明.化学进展),2013,25(10):1763-1770.
[6] Chelucci G,Thummel R P.Chem.Rev.,2002,102(9):3129-3170.
[7] Bu X H,Tong M L,Chang H C,Kitagawa S,Batten S R.Angew.Chem.Int.Ed.,2004,43(2):192-195.
[8] And Y C,Bernasek S L.J.Phys.Chem.B,2005,109(10):4514-4519.
[9] Dybtsev D N,Nuzhdin A L,Chun H,Bryliakov K P,Talsi E P,Fedin V P,Kim K.Angew.Chem.Int.Ed.,2006,45(6):916-920.
[10] Zhang J,Chen S,Wu T,Feng P,Bu X.J.Am.Chem.Soc.,2008,130(39):12882-12883.
[11] Ma L,Abney C,Lin W.Cheminform,2009,40(33):1248-1256.
[12] Jiang J,Babarao R,Hu Z.Chem.Soc.Rev.,2011,40(7):3599-3612.
[13] Yuan L M.ChiralRecognitionMaterials.2rd ed.Beijing:Science Press (袁黎明.手性识别材料.2版.北京:科学出版社),2010.
[14] Tu H S,Fan J,Tan Y,Lin C,Hua J Y,Zhang W G.Chin.J.Chromatogr.( 涂鸿盛,范军,谭艺,林纯,华江颖,章伟光.色谱),2014,32(5):452-457.
[15] He X R,Wu Z Y,Ye Y L,Gao X D,Chen S E,Ma Z R.J.Instrum.Anal.(赫欣睿,武中庸,叶永丽,高旭东,陈士恩,马忠仁.分析测试学报),2016,35(6):922-928.
[16] Zhang Q C,Yang Y Q,Su Y,Li H M,Li M G,Wu S Q.J.Instrum.Anal.(张仟春,杨燕群,苏姚,栗惠敏,李明刚,吴诗琪.分析测试学报),2017,36(6):718-724.
[17] Yue Q,Huang Q,Gao Y Y,Gao E Q.Inorg.Chim.Acta,2016,443:110-117.
[18] Guchhait N,Takayuki Ebata A,Mikami N.J.Am.Chem.Soc.,1999,121(24):5705-5711.
[19] Nuzhdin A L,Dybtsev D N,Bryliakov K P,Talsi E P,Fedin V P.J.Am.Chem.Soc.,2007,129(43):12958-12959.
[20] Padmanaban M,Müller P,Lieder C,Gedrich K,Grünker R,Bon V,Senkovska I,Baumgärtner S,Opelt S,Paasch S,Brunner E,Glorius F,Klemm E,Kaskel S.Chem.Commun.,2011,47(44):12089-12091.
[21] Zhang M,Pu Z J,Chen X L,Hong X L,Zhu A X,Yuan L M.Chem.Commun.,2013,49(45):5201-5203.
[22] Zhang M,Zhang J H,Zhang Y,Wang B J,Xie S M,Yuan L M.J.Chromatogr.A,2014,1325:163-170.
[23] Kong J,Zhang M,Duan A H,Yang R,Yuan L M.J.Sep.Sci.,2015,38(4):556-561.
Separation of Chiral Compounds Using a Chiral Metal-Organic Framework [Cu3(HL)2(L)2(bpy)3]·4H2O for High Performance Liquid Chromatography
LI Li,FU Shi-guo,YUAN Bao-yan,XIE Sheng-ming*,YUAN Li-ming*
(Faculty of Chemistry and Chemical Engineering,Yunnan Normal University,Kunming 650500,China)
Chiral metal-organic frameworks(MOFs),as a novel type of porous material with many properties such as large surface area,diverse structure,adjustable pore size and good chemical stability,have aroused much attention in the field of chromatographic separation.In this paper,a homochiral MOF [Cu3(HL)2(L)2(bpy)3]·4H2O with 2D chiral network was synthesized through the reaction of two kinds of ligands((1R,2R)-1,2-cyclohexanedicarboxylic acid(H2L) and 4,4′-bipyridine(bpy)) with copper ion via a solvothermal approach.The homochiral MOF [Cu3(HL)2(L)2(bpy)3]·4H2O was used as chiral stationary phase to fabricate a packed column for high-performance liquid chromatography.To investigate the MOF′s chiral recognition ability,a series of racemates were separated on the homochiral MOF column under normal phase condition usingn-hexane-isopropanol as mobile phase.The homochiral MOF column exhibited a good resolving ability towards 10 kinds of chiral compounds,including alcohols,ketones,acids,epoxy compounds and ethers,etc.The reproducibility and stability of the homochiral MOF column were evaluated.The effect of the injected mass of chiral compound on separation was also investigated.Results indicated that the homochiral MOF column has a good reproducibility and stability for enantioseparation.
metal-organic framework;high-performance liquid chromatography;chiral stationary phase;chiral separation
2017-08-14;
2017-08-29
国家自然科学基金资助项目(21365024,21675141)
*
袁黎明,博士,教授,研究方向:生化分离分析,Tel:0871-65941088,E-mail:yuan_limingpd@126.com
谢生明,博士,副教授,研究方向:手性识别材料,Tel:0871-65941088,E-mail:xieshengming_2006@163.com
10.3969/j.issn.1004-4957.2017.12.004
O657.7
A
1004-4957(2017)12-1439-06
