局部晚期非小细胞肺癌患者同步放化疗急性食管炎预测因素研究*
2017-11-13吉福志戴婷婷王加阳
张 泉,陈 力,吉福志 ,彭 进 ,戴婷婷 ,王加阳 ,王 浩△
1.南京医科大学附属淮安第一医院肿瘤放疗科(淮安223300),2.陕西省肿瘤医院肿瘤放疗科(西安710061)
局部晚期非小细胞肺癌患者同步放化疗急性食管炎预测因素研究*
张 泉1,陈 力2,吉福志1,彭 进1,戴婷婷1,王加阳1,王 浩2△
1.南京医科大学附属淮安第一医院肿瘤放疗科(淮安223300),2.陕西省肿瘤医院肿瘤放疗科(西安710061)
目的:研究局部晚期非小细胞肺癌(NSCLC)患者强调放射治疗(IMRT)合并化疗时急性食管炎的发生率及相关预测因素。 方法:收集IMRT同步化疗未手术Ⅲ期NSCLC 患者156例。放疗靶区包括原发肺肿瘤及受累淋巴引流区,中位剂量为60Gy,分30次(50~70Gy)。放疗期间及放疗结束后3个月内出现≥2级急性食管炎作为终点事件,采用 CTCAE3.0评估急性食管炎级别,并采用Logistic 回归模型对预测因素进行分析。结果:156例中,出现治疗相关≥2 级急性食管炎122例( 78.2%),其中2 级99例( 63.5%)、3级23例( 14.7%);≥2 级急性食管炎发生时的中位剂量为26Gy(8~64 Gy);食管V5-V60、食管平均剂量及年龄是≥2级急性食管炎的预测因素(P=0.019、0.0.0.02),其中高龄和高体重指数是保护性因素。结论:局部晚期NSCLC 患者IMRT同步化疗时,食管V50对预测≥2级急性食管炎有较高价值。
肺癌中非小细胞肺癌(Non-small cell lung cancer,NSCLC)占 85%左右,且大约有近三分之一的患者确诊时,因局部晚期而无法进行手术切除。假如这些患者有良好的身体状态,同步放化疗是标准的治疗方案[1]。相对于序贯放化疗,同步放化疗可以提高局控率,总生存率大约可以提高5%[1]。尽管同步放化疗有更好的治疗效果,但是会增加风险和急性毒性反应,特别是增加了急性食管炎的发生。Meta分析中,NSCLC协作组包含6个随机临床试验,CCRT组中3~4级食管炎发生率18%,高于序贯放化疗组的4%(RR=4.9,P<0.01)[1]。对于单纯放疗,发生大于3级以上食管炎的发生率约为1%,在CCRT组中有增加到6%~24%[2]。
放化疗致食管炎通常发生在放疗开始后2~4周,并且可能持续2~7周[3]。强调放射治疗(Intensity modulated rediation therapoy,IMRT)可以产生更加适合的剂量分布,相对于3DCRT,可以产生符合肿瘤形状体积的剂量分布,更好的避开食管。对于NSCLC,IMRT潜在具备提高靶体积的剂量,而没有相应增加正常肺和食管的受照射剂量。在许多中心,IMRT已成为用于减少NSCLC局部复发和保护关键危及器官的标准放疗技术。
尽管在之前的研究已经有许多食管炎临床和剂量等危险参数报道,但目前没有作为被广泛接受最佳的剂量学预测参数。此外,其中大多数研究都是建立在3DCRT治疗基础上的。本项研究目的是回顾性研究局部晚期NSCLC患者在接受IMRT合并化疗时,急性症状性食管炎的发生率及预测食管炎因素。
资料和方法
1 一般资料 收集2010年1月至 2016 年12月间在本院肿瘤放疗科治疗的未手术NSCLC 患者156例。纳入标准:组织学和细胞学证明是NSCLC,临床AJCC分期(7th)Ⅲ期,ECOG 0~1分,体重减轻≤10%,有足够的肝肾功能,FEV≥1.0,在治疗前有胸部和上腹部的增强CT和(或)全身PET-CT。排除有胸腔积液、过去5年伴其他活动性恶性肺瘤而化疗患者。156例中,男129 例(83%),女 27例(17%),年龄30~78岁,>60岁85例,<60岁71例;病理诊断鳞癌 93例( 59.6%),腺癌 48例( 30.8%),腺鳞癌8例( 5.1%),大细胞癌 3例( 1.9%),肉瘤样癌 2 例( 1.3%),不典型类癌 2例 (1.3%);病变位于下叶46例,中上叶110例;肿瘤分型中央型119例,周围型37例;肿瘤分期N3期65例,余91例;体重减轻89例,吸烟127例。
2 放疗方法 所有患者均采用IMRT固定野治疗,采用仰卧体膜固定和CT增强定位。CT扫描层厚5mm,重建层厚3mm;CT扫描范围上界为下颌角下缘,下界为肾脏下缘。 GTV 包括CT等影像学所见肺部肿瘤和纵膈转移淋巴结,CTV包括 GTV及受累淋巴引流区域,外扩6~8mm,遇到血管和骨性结构适当内收。 PTV为 CTV 外放5~10mm。 95%PTV 接受中位剂量为60Gy(50~70Gy),2Gy/次,5次/周。正常器官组织剂量限制:脊髓<45Gy,双肺V20<30%,肝脏V30<40%,心脏V30<40%。放疗期间每周使用EPID或 CBCT验证治疗位置。所有患者食管由同一医生勾画,从环状软骨下缘向胃食管交界在每一个CT层面上勾画食管轮廊。每一患者都利用DVH来计算剂量体积的数值。从DVH中获取多组剂量体积参数。基于DVH 计算PTV剂量及食管剂量体积,包括、V5、V10、V13、V15、V20、V25、V30、V35、V40、V45、V50、V55、V60、食管最大及平均剂量、食管总体积。
3 化疗方案 同期化疗使用多以铂类为基础的双药方案,其中依托泊甙 + 顺铂 92例(58.7%)、 紫杉醇 +顺铂24例(15.4%) 、紫杉醇+卡铂 21例( 13.5%)、培美曲塞+顺铂 19 例( 12.2%) 。
4 急性食管炎评估 根据NCI-CTCAE 3.0标准进行分级,从放疗开始至放疗后3月。在放化疗期间,医师对患者每周评估一次,包括患者一般情况、临床症状、临床体征以及相关实验室检查,评估疗效及并发症。 治疗结束后 1 个月评估近期疗效,此后第1~2 年每3 个月、第 3~5 年每6个月以及5 年后每年随访1 次。 随访检查内容包括患者一般情况、临床症状、临床体征、相关实验室检查及胸部CT 扫描。以放化疗期间及放化疗结束后3月内患者发生≥2 级急性食管炎作为终点事件,医师填写急性食管炎出现的放疗剂量和时间。
5 统计学方法 采用 SPSS20.0统计学软件,进行Logistic 回归模型的预测因素分析。多因素P<0.05 的变量被认为是有统计学意义的独立预测因素。 应用 ROC 曲线选择设定连续变量的最佳分界点,可以将连续变量转换为分类变量,采用χ2检验。P<0.05为差异有统计学意义。
结 果
1 治疗结果 在接受IMRT和同步化疗后,所有患者均完成治疗。放疗结束与开始中位时间间隔34~60d,平均41d;在6 周内完成放疗124例(79.5%),8 周内完成放疗154例(98.7%)。
2 放射性食管炎发生情况 发生≥2 级急性食管炎122 例(78.2%),其中,2 级99例(63.5%),3 级23例(14.7%)。发生≥2级急性食管炎时中位照射剂量8~64Gy,平均26Gy;发生食管炎距放疗开始时间 4~66d,平均18d。未发生≥4级急性食管炎。整个放化疗期间未出现或仅出现1级急性食管炎34例(21.8%)。急性食管炎的患者放疗剂量体积相关资料的单因素分析显示,PTV D95<50Gy 72例,≥50Gy 84例;食管总体积<33 cm374例,≥33 cm382例;食管最大剂量<50Gy 74例,≥50Gy 82例;食管平均剂量 <25Gy 66例,≥25Gy 90例。
3 ≥2级急性食管炎分析 ≥2 级急性食管炎单因素分析中食管平均剂量、食管 V5-V40、食管V45-V60、≥N3 期。将食管 V5-V60、食管平均剂量进行因子分析( KM0=0.833,P=0),降维后得出2个主成分,即食管 V5-V25、食管 V30-V60 和食管平均剂量。将每个主成分再次进行单因素分析显示食管 V5-V25 的P=0.009 、OR=1.77 ,食管 V30-V60 和食管平均剂量的P=0.000 、OR=51.62 。最终纳入多因素分析的变量,包括有年龄、≥N3 期、食管 V5-V25、食管V30-V60和食管平均剂量。 将多因素分析有意义的连续变量转变为二分类变量,再分别与其他因素进行多因素分析,得出各剂量学参数所致 ≥2 级急性食管炎的发生率及危险度,见表1。
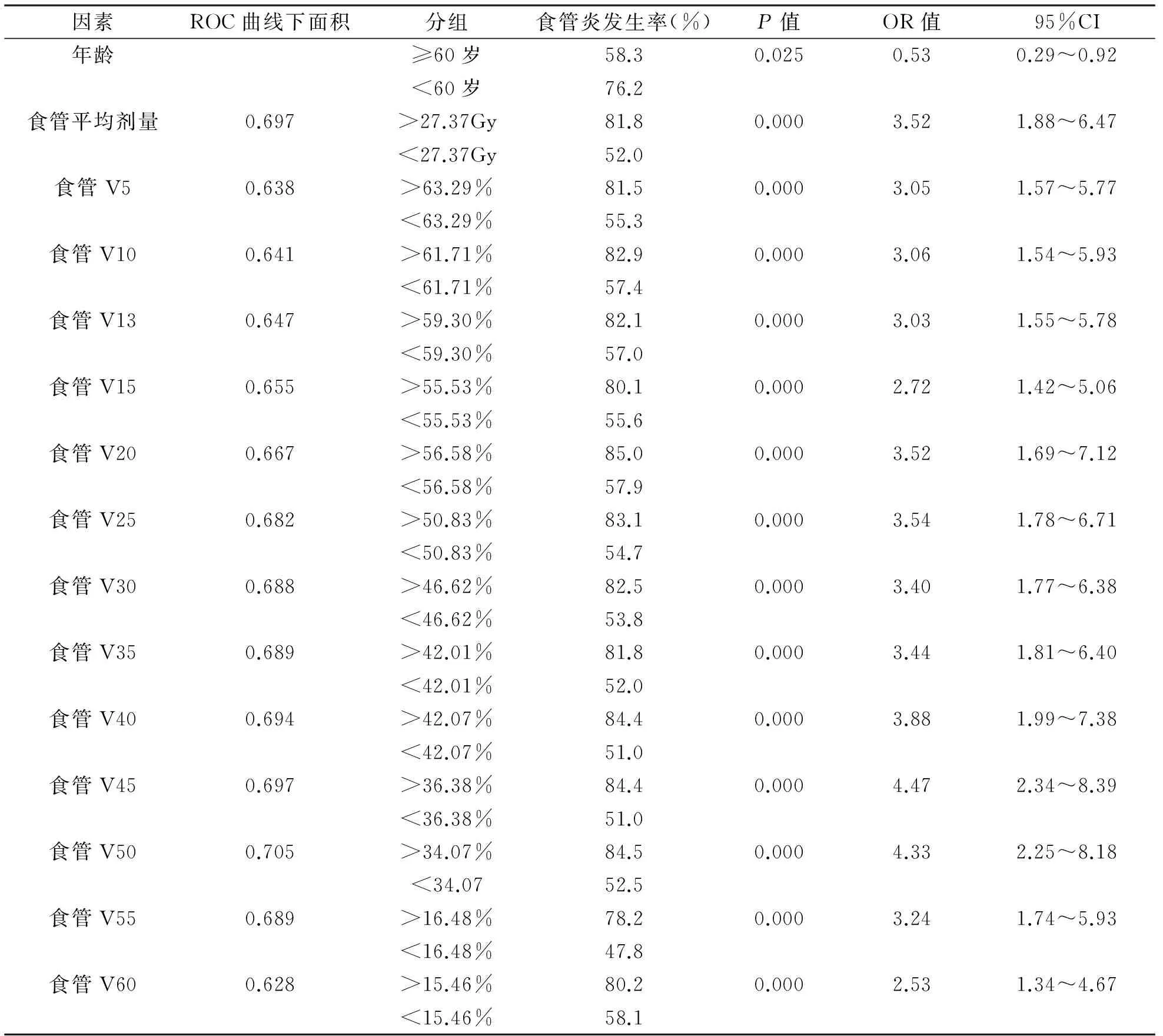
表1 156例NSCLC患者≥2级急性食管炎相关剂量学参数危险度分析
从本项研究结果可以发现,患者年龄越小、食管 V5-V60和食管平均剂量越高,患者的≥2 级急性食管炎发生率越高。发现在剂量学因素中,食管 V40-V50 对≥2级急性食管炎有较大的预测价值。
讨 论
急性食管炎是肺癌放疗常见的并发症之一。同步放化疗后急性重症食管炎的发生率达 14%~25%[4-5],严重影响了治疗及患者生活质量。以前已经有大量的剂量参数用于研究与急性食管炎的相关性。然而,这些研究结果主要是基于3DCRT和常规放疗。到目前为止,只有很少的研究报道了给予IMRT和同步化疗发生的食管炎,随着IMRT作为选择治疗方案的越来越广泛应用,用以前的研究结果来评估IMRT引起的食管毒性反应是不够准确的。本项研究探索接受IMRT放疗同步化疗的局部晚期NSCLC患者,结合既往相关研究结果,将患者临床资料、治疗模式及剂量学等因素与食管炎纳入分析。
在研究患者临床资料的相关研究中,发现食管炎相关预测因素有高龄[6]、N 分期和较低的体重指数[7]等。 本研究有类似的研究结果,发现年龄及体重指数有对急性食管炎的发生有预测价值,<60岁组的≥2 级急性食管炎发生率明显高于≥60岁组。 低体重指数(< 22.65 ) 组≥2 级急性食管炎的发生率明显高于低体重指数(>22.65)组,这与Wang等[7]的研究结果相符合。Deking[8]和Wijsman[9]在当今的研究中发现,性别和食管炎之间有明显统计学的显著相关性。
局部晚期NSCLC标准治疗模式是同期放化疗,同期放化疗相较较序贯放化疗及单纯放疗,患者明显增加了重症急性食管炎的发生率。孙帅等[10]研究显示同期化疗是急性重症食管炎的最终预测因素之一,研究中发现局部晚期NSCLC同期放化疗组急性重症食管炎发生率明显高于序贯放化疗与单纯放疗组,这与既往研究结果相似。其中有深入研究发现化疗方案也可能影响食管炎的发生率[11],但孙帅等[10]研究发现不同的同期化疗方案的治疗组间比较,各组的重症食管炎发生率相近。
目前对于用于预测急性食管炎的剂量体积参数还没有形成定论。既往研究中曾报道食管V20-V70[7,12-13]、食管照射的最大剂量[14]、食管高剂量区的周径或表面面积所占比例[15]、 食管体积及长度[9]、 剂量分割模式[6]与急性食管炎的发生相关。有研究报道食管V40-V60等剂量学参数中,尤其是V50对急性食管炎可能有较大的预测价值[5,7]。但是目前研究者认为单一剂量学参数的预测价值有限并且准确性有限,联合两种及两种以上剂量学参数来预测急性食管炎可能提高预测准确性。Yi等[16]研究发现相对于其他剂量学参数V40和V50与IMRT治疗的NSCLC患者的≥2级食管炎最密切相关;V40和L40(受照射≥40Gy的食管长度)是预测2级或2级以上食管炎最为有效的剂量预测参数;V40或L40的选择应用取决于医生倾向于选择获取信息的便利性。
本研究为了详细分析剂量学对急性食管炎的预测价值,将 DVH 信息中剂量体积导出,选取 V5-V60 等进行分析,并采用因子分析方法将连续的剂量学数据进行降维处理以方便统计分析。因子分析是目前常用的统计方法,已逐步应用于医疗卫生领域[17]。 它的优势在于可将大量具有线性关系的连续变量数据转换成相互之间无相关性的几组数据,从而方便研究者进行风险因素分析。
本研究结果提示食管的剂量体积参数Vx是急性食管炎的主要预测因素。食管V5-V60 及食管平均剂量的数值与≥2级急性食管炎发生呈正相关,而其中食管V50-V60 与≥2级急性食管炎明显相关,提示 V50 对≥2级急性食管炎均有较高的预测价值,此结果与既往研究基本一致。本项研究选择病例时, 仅选择了常规分割病例 (2Gy/次,5次/周),所以未能分析放疗分割剂量高低与急性食管炎的相关性。而国外Kwint等[18]报道在IMRT中分别是38%和22%,发生率较高,可能就是因为在他们研究中每次放疗剂量是2.75Gy(66Gy/24F)。
目前,评价食管炎最常用的评分系统是CTC量表。它评价食管炎的发生和严重程度主要依靠患者的症状和医生使用的治疗方法,这些对于临床管理是便利的,然而,患者的主观感觉和医生的判断因人而异。这些可能导致高估或低估食管炎的发生率。这结果表明,毒性反应评估本质是困难的,需要持续的教育和讨论如何尽可能准确评分毒性反应。
综上所述,局部晚期 NSCLC 患者 IMRT同步化疗后急性症状性食管炎是常见的可以接受的并发症。食管剂量体积Vx是急性食管炎的主要预测因素。 食管V5-V60 及平均剂量、高龄与≥2级急性食管炎密切相关,其中高龄和高体重指数是保护性因素。而V50对≥2级急性食管炎有明显高的预测价值。本研究认为可通过控制食管剂量体积参数Vx,临床治疗时可以应用辐射保护药物等药物来降低急性食管炎发生率。将来评定食管晚期毒性,并且联合多种剂量学因素建立综合预测模型是发展趋势,这需要在一个大的独立患者研究中进一步验证本研究结果。
[1] Auperin A, Le Pechoux C, Rolland E,etal. Metaanalysis of concomitant versus sequential radiochemotherapy in locallyadvanced non-small-cell lung cancer[J]. J Clin Oncol,2010,28:2181-2190.
[2] Werner-Wasik M, Yorke E, Deasy J,etal. Radiation dose-volume effects in the esophagus[J]. Int J Radiat Oncol Biol Phys,2010,76:S86-93.
[3] Uyterlinde W, Chen C, Kwint M,etal. Prognostic parameters for acute esophagus toxicity in intensity modulated radiotherapy and concurrent chemotherapy for locally advanced non-small cell lung cancer[J]. Radiother Oncol,2013,107:392-397.
[4] 朱向帜,王绿化,王颖杰,等.三维适形放疗局部晚期非小细胞肺癌的放射性肺炎风险因素研究[J].中华放射肿瘤学杂志,2007,16(6):421-426.
[5] 王 澜,李晓宁,吕冬婕,等. 肺低剂量区体积预测急性放射性肺炎价值探讨[J]. 中华放射肿瘤学杂志,2010,19(4):296-300.
[6] Palma DA, Senan S, Tsujino K,etal. Predicting radiation pneumonitis after chemoradiation therapy for lung cancer: an international individual patient data meta-analysis [J].Int J Radiat Oncol Biol Phys,2013,85(2):444-450.
[7] Wang LH,Wu SX, Ou GF,etal. Randomized phase II study of concurrent cisplatin / etoposide or paclitaxel / carboplatin and thoracic radiotherapy in patients with stage III non-small cell lung cancer [J] . Lung Cancer, 2012, 77 ( 1 ) : 89-96.
[8] Deking-Oberije C, De Ruysscher D, Petit S,etal. Development, external validation and clinical usefulness of a practical prediction model for radiation-induced dysphagia in lung cancer patients[J]. Radiother Oncol,2010,97:455-461.
[9] Wijsman R, Dankers F, Troost EG,etal. Multivariable normal-tissue complication modeling of acute esophageal toxicity in advanced stage non-small cell lung cancer patients treated with intensity-modulated (chemo-)radiotherapy[J]. Radiother Oncol,2015,117:49-54.
[10] 孙 帅,王静波,吉 喆,等.256例局部晚期NSCLC患者IMRT后急性症状性食管炎预测因素分析[J].中华放射肿瘤学杂志,2015,24(6):605-610.
[11] Perrier L, Buja A, Mastrangelo G,etal. Transferability of health cost evaluation across locations in oncology:cluster and principal component analysis as an explorative tool [J].BMC Health Serv Res,2014,14:537.
[12] Holmes GM, Pink GH. Adoption and perceived effectiveness of financial improvement strategies in critical access hospitals[J]. J Rural Health,2012,28(1):92-100.
[13] Dang J,Li G,Ma LH,etal. Predictors of grade ≥ 2 and grade ≥ 3 radiation pneumonitis in patients with locally advanced non-small cell lung cancer treated with three-dimensional conformal radiotherapy [J].Acta Oncol,2013,52(6):1175-1180.
[14] Shi AH,Zhu GY,Wu H,etal. Analysis of clinical and dosimetric factors associated with severe acute radiation pneumonitis in patients with locally advanced non-small cell lung cancer treated with concurrent chemotherapy and intensity-modulated radiotherapy [J].Radiat Oncol,2010,5:35.
[15] Rodrigues G,Lock M,D Souza D,etal. Prediction of radiation pneumonitis by dose?volume histogram parameters in lung cancer?a systematic review [J].Radiother Oncol,2004,71(2):127-138.
[16] Yi Pan, Carsten Brink, Marianne Knap,etal.Acute esophagitis for patients with local-regional advanced non small cell lung cancer treated with concurrent chemoradiotherapy[J].Radiother Oncol,2016,118:465-470.
[17] Yorke ED, Jackson A, Rosenzweig KE,etal. Correlation of dosimetric factors and radiation pneumonitis for non-small-cell lung cancer patients in a recently completed dose escalation study [J] . Int J Radiat Oncol Biol Phys, 2005, 63 ( 3 ) : 672-682.
[18] Kwint M, Uyterlinde W, Nijkamp J,etal. Acute esophagus toxicity in lung cancer patients after intensity modulated radiation therapy and concurrent chemotherapy[J]. Int J Radiat Oncol Biol Phys,2012,84:e223-228.
Predictivefactorsforacuteesophagitisinpatientswithlocallyadvancednon-smallcelllungcancertreatedwithintensitymodulatedradiationconcurrentchemotherapy
Zhang Quan,Chen Li, Ji Fuzhi, et al. Department of Radiation Oncology,
Huai’an First People’s Hospital ,Nanjing Medical University(Huai’an 223300)
Objective: To study the incidence and related predictive factors for acute esophagitis in patients with locally advanced non-small cell lung cancer (NSCLC) treated with intensity modulated radiation (IMRT) concurrent chemotherapy. Methods: Data were collected retrospectively from 156 patients with inoperable or unresectable stage Ⅲ NSCLC treated in our hospital between January 2010 and December 2016.The radiotherapy target volume included primary lung cancer and lymphatic drainage area involved ,with a median dose of 60 Gy in 30 fractions(50-70Gy).Grade ≥ 2 acute esophagitis (AE) which occurred during radiotherapy and within 3 months after completion of radiotherapy served as the outcome event.National Cancer Institute Common Terminology Criteria for Adverse Events version 3.0(NCI-CTCA3.0) was used to evaluated the grade of AE. The logistic regression model was used to analyze the predictive factors. Results: A total of 122 patients(78.2%)had treatment-related grade ≥2AE;99 patients (63.5%) had grade 2 AE and 23 patients (14.7%) had grade 3 AE .The median dose when grade ≥2 AE occurred was 26 Gy(8-64Gy).For grade ≥2 AE,multivariate analysis showed that esophageal V5-V60,mean dose , and age were independent predictive factors(P=0.021,0,0.010).Old age and higher BMI were the predictive factors .Conclusions For patients with locally advanced NSCLC treated with IMRT concurrent chemotherapy, esophageal V50 are high predictive value for grade ≥2AE.
Carcinoma,non-small cell lung/therapy Esophagitis/etiology Radiotherapy side-effects Forecasting
*南京医科大学科技发展基金资助项目(2011NJMU239)
△通讯作者
癌,非小细胞肺/治疗 食管炎/病因学 放疗反应 预测
R734
A
10.3969/j.issn.1000-7377.2017.11.025
(收稿:2017-09-01)
