高效液相色谱-光电二极管阵列-高分辨质谱联用鉴定马鞭草提取物中的化学成分
2017-09-14孙玉明王月月王玉林
孙玉明, 王月月, 蔡 蕊, 张 华, 王玉林
(1. 大连理工大学化工学院, 辽宁 大连 116024; 2. 大连医科大学基础医学院, 辽宁 大连 116044)
研究论文
高效液相色谱-光电二极管阵列-高分辨质谱联用鉴定马鞭草提取物中的化学成分
孙玉明1, 王月月1, 蔡 蕊1, 张 华1, 王玉林2*
(1. 大连理工大学化工学院, 辽宁 大连 116024; 2. 大连医科大学基础医学院, 辽宁 大连 116044)
采用高效液相色谱-光电二极管阵列-高分辨质谱联用(HPLC-PDA-HRMS)技术对马鞭草中的主要化学成分进行分析和鉴定。通过综合分析所检测到化合物的色谱、一级和多级全扫描质谱数据,对马鞭草提取物中的化学成分进行分析鉴定。马鞭草提取物中检测到环烯醚萜苷类、黄酮类、三萜类、苯乙醇苷类和二萜酚类化合物等共21种化学成分,其中鼠尾草酸、鼠尾草酚、迷迭香酚、异迷迭香酚、迷迭香酸以及金合欢素-7-O-芸香糖苷6种化合物并未在其他有关马鞭草提取物鉴定的文献中出现。该方法简单快速,准确度高,为鉴定中药材真伪和品质提供了可靠的科学依据。
高效液相色谱;光电二极管阵列检测;高分辨质谱;质谱裂解;结构鉴定;马鞭草;提取物
马鞭草(VerbenaofficinalisL.)为马鞭草科植物马鞭草的干燥地上部分,马鞭草以全草入药,始载于《名医别录》,具有活血化瘀、清热解毒、截疟、利水消肿的作用[1]。研究[2-4]表明,马鞭草还具有抗肿瘤、抗炎镇痛、保护神经、抗真菌、抗氧化和抗早孕等作用。
由于马鞭草中的活性成分具有临床治疗意义,其提取物中的化学成分得到了深入的研究[1,4-9]。文献[1,5,6,9]中多采用传统方法将大量药材进行提取分离得到纯品,再对化合物进行光谱鉴定。据报道[5-10],马鞭草提取物含有环烯醚萜苷、黄酮类、苯乙醇苷类、三萜类及挥发油类化合物,其中环烯醚萜苷是马鞭草的特征性成分,也是有效成分之一。近年来,HPLC-MS技术因其高效的分离能力和较强的鉴别能力而被广泛应用于中药化学组分的鉴别中[11-13]。
本文旨在采用高效液相色谱-光电二极管阵列-高分辨质谱联用(HPLC-PDA-HRMS)技术对马鞭草中的化学成分进行分离检测,通过综合分析色谱及一级和多级全扫描质谱数据对各化学成分进行结构验证,为进一步分离马鞭草中的活性成分提供前期依据,为中药材鉴定真伪和品质提供可靠的科学依据。
1 实验部分
1.1仪器与试剂
LTQ Orbitrap XL配Thermo Xcalibur 2.1数据处理系统、Accela液相色谱系统(包括Accela1250四元梯度泵、Accela AS自动进样器、Accela PDA检测器)、Hypersil Gold C18柱(150 mm×2.1 mm, 5 μm)(美国赛默飞世尔公司); BS124S万分之一电子天平(德国赛多利斯科学仪器有限公司); KQ-200DB数控超声波清洗器(昆山市超声仪器有限公司); Milli-Q超纯水机(美国Millipore公司); RE-52C旋转蒸发仪(巩义市英峪予华仪器厂); AK-1000A摇摆式中药粉碎机(温岭市奥力中药机械有限公司)。
甲醇(色谱纯,德国Merck公司);乙酸(色谱纯,北京Dikma公司);无水乙醇(分析纯,天津富宇精细化工有限公司);马鞭草(安徽德昌药业饮片有限公司,由大连医科大学第一附属医院中药剂科李永杰鉴定并确认);木犀草素原料药(纯度>98%,西安沃森生物科技有限公司);鼠尾草酸(纯度>60%,上海源叶生物科技有限公司);齐墩果酸(纯度>95%,西安小草植物科技有限责任公司);迷迭香酸、蒙花苷(纯度均不小于98%,上海源叶生物科技有限公司)。实验用水为自制超纯水。
1.2样品处理
将马鞭草粉碎得粗粉,取适量马鞭草粗粉和无水乙醇,以1 g马鞭草粗粉中加入10 mL无水乙醇的比例混匀,于20 ℃超声(50 Hz)提取2 h,静置过夜。真空抽滤后于55 ℃减压浓缩得到马鞭草提取物浸膏。
称取适量马鞭草提取物浸膏,加入无水乙醇超声溶解,配制成200 g/L的溶液,用甲醇-水(1∶1, v/v)溶液将上述溶液稀释至5 g/L,经0.22 μm的微孔有机滤膜过滤后进样。
1.3色谱和质谱条件
色谱条件:色谱柱为Hypersil Gold C18柱;柱温为室温;进样量为5 μL。流动相A为甲醇,流动相B为体积分数为0.3%的冰醋酸水溶液;流速为0.2 mL/min。梯度洗脱程序为:0~20 min, 20%A~40%A; 20~30 min, 40%A~100%A; 30~40 min, 100%A。PDA检测器波长范围:200~400 nm。
质谱条件:ESI源,分别采用正、负两种模式进行检测;源喷射电压在正、负模式下分别为3.5和3.0 kV;鞘气和辅助气均为氮气,流速分别为15和5 L/min;加热毛细管温度为350 ℃;扫描方式为一级和多级全扫描;分辨率为30 000;最大允许偏差为±5×10-6。
2 结果与讨论
本文采用HPLC-PDA-HRMS技术对马鞭草提取物的化学组分进行了分析和鉴定。通过综合分析化合物的色谱(见图1)及一级和多级质谱数据,分别采用ESI+和ESI-模式对样品进行检测,共检测到21种化合物,各化合物相关数据见表1和图2。
化合物1和2为环烯醚萜苷类化合物,分别为戟叶马鞭草苷和马鞭草苷。该类化合物在ESI+和ESI-模式下均有质谱响应,且在ESI+模式下易形成[M+Na]+峰(m/z427.120 8和411.125 9)和[2M+Na]+峰(m/z831.253 6和799.263 5),而在ESI-模式下易形成甲酸加合峰[M-H+CH3COOH]-(m/z463.145 2和447.150 3)。为进一步确定化合物结构,在ESI+模式下对化合物的准分子离子峰进行二级全扫描质谱分析,通过综合分析化合物的元素组成和碎片信息,确证化合物结构。如化合物1的[M+H]+峰(m/z405)产生的主要碎片离子m/z为243、225、207和193,与文献[14]报道一致。其中m/z243比m/z405少162,推测为糖苷键断裂脱掉1分子葡萄糖产生的碎片离子[M+H-C6H10O5]+;m/z225为m/z243脱掉1分子水形成的碎片离子[M+H-C6H12O6]+;m/z207为m/z225脱掉1分子水形成的碎片离子[M+H-C6H12O6-H2O]+,说明化合物1的苷元部分含有游离的羟基;m/z193为m/z225脱掉1分子甲醇形成的碎片离子[M+H-C6H12O6-CH3OH]+,说明苷元结构中含有甲氧基的结构单元。综上,确定化合物1为戟叶马鞭草苷。同理确定化合物2为马鞭草苷。

图 1 高效液相色谱-高分辨质谱联用检测马鞭草提取物的典型色谱图Fig. 1 Typical chromatograms of Verbena officinalis L. extract detected by HPLC-high resolution mass spectrometry (HRMS) a. detected by photodiode array (PDA) detector; b. detected by MS in ESI+mode; c. detected by MS in ESI- mode. Peak Nos.: 1. hastatoside; 2. verbenalin; 3. quercetin-3-O-glucoside; 4. verbascoside; 5. luteolin-7-O-glucoside; 6. isoverbascoside; 7. pedalitin-6-O-glucoside; 8. rosmarinic acid; 9. apigenin-7-O-glucoside; 10. 4′-hydroxyl wogonoside; 11. acacetin-7-O-rutinoside; 12. luteolin; 13. isorosmanol; 14. rosmanol; 15. 4′- hydroxyl wogonin; 16. apigenin; 17. carnosol; 18. barbinervic acid; 19. carnosic acid; 20. ursolic acid; 21. oleanolic acid.
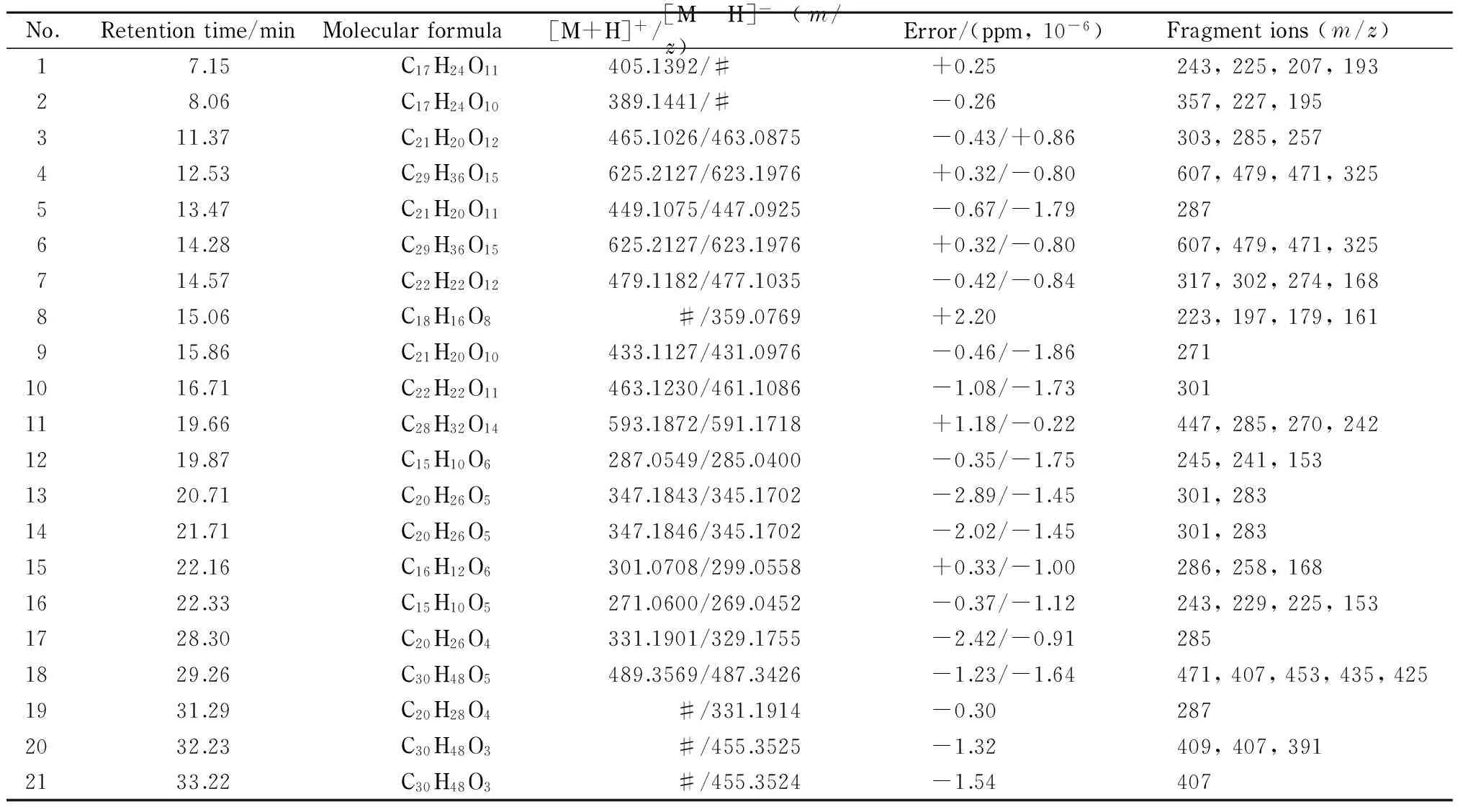
No.Retentiontime/minMolecularformula[M+H]+/[M-H]-(m/z)Error/(ppm,10-6)Fragmentions(m/z)17.15C17H24O11405.1392/#+0.25243,225,207,19328.06C17H24O10389.1441/#-0.26357,227,195311.37C21H20O12465.1026/463.0875-0.43/+0.86303,285,257412.53C29H36O15625.2127/623.1976+0.32/-0.80607,479,471,325513.47C21H20O11449.1075/447.0925-0.67/-1.79287614.28C29H36O15625.2127/623.1976+0.32/-0.80607,479,471,325714.57C22H22O12479.1182/477.1035-0.42/-0.84317,302,274,168815.06C18H16O8#/359.0769+2.20223,197,179,161915.86C21H20O10433.1127/431.0976-0.46/-1.862711016.71C22H22O11463.1230/461.1086-1.08/-1.733011119.66C28H32O14593.1872/591.1718+1.18/-0.22447,285,270,2421219.87C15H10O6287.0549/285.0400-0.35/-1.75245,241,1531320.71C20H26O5347.1843/345.1702-2.89/-1.45301,2831421.71C20H26O5347.1846/345.1702-2.02/-1.45301,2831522.16C16H12O6301.0708/299.0558+0.33/-1.00286,258,1681622.33C15H10O5271.0600/269.0452-0.37/-1.12243,229,225,1531728.30C20H26O4331.1901/329.1755-2.42/-0.912851829.26C30H48O5489.3569/487.3426-1.23/-1.64471,407,453,435,4251931.29C20H28O4#/331.1914-0.302872032.23C30H48O3#/455.3525-1.32409,407,3912133.22C30H48O3#/455.3524-1.54407
# not detected.
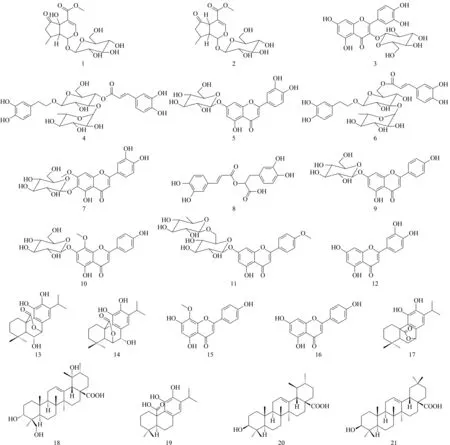
图 2 21种马鞭草提取物化学成分的结构式Fig. 2 Structural formulas of the 21 chemical compositions of Verbena officinalis L. extract 1-21 are the same as those in Fig. 1.
化合物3、5、7、9~12、15、16均为黄酮类化合物,其中化合物3、5、7、9~11均为黄酮苷类化合物,分别为槲皮素-3-O-葡萄糖苷、木犀草素-7-O-葡萄糖苷、胡麻黄素-6-O-葡萄糖苷、芹菜素-7-O-葡萄糖苷、4′-羟基汉黄芩苷和金合欢素-7-O-芸香糖苷;化合物12、15和16为黄酮苷元类化合物,分别为木犀草素、4′-羟基汉黄芩素和芹菜素。本文所检测到的9种黄酮类化合物在ESI+和ESI-模式下均有质谱响应,其中化合物11(金合欢素-7-O-芸香糖苷也称蒙花苷)在有关马鞭草提取物化学成分鉴定的文献中未见报道,因此本文将以化合物11为例阐述黄酮类化合物的结构推测过程。
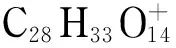

图 3 化合物11的质谱图Fig. 3 Mass spectra of compound 11

图 4 化合物11的质谱裂解途径Fig. 4 Mass spectral fragmentation pathways of compound 11


图 5 化合物13和14的质谱图Fig. 5 Mass spectra of compounds 13 and 14
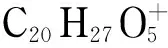

图 6 齐墩果酸对照品和化合物21的质谱图Fig. 6 Mass spectra of the oleanolic acid reference substance and compound 21
其余化合物的结构推测过程见补充材料(http://www.chrom-China.com/UserFiles/File/170 5010-S1.pdf)。
综上,本研究采用HPLC-HRMS技术分别在ESI+和ESI-模式下对马鞭草提取物的化学组分进行了分析和鉴定。在ESI+模式下检测到17种化合物,在ESI-模式下检测到19种化合物,其中15种化合物在ESI+和ESI-两种模式下均有质谱响应。综合ESI+和ESI-两种检测模式下的结果,在马鞭草提取物中共检测到21种化合物:2种环烯醚萜苷类分别马鞭草苷和戟叶马鞭草苷;9种黄酮类化合物分别为木犀草素、木犀草素-7-O-葡萄糖苷、芹菜素、芹菜素-7-O-葡萄糖苷、4′-羟基汉黄芩素、4′-羟基汉黄芩苷、槲皮素-3-O-葡萄糖苷、胡麻黄素-6-O-葡萄糖苷和金合欢素-7-O-芸香糖苷;3种三萜类化合物分别为熊果酸、齐墩果酸和马尾柴酸;2种苯乙醇苷类分别为毛蕊花糖苷和异毛蕊花糖苷;5种二萜酚类分别为鼠尾草酚、鼠尾草酸、迷迭香酚、异迷迭香酚和迷迭香酸。其中6种化合物并未在其他有关马鞭草提取物鉴定的文献中出现,分别为鼠尾草酚、鼠尾草酸、迷迭香酚、异迷迭香酚、迷迭香酸和金合欢素-7-O-芸香糖苷。
3 结论
采用HPLC-PDA-HRMS技术鉴定马鞭草提取物中的化学成分,既利用了色谱的分离技术又结合了质谱的高选择性和较强的结构鉴别能力,具有分离速度快、检测效率高、准确性好等优点。用该方法共检测出马鞭草提取物中的21种化合物,并对每种化合物进行多级全扫描质谱分析,使所推测化合物的结构得到了进一步的确证。该方法操作简便、快速高效、准确可靠,可作为马鞭草药材鉴别和质量控制的有效方法。
致谢
感谢大连医科大学第一附属医院中药剂科李永杰对本研究中所使用的中药材马鞭草的鉴定。
[1] Zhang T, Ruan J L, Lü Z M, et al. China Journal of Chinese Materia Medica, 2000, 25(11): 676
张涛, 阮金兰, 吕子敏. 中国中药杂志, 2000, 25(11): 676
[2] Lai S W, Yu M S, Yuen W H, et al. Neuropharmacol, 2006, 50(6): 641
[3] Calvo M I. J Ethnopharmacol, 2006, 107(3): 380
[4] Yang H G, Fang L H, Du G H, et al. Chinese Pharmaceutical Journal, 2013, 48(12): 949
杨海光, 方莲花, 杜冠华, 等. 中国药学杂志, 2013, 48(12): 949
[5] Tian J, Zhao Y M, Luan X H, et al. China Journal of Chinese Materia Medica, 2005, 30(4): 268
田菁, 赵毅民, 栾新慧, 等. 中国中药杂志, 2005, 30(4): 268
[6] Chen G M, Zhang J Y, Zhang X P, et al. Chinese Medicinal Materials, 2006, 29(7): 677
陈改敏, 张建业, 张向沛, 等. 中药材, 2006, 29(7): 677
[7] Zhang Y X. [MS Dissertation]. Shanghai: Shanghai Jiao Tong University, 2010
张玉雪. [硕士论文]. 上海: 上海交通大学, 2010
[8] Liu H M, Bao F Y, Yan X B, et al. Chinese Traditional and Herbal Drugs, 2002, 33(6): 492
刘宏民, 鲍峰玉, 阎学斌, 等. 中草药, 2002, 33(6): 492
[9] Xin F, Jin Y S, Sha Y, et al. Modern Chinese Medicine, 2008, 10(10): 21
辛菲, 金艺淑, 沙沂, 等. 中国现代中药, 2008, 10(10): 21
[10] Encalada M A, Rehecho S, Ansorena D. LWT-Food Sci Technol, 2015, 63(2): 1016
[11] Rehecho S, Hidalgo O, De Cirano M G I. LWT-Food Sci Technol, 2011, 44(4): 875
[12] Han F, Li Y, Zhang X. Inter J Mass Spec, 2016, 405: 32
[13] Lai J P, Lim Y H, Su J, et al. J Chromatogr B, 2007, 848(2): 215
[14] Wang H, Ren F, Duan K F, et al. Modern Journal of Integrated Traditional Chinese and Western Medicine, 2015, 24(3): 235
王华, 任非, 段坤峰. 现代中西医结合杂志, 2015, 24(3): 235
[15] Wojakowska A, Piasecka A, García-López P M. Phytochemistry, 2013, 92: 71
[16] Chen W, Shen T T, Li Y Z, et al. Food Industry, 2015, 36(1): 287
陈文, 申婷婷, 李雨竹, 等. 食品工业, 2015, 36(1): 287
[17] Zhang Y, Smuts J P, Dodbiba E. J Agri Food Chem, 2012, 60(36): 9305
[18] Kumar S, Chandra P, Bajpai V, et al. Indus Crops Products, 2015, 69: 143
[19] Kim E, Noh K, Lee S J, et al. J Pharm Biomed Anal, 2016, 118: 96
[20] Kontogianni V G, Exarchou V, Troganis A, et al. Anal Chimica Acta, 2009, 635(2): 188
Identification of the chemical compositionsofVerbenaofficinalisL. extract by high performance liquid chromatography-photodiode array-high resolution mass spectrometry
SUN Yuming1, WANG Yueyue1, CAI Rui1, ZHANG Hua1, WANG Yulin2*
(1. School of Chemical Engineering, Dalian University of Technology, Dalian 116024, China;2. Basic Medical College, Dalian Medical University, Dalian 116044, China)
To investigate the main chemical compositions ofVerbenaofficinalsL. extract, a qualitative high performance liquid chromatography-photodiode array-high resolution mass spectrometry (HPLC-PDA-HRMS) method was established. The structures of the compounds detected were identified by analyzing the chromatographic profiles and the corresponding mass spectra obtained by full scan and MSnfull scan. Twenty one compounds including iridoid glycosides, flavonoids, triterpenoids, phenylpropanoids and phenolic diterpenoids were identified, and six of them were not reported in other literatures aboutVerbenaofficinalisL. extract, such as carnosic acid, carnosol, rosmanol, isorosmanol, rosmarinic acid and acacetin-7-O-rutinoside. This method is simple, rapid, accurate and sensitive. It provides a reliable scientific basis for the identification of the authenticity and quality control of Chinese medicinal materials.
high performance liquid chromatography (HPLC); photodiode array detection; high resolution mass spectrometry (HRMS); mass fragmentation; structure identification;VerbenaofficinalisL.; extract
10.3724/SP.J.1123.2017.05010
2017-05-19
.E-mail:wangyulin1971@126.com.
O658
A
1000-8713(2017)09-0987-08
*
猜你喜欢
杂志排行
色谱的其它文章
- 超高效液相色谱-四极杆-飞行时间质谱法快速筛查姜和葱中44种农药残留
- Separation and purification of acteoside from Rehmanniaglutinosa by combining macroporous resin with high-speed countercurrent chromatography
- Preparation of filter paper with chiral separation function by oxidation and Schiff-base reaction
- 气相色谱法测定及预测有机磷阻燃剂的蒸气压
- 固相萃取-超高效液相色谱-高分辨质谱法快速测定食用油中4种酚类环境雌激素残留
- 《色谱》论文中可直接使用的缩略词
