一种改良诊断量表在急性药物性肝损伤诊断中的应用
2017-08-07仇丽霞范作鹏刘义荣胡中杰
仇丽霞, 范作鹏, 刘 颖, 梁 珊, 聂 巍, 林 伟, 刘义荣, 张 晶, 胡中杰
(首都医科大学附属北京佑安医院 丙肝与中毒性肝病科, 北京 100069)
一种改良诊断量表在急性药物性肝损伤诊断中的应用
仇丽霞, 范作鹏, 刘 颖, 梁 珊, 聂 巍, 林 伟, 刘义荣, 张 晶, 胡中杰
(首都医科大学附属北京佑安医院 丙肝与中毒性肝病科, 北京 100069)
目的 建立一种急性药物性肝损伤(DILI)的改良诊断量表并在临床验证使用。方法 收集2011年1月-2015年12月在首都医科大学附属北京佑安医院治疗的82例急性DILI患者,其中DILI组52例,非DILI组30例。在Roussel Uclaf因果关系评价表(RUCAM)基础上,参考DDW-J量表,新增“中药单药或成药有肝损伤的报道”、“嗜酸性粒细胞计数”和“基于CCK-8法的药物淋巴细胞刺激试验”3个参数,建立一种改良诊断量表。对2组患者的每种可疑药物分别进行RUCAM和改良诊断量表评分,验证新量表对DILI诊断的敏感度和特异度。计数资料组间比较采用χ2检验。结果 DILI组共75个可疑药物;非DILI组共41个可疑药物。与RUCAM相比,改良诊断量表可将DILI组中评估为“高度可能”和“很可能”的诊断敏感度由74.7%提高至94.7%(χ2=11.554,P=0.001);而非DILI组只有2个药物(4.9%)的评估结果由“可能”变为“很可能”,其余药物均维持“可能”、“不太可能”和“可除外”,诊断特异度由100%降至95.1%(χ2=0.512,P=0.474)。 结论 建立了一种急性DILI的改良诊断量表,与RUCAM相比,诊断敏感度提高,特异度有所降低,可在临床中进一步验证使用。
药物性肝损伤; 诊断量表
笔者前期采用细胞计数试剂盒(cell counting kit-8,CCK-8)细胞计数法取代3H-脱氧胸苷(3Hydrogen -thymine deoxyriboside,3H-TdR)摄取率的检测,建立了一种基于CCK-8法的药物淋巴细胞刺激试验(drug lymphocyte stimulation test,DLST)[1],为将DLST引入药物性肝损伤(drug-induced liver injury,DILI)诊断量表创造了条件。本研究在Roussel Uclaf因果关系评价表(Roussel Uclaf causality assessment method,RUCAM)[2]的基础上,参考DDW-J量表[3],加入基于CCK-8法的DLST、嗜酸性粒细胞计数,并结合我国中药使用较多的情况,加入中药有关肝损伤报道的参数,建立一种更符合我国国情的诊断量表,并初步验证其有效性。
1 资料与方法
1.1 研究对象 收集2011年1月-2015年12月在本院住院治疗,入院时有肝损伤,且在3个月内有药物服用史,临床拟诊为“急性药物性肝损伤”的患者,年龄18~85岁,性别不限。由2名具备主任医师职称的肝病专业临床医师和1名病理专业医师组成病例评判小组,在临床资料完善后,采用专家共识意见的方法[4],对病例资料进行综合评估,对可能的原因进行全面综合性评价,并参考我国《药物性肝损伤诊治指南》[5]中的诊断标准和RUCAM[2,6]进行评判。排除恶性肿瘤、吸毒、临床资料不全、服用中医汤药或不能提供所用药物以及不能完成基于CCK-8法的患者。入选病例经病例评判小组评判后,临床诊断为急性DILI者进入“DILI组”,临床排除DILI者进入“非DILI组”。
1.2 研究方法
1.2.1 基于CCK-8法的DLST 对入选患者的每种可疑药物分别进行基于CCK-8法的DLST,实验步骤简述如下:取患者所用可疑药物制备实验药物备用。采用密度梯度离心法分离患者外周血单个核细胞(PBMC),PBS洗涤后,重悬于2 ml RPMI-1640培养液(含10% FBS+青链霉素)并计数,调整细胞浓度加入96孔板中(每孔1×105细胞/100 μl),再加入刺激药物5 μl。设置阴性对照孔(相同浓度的药物溶解介质+培养液+细胞)、阳性对照孔(植物血凝素 5 μg/ml+培养液+细胞)和调零孔(仅培养液),均设3个复孔。同时设立健康对照组。将培养板置于37 ℃,5% CO2培养箱培养60 h,随后向每孔加入10 μl CCK-8溶液,继续培养12 h后,用酶标仪测定各孔在450 nm处的吸光度(OD),计算刺激指数(stimulation index,SI),SI=(刺激孔OD-调零孔OD)/(阴性对照孔OD-调零孔OD),结果判断:SI≥1.8为DLST阳性。如果阳性对照的SI<1.8,或3个复孔的偏差过大,则判定该药物的DLST结果不可靠,结果不可靠或药物的SI<1.8均判定该药的DLST阴性。
1.2.2 改良诊断量表评分 改良诊断量表评分是在RUCAM评分基础上,参考DDW-J量表,新增3个参数:(1)将“药物既往肝损伤的报道”分为西药和中药2类,西药的赋分不变。新增中药单药或成药有肝损伤的报道,加2分;中药单药或成药无肝损伤的报道,0分。(2)新增基于CCK-8法的DLST。DLST阳性,加2分;DLST阴性或未做,0分。(3)新增嗜酸性粒细胞计数。≥6%,加1分;<6%,0分。结果判断保持不变,>8分:极可能;6~8分:很可能;3~5分:可能;1~2分:不太可能;≤0:可除外。
1.2.3 RUCAM评分和改良诊断量表评分 对入选患者的每种药物分别进行RUCAM评分和改良诊断量表评分,比较两种评分方法对急性DILI诊断的敏感度和特异度。
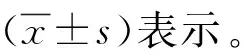
2 结果
2.1 一般资料 共筛选168例疑似急性DILI患者,82例符合入选标准纳入本研究,其中DILI组52例,非DILI组30例。DILI组共75个可疑药物,经基于CCK-8法的DLST检测,48例70个药物结果可靠,19例22个药物DLST阳性。非DILI组共41个可疑药物,经基于CCK-8法的DLST检测,3例3个药物DLST阳性。
DILI组有13例患者进行了肝穿刺病理学检查,支持DILI的诊断;非DILI组均发现了导致肝损伤的其他病因,最多见的是HBV感染(56.7%),其次是HCV或HEV感染,均未进行肝穿刺病理学检查。病例入选情况和一般资料见表1。
2.2 将中药、嗜酸性粒细胞、DLST参数引入RUCAM对DILI诊断敏感度的影响 对DILI组的75个药物分别进行RUCAM评分,13例>8分,43例为6~8分,19例为3~5分。分别加入中药、嗜酸性粒细胞和DLST参数后,均可将评估结果为“极可能”和“很可能”的药物比例提高,尤其以加入DLST参数后更为明显。将3个参数均加入的改良诊断量表可将DILI诊断的敏感度由74.7%提高至94.7%(χ2=11.554,P=0.001)(图1)。
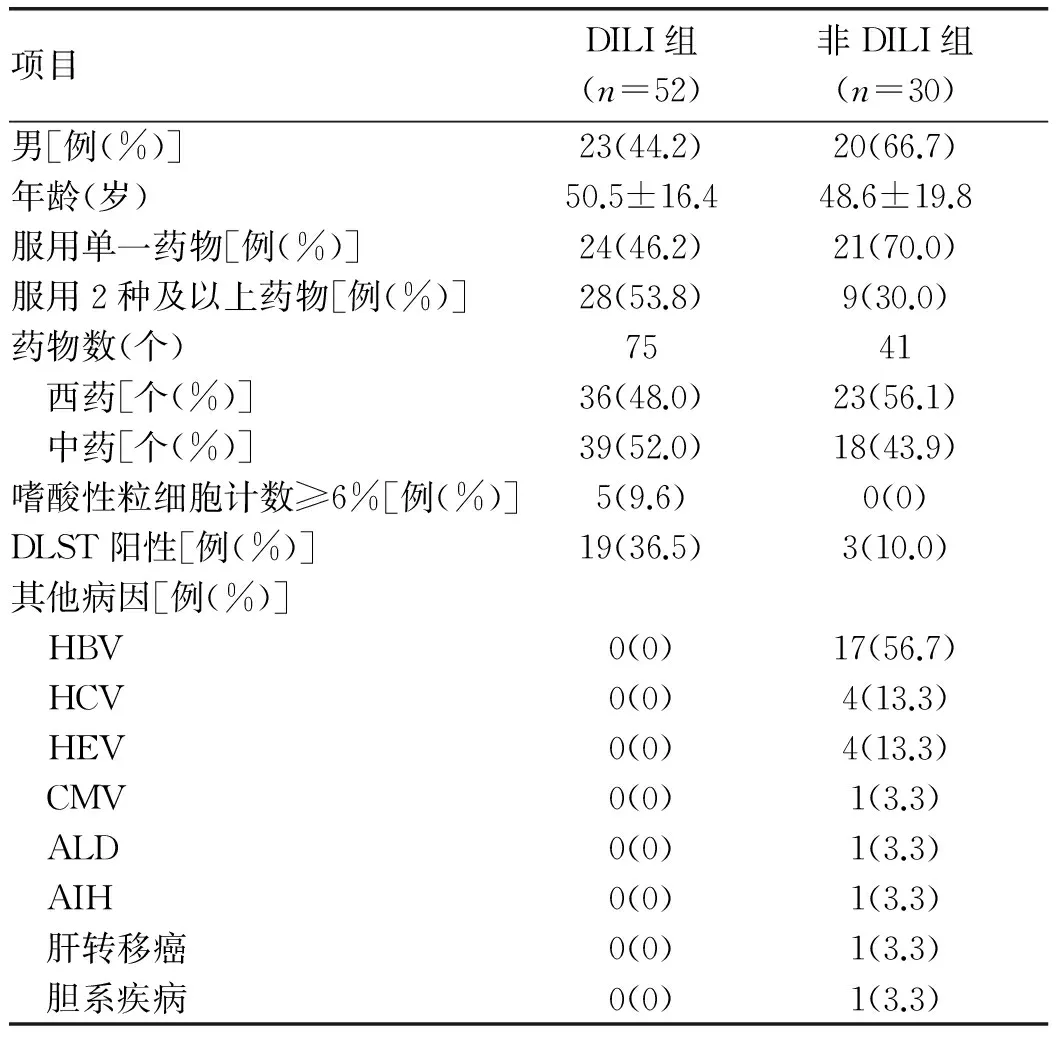
表1 病例入选情况和一般资料
注:CMV,巨细胞病毒;ALD,酒精性肝病;AIH,自身免疫性肝炎
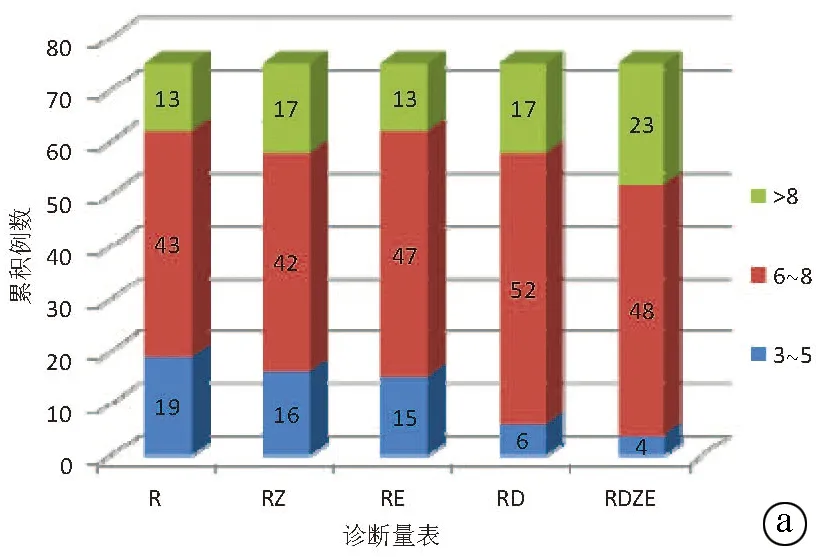
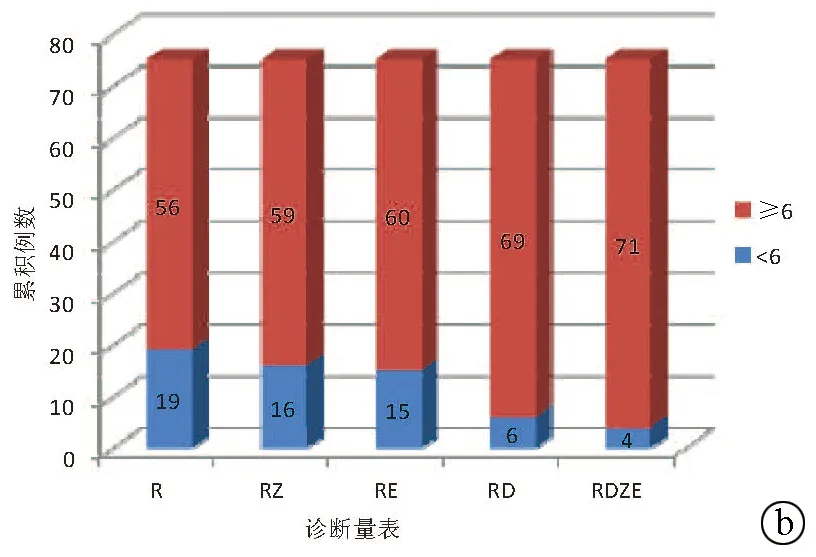
图1 中药、嗜酸性粒细胞、DLST参数引入RUCAM对DILI诊断敏感度的影响 a:结果按>8分(极可能)、6~8分(很可能)、3~5分(可能)分类;b: 结果按是否≥6分类;R:RUCAM;RZ:RUCAM+中药参数;RE:RUCAM+嗜酸性粒细胞参数;RD:RUCAM+DLST参数;RDZE:RUCAM+中药、嗜酸性粒细胞、DLST参数(改良诊断量表)
2.3 将中药、嗜酸性粒细胞、DLST参数引入RUCAM对DILI诊断特异度的影响 对非DILI组的41个药物分别进行RUCAM评分,10例为3~5分,26例为1~2分,5例为<1分。分别加入中药、嗜酸性粒细胞参数后,仍无药物的评分结果为“极可能”和“很可能”,在加入DLST参数后,有2个药物的评分≥6分。将3个参数均加入的改良诊断量表仍只有2个药物(4.9%)的评估结果变为“很可能”,其余药物均维持“可能”、“不太可能”和“可除外”,诊断特异度由100%降至95.1%(χ2=0.512,P=0.474)(图2)。
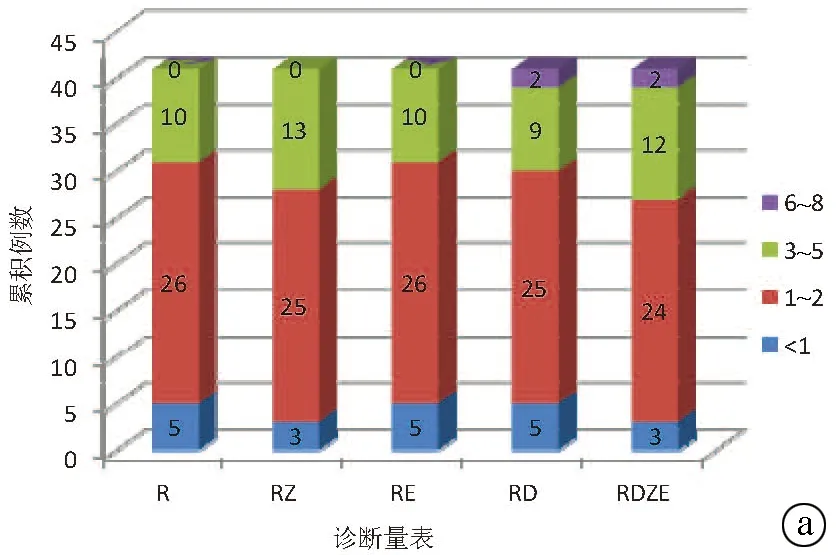
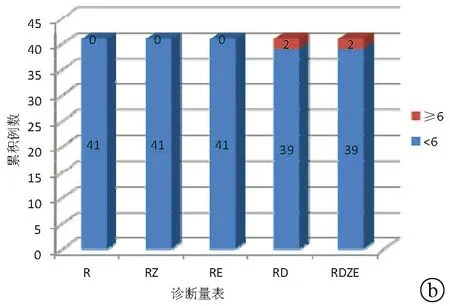
图2 中药、嗜酸性粒细胞、DLST参数引入RUCAM对DILI诊断特异度的影响 a: 结果按6~8分(很可能)、3~5分(可能)、1~2分(不太可能)、<1分(可除外)分类;b: 结果按是否≥6分类
3 讨论
急性DILl的诊断目前仍是一种主观的临床诊断,缺乏特异性诊断标志物。近30年来,先后建立了一些临床诊断量表用于药物与肝损伤的因果关系评估,如Naranjo药物不良反应可能性量表[7]、RUCAM、Maria & Victorino临床诊断量表[8]等,但临床使用均不够充分[9]。其原因在于这些量表诊断参数比较复杂,有些概念界定模糊,临床可操作性欠佳。其中RUCAM被认为是当前设计最合理、要素最全面、操作最方便、诊断准确率相对较高的诊断工具,在科学研究和临床实践中得到了广泛的应用,也得到了我国专家的推荐,但其诊断的敏感度有待进一步提高。另外,即使诊断量表评分结果强烈怀疑肝损伤和药物相关,仍难以从众多可疑药物中鉴别出真正引起DILI的药物。因此,在2004年的日本消化疾病周上,DDW-J改良量表引入了DLST,使改良量表的敏感度较RUCAM显著提高,且能针对患者服用的每个可疑药物分别进行DLST和评分。但由于DLST需要使用3H-TdR,需具备专门的放射性同位素实验室,故限制了它的临床使用。笔者研究团队前期建立了一种基于CCK-8法的DLST,实验要求更低,为将DLST引入DILI诊断量表创造了条件。因此,本研究参考DDW-J量表,在RUCAM的基础上,加入了基于CCK-8法的DLST和嗜酸性粒细胞的参数。
另外,考虑到现有量表均为国外引入,对中草药导致肝损伤的考虑不够,如RUCAM的“药物既往肝损伤的报道”中,只有肝损伤反应已在产品说明中标明才能加2分,如果未在产品说明中标明,即使有较多肝损伤的报道,也只能加1分。而我国中成药的说明中,大部分不良反应为“尚不明确”,导致中草药的权重偏低,而中草药在我国DILI的发生中占有重要的地位,在部分地区甚至是第一位的原因[10],有必要加强中草药在量表中的权重。因此,新诊断量表中,将“药物既往肝损伤的报道”分为西药和中药2类,西药的赋分不变,中药单药或成药如果有肝损伤的报道,直接加2分,无论是否在药品说明中标明。
在加入中药、嗜酸性粒细胞和DLST参数后,必将使评分结果升高,由于结果判断标准保持不变,新诊断量表评估为“极可能”和“很可能”的药物比例将有所提高,结果也正是如此,新量表诊断DILI的敏感度由RUCAM的74.7%提高到了94.7%。在诊断敏感度提高的同时,有可能导致特异度的降低,在对非DILI组的41个药物的验证评分中,有2例患者2个药物的评分结果由RUCAM的4分提高到了新量表的6分。1例患者服用十一酸睾酮,发现有HEV感染;另1例患者服用阿奇霉素,发现有HBV感染。其余39个药物的评分均在6分以下,提示新量表的诊断特异度可保持在95.0%以上。
本研究是对新诊断量表的初步验证,病例数和药物数尚显不足,对中药有肝损伤的报道是否需要进一步设定标准,对各参数的权重、对评分结果的评判是否需要进一步调整,还有待进一步的研究和更多病例的验证。总之,本研究建立了一个急性DILI的改良诊断量表,与RUCAM相比,新量表可将急性DILI的诊断敏感度由74.7%提高至94.7%,尽管特异度有所降低,但仍可达95.1%,可在临床中进一步验证使用。
[1] FAN ZP, LIANG S, NIE W, et al. The application of a novel drug lymphocyte stimulation test using Cell Counting Kit-8 assay in diagnosis of drug-induced liver injury[J]. J Clin Hepatol, 2016, 32(8): 1562-1565. (in Chinese) 范作鹏, 梁珊, 聂巍, 等. 基于细胞计数试剂盒8的药物淋巴细胞刺激试验在急性药物性肝损伤诊断中的应用[J]. 临床肝胆病杂志, 2016, 32(8): 1562-1565.
[2] DANAN G, BENICHOU C. Causality assessment of adverse reactions to drugs——I. A novel method based on the conclusions of international consensus meetings: application to drug-induced liver injuries[J]. J Clin Epidemiol, 1993, 46(11): 1323-1330.
[3] WATANABE M, SHIBUYA A.Validity study of a new diagnostic scale for drug-induced liver injury in Japan-comparison with two previous scales[J]. Hepatol Res, 2004, 30(3): 148-154.
[4] CHALASANI NP, HAYASHI PH, BONKOVSKY HL, et al. ACG Clinical Guideline: the diagnosis and management of idiosyncratic drug-induced liver injury[J]. Am J Gastroenterol, 2014, 109(7): 950-966.[5] Drug-induced Liver Disease Study Group, Chinese Society of Hepatology, Chinese Medical Association. Guidelines for the management of drug-induced liver injury[J]. J Clin Hepatol, 2015, 31(11): 1752-1769. (in Chinese) 中华医学会肝病学分会药物性肝病学组. 药物性肝损伤诊治指南[J]. 临床肝胆病杂志, 2015, 31(11): 1752-1769.
[6] HAO KY, YU YC, HE CL.RUCAM sacle-based diagnosis, clinical features and prognosis of 140 cases of drug-induced liver injury[J]. Chin J Hepatol, 2014, 22(12): 938-941. (in Chinese) 郝坤艳, 于乐成, 何长伦. 基于Roussel uclaf因果关系评估量表的药物性肝损伤140例诊治分析[J].中华肝脏病杂志, 2014, 22(12): 938-941.
[7] NARANJO CA, BUSTO U, SELLERS EM, et al. A method for estimating the probability of adverse drug reactions[J]. Clin Pharmacol Ther, 1981, 30(2): 239-245.
[8] MARIA VA, VICTORINO RM. Development and validation of a clinical scale for the diagnosis of drug-induced hepatitis[J]. Hepatology, 1997, 26(3): 664-669.
[9] TAJIRI K, SHIMIZU Y. Practical guidelines for diagnosis and early management of drug-induced liver injury[J]. World J Gastroenterol, 2008, 14(44): 6774-6785.
[10] JIANG WH, SHI XH, LIANG WF, et al. Clinical analysis of 124 patients with drug - induced hepatitis[J].Chin J Med, 2012, 47(6): 58-59. (in Chinese) 江文华, 石晓红, 梁伟峰, 等. 药物性肝炎124例临床分析[J]. 中国医刊, 2012, 47(6): 58-59.
引证本文:QIU LX, FAN ZP, LIU Y, et al. Application of a modified diagnostic scale in diagnosis of acute drug-induced liver injury[J]. J Clin Hepatol, 2017, 33(7): 1328-1331. (in Chinese) 仇丽霞, 范作鹏, 刘颖, 等. 一种改良诊断量表在急性药物性肝损伤诊断中的应用[J]. 临床肝胆病杂志, 2017, 33(7): 1328-1331.
(本文编辑:林 姣)
Application of a modified diagnostic scale in diagnosis of acute drug-induced liver injury
QIULixia,FANZuopeng,LIUYing,etal.
(DepartmentofHepatitisC&ToxicLiverDiseases,BeijingYouAnHospital,CapitalMedicalUniversity,Beijing100069,China)
Objective To investigate the application of a modified diagnostic scale in the diagnosis of acute drug-induced liver injury (DILI). Methods A total of 82 patients with acute DILI who were treated in Beijing YouAn Hospital, Capital Medical University from January 2011 to December 2015 were enrolled, among whom 52 were enrolled in DILI group and 30 were enrolled in non-DILI group. On the basis of Roussel Uclaf Causality Assessment Method (RUCAM) scale and with reference to Digestive Disease Week Japan scale, three parameters, i.e., “report of liver injury induced by single Chinese materia medica or Chinese patent medicine”, “eosinophil count”, and “drug lymphocyte stimulation test based on Cell Counting Kit-8”, were added to establish a modified diagnostic scale. The RUCAM scale and the modified diagnostic scale were used to evaluate each suspected drug to verify the sensitivity and specificity of this new scale in the diagnosis of DILI. The chi-square test was used for comparison of categorical data between groups. Results There were 75 suspected drugs in the DILI group and 41 suspected drugs in the non-DILI group. Compared with the RUCAM scale, the modified diagnostic scale increased the number of drugs evaluated as “highly probable” and “probable” from 74.7% to 94.7% (χ2=11.554,P=0.001) in the DILI group. In the non-DILI group, only 2 drugs (4.9%) were changed from “possible” to “probable”, and the other drugs were maintained as “possible”, “unlikely”, or “excluded”; the specificity of diagnosis was reduced from 100% to 95.1% (χ2=0.512,P=0.474). Conclusion Compared with the RUCAM scale, this modified diagnostic scale has an increased sensitivity and a reduced specificity of diagnosis and needs to be further validated in clinical practice.
drug-induced liver injury; diagnostic scale
10.3969/j.issn.1001-5256.2017.07.025
2017-01-13;
2017-01-25。
中国肝炎防治基金会天晴肝病研究基金(TQGB20140052);中国初级保健基金会佑安肝病艾滋病基金(YNKT20160016)
仇丽霞(1982-),女,主治医师,博士,主要从事肝脏疾病的临床和基础研究。
胡中杰,电子信箱: yfcyt@139.com;
R575
A
1001-5256(2017)07-1328-04
张晶,电子信箱: drzhangjing@163.com。
