煎炸和焙烤过程中油脂对丙烯酰胺形成影响研究进展
2017-08-07王鹏璞朱雨辰刘炎冰陈伟娜胡小松
王鹏璞 朱雨辰 刘炎冰 陈伟娜 胡小松 陈 芳
(中国农业大学食品科学与营养工程学院;国家果蔬加工工程技术研究中心;农业部果蔬加工重点实验室;教育部果蔬加工工程技术研究中心,北京 100083)
煎炸和焙烤过程中油脂对丙烯酰胺形成影响研究进展
王鹏璞 朱雨辰 刘炎冰 陈伟娜 胡小松 陈 芳
(中国农业大学食品科学与营养工程学院;国家果蔬加工工程技术研究中心;农业部果蔬加工重点实验室;教育部果蔬加工工程技术研究中心,北京 100083)
丙烯酰胺是一种对人有神经毒性和潜在致癌性的化合物,自2002年被报道在一些高温加工的淀粉类食品中有较高含量后,引起各国学者的广泛研究。综述了煎炸和焙烤食物加工过程中油脂对丙烯酰胺形成的影响,主要包括油炸食品加工参数、油脂种类、油脂氧化和抗氧化剂对丙烯酰胺形成的影响,以及油脂热解产物对丙烯酰胺形成的影响及其可能机制。同时展望了今后的研究方向,旨在为从油脂角度控制丙烯酰胺的形成提供参考。
丙烯酰胺 油脂 煎炸 焙烤
2002年4月,瑞典国家食品管理局和斯德哥尔摩大学共同宣布在一些经高温(>120 ℃)加工或焙烤的淀粉类食品中有较高含量的丙烯酰胺[1],并且其远超世界卫生组织规定的饮用水中丙烯酰胺的最大允许量0.5 μg/L[2]。瑞典的这一发现很快被英国食品标准局所证实[3],并且迅速引起了世界卫生组织和美国食品药品管理局以及世界各地科学家的重视。原因是丙烯酰胺在1994年被国际癌症研究中心列为2A类致癌物[4];对人和动物都具有神经毒性[5],对动物具有生殖毒性[6]、致突变性和潜在的致癌性[7]。
丙烯酰胺是一种不饱和酰胺,CAS编号为79-06-1,相对分子质量71.08,化学式CH2CHCONH2,
沸点125 ℃,熔点82~86 ℃,密度1.122 g/cm3(30 ℃)。常温下为白色无味晶体,易溶于水、乙醇、乙醚、丙酮、氯仿,不溶于苯及庚烷中。结构式见图1。
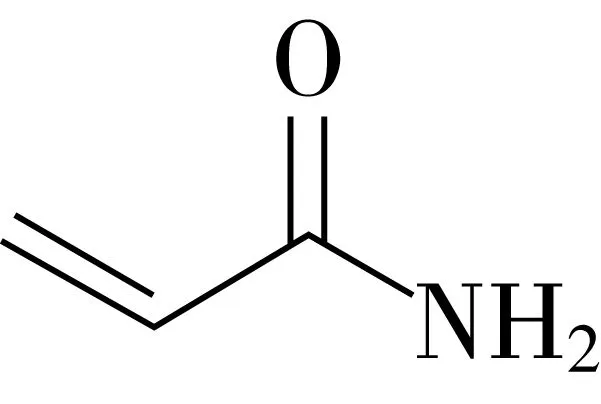
图1 丙烯酰胺的结构式
目前普遍认为在富含淀粉的食物中丙烯酰胺主要通过天冬酰胺和还原糖发生美拉德反应形成[8-10]。但由于富含油脂的食物在热加工过程中往往伴随油脂的氧化和水解等反应,近几年的研究表明油脂热解产物对丙烯酰胺的形成同样具有贡献,本文将总结煎炸和焙烤食物加工过程中油脂对丙烯酰胺形成的影响。
1 油炸食品加工参数对丙烯酰胺形成的影响
动力学研究表明无论是在模拟体系还是在实际体系中,油炸温度和时间是影响终产物中丙烯酰胺含量的重要因素[11-14]。Knol等[11]用等量的葡萄糖和天冬酰胺在密闭条件下进行不同温度加热,结果如图2所示,在反应5 min之内,丙烯酰胺大量形成,当温度高于120 ℃时,每升高20 ℃,丙烯酰胺形成量成倍数增加。作者通过用阿伦尼乌斯方程计算,表明温度通过影响反应速率和活化能来影响丙烯酰胺的形成。温度低于160 ℃时,45 min内丙烯酰胺含量随加热时间延长先增加,后趋于平稳,温度高于160 ℃时,丙烯酰胺含量随加热时间延长先剧烈增加后减小,最后趋于平稳。油炸时间对丙烯酰胺含量的影响与油炸温度有关,Knol等[13]在预热到180 ℃的油中加入鲜切土豆片炸6 min,对油炸过程中的油温、薯片外层温度以及二者之差进行实时监测,结果如图3所示,在第35 s时,薯片外层温度上升到140 ℃,之后释放水蒸气,温度降到135 ℃,到210 s时,温度上升到160 ℃趋于平稳,这个过程中锅底的油温从180 ℃逐渐下降,一直到160 ℃趋于平稳。

图2 不同温度加热对葡萄糖/天冬酰胺模拟体系(0.2 mol/L, pH 6.8)中丙烯酰胺形成的影响

图3 油炸马铃薯片过程中油温的温度轮廓
研究表明植物油煎炸次数越多,由甘油三酯降解和聚合形成的极性化合物越多[15]。Gertz等[16]认为极性化合物通过增加油脂和食物间的热传递增加丙烯酰胺含量,但后来有学者通过油炸薯片试验证明油炸过程中形成的极性化合物量和植物油煎炸次数与薯片中丙烯酰胺含量均无显著相关性(P>0.05)[17-18]。目前关于植物油煎炸次数对丙烯酰胺含量的影响尚不清楚。
2 油脂种类对丙烯酰胺形成的影响
目前对于油脂种类对丙烯酰胺形成的影响存在一定争议。有研究报道油脂种类不同,其产物中丙烯酰胺含量有显著差异。Becalski 等[19]在模拟炸薯片试验中,分别以橄榄油和玉米油为煎炸介质,结果经橄榄油煎炸的薯片中丙烯酰胺含量比经玉米油煎炸的高。Tareke[20]也报道了与玉米油和橄榄油相比,薯片在芝麻油中经过煎炸后形成的丙烯酰胺含量最高。由于不同种类油脂的不饱和度有差异,而油脂的不饱和度越高,产生的丙烯酰胺越多[21]。Ehling 等[21]将天冬酰胺与鱼肝油、沙丁鱼油、脱α-生育酚的玉米油、橄榄油、菜籽油、大豆油、玉米油、牛油和猪油分别在180 ℃油浴下加热30 min,形成丙烯酰胺含量从高到底的顺序为沙丁鱼油(642 μg/g 天冬酰胺)>鱼肝油(435.4 μg/g)>大豆油(135.8 μg/g)>玉米油(80.7 μg/g)>橄榄油(73.6 μg/g)>菜籽油(70.7 μg/g)>脱α-生育酚的玉米油(62.1 μg/g)>牛油(59.3 μg/g)>猪油(36.0μg/g)。沙丁鱼油和鱼肝油因富含高度不饱和脂肪酸而产生丙烯酰胺最多;大豆油中富含亚麻酸,其体系也会产生较多丙烯酰胺;但猪油和牛油中含有的不饱和脂肪较少,其体系产生丙烯酰胺量最少;玉米油中既有单不饱和脂肪又有多不饱和脂肪,比主要含单不饱和脂肪的菜籽油和橄榄油体系形成的丙烯酰胺量多。Capuano 等[22]在180 ℃条件下模拟曲奇焙烤试验中也得出了相同的结论,棕榈油(碘值为110)体系中形成的丙烯酰胺量显著低于葵花籽油(碘值>130)体系。一些实际油炸制品体系中煎炸油种类与丙烯酰胺形成关系的研究结果都与上述结论一致[23-24]。不饱和度不同的油脂对丙烯酰胺形成的影响,可能因为其中含有的甘油三酸酯量不同而异,高甘油三酸酯含量水解产生大量甘油,进而产生更多丙烯醛和丙烯酰胺[25]。
也有一部分研究报道指出,油脂种类对丙烯酰胺形成无影响。Matthäus 等[26]将土豆片分别在精炼葵花籽油、冷压榨葵花籽油、亚麻荠油、花生油、棕榈油、半固体深度煎炸脂肪、冷压榨菜籽油、精炼菜籽油、Biskin和Pomfrim中175 ℃煎炸6 min,结果表明不同食物油与丙烯酰胺的浓度无显著相关(P>0.05)。同样地,Mestdagh等[27]和Williams[28]用不同植物油分别煎炸薯片,发现不同煎炸油中薯片丙烯酰胺含量差异不显著(P>0.05)。这在焙烤曲奇和牛肉汉堡这样的实际体系中也得到了证实[29-30]。
3 油脂氧化对丙烯酰胺形成的影响
油炸过程就是在高温下将食物浸在油中,油中的高温为食物提供热量,使得食物表面温度升高,食物内部的水分迅速汽化并且从食物内部向食物外部转移,同时食物内部孔隙被煎炸油取代的过程[31]。油脂在煎炸过程中经过长时间的高温加热,会发生一系列的化学变化,其中最主要的是油脂氧化、水解和聚合反应[32]。有研究报道油脂氧化会促进丙烯酰胺的形成。Arribas-Lorenzo 等[33]在曲奇体系中,以未氧化葵花籽油做对照,探讨了经热氧化的葵花籽油对丙烯酰胺生成量的影响。结果表明,曲奇中丙烯酰胺含量随焙烤时间延长而增加,且在第16 min时试验组中丙烯酰胺含量比对照组高出约59%。进一步说明随焙烤时间延长,油脂热氧化会大幅促进曲奇体系中丙烯酰胺的形成。Capuano 等[22]在模拟曲奇焙烤的无糖试验中也得出了相同的结论。作者将不同氧化程度的葵花籽油加入不同配方中制作曲奇,180 ℃加热30 min,结果表明经氧化的油脂会显著促进曲奇中丙烯酰胺的形成(P<0.05),并且这种促进作用在无糖的体系中更显著。
但也有部分研究表明油脂氧化对丙烯酰胺形成无显著影响[17, 29, 34-35]。Mestdagh 等[17]分别进行的密闭管式反应和模拟法式薯片煎炸试验证明,在薯片煎炸过程中油脂氧化对丙烯酰胺形成无显著影响。Mestdagh等[34]将油脂氧化产生的一些醛类物质与天冬酰胺组成模拟体系加热,以天冬酰胺单独加热作为空白对照,结果表明二者生成的丙烯酰胺无显著性差异,说明醛类物质和天冬酰胺混合生成的丙烯酰胺主要源于天冬酰胺的脱羧和脱氨作用,醛类物质本身不会促进丙烯酰胺的形成。
4 抗氧化剂对丙烯酰胺形成的影响
抗氧化剂可抑制油脂氧化,提高食品感官和稳定性,但对于丙烯酰胺,不同结构的抗氧化剂却存在抑制和促进两种相反的作用机制。首先,抗氧化剂可通过防止油脂氧化抑制丙烯酰胺形成[36]。另外,研究表明类黄酮类抗氧化剂可通过捕捉美拉德反应中间体抑制丙烯酰胺形成。Cheng等[37]证明柚皮素结构中A环的活性位点6位和8位碳原子可与丙烯酰胺形成的前体物反应,形成两种新的化合物:(E)-8-丙烯酰胺-柚皮素和(E)-6-丙烯酰胺-柚皮素,阻止丙烯酰胺形成。同样,表儿茶素结构中A环的这两个相同的活性位点也可捕捉美拉德反应形成的羰基中间体[38]。还有一些抗氧化剂如N-乙酰半胱氨酸、谷胱甘肽、半胱氨酸、大蒜素等其结构中的巯基可抑制丙烯酰胺[39-40]。但是,也有一部分抗氧化剂可促进丙烯酰胺形成。一方面,本身含有羰基的抗氧化剂,如姜黄素和水飞蓟素,可与天冬酰胺反应形成丙烯酰胺[41-42]。另一方面,因美拉德反应中间体5-羟甲基糠醛结构中的α, β, γ, δ-不饱和羰基基团可将天冬酰胺转化为丙烯酰胺,而酚类抗氧化剂可促进蔗糖分解为5-羟甲基糠醛,从而促进丙酰胺的形成[43]。
5 由油脂形成丙烯酰胺的可能机制
5.1 丙烯醛/丙烯酸途径
目前普遍认为在富含淀粉的食物中丙烯酰胺形成主要通过天冬酰胺和还原糖发生美拉德反应,但是仍有文献报道在少糖、多油脂的食物中丙烯酰胺主要通过丙烯醛或丙烯酸形成[44-45]。油脂热解可产生丙烯醛[46],丙烯醛或丙烯酸可在氨的存在下通过氨基脱羟基反应生成丙烯酰胺[47]。Yasuhara等[44]在研究中发现单独1 g 天冬酰胺热解产生0.99 μg丙烯酰胺;1 g 天冬酰胺和甘油三油酸酯同时加热时生成丙烯酰胺的量为88.6 μg,故油脂对丙烯酰胺的形成有一定贡献。同时,甘油三酸酯加热后在顶空产生(1.82±0.31) mg/L的丙烯醛;1 g 天冬酰胺和丙烯醛气体加热反应时产生114 μg丙烯酰胺;丙烯醛和氨气加热可形成大量丙烯酰胺(753μg/g 氨);当用丙烯醛的氧化产物丙烯酸和氨气反应时,产生丙烯酰胺的量为190 000 μg/g 氨,由此推测在富含油脂的食品中氨和丙烯醛对于丙烯酰胺的形成起重要作用。Gertz 等[45]在研究煎炸食品中丙烯酰胺的形成机理时指出,当油脂与食物中的水分接触并加热时,通过水解释放甘油三酯,甘油三酯进一步水解产生游离脂肪酸、单酰甘油、二酰甘油和丙三醇,丙三醇加热脱水形成丙烯醛,丙烯醛氧化生成丙烯酸,由此促使丙烯酰胺生成(见图4、图5)。
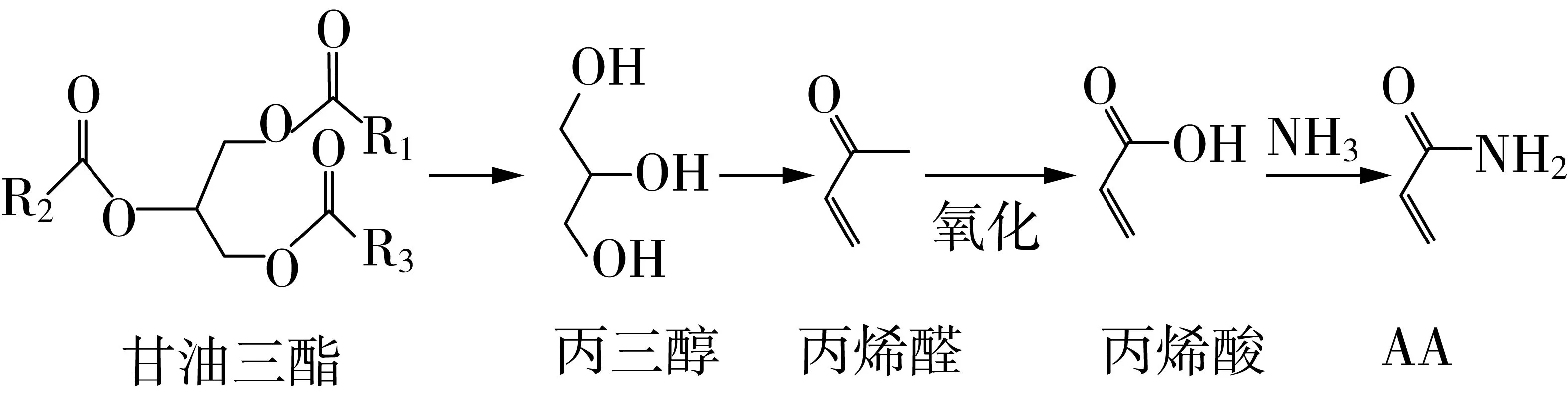
图4 甘油三酯水解形成丙烯酰胺
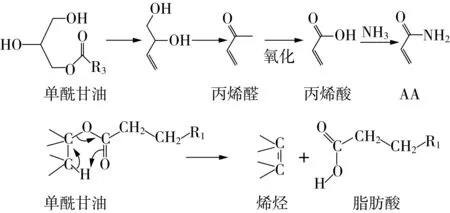
图5 由单酰甘油形成丙烯酰胺的机理
但是,Maurus等[48]在干模拟体系中加入食用油或甘油,经加热发现食用油或甘油对丙烯酰胺形成没有显著性影响。Becalski 等[19]模拟薯片煎炸试验,分别以石蜡油和玉米油作为煎炸介质,在煎炸过程中加入碳酸铵,175 ℃炸10 min,结果显示两种煎炸介质中的薯片中丙烯酰胺含量差异不显著。但石蜡油中不含甘三酯,因而在煎炸过程中不会产生丙烯醛,说明丙烯酰胺的形成不是由于油中的物质,尤其是丙烯醛引起的。Mestdagh 等[34]在研究煎炸油降解成分对煎炸食物中丙烯酰胺形成的影响时指出在密闭的丙烯醛/天冬酰胺模拟体系中经过加热产生的丙烯酰胺含量(1 430 μg/kg)与只含天冬酰胺的密闭模拟体系(360 μg/kg)相比显著升高(P<0.05),但是却显著低于天冬酰胺/葡萄糖模拟体系中形成的丙烯酰胺(9 925 μg/kg)(P<0.05),说明在体系中含有葡萄糖时,丙烯醛对丙烯酰胺的形成贡献较小。另外,实际体系中是开放环境,丙烯醛极易挥发,加之游离氨的形成有限,因此它对丙烯酰胺的形成贡献的程度还有待深入研究。
5.2 羰基化合物途径
煎炸或焙烤食物中油脂加热会发生水解、氧化和聚合等反应,产生的醛、酮等物质可作为丙烯酰胺形成的羰基化合物来源[49-50]。因此,也有文献指出油脂对丙烯酰胺形成的贡献在于油脂产生的羰基化合物参与美拉德反应:一方面,羰基化合物和还原糖竞争性地与天冬酰胺反应[51-52],另一方面也可与美拉德反应途径中重要中间体3-氨基丙酰胺(3-aminopropionamide, 3-APA)反应[53],这2条途径均为羰基化合物途径。羰基化合物在以上途径中涉及关键的两步,一是羰基化合物存在的情况下氨基酸的脱羧,二是3-APA的脱氨。

图6 油脂热解产生的羰基化合物通过美拉德反应形成丙烯酰胺的可能途径
油脂热解产物的美拉德反应途径如图6所示。首先,羰基化合物可通过Strecker 降解将胺类物质或氨基酸降解为相应的Stecker醛[54-59],进而生成丙烯酰胺。羰基化合物与天冬酰胺反应先形成相应的亚胺,经过电子重排和脱羧反应,进而形成两种新的亚胺,其中一种通过酶促转氨作用形成α-酮酸,该化合物对热不稳定,进一步转变为Strecker醛,同时,经过脱羧的另一种新的亚胺经水解可形成Strecker醛,Strecker 醛还原成Strecker 醇,最后经过脱水形成丙烯酰胺。
另外,如图所示,羰基化合物可与天冬酰胺反应形成唑烷-5-酮中间体,再形成丙烯酰胺。Hidalgo等[51]通过重水试验提出了在羰基化合物存在情况下天冬酰胺可能的脱羧途径,即氨基酸在重水的存在下迅速在羧基端交换重氢,由于烯醇化的作用再置换α端的氢,羰基化合物与含重氢的天冬酰胺反应可产生亚胺,经过唑烷-5-酮脱掉一个CO2后,这些亚胺会经过脱羧形成相对稳定的甲亚胺叶立德,进而形成两种共轭亚胺。其中一种共轭亚胺通过消去一个亚胺基团而直接裂解形成丙烯酰胺[60]。另外一种先形成3-APA,3-APA一方面脱氨基直接形成丙烯酰胺[61],另一方面通过先烷基化后再消去生成丙烯酰胺[44]。
研究表明油脂热解产生的羰基化合物可直接与3-APA反应形成丙烯酰胺[53],如图7。有研究报道在众多油脂热解产物中二烯醛与天冬酰胺反应的活性最高[49]。Zamor等[53]用2,4-癸二烯醛与3-APA反应,提出在2,4-癸二烯醛存在下由3-APA降解形成丙烯酰胺的可能途径。二烯醛与3-APA可以形成中间体亚胺和亚胺离子,通过消去反应脱掉吡啶环,生成丙烯酰胺,该途径中的吡啶环也有可能是3-APA与羰基化合物发生Michael加成反应得到,目前对于具体形成过程还不清楚。
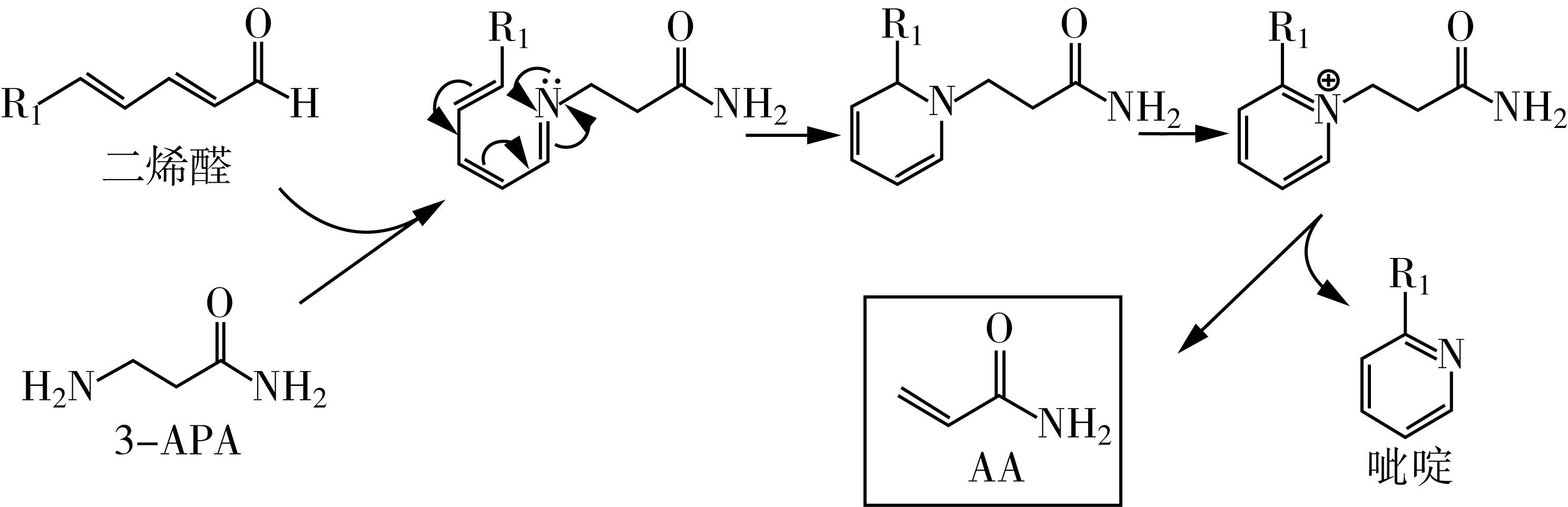
图7 二烯醛与3-APA形成丙烯酰胺的可能途径
6 结论与展望
综述了食品热加工过程中油脂对丙烯酰胺形成的影响,以油炸和焙烤两种代表方式探讨了油脂加工参数、油脂种类、油脂氧化、油脂抗氧化剂以及油脂热解产生的羰基化合对丙烯酰胺形成的影响及其可能机制。目前对于丙烯酰胺形成的美拉德反应机制研究较为普遍,对于油脂参与的途径研究较少,且目前研究结果不能证明油脂形成丙烯酰胺的丙烯醛/丙烯酸途径在含还原糖的体系中是否存在,以及丙烯醛在实际的开放体系中是否会富集。但是,对于油脂导致丙烯酰胺形成的羰基化合物途径,不论体系中是否含富含糖,糖基化合物都可以参与氨基酸的降解,因此,还应从第二条途径入手,综合油脂热解反应和美拉德反应两大反应体系,深入研究富含油脂食品中油脂对丙烯酰胺形成的贡献大小。
[1]Swedish National Food Administration. Information about acrylamide in food[EB/OL].[2002-4-24]http:/ /www.slv. se/ engdefault.asp
[2]World Health Organization. Guidelines for drinking-water quality.Third edition incorporating the first and second addenda[R].Geneva:WHO, 2008
[3]Food Standards Agency. FSA study of acrylamide in food, background information and research findings[EB/OL].[2002-5-17]http://www.food.gov.uk/news/newsarchive/6526
[4]International Agency for Research on Cancer. Some industrial chemicals. IRAC monographs on the evaluation of carcinogenic risk for chemicals to humans[R].Lyon,IARC,1994
[5]Lopachin R M,Lehning E J. Acrylamide induced distal axon degeneration: a proposed mechanism of action[J].Neurotoxicology,1994,15(2):247-260
[6]Dearfield K L, Abernathy C O, Ottley M S, et al. Acrylamide: its metabolism, developmental and reproductive effects, genotoxicity, and carcinogenicity[J].Mutation Research,1988,195(1):45-77
[7]Dearfield K L, Douglas G R, Ehling U H, et al. Acrylamide: a review of its genotoxicity and an assessment of heritable genetic risk[J].Mutation Research,1995,330(1-2):71-99
[8]Mottram D S, Wedzicha B L, Dodson A T.Acrylamide is formed in the Maillard reaction[J].Nature,2002,419:448-449
[9]Stadler R H, Blank I, Varga N,et al. Acrylamide from Maillard reaction products[J].Nature, 2002,419:449-450
[10]Yaylayan V A, Wnorowski A, Locas C P. Why asparagine needs carbohydrates to generate acrylamide[J].Journal of Agricultural and Food Chemistry,2003,51(6):1753-1757
[11]Knol J J, Van Loon W A M, Linssen J P H, et al.Toward a kinetic model for acrylamide formation in a glucose-asparagine reaction system[J].Journal of Agricultural and Food Chemistry,2005,53(15):6133-6139
[12]Claeys W L, Vleeschouwer K D, Hendrickx M E, et al. Kinetics of acrylamide formation and elimination during heating of asparagine-sugar model system[J].Journal of Agricultural and Food Chemistry,2005,53(26):9999-10005
[13]Knol J J, Viklund G A I, Linssen J P H, et al. A study on the use of empirical models to predict the formation of acrylamide in potato crisps[J].Molecular Nutrition & Food Research,2008,52(3):313-321
[14]Franke K, Strijowski U, Reimerdes E H, et al. Kinetics of acrylamide formation in potato powder[J].Journal of Food Engineering,2009,90(1):135-140

[16]Gertz C. Optimising the baking and frying process using oil-improving agents[J].European Journal of Lipid Science and Technology,2004,57(2):671-678
[17]Mestdagh F, Meulenaer B D, Peteghem C V. Influence of oil degradation on the amounts of acrylamide generated in a model system and in French fries[J].Food Chemistry,2007,100(3):1153-1159
[18]Zhang H, Zhang H, Cheng L L, et al. Influence of deep-frying using various commercial oils on acrylamide formation in French fries[J].Food Additives & Contaminants: Part A,2015,32(7):1083-1088
[19]Becalski A,Lau B P Y, Lewis D, et al. Acrylamide in foods: occurrence, sources, and modeling[J].Journal of Agricultural and Food Chemistry,2003,51(3):802-808
[20]Tareke E. Identification and origin of potential background carcinogens: Endogenous isoprene and oxiranes, dietary acrylamide[D].Stockholm: Stockholm University,2003
[21]Friedman M and Mottram D.Chemistry and safety of acrylamide in food[M]//Ehling S, Hengel M, Shibamoto T. Formation of acrylamide from lipids. New York:Springer Science+Business Media,2005,561:223-233
[22]Capuano E, Oliviero T, Açar Ö Ç, et al. Lipid oxidation promotes acrylamide formation in fat-rich model systems[J].Food Research International,2010,43(4):1021-1026
[23]Özkaynak E, Ova G. Effects of various cooking conditions on acrylamide formation in rolled patty[J].Food Additives and Contaminants Part A-Chemistry Analysis Control Exposure & Risk Assessment,2009,26(6):793-799
[24]Lim P K, Jinap S, Sanny M, et al. The influence of deep frying using various vegetable oils on acrylamide formation in sweet potato (IpomoeabatatasL. Lam) chips[J].Journal of Food Science,2014,79(1):T115-T121
[25]Muchtaridi M, Levita J, Rahayu D, et al. Influence of using coconut, palm, and corn oils as frying medium on concentration of acrylamide in fried tempe[J].Food and Public Health,2012,2(2):16-20
[26]Matthäus B, Haase N U, Vosmann K. Factors affecting the concentration of acrylamide during deep-fat frying of potatoes[J].European Journal of Lipid Science and Technology,2004,106(11):793-801
[27]Mestdagh F J, Meulenaer B D, Poucke C V, et al. Influence of oil type on the amounts of acrylamide generated in a model system and in french fries[J].Journal of Agricultural and Food Chemistry,2005,53(15):6170-6174
[28]Williams J S E. Influence of cariety and processing conditions on acrylamide levels in fried potato crisps[J].Food Chemistry,2005,90(4):875-881
[29]Kotsiou K, Tsaioula-Margari M, Fiore A, et al.Acrylamide formation and colour development in low-fat baked potato products as influenced by baking conditions and oil type[J].European Journal of Lipid Science and Technology,2013,236(5):843-851
[30]Ghasemian S, Rezaei K, Abedini R, et al. Investigation of different parameters on acrylamide production in the fried beef burger using Taguchi experimental design[J].Journal of Food Science and Technology,2014,51(3):440-448
[31]Datta A K. Moisture, oil and energy transport during deep-fat frying of food materials[J].Food and Bioproducts Processing,1999,77(3):194-204
[32]Choe E, Min D B. Chemistry of deep-fat frying oils[J].Journal of Food Science,2007,72(5):77-86
[33]Arribas-Lorenzo G, Fogliano V, Morales F J. Acrylamide formation in a cookie system as influenced by the oil phenol profile and degree of oxidation[J].European Food Research and Technology,2009,229(1):63-72
[34]Mestdagh F, Castelein P, Peteghem C V, et al. Importance of oil degradation components in the formation of acrylamide in fried foodstuffs[J].Journal of Agricultural and Food Chemistry,2008,56(15):6141-6144
[35]Hedegaard R V, Granby K, Frandsen H, et al. Acrylamide in bread. Effect of prooxidants and antioxidants[J].European Food Research and Technology,2008,227(2):519-525
[36]Liu Y B, Wang P P, Chen F, et al. Role of plant polyphenols in acrylamide formation and elimination[J].Food Chemistry,2015,186(S1):46-53
[37]Cheng K W, Zeng X, Tang Y S, et al. Inhibitory mechanism of naringenin against carcinogenic acrylamide formation and nonenzymatic browning in Maillard model reactions[J].Chemical Research in Toxicology,2009,22(8):1483-1489
[38]Totlani V M, Peterson D G. Epicatechin carbonyl-trapping reactions in aqueous maillard systems: Identification and structural elucidation[J].Journal of Agricultural and Food Chemistry,2006,54(19):7311-7318
[39]Hidalgo F J, Delgado R M, Zamora R. Positive interaction between amino and sulfhydryl groups for acrylamide removal[J].Food Research International,2011,44(4):1083-1087
[40]Yuan Y, Shu C, Zhou B, et al. Impact of selected additives on acrylamide formation in asparagine/sugar Maillard model systems[J].Food Research International,2011,44(1):449-455


[44]Yasuhara A, Tanaka Y, Hengel M, et al. Gas chromatographic investigation of acrylamide formation in browning model systems[J].Journal of Agricultural and Food Chemistry,2003,51(14):3999-4003
[45]Gertz A, Klostermann S.Analysis of acrylamide and mechanisms of its formation in deep-fried products[J].European Journal of Lipid Science and Technology,2002,104(11):762-771
[46]Umano K, Shibamoto T. Analysis of acrolein from heated cooking oils and beef fat[J].Journal of Agricultural and Food Chemistry,1987,35(6):909-912
[47]Smith M B, March J. March’s advanced organic chemistry. reaction, mechanisms, and structure[M].New York:Wiley-Interscience,2001:508-509
[48]Maurus B, Anja N, Sandra B, et al. Experiments on acrylamide formation and possibilities to decrease the potential of acrylamide formation in potatoes[J].Mitteilungen aus Lebensmitteluntersuchung und Hygiene,2002,93(6):668-687
[49]Zamora R, Hidalgo F J. Contribution of lipid oxidation products to acrylamide formation in model system[J].Journal of Agricultural and Food Chemistry,2008,56(15):6075-6080
[51]Hidalgo F J, Delgado R M, Navarro J L, et al.Asparagine decarboxylation by lipid oxidation products in model systems[J].Journal of Agricultural and Food Chemistry,2010,58(19):10512-10517
[52]Zamora R, Hidalgo F J. The Maillard reaction and lipid oxidation[J].Lipid Technology,2011,23(3):59-62
[53]Zamora R, Delgado R M, Hidalgo F J. Conversion of 3-aminopropionamide and 3-alkylaminopropionamides into acrylamide in model systems[J].Molecular Nutrition & Food Research,2009,53(12):1512-1520
[54]Hidalgo F J, Zamora R.Strecker-type degradation produced by the lipid oxidation products 4,5-epoxy-2-alkenals[J].Journal of Agricultural and Food Chemistry,2004,52(23):7126-7131
[55]Zamora R, Gallardo E, Navarro J, et al.Strecker-type degradation of phenylalanine by methyl 9,10-epoxy-13-oxo-11-octadecenoate and methyl 12,13-epoxy-9-oxo-11-octadecenoate[J].Journal of Agricultural and Food Chemistry,2005,53(11):4583-4588
[56]Hidalgo F J, Gallardo E, Zamora R.Strecker type degradation of phenylalanine by 4-hydroxy-2-nonenal in model systems[J].Journal of Agricultural and Food Chemistry,2005,53(26):10254-10259
[57]Zamora R, Gallardo E, Hidalgo F J.Amine degradation by 4,5-epoxy-2-decenal in model systems[J].Journal of Agricultural and Food Chemistry,2006,54(6):2398-2404[58]Zamora R, Gallardo E, Hidalgo F J.Strecker degeadation of phenylalanine initiated by 2,4-decadienal or methyl 13-oxooctadeca-9,11-dienoate in model systems[J].Journal of Agricultural and Food Chemistry,2007,55(4):1308-1314[59]Hidalgo F J, Zamora R.Conversion of phenylalanine into styrene by 2,4-decadienal in model systems[J].Journal of Agricultural and Food Chemistry,2007,55(12):4902-4906[60]Zyzak D V, Sanders R A, Stojanovic M, et al. Acrylamide formation mechanism in heated foods[J].Journal of Agricultural and Food Chemistry,2003,51(16):4782-4787
[61]Granvogl M, Jezussek M, Koehler P, et al. Quantation of 3-aminopropionamide in potatoes-a minor but potent precursor in acrylamide formarion[J].Journal of Agricultural and Food Chemistry,2004,52(15):4751-4757.
Research Process of Effect of Lipid on Acrylamide Formation During Frying and Baking
Wang Pengpu Zhu Yuchen Liu Yanbing Chen Weina Hu Xiaosong Chen Fang
(College of Food Science and Nutritional Engineering, China Agricultural University; National Engineering Research Centre for Fruits and Vegetables Processing; Key Laboratory of Fruits and Vegetables Processing, Ministry of Agriculture;Engineering Research Centre for Fruits and Vegetables Processing, Ministry of Education,Beijing 100083)
Acrylamide is known to be neurotoxic and potentially carcinogenic to human. It has been widely researched by many researchers all over the word since it was reported that significantly higher acrylamide level was produced in high-temperature processed staple food in 2002. This paper summarized the effect of lipid on acrylamide formation in the process of frying and baking foods, including the influence of processing parameters of fried food, lipid types, lipid oxidation, antioxidant on formation of acrylamide and the effect of pyrolysis product on acrylamide formation and its possible mechanism. Meanwhile, the research direction were prospected to provide a theoretical basis for controlling of acrylamide formation in terms of lipid.
acrylamide,lipid, frying, baking
973计划(2012CB720805),国家自然科学基金优秀青年基金(31222044)
2015-07-10
王鹏璞,女,1989年出生,博士,农产品加工及贮藏工程
陈芳,女,1972年出生,教授,食品安全控制与干预技术
TS201.6
A
1003-0174(2017)02-0140-07
